Клинико-анатомическое исследование нового способа уменьшения внутрибрюшного давления при протезирующей пластике срединных послеоперационных грыж передней брюшной стенки
Автор: Черных Александр Васильевич, Белянский Константин Дмитриевич, Закурдаев Евгений Иванович, Налетова Диана Марфеловна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.25, 2017 года.
Бесплатный доступ
Топографо-анатомическое исследование выполнено на 24 трупах с признаками диастаза прямых мышц живота и заключалось в изучении натяжения узлового шва, наложенного на края предварительно рассеченной белой линии живота, до и после выполнения различных послабляющих разрезов апоневротических структур передней брюшной стенки. В экспериментальной части работы, проведенной на 5 кроликах породы шиншилла, изучались возможные интра- и послеоперационные осложнения при выполнении предложенного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота. В клиническое исследование включено 20 пациентов со срединными послеоперационными грыжами, которые были распределены на основную и контрольную группы. В основной группе (n=10) при грыжесечении использовалась протезирующая герниопластика методом «sublay» с разработанным волнообразным послабляющим разрезом передней стенки апоневротического влагалища прямой мышцы живота, а в контрольной группе (n=10) операция выполнялась по классической методике...
Передняя брюшная стенка, вентральные грыжи, герниопластика
Короткий адрес: https://sciup.org/143177195
IDR: 143177195 | УДК: 10.20340/mv-mn.17(25).03
The clinical-anatomical study of a new method of the reduction of intraperitoneal pressure at plastic prosthetic operations of middle postoperative hernias of the anterior abdominal wall
We performed a topographic and anatomical study on 24 cadavers with signs of diastasis of the rectus abdominal muscles. The research consisted in studying the tension of the nodal suture superimposed on the edges of the previously dissected linea alba before and after performing various relaxing incisions of the aponeurotic structures of the anterior abdominal wall. In the experimental part of the work carried out on 5 rabbits of the chinchilla breed was investigated the possible intra- and postoperative complications during implementation of the proposed wavelike relaxing incision of anterior wall of rectus sheath. In the clinical study included 20 patients with incisional hernias. The patients were divided into main and control groups. In the main group (n=10) hernia repair was performed using the sublay method with a developed wavelike relaxing incision of anterior wall of rectus sheath, and in the control group (n=10) the operation was performed according to the classical technique...
Текст научной статьи Клинико-анатомическое исследование нового способа уменьшения внутрибрюшного давления при протезирующей пластике срединных послеоперационных грыж передней брюшной стенки
Черных А.В., Белянский К.Д., Закурдаев Е.И., Налетова Д.М. Клинико-анатомическое исследование нового способа уменьшения внутрибрюшного давления при протезирующей пластике срединных послеоперационных грыж передней брюшной стенки// Морфологические ведомости.- 2017.- Том 25.- № 3.- С. 26-31. (25).03.26-31
Chernykh AV, Belyansky KD, Zakurdaev EI, Naletova DM. The clinical-anatomical study of a new method of the reduction of intraperitoneal pressure at plastic prosthetic operations of middle postoperative hernias of the anterior abdominal wall. Morfologicheskie Vedomosti – Morphological Newsletter. 2017 Sep 30;25(3):26-31. (25).03.26-31
Введение. Грыжи передней брюшной стенки – одно из самых распространенных общехирургических заболеваний. Частота возникновения наружных грыж живота варьирует от 4 до 7% [1-2]. Доля послеоперационных грыж от общего числа случаев грыж живота достигает 10-15% [3-4]. Послеоперационные грыжи чаще всего возникают после срединной лапаротомии [5-6]. В лечении пациентов со срединными послеоперационными грыжами наиболее эффективным и часто используемым способом пластики грыжевых ворот является протезирующая герниопластика методом «sublay». При данной методике герниопластики сетчатый протез в большинстве случаев размещают между брюшиной и внутрибрюшной фасцией («preperitoneal») [7-8]. Одним из этапов выполнения протезирующей герниопластики методом «sublay» является ушивание грыжевых ворот, что в случае их ширины более 5,0 см приводит к повышению внутрибрюшного давления и высокому риску послеоперационных осложнений [9-11]. Следовательно, поиск технических приемов, направленных на уменьшение внутрибрюшного давления при данной методике герниопластики, актуален и практически значим. В решении вопроса профилактики значительного повышения внутрибрюшного давления при протезирующей герниопластике срединных послеоперационных грыж методом «sublay» могут быть полезны послабляющие разрезы апоневротических структур передней брюшной стенки, которые обычно используются при аутогерниопластике с целью уменьшения натяжения швов при ушивании грыжевых ворот [12-14].
Цель исследования – разработать способ уменьшения внутрибрюшного давления при протезирующей герниопластике срединных послеоперационных грыж методом «sublay» в эксперименте и изучить его эффективность в рандомизированном клиническом исследовании.
Материалы и методы исследования. Работа состоит из топографо-анатомического, экспериментального и клинического разделов исследований. Проведение исследований было одобрено Этическим комитетом при Воронежском государственном медицинском университете им. Н.Н. Бурденко Минздрава России (протокол заседания № 1 от 29.09.2016 г.). Объектами топографо-анатомической части исследования послужили 24 нефиксированных трупа лиц разного пола и возраста. Среди них было 11
трупов лиц мужского пола (46%), умерших в возрасте 50,2±8,1 лет, и 13 трупов лиц женского пола (54%), скончавшихся в возрасте 49,5±7,6 лет. Во всех наблюдениях отмечались признаки диастаза прямых мышц живота в области пупочного кольца, так как ширина белой линии на его уровне составляла более 3 см
Таблица 1
Характеристика групп топографо-анатомического исследования
|
Признак |
Первая |
Вторая |
Третья |
Четвертая |
|
|
Количество наблюдений, абс. |
7 |
6 |
5 |
6 |
|
|
Пол, абс. (%) |
Мужской |
3 (43) |
3 (50) |
2 (40) |
3 (50) |
|
Женский |
4 (57) |
3 (50) |
3 (60) |
3 (50) |
|
|
Возраст, M±δ (лет) |
52,4±6,5 |
53,2±7,1 |
49,4±7,9 |
54,5±6,9 |
|
|
Ширина белой линии живота на уровне пупочного кольца, M±δ (см) |
3,6±0,3 |
3,4±0,5 |
3,4±0,2 |
3,5±0,2 |
|
Примечание. Различия между группами по всем исследуемым признакам статистически не значимы – p>0,05.
-
[13] . Набор материала осуществлялся на базе Воронежского областного бюро судебно-медицинской экспертизы. Секционное исследование трупов проводили через 10-20 часов от момента констатации смерти, в закрытом помещении с искусственным освещением при температуре воздуха 22°С и его относительной влажности 65-68%. Во время аутопсии
трупов с использованием пружинного динамометра измерялось натяжение узлового шва, наложенного на края предварительно рассеченной в продольном направлении белой линии живота, до и после выполнения с обеих сторон послабляющего разреза апоневротического влагалища прямой мышцы живота. Указанный шов накладывался на уровне пупочного кольца, так как в этом месте всегда определялась максимальная ширина белой линии живота. Величина натяжения исследуемого узлового шва отмечалась при сопоставлении медиальных краев прямых мышц живота, то есть в момент устранения диастаза этих мышц. Объекты исследования в зависимости от используемого варианта послабляющего разреза апоневротического влагалища прямой мышцы живота случайным образом были распределены на четыре группы, сопоставимые по количеству наблюдений, полу, возрасту и ширине белой линии живота на уровне пупочного кольца (табл. 1). В первой группе исследования (n=7) выполнялся предложенный волнообразный послабляющий разрез передней стенки апоневротического влагалища прямой мышцы живота (заявка на получение патента РФ № 2016139385, приоритет от 07.10.2016 г.). Во второй группе (n=6) изучался дугообразный послабляющий разрез передней стенки апоневротического влагалища прямой мышцы живота в области середины ее ширины по А.К. Аксенову [12] . В третьей группе (n=5) исследовался вертикальный послабляющий разрез в области латерального края передней стенки апоневротического влагалища прямой мышцы живота по методике Т.К. Калантарова [14] . В четвертой группе (n=6) по способу У.З. Загирова [13] на передней (с одной стороны) и задней (с другой стороны) стенке апоневротического влагалища прямой мышцы живота применялись вертикальные разрезы длиной 3-4 см, расположенные в шахматном порядке.
Экспериментальное исследование выполнено на 5 кроликах породы шиншилла массой 5,8±0,6 кг и было направлено на изучение возможных интра- и послеоперационных осложнений при выполнении разработанного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота. Базой проведения исследования являлась кафедра оперативной хирургии с топографической анатомией Воронежского государственного медицинского университета им. Н.Н. Бурденко Минздрава России. Для анестезии животным внутримышечно вводились препараты «Золетил» (15 мг/кг) и «Рометар» (5 мг/кг). После обработки операционного поля производился разрез кожи передней брюшной стенки по средней линии. Далее на передней стенке апоневротического влагалища прямой мышцы живота справа и слева выполнялся предложенный волнообразный послабляющий разрез. После этого произведенные послабляющие разрезы ушивались 3-4 узловыми швами. Операция завершалась наложением узловых швов на кожу. Состояние послеоперационной раны оценивалось на протяжении 5 суток до момента снятия швов. Для послеоперационного обезболивания животным 1 раз в сутки на протяжении всего периода исследования подкожно вводился мелоксикам из расчета 0,2 мг/кг. С целью профилактики инфекционных осложнений прооперированные кролики 2 раза в сутки в течение 2-3 дней получали внутримышечные инъекции энрофлоксацина (5 мг/кг). Выбор препаратов и их дозировок соответствовали общепринятым рекомендациям по использованию лабораторных животных [16] .
Рандомизированное проспективное клиническое исследование проведено на базе БУЗ ВО «ВГКБСМП №1» и научно-исследовательского института герниологии им. проф. Е.Н. Любых при ВГМУ им. Н.Н. Бурденко Минздрава России. Всего в исследование включено 20 пациентов со срединными послеоперационными грыжами в возрасте 52,5±6,4 лет, среди которых было 7 мужчин (35%) и 13 женщин (65%). Критерий включения пациентов в исследование – ширина грыжевых ворот 5-10 см. Критерии исключения: наличие грыжи в другой области, обострение сопутствующих заболеваний, отсутствие информированного согласия на участие в исследовании. Во время грыжесечения у всех пациентов использовалась протезирующая герниопластика методом «sublay» с размещением полипропиленового сетчатого протеза между брюшиной и внутрибрюшной фасцией («preperitoneal»). В основной группе (n=10) при герниопластике выполнялся предложенный волнообразный послабляющий разрез передней стенки апоневротического влагалища прямой мышцы живота, а в контрольной группе (n=10) операция производилась по классической методике. При рандомизации пациентов сначала в 2 столбца (соответственно количеству групп исследования) по 10 строк (соответственно количеству пациентов в группе) были сгенерированы случайные числа от 1 до 20. Каждое число было запечатано в конверт, который вскрывался при грыжесечении в случае наличия грыжевых ворот шириной 5-10 см. Если случайное число соответствовало 1-му столбцу – пациент попадал в основную группу, 2-му столбцу – в контрольную. Рандомизированные группы оказались сопоставимыми по количеству пациентов, полу, возрасту, максимальной ширине грыжевых ворот (табл. 2).
Таблица 2
Характеристика рандомизированных клинических групп
|
Исследуемый параметр |
Основная |
Контрольная |
|
|
Количество больных |
10 |
10 |
|
|
Пол |
Мужчины |
4 (40) |
3 (30) |
|
Женщины |
6 (60) |
7 (70) |
|
|
Возраст, M±δ (лет) |
55,6±4,8 |
49,2±5,2 |
|
|
Максимальная ширина грыжевых ворот, M±δ (см) |
7,2±0,9 |
7,5±1,2 |
|
Различия между рандомизированными группами по всем исследуемым параметрам не значимы – p>0,05.
У обследованных пациентов с использованием методики J.L. Kron et al. [17] определялся показатель внутрибрюшного давления до операции, во время ее завершения и через сутки после хирургического вмешательства. При этом сначала в мочевой пузырь через катетер вводилось 80-100 мл физиологического раствора. Далее к катетеру присоединялась трубка от обычной инфузионной системы, которая размещалась вертикально. После этого определялась длина трубки от уровня верхнего края лобкового сочленения до границы столбца жидкости. При интерпретации полученных данных 1 см длины трубки соответствовал 1 см вод. ст. (0,735 мм рт. ст.). В послеоперационном периоде пациенты находились под наблюдением в течение 10-14 суток в зависимости от состояния раневого процесса. В отдаленные сроки пациенты обследовались каждые 6 месяцев на протяжении года. При статистической обработке результатов исследования определялись среднее арифметическое (M), среднее квадратическое отклонение (δ), критерии Манна-Уитни (U) и Вилкоксона (W), выполнялся ранговый дисперсионный анализ Краскела-Уоллиса (H). Различия показателей считались значимыми при доверительной вероятности 0,95 и более (p≤0,05).
Результаты исследования и обсуждение. В данной работе с целью уменьшения внутрибрюшного давления при протезирующей герниопластике срединных послеоперационных грыж методом «sublay» был предложен волнообразный послабляющий разрез передней стенки апоневротического влагалища прямой мышцы живота (заявка на получение патента РФ № 2016139385, приоритет от 07.10.2016 г.). По предлагаемой в данной работе методике (рис. 1) на передней стенке апоневротического влагалища прямой мышцы живота (1) справа и слева определяются границы участков для выполнения послабляющего разреза. Наружная граница (2) данных участков соответствует латеральному краю прямой мышцы живота, а внутренняя (3) – медиальному. Верхней (4) и нижней (5) границами являются условные горизонтальные линии, проведенные на 1,5-2,0 см выше и ниже центра грыжевого дефекта. После этого на обозначенных участках передней стенки апоневротического влагалища прямых мышц живота выполняется послабляющий разрез в виде волнообразной линии, в результате чего формируются наружный (6) и внутренний (7) апоневротические лоскуты. Далее над сетчатым протезом (8) ушиваются грыжевые ворота, а сформированные в результате послабляющего разреза лоскуты передней стенки апоневротического влагалища прямой мышцы живота перемещаются друг относительно друга и сшиваются между собой редкими узловыми швами. В топографо-анатомическом исследовании на 24 нефиксированных трупах изучена сравнительная эффективность предложенного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота и его классических аналогов. При этом измерялось натяжение узлового шва, наложенного на края предварительно рассеченной белой линии живота, до и после выполнения с обеих сторон послабляющего разреза апоневротического влагалища прямой мышцы живота (рис. 2).
В результате установлено, что при выполнении волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота натяжение узлового шва уменьшилось на 53% (табл. 3). Вертикальный послабляющий разрез передней стенки апоневротического влагалища прямой мышцы живота в области ее латерального края по методике Т.К. Калантарова позволил снизить натяжение исследуемого шва на 45%. В случае применения дугообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота в области середины ее ширины по А.К. Аксенову натяжение узлового шва уменьшилось на 39%. При выполнении послабляющего разреза апоневротического влагалища прямой мышцы живота по У.З. Загирову натяжение указанного шва сократилось лишь на 25%.
Далее в эксперименте на 5 кроликах породы шиншилла были изучены возможные осложнения при выполнении предложенного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота. Во время операции в одном наблюдении (20%) выполнение исследуемого послабляющего разреза сопровождалось повреждением прямой мышцы живота и развитием кровотечения из мышечной ткани (рис. 3). В послеоперационном периоде у этого же объекта возникла подкожная гематома в области послеоперационной раны, которая разрешилась самостоятельно через 3 суток после операции. В остальных наблюдениях интра- и послеоперационных осложнений не отмечалось.
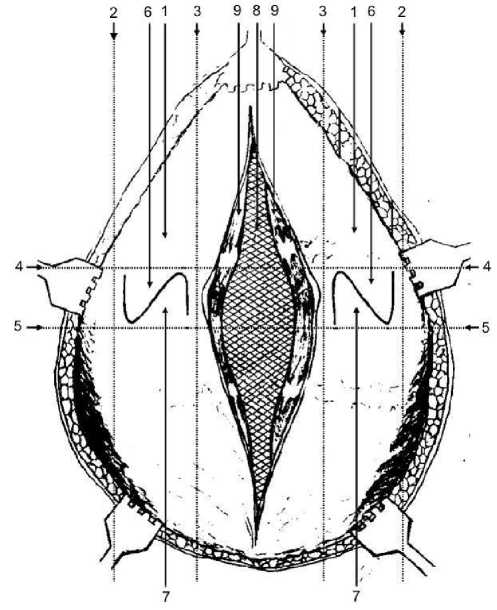
Рис. 1. Схема выполнения разработанного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота. 1 – передняя стенка апоневротического влагалища прямой мышцы живота; 2, 3, 4, 5 – наружная, внутренняя, верхняя и нижняя границы участка передней стенки апоневротического влагалища прямой мышцы живота для выполнения послабляющего разреза; 6, 7 – наружный и внутренний лоскуты передней стенки апоневротического влагалища прямой мышцы живота, 8 – сетчатый протез; 9 – медиальный край прямой мышцы живота.
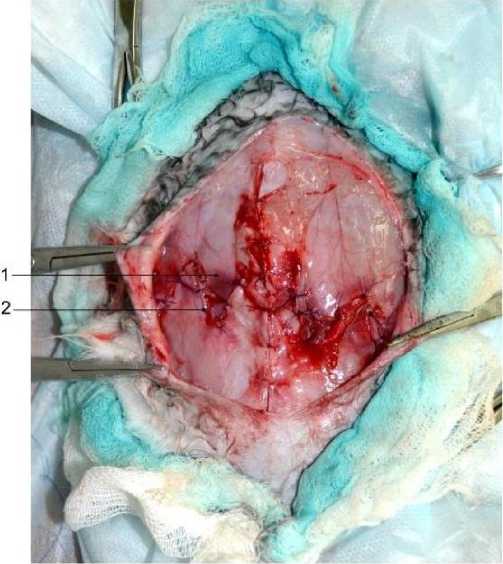
Рис. 3. Интраоперационная травматизация прямой мышцы живота при выполнении разработанного волнообразного послабляющего разреза передней стенки ее апоневротического влагалища в эксперименте на животном; 1 – скопление крови под передней стенкой апоневротического влагалища прямой мышцы живота; 2 – швы, наложенные при ушивании послабляющего разреза.
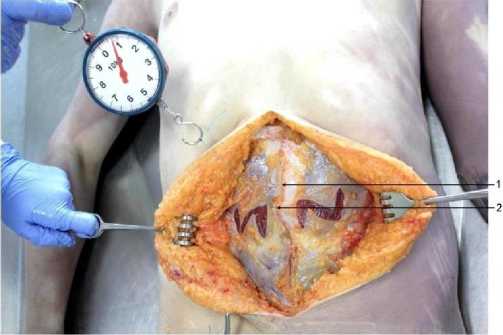
Рис. 2. Измерение натяжение узлового шва при выполнении предложенного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота на нефиксированном трупе; 1 – края рассеченной белой линии живота; 2 – узловой шов.
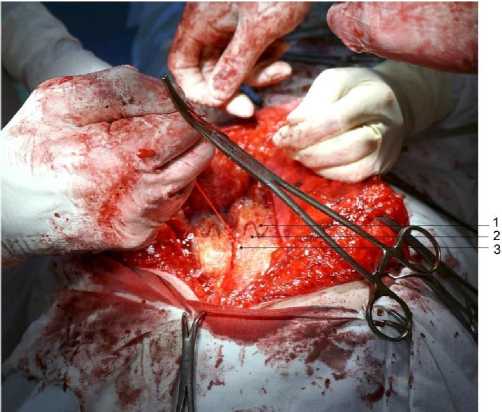
Рис. 4. Выполнение предложенного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота при грыжесечении по поводу срединной послеоперационной грыжи; 1, 2 – наружный и внутренний лоскуты передней стенки апоневротического влагалища прямой мышцы живота, образованные в результате послабляющего разреза; 3 –
швы, наложенные на края грыжевых ворот.
Таблица 4
Показатель внутрибрюшного давления у обследованных больных на различных этапах клинического исследования, M±δ (мм рт.ст.)
|
Клиническая группа |
До операции |
Во время завершения операции |
Через сутки после операции |
|
Основная |
8,6±0,4 |
11,7±0,6* |
9,8±0,5* |
|
Контрольная |
8,5±0,3 |
14,2±0,5 |
12,3±0,4 |
Примечание: *– различия по сравнению с контрольной группой значимы при p=0,05
Таблица 3
Натяжение узлового шва до и после выполнения различных послабляющих разрезов апоневротического влагалища прямой мышцы живота, M±δ (Н)
|
Вид послабляющего разреза |
Исходное натяжение |
Натяжение после разреза |
|
Волнообразный |
25,4±0,6 |
11,9±0,2 |
|
Методика А.К. Аксенова |
23,9±0,3 |
14,6±0,1* |
|
Методика Т.К. Калантарова |
24,2±0,5 |
13,4±0,2 |
|
Методика У.З. Загирова |
24,5±0,4 |
18,3±0,3** |
Примечание: *– различия по сравнению с методиками А.К.Аксенова и Т.К.Калантарова значимы при p=0,05; ** – различия по сравнению с методикой У.З.Загирова значимы при p=0,01
Оценка течения послеоперационного периода показала, что в основной группе, где применялась протезирующая герниопластика методом «sublay» с волнообразным послабляющим разрезом передней стенки апоневротического влагалища прямой мышцы живота (рис. 4), послеоперационных осложнений не наблюдалось. У пациентов контрольной
Полученные в топографо-анатомическом и экспериментальном исследованиях данные позволили апробировать предложенный волнообразный послабляющий разрез передней стенки апоневротического влагалища прямой мышцы живота в клинической практике. Результаты клинического исследования показали, что выполнение волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота при протезирующей герниопластике срединных послеоперационных грыж методом «sublay» способствует значительному уменьшению внутрибрюшного давления (табл. 4).
группы, которым выполнялся классический вариант протезирующей герниопластики методом «sublay», ранние послеоперационные осложнения возникли в 20% (серозное воспаление послеоперационной раны – 10%; парез кишечника – 10%), а поздние (хронический болевой синдром) – в 40% (p=0,05). Серозное воспаление послеоперационной раны, очевидно, объясняется экссудативно-пролиферативной реакцией на контакт мягких тканей с сетчатым протезом, а парез кишечника – повышением внутрибрюшного давления. Рецидивов грыж в срок наблюдения до 1 года у пациентов обеих групп исследования не отмечено.
Заключение. Выполнение предложенного волнообразного послабляющего разреза передней стенки апоневротического влагалища прямой мышцы живота при протезирующей герниопластике срединных послеоперационных грыж методом «sublay» позволяет значительно уменьшить внутрибрюшное давление и сократить риск возникновения послеоперационных осложнений.
Список литературы Клинико-анатомическое исследование нового способа уменьшения внутрибрюшного давления при протезирующей пластике срединных послеоперационных грыж передней брюшной стенки
- Parshikov V.V., Loginov V.I. Tehnika razdelenija komponentov brjushnoj stenki v lechenii pacientov s ventral'nymi i posleoperacionnymi gryzhami. STM. 2016; 8(1): 183-194.
- Belokonev V.I., Pushkin S.Ju., Shifrin G.I. Morfofunkcional'nye izmenenija v tkanjah pri formirovanii zhidkostnyh obrazovanij v podkozhnoj kletchatke u pacientov posle gryzhesechenija. Toljattinskij medicinskij konsilium. 2011; 3: 20-21.
- Haskins I.N., Amdur R.L., Lin P.P., Vaziri K. The use of mesh in emergent ventral hernia repair: effects on early patient morbidity and mortality. J Gastrointest Surg. 2016; 20(11): 1899-1903.
- Cherkasov M.F., Hindikajnen A.Ju., Pomazkov A.A. Metody diagnostiki, profilaktiki i lechenija oslozhnenij gernioplastiki. Astrahanskij medicinskij zhurnal. 2016; 11(4): 50-64.
- Tarasova N.K., Dyn'kov S.M., Teterin A.Ju., Kuznecov A.A. Profilaktika oslozhnenij v rannem posleoperacionnom periode i recidiva pri lechenii bol'nyh s posleoperacionnymi ventral'nymi gryzhami. Annaly hirurgii. 2012; 6: 26-30.
- Oprea V., Radu V.G., Moga D. Transversus abdominis muscle release (TAR) for large incisional hernia repair. Chirurgia. 2016; 6: 535-540.
- Yang P.G., Tung L.K. Preperitoneal onlay mesh repair for ventral abdominal wall and incisional hernia: a novel technique. AsianJEndoscSurg. 2016; 9(4): 344-347.
- Shapoval'janc S.G., Mihalev A.I., Mihaleva L.M., Dzavarjan T.G., Pulatov M.M. Sravnitel'naja ocenka vlijanija razlichnyh metodov separacii perednej brjushnoj stenki na uvelichenie obema brjushnoj polosti. Zhurnal anatomii i gistopatologii. 2017; 6(1): 115-120.
- Desai N.K., Leitman I.M., Mills C., Lavarias V., Lucido D.L., Karpeh M.S. Open repair of large abdominal wall hernias with and without components separation; an analysis from the ACS-NSQIP database. Ann Med Surg (Lond). 2016; 7: 14-19.
- Novitsky Y.W., Fayezizadeh M., Majumder A., Neupane R., Elliott H.L., Orenstein S.B. Outcomes of posterior component separation with transversus abdominis muscle release and synthetic mesh sublay reinforcement. Ann Surg. 2016; 264(2): 226-232.
- Pauli E.M., Rosen M.J. Open ventral hernia repair with component separation. SurgClinNorth Am. 2013; 93(5): 1111-1133.
- Aksenov A.K., Tatjanchenko V.K., Emel'janov V.A., Moskalev A.I., Ovsjannikov A.V., Gimbarov S.N. Sposob lechenija posleoperacionnyh gryzh beloj linii zhivota. Patent RF № 2134551. 1999.
- Zagirov U.Z., Salihov M.A., Isaev U.M. Anatomo-funkcional'noe obosnovanie novogo sposoba kombinirovannoj plastiki sredinnyh ventral'nyh gryzh. Hirurgija. Zhurnal im. N.I. Pirogova. 2008; 7: 41-43.
- Kalantarov T.K., Chirkov R.N., Babajan K.V. Sposob uvelichenija obema brjushnoj polosti pri lechenii pacientov s bol'shimi ventral'nymi gryzhami. Patent RF № 2449735. 2012.
- Sperstad J.B., Tennfjord M.K., Hilde G., Ellstrom-Engh M., Bo K. Diastasis recti abdominis during pregnancy and 12 months after childbirth: prevalence, risk factors and report of lumbopelvic pain. Br J Sports Med. 2016; 50(17): 1092-1096.
- Guide for the Care and Use of Laboratory Animals, National Research Council, National Academy Press. 2011.
- Kron J.L., Harman P.K., Nolan S.P. The measurement of intraabdominal pressure as a criterion for abdominal reexploration. Ann. Surg. 1984; 199(1): 28-30.


