Клинико-функциональная оценка результатов коронарного шунтирования и реконструкции левого желудочка у больных ишемической болезнью сердца с выраженной левожелудочковой дисфункцией
Автор: Чернявский Александр Михайлович, Марченко Андрей Викторович, Мироненко Светлана Павловна, Чармадов Манолис Васильевич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Ишемическая болезнь сердца
Статья в выпуске: 1 т.13, 2009 года.
Бесплатный доступ
Статья посвящена анализу рандомизированного исследования, посвященного хирургическому лечению больных ИБС с выраженной дисфункцией левого желудочка (ЛЖ) и фракцией выброса (ФВ) менее 35 %. Представлены непосредственные и отдаленные результаты, уровень госпитальной летальности и 3-летняя выживаемость пациентов с изолированным коронарным шунтированием (АКШ) и пластикой ЛЖ в сочетании с АКШ у больных ИБС с выраженной дисфункцией ЛЖ. Пластика ЛЖ в сочетании с реваскуляризацией миокарда считается наиболее подходящим методом хирургического лечения хронической сердечной недостаточности (ХСН).
Сердечная недостаточность, низкая фракция выброса, коронарное шунтирование, реконструкция левого желудочка
Короткий адрес: https://sciup.org/142233487
IDR: 142233487 | УДК: 616.127-005.4-089.168:616.124.2.
Clinical/functional evaluation of coronary artery bypass grafting and left ventricle repair in CHD patients with expressed left ventricle dysfunction
The paper focuses on the analysis of randomized study focused on surgical treatment of CHD patients with pronounced dysfunction of the left ventricle (LV) and ejection fraction (EF) of less than 35 %. Immediate and long-term results, level of hospital lethality and 3-year survival of patients with isolated coronary artery bypass grafting (CABG) and LV repair in combination with CABG in CHD patients with pronounced LV dysfunction are presented. LV repair in combination with myocardium revascularization is thought to be the most appropriate technique for surgical treatment of chronic cardiac insufficiency (CCI).
Текст научной статьи Клинико-функциональная оценка результатов коронарного шунтирования и реконструкции левого желудочка у больных ишемической болезнью сердца с выраженной левожелудочковой дисфункцией
Результаты рандомизированных исследований показали, что у большинства пациентов развитие ХСН обусловлено ИБС, как следствие перенесенного инфаркта миокарда (ИМ). Выживаемость этой группы пациентов с III-IV функциональным классом (ФК) ХСН (NYHA) в течение года составляет 40-60% [2]. Неуклонно растет число больных ИБС с осложненными формами, в частности с обширными зонами акинетичного миокарда и низкой сократительной способностью ЛЖ [8]. Гибель части кардиомиоцитов в результате ИМ приводит к активации регуляторных нейрогуморальных систем, которые запускают процесс ремоделирования ЛЖ, продолжающийся и после непосредственного повреждающего воздействия на миокард ишемического фактора [1]. Постинфарктное ремоделирование ЛЖ ассоциируется с его прогрессирующей дилатацией, ростом напряжения стенки желудочка, изменением формы и толщины его стенок и выраженной дисфункцией ЛЖ [7]. Основным клиническим проявлением данной патологии является сердечная недостаточность, обусловленная выраженной систолической дисфункцией ЛЖ. Лечение ХСН становится наиболее значимой задачей сердечной хирургии в ближайшем будущем. Прогноз у больных ИБС с систолической дисфункцией ЛЖ (EF<35%) при применении только медикаментозного лечения остается плохим, 5-летняя выживаемость составляет 38% [15]. Альтернативным методом лечения, улучшающим качество жизни и отдаленный прогноз, является в данном случае изолированная реваскуляризация миокарда или коронарное шунтирование с реконструкцией ЛЖ [12]. Однако до сих пор не существует единого мнения о преимуществе того или иного метода хирургического лечения, не проведен сравнительный анализ эффективности результатов коронарного шунтирования с реконструкцией ЛЖ и изолированной реваскуляризацией миокарда. Цель настоящего исследования - провести сравнительную оценку эффективности КШ в сочетании с реконструкцией ЛЖ и изолированной реваскуляризации миокарда у больных ИБС с низкой фракцией выброса ЛЖ.
МАТЕРИАЛ И МЕТОДЫ
В рамках данного исследования обследовано 146 больных ИБС с выраженной дисфункцией ЛЖ (ФВ менее 35%), оперированных в ФГУ «ННИИПК Росмедтехнологий» за период с 12.02.2004 по 08.11.2007 г. Все больные имели в анамнезе один или несколько ИМ. Пациенты методом случайной выборки были разделены на две группы: В 1-ю группу включены 68 (46,6%) пациентов, которым было выполнено АКШ в сочетании с реконструкцией ЛЖ. Во 2-ю группу вошли 78 (53,4%) пациентов, которым выполнили изолированную реваскуляризацию миокарда.
Критерии включения пациентов в исследование - верифицированная ИБС с поражение коронарного русла, подлежащая хирургической реваскуляризации; ФВ ЛЖ менее 35%.
Критерии исключения из исследования -острый инфаркт миокарда; патология клапанного аппарата сердца, кроме митральной недостаточности ишемической этиологии; сопутствующая патология других органов в стадии декомпенсации.
Больные в первой и во второй группах были сопоставимы по всем клинико-демографическим показателям (таблица).
В I группе пациенты с реконструкцией ЛЖ, большинство были лица мужского пола (95,5%), в возрасте от 30 до 79 лет (средний возраст больных составил 55,3±9 лет). Во II группе также превалировали мужчины (85,5%), количество пациентов женского пола составило 11 (14,5%), в группе возраст варьировал от 40 до 76 лет (56,6±8,4).
По классу стенокардии больные в исследуемых группах относились к II-IV ФК CCS. В обеих группах большинство пациентов имели III ФК стенокардии (CCS). В первой группе (КШ с реконструкцией ЛЖ) количество больных с III ФК (CCS) составило 41 (60,3%), а во II группе с изолированным АКШ - 40 (51,3%). По ФК ХСН (NYHA), большинство больных относились к III ФК (NYHA), что составило в I группе с реконструкцией ЛЖ - 55 (80,9%), во II группе 58 (74,4%).
Согласно критерию Манна-Уитни группы по возрасту, ФК стенокардии (CCS), ФК ХСН (NYHA), достоверно не различались. По данным ЭхоКГ, объемные исходные показатели (КДО, КСО) и величина ФВ ЛЖ в обеих группах также достоверно не различались.
По данным коронарографии (КГ) в обеих группах преобладали пациенты с трехсосудистым поражением коронарного русла с правым типом коронарного кровообращения. Шунтирование ПНА с использованием левой ВГА выполнено у всех исследуемых больных в обеих группах. Среднее количество шунтов в группах составило 2,6±0,9 и не различалось в обеих группах.
Выбор метода пластики ЛЖ был основан на данных предоперационного моделирования оптимального объема ЛЖ и расчета допустимой площади выключения ЛЖ. При соответствии необходимой площади резекции ЛЖ допустимой площади выключения, рассчитанной до операции, были применены методы линейной пластики ЛЖ или аутовентрикулопластика. У больных, у которых площадь выключения ЛЖ была больше расчетной, использовали метод эндо вентрикулопластики заплатой, чтобы избежать неадекватного уменьшения полости ЛЖ [9]. Были выполнены следующие виды пластики ЛЖ: линейная пластика по Кули 10 (14,7%), аутовентрикулопластика по Стоуни-Хапаеву 23 (33,8%), эндовентрикулопластика по Дору 35 (51,5%).
Протокол обследования включал, помимо клинических, инвазивные и неинвазивные методы исследования. Селективная коронарография по методике Джадкинса проводилась на аппарате Tridofos Optimatic фирмы «Toshiba». Трансторокальная и чреспищеводная эхокардиография («Sonos» модели 4500 и 5500 фирмы «Philips-Hewlett-Packard», Vivid-7 фирмы «General Electric»). Обработку данных осуществляли при помощи статистической программы «Statistica 6.0». Все количественные величины представляли как среднее±стандартное отклонение. Величину уровня значимости (р) принимали равной и/или меньше 0,05. Анализ времени до наступления исхода проводили методом Каплана-Мейера.
РЕЗУЛЬТАТЫ
Клинико-функциональное обследование больным проводили до операции, в раннем послеоперационном периоде, на госпитальном этапе и в отдаленные сроки после операции через 4,12 месяцев после выписки из стационара. Проанализированы такие факторы, как госпитальная летальность в группах, динамика ФК стенокардии, ФК ХСН, динамика изменения объемных показателей ЛЖ (КДО, КСО), ФВ ЛЖ, оценка трехгодичной выживаемости по методу Каплана-Майера.
Госпитальная летальность в группе больных с реконструкцией ЛЖ составила 5,9%, с изолированным КШ 5,1%.
Сравнительная характеристика больных
|
Параметры |
1 группа |
II группа |
р |
|
Возраст |
55,3±9 |
56,6±8,4 |
р=0,377 |
|
Пол |
|||
|
муж. |
65 (95,5%) |
65 (85,5%) |
|
|
жен. |
3 (4,4%) |
11 (14,5%) |
|
|
ФКССЗ |
2,7±0,5 |
2,6±0,7 |
р=0,976 |
|
ФКNYHA |
2,9±0,3 |
2,9±0,4 |
р=0,939 |
|
КДО, мл |
235,8±45 |
227,4±50,5 |
р=0,981 |
|
КСО, мл |
161,3±40 |
157,9±55,3 |
р=0,474 |
|
ФВ ЛЖ, % |
31,1±4,5 |
30,7±7,1 |
р=0,461 |
ФК стенокардии в исследуемых группах пациентов с выраженной ишемической дисфункцией ЛЖ снижался в отдаленном периоде в обеих группах. В I группе через 4, 12 месяцев после операции отмечается достоверная положительная динамика значений ФК, с исходных значений 2,8±0,5 до 1,7±0,9 и 1,5±0,9, соответственно (р =0,0001). В группе пациентов с изолированной реваскуляризацией миокарда (II группа), также выявлена положительная динамика средних величин ФК стенокардии, снижался с 2,7±0,7 до 1,6±0,8 через 4 месяца и 1,6±0,6 через год после операции. ФК стенокардии в отдаленном периоде между исследуемыми выборками достоверно не различался (р=0,005).
В эти же сроки проводилось исследование ФК ХСН (NYHA). На этапах исследования ФК ХСН достоверно снижался в обеих группах, (р=0,0001). В I группе больных исходные значения ФК ХСН 2,9±0,3 через 4 месяца снизились до 2,3±0,5 (р=0,0001). После промежуточного контрольного исследования (4 мес.) при анализе годовых результатов отмечается не значимое увеличение ФК ХСН до 2,5±0,4 (р=0,086). В группе с изолированным коронарным шунтированием исходные значения ФК ХСН 2,8±0,5 через 4 месяца после операции снизились до 2,5±0,5 (р=0,010), а по годовым результатам значения ФК NYHA в группе составили 2,6±0,5 (р=0,033). Между группами статистически достоверной разницы не выявлено (р=0,072). В отдаленном периоде (4, 12 мес.) ведущим в двух группах является II ФК ХСН.
По данным 6-минутного теста ходьбы, толерантность к физическим нагрузкам в отдаленном послеоперационном периоде возрастает, с уменьшением ФК ХСН. Средняя дистанция (I гр. - 294,7 м; II гр. - 289,6 м), преодолеваемая больным в обеих выборках до операции, соответствовала III ФК NYHA. В отдаленном периоде (4, 12 мес.), толерантность к физическим нагрузкам в группах повысилась, что соответствовало II ФК NYHA, средняя дистанция в I группе составила 387-401 и 363-367 м, соответственно.
Исходные значения объемных показателей в исследуемых группах достоверно не различались. При оценке динамики объемных показателей ЛЖ (КДО, КСО) у пациентов I группы в послеоперационном периоде и в отдаленные сроки (4, 12 месяцев), определяется статистически достоверное (р=0,001) уменьшение указанных показателей ЛЖ. Во II группе больных, которым было выполнено изолированное АКШ, отмечено снижение объемных характеристик ЛЖ, статистически достоверное (р=0,003) в ближайшем послеоперационном периоде и через 4 месяца, по данным контрольной ЭхоКГ. При анализе динамики изменения КДО, КСО ЛЖ в отдаленном периоде через 12 месяцев в обеих исследуемых группах имеется тенденция к увеличению объемных показателей, что может свидетельствовать о дальнейшем прогрессировании ишемического ремоделирования ЛЖ. Однако значения объемных показателей (КДО, КСО) ЛЖ через год в группе с реконструкцией ЛЖ остаются достоверно ниже исходных, во II группе годовые значения КДО, КСО ЛЖ достоверно не различались от исходных средних значений (р=0,4), рис. 1,2.
Исходные значения ФВ ЛЖ в исследуемых группах достоверно не различались (р=0,068). В послеоперационном периоде у пациентов I группы исходные значения ФВ ЛЖ 31,1±4,3%, статистически достоверно увеличиваются (р=0,005). На госпитальном этапе после операции значения ФВ ЛЖ возрастают до 38±6,1%. В отдаленном периоде (4 и 12 мес.) отмечается тенденция уменьшения ФВ ЛЖ до 37±4,5 и 36,4±4%, соответственно, но значения ФВ остаются достоверно выше исходных (р=0,005). При анализе динамики изменения ФВ ЛЖ пациентов II группы исходные значения 30,7±5,7% возрастают после операции до 33,2±5,8%, статистическая значимость р=0,0005, через 4 месяца средние значения ФВ составляют 33,4±10,6% (р=0,0350). По данным годовых результатов значения ФВ 32,1±8,5% достоверно не отличаются от исходных (р=0,121), рис. 3.
Мы проанализировали динамику митральной недостаточности в зависимости от метода лечения пациентов с ИБС и выраженной систолической дисфункцией ЛЖ. Так, митральная регургитация возросла с 1,4±0,6 до 1,6±0,7 через 12 месяцев после коронарного шунтирования. При хирургической реконструкции ЛЖ. в сочетании с коронарной реваскуляризацией миокарда митральная регургитация снизилась с 1,4±0,6 до 1,2±0,6, однако вне зависимости от метода лечения статистически достоверной динамики степени митральной регургитации не обнаружено.
Годовая выживаемость, определенная по методу Каплана-Майера в I группе с реконструкцией ЛЖ составила 92%, во II группе -83%. По кривым выживаемости видно, что в I группе выживаемость по годам распределя-
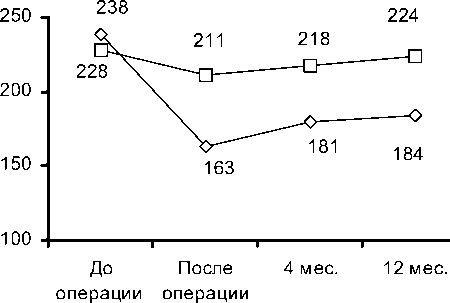
—О— I группа —□— II группа
Рис. 1. Динамика КДО ЛЖ в исследуемых группах.
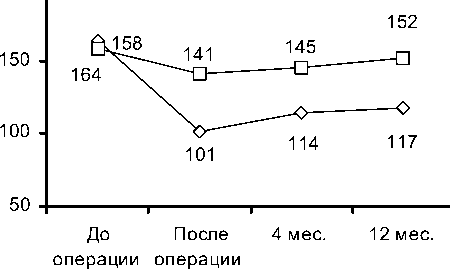
—О— I группа —□— II группа
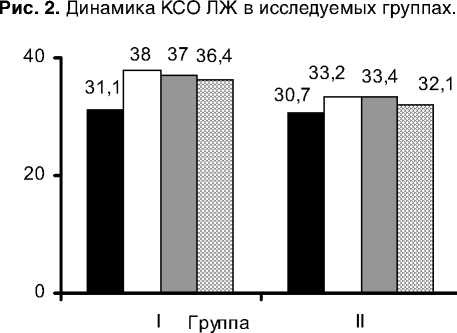
■ До операции □ 4 мес. п/о
□ после операции щ 12 мес. п/о
Рис. 3. Динамика ФВ ЛЖ.
ется более равномерно, во II группе распределение неравномерное, наибольшая летальность приходится на первый год - 17%. Трехлетняя выживаемость в обеих группах достоверно не различалась (р=0,375) в группе с реконструкцией
Cumulative Proportion Surviving (Kaplan-Meier)
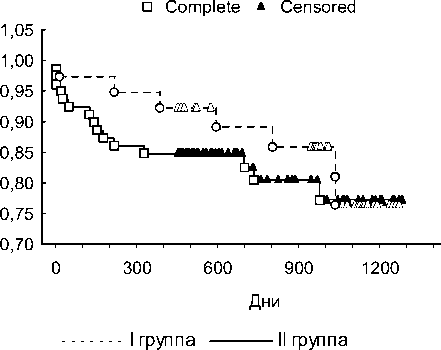
Рис. 4. Динамика выживаемости.
ЛЖ составила 76%, у пациентов с изолированным КШ - 77%. Кривые выживаемости в исследуемых группах представлены на рис. 4.
ОБСУЖДЕНИЕ
Хирургическими методами лечения больных ИБС с выраженной систолической дисфункцией ЛЖ, улучшающими качество жизни и отдаленный прогноз, являются методы прямой реваскуляризации миокарда (операция КШ), выполненные изолированно или в сочетании с реконструкцией ЛЖ [3].
Послеоперационная летальность у пациентов со сниженной ФВ ЛЖ в три раза выше, чем у пациентов с нормальным показателем ФВ, а выживаемость в течение первых пяти лет - на 1/3 меньше. Согласно результатам недавних исследований, госпитальная летальность после операции КШ у больных с ФВ ЛЖ менее 35% составляет от 1,7 до 6,9%, по данным разных авторов [13]. По нашим данным, госпитальная летальность в группе пациентов с изолированным КШ составила 5,1%.
Преимущества КШ, согласно мнению различных авторов, превышают хирургический риск [11]. Многие авторы указывают, что КШ приводит к повышению выживаемости среди пациентов с ИБС с дисфункцией ЛЖ [7]. После реваскуляризации миокарда отмечается снижение ФК ХСН и стенокардии у пациентов с исходно низкой ФВ ЛЖ [14]. Результаты данного исследования подтвердили, что ФК стенокардии и ФК ХСН достоверно снижается после КШ с тенденцией к возобновлению симптомов ХСН в отдаленном периоде.
C. Athanasuleas et al. [5] из группы RESTORE показали возможность выполнения реконструкции ЛЖ у пациентов с ишемической левожелудочковой дисфункцией и акинетичны-ми рубцами. Госпитальная летальность в группе с реконструкцией ЛЖ, по данным разных авторов, составляет от 5,3 до 9,4% [5, 10]. Анализ госпитальной летальности в настоящем исследовании показал, что реконструкция ЛЖ не увеличивает хирургический риск, госпитальная летальность составила 5,9%. Реконструкция ЛЖ с реваскуляризацией миокарда у больных ИБС, осложненной ХСН, направлены на улучшение геометрии и функции ЛЖ путем уменьшения миокардиального стресса в соответствии с законом Лапласа, что в конечном итоге ведет к улучшению систолической и диастолической функции ЛЖ [5]. Показатели объема ЛЖ влияют на развитие фатальных желудочковых аритмии [6], что может объяснить высокую годичную летальность (15%) в группе с изолированным КШ, во второй группе с реконструкцией ЛЖ летальность составила 7,5% за первый год после хирургического лечения. Концепция снижения напряжения стенки ЛЖ путем хирургического восстановления размера полости и геометрии ЛЖ остается ведущим принципом многих инновационных хирургических методов. В своих исследованиях ряд авторов показал, что в группе больных с реконструкцией ЛЖ в отличие от изолированного КШ более значительно увеличивается ФВ и уменьшаются объемные показатели ЛЖ (КДО, КСО), уменьшается ФК ХСН [4]. Наиболее выраженное снижение КДО, КСО ЛЖ, снижение ФК ХСН в нашем исследовании наблюдалось в группе с реконструкцией ЛЖ, нежели после изолированного КШ.
ВЫВОДЫ
Хирургическое лечение осложненных форм ИБС методом КШ изолированно или в сочетании с реконструкцией полости ЛЖ позволяет улучшить клиническое состояние, повысить отдаленную выживаемость больных с допустимым операционным риском. Несмотря на более агрессивную хирургическую тактику, риск операционной летальности (5,9%) при КШ с реконструкцией ЛЖ сопоставим с изолированным КШ (5,1%). Непосредственные и отдаленные результаты реконструкции ЛЖ в сочетании с реваскуляризацией миокарда свидетельствуют о более значимом увеличении ФВ ЛЖ, снижении объемных показателей ЛЖ и улучшении ФК ХСН.
Список литературы Клинико-функциональная оценка результатов коронарного шунтирования и реконструкции левого желудочка у больных ишемической болезнью сердца с выраженной левожелудочковой дисфункцией
- Беленков Ю.Н. // Русский медицинский журнал. 2000. Т. 8, № 17. С. 693.
- Бола С.Д., Кемпбелла Р.В.Ф., Френсиса Г.С. Международное руководство по сердечной недостаточности / Пер. с англ. М.,1995. 89 с.
- Саидова М.А. Возможности медикаментозного и хирургического восстановления сократимости жизнеспособного миокарда у больных ИБС и ДКМП с хронической недостаточностью кровообращения: автореф.... дис. д-ра мед. наук. М., 1999.
- Aguiar R., Antoniali F., Lopes M.M. et al. // J. Card. Fail. 2006. V. 12. P. 189-194.
- Athanasuleas C.L., Stanley A., Buckberg G.D. et al. //J. Am. Coll. Cardiol. 2001. V. 37. P. 1199.
- EDN: BDMHSX


