Клинико-экспериментальное обоснование применения биопластического материала "Экофлон" в реконструктивной хирургии гортани и трахеи
Автор: Инкина А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.15, 2020 года.
Бесплатный доступ
До настоящего времени остаются нерешенными вопросы восстановления опорного каркаса дыхательных путей при обширных дефектах их стенок в результате рубцового стеноза, продолжается поиск материалов, способных воссоздать утраченный хрящевой каркас гортани и трахеи. Цель исследования: клинико-экспериментальное обоснование использования имплантатов из пористого политетрафторэтилена в качестве материала для замещения дефектов гортани и трахеи в оториноларингологии. В эксперименте на 8 кроликах взамен резецированного участка ушного хряща имплантировали пластину из политетрафторэтилена. Динамическое наблюдение за послеоперационной областью в течение 3 месяцев завершалось гистологическим исследованием пластины в окружающих тканях. В клинической части исследования имплант заданной формы из политетрафторэтилена использовали при ушивании ларинготрахеального дефекта на завершающем этапе лечения у 12 больных с хроническими рубцовыми стенозами гортани и трахеи. Длительность послеоперационного наблюдения 3-12 месяцев, в течение которых проводили осмотр послеоперационной области, оценку дыхательной функции, а также эндоскопический осмотр гортани и трахеи. Выявлено, что при использовании биоимпланта из политетрафторэтилена происходит быстрое заживление раны, экссудативная фаза воспаления протекает невыраженно, перифокальный отек минимальный. Имплант надежно фиксируется к окружающим тканям прорастающей его соединительной тканью и не имеет тенденции к смещению, при этом не вызывает реакции со стороны окружающих его тканей. Клинический опыт использования импланта из политетрафторэтилена для замещения дефектов гортани и трахеи показал легкость их моделирования и последующей имплантации, способность выполнять опорную функцию, стабильность приданного положения за счет быстрой интеграции с окружающими тканями, а также отсутствие воспалительной реакции со стороны окружающих тканей. Биоимплант на основе политетрафторэтилена можно рекомендовать для восстановления каркасных свойств гортани и трахеи в лечении больных с хроническими рубцовыми стенозами гортани и трахеи.
Имплант, политетрафторэтилен, рубцовый стеноз гортани и трахеи
Короткий адрес: https://sciup.org/140260056
IDR: 140260056 | DOI: 10.25881/BPNMSC.2020.43.70.007
Clinical and experimental substantiation of the use of Ecoflon bioplastic material in reconstructive surgery of the larynxand trachea
The purpose of the study: clinical and experimental justification for the use of porous polytetrafluoroethylene implants as a material for the replacement of defects of the larynx and trachea in otorhinolaryngology. In an experiment on 8 rabbits, a polytetrafluoroethylene plate was implanted instead of the resected portion of the ear cartilage. Dynamic observation of the postoperative area for 3 months was completed by histological examination of the plate in the surrounding tissues. In the clinical part of the study, an implant of a given form made of polytetrafluoroethylene was used to suture a laryngotracheal defect at the final stage of treatment in 12 patients with chronic cicatricial stenosis of the larynx and trachea. The duration of postoperative follow-up was 3-12 months, during which the postoperative area was examined, respiratory function was assessed, as well as endoscopic examination of the larynx and trachea. It was revealed that when using a bioimplant from polytetrafluoroethylene, wounds heal quickly, the exudative phase of inflammation is not pronounced, and peripheral edema is minimal. The implant is firmly fixed to surrounding tissues by connective tissue sprouting it and has no tendency to displacement, while it does not cause a reaction from the surrounding tissues. Clinical experience with the use of an implant made of polytetrafluoroethylene to replace defects in the larynx and trachea showed the ease of their modeling and subsequent implantation, the ability to perform a support function, stability of the attached position due to rapid integration with surrounding tissues, and the absence of an inflammatory reaction from surrounding tissues. Bioimplant based on polytetrafluoroethylene can be recommended to restore the framework properties of the larynx and trachea in the treatment of patients with chronic cicatricial stenosis of the larynx and trachea.
Текст научной статьи Клинико-экспериментальное обоснование применения биопластического материала "Экофлон" в реконструктивной хирургии гортани и трахеи
При выполнении этапных реконструктивно-пластических операций (ЭРПО) у больных с хроническими рубцовыми стенозами гортани и трахеи на заключительном этапе производится пластическое закрытие стойкого ларинготрахеального дефекта [1; 2]. При площади стомы более 2 см2 возникает необходимость в использовании опорных материалов из-за нарушения каркасной функции дыхательной трубки [3; 4]. Это связано с тем, что при пластике обширных дефектов гортани и трахеи только местными тканями создаются условия для западения и патологической флотации вновь образованной передней стенки с сужением созданного просвета дыхательных путей [5]. Для пластического закрытия ларинготрахеального дефекта используются различные материалы: аутотканей, аллогенные и искусственные материалы в различных технических модификациях [6–11].
С середины XX в. применяются сетки на основе полипропилена [12]. Сегодня существуют десятки видов эндопротезов из полипропилена, которые различаются по размеру, форме ячеек, толщине волокна, пористости и другим свойствам. Все современные сетчатые протезы считаются инертными. Однако при изучении отдаленных результатов использования протезов из этого материала выявлено, что имплант не прорастает соединительной тканью, а между волокнами полимера и тканями реципиента сохраняется персистирующая воспалительная реакция [13].
Из многочисленных современных искусственных материалов, прошедших экспериментальную и клиническую апробацию, наиболее перспективными для имплантации были признаны полимеры, в том числе политетрафторэтилен (ПТФЭ) [14], который отличается биологической

Инкина А.В.
КЛИНИКО-ЭКСПЕРИМЕНТАЛЬНОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ БИОПЛАСТИЧЕСКОГО МАТЕРИАЛА «ЭКОФЛОН» В РЕКОНСТРУКТИВНОЙ ХИРУРГИИ ГОРТАНИ И ТРАХЕИ инертностью и устойчивостью к биодеструкции. Он обладает оптимальным соотношением пористости и механической прочности, уникальной химической инертностью, в нем отсутствуют сложноэфирные связи и углеродные соединения, он устойчив к биодеструкции [15]. Средний размер микропор в толще полимера равен 100–250 мкм. Одной из его разновидностей является пористый ПТФЭ. Российский синтетический материал «Экофлон» создан на основе ПТФЭ, имплантаты изготавливают путем порошкового спекания. В результате получается пористая структура, предполагающая возможность врастания как хряща, так и соединительнотканной капсулы внутрь имплантата. Протезы из него обладают доступностью, гибкостью, эластичностью, устойчивостью к изгибу и скручиванию. Материал был впервые применен в 2008 г. при торакоскопическом доступе для пластики обширных дефектов диафрагмы. В настоящий момент ПТФЭ имплантаты успешно используются в сердечно-сосудистой, абдоминальной и челюстно-лицевой хирургии, урологии, гинекологии, офтальмологии.
Область применения ПТФЭ в оториноларингологии до сих пор остается малоизученной. Перспективным направлением применения пористого ПТФЭ является замещение дефектов гортани и трахеи после этапных реконструктивных операций. Целью исследования явилось экспериментальное и клиническое обоснование возможности использования имплантатов из пористого ПТФЭ в качестве материала для замещения дефектов гортани и трахеи в оториноларингологии.
Задачи:
-
1. Оценить у экспериментальных животных возможность использования имплантатов из пористого ПТФЭ для замещения дефектов хрящевой ткани.
-
2. Изучить тканевую реакцию при использовании пористого ПТФЭ при замещении дефектов хряща у экспериментальных животных.
-
3. Разработать технику замещения дефектов гортани и трахеи имплантатами из ПТФЭ.
-
4. Провести анализ непосредственных и отдаленных результатов замещения дефектов гортани и трахеи имплантом из пористого ПТФЭ у пациентов на завершающем этапе реконструктивных операций.
Научная новизна : впервые выполнено экспериментальное исследование реакции окружающих тканей на имплантацию отечественного пористого ПТФЭ при замещении дефектов хряща у экспериментальных животных.
Выполнены гистологические исследования имплантатов из ПТФЭ у экспериментальных животных. При клиническом исследовании имплантатов из ПТФЭ для замещения дефектов хряща выявлена легкость их моделирования и имплантации, отсутствие миграции, инфицирования и отторжения.
Экспериментальная часть . Цель эксперимента: оценить использование имплантатов из пористого ПТФЭ («Экофлон») для замещения дефектов хрящевой ткани.
В эксперименте участвовали 8 кроликов. Животных погружали в сон с помощью внутривенного наркоза. Предварительно выбривали участок кожи наружной поверхности ушной раковины, затем проводили гидроотсепаровку мягких тканей от хряща с помощью 0,5% р-ра новокаина. Далее выкраивали языкообразный кожный лоскут под размер импланта (Рис. 1) и отсепаровывали его.
После выделения ушного хряща из него вырезали круглый фрагмент диаметром около 1,0 см (Рис. 2).
Биоматериал извлекали из упаковки, выкраивали стерильными ножницами аналогичный по размеру фрагмент. Материал легко режется, что позволяет дополнительно моделировать имплантат по ходу операции. Образовавшийся дефект хрящевой ткани закрывали смоделированным участком «Экофлона» точно под размер дефекта и фиксировали его двумя отдельными узловыми швами (Рис. 3). Затем кожный лоскут вновь возвращали на место и фиксировали к коже отдельными узловыми швами из капрона.
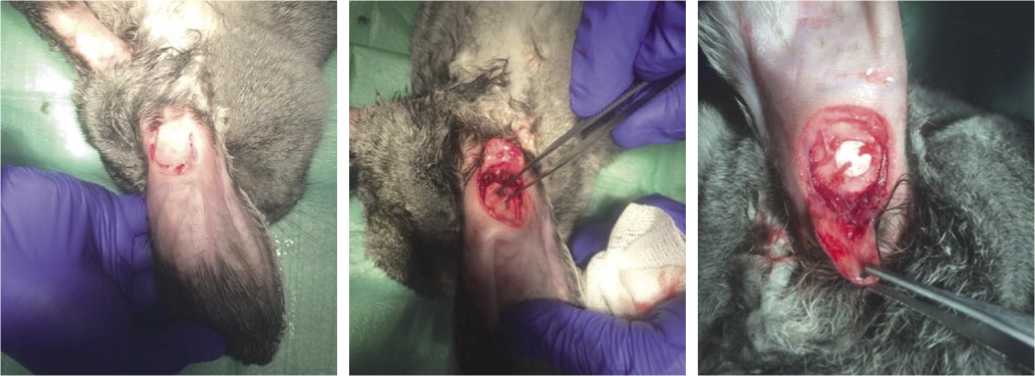
Рис. 2. Эксперимент. Вырезание фрагмента Рис. 3.
Рис. 1. Эксперимент. Выкраивание кожного лоскута.
хряща.
Эксперимент. Имплант фиксирован швами.
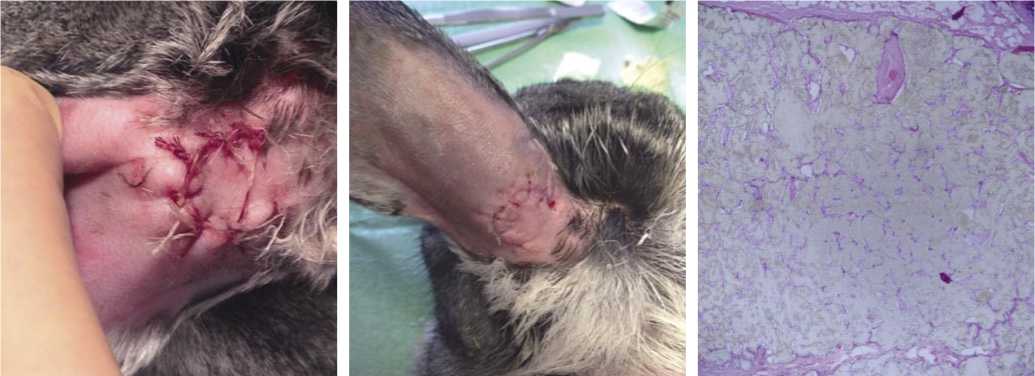
Рис. 5. Эксперимент. 10-е сутки после операции. Рис. 6. Эксперимент. Гистологический срез — материал импланта.
Рис. 4. Эксперимент. 1-е сутки после операции.
Оценивали заживление на 1, 3, 7 и 10 сутки после операции, а также через 1 и 2 месяца после хирургического вмешательства. Через 3 месяца проводили гистологическое исследование имплантированного материала.
Результаты эксперимента и их обсуждение
1-е сутки после операции: швы состоятельны, кожа несколько инфильтрирована (Рис. 4).
3-и сутки после операции: швы состоятельны, минимальные реактивные изменения, незначительное количество экссудата.
7-е сутки после операции: швы состоятельны, рана практически зажила первичным натяжением, реактивных изменений со стороны окружающих тканей нет.
10-е сутки после операции: рана зажила первичным натяжением, сняты швы (Рис. 5).
1 и 2 месяца после операции: имплант хорошо фиксирован в окружающих тканях, кожа в послеоперационной области не изменена, тонкий рубец. Таким образом, у всех животных рана зажила первичным натяжением, реакции окружающих тканей на имплант не было. В течение всего эксперимента инфицирования, миграция, отторжения пересаженного материала не было отмечены. Через 2 месяца после операции при осмотре выявлена хорошая фиксация импланта в тканях на прежнем месте, окружающий его хрящ без признаков воспаления.
Животных выводили из эксперимента через 3 месяца после операции. Забор материала для гистологического исследования был произведен посредством резекции уха кролика с имплантом путем проведения перпендикулярных поверхности кожи и длинной оси уха разрезов в зоне имплантации. Размеры фрагментов — 3-4 см х2-2,5 см х0,5 см. При макроскопическом осмотре попытки отделить ПТФЭ от окружающих тканей оказались безуспешными.
Материал фиксировали в 10% нейтральном растворе формалина. Далее гистологическая обработка образцов велась по стандартному протоколу с изготовлением парафиновых срезов толщиной 4 мкм и окрашиванием их гематоксилином и эозином. При гистологическом исследовании визуализировался материал имплантата, представленный комплексом прямоугольной формы с четкими границами, из волокнистого неокрашенного материала (Рис. 6).
По граням имплантата (перпендикулярной поверхности кожи), расположенным в непосредственной близости от хряща, в дерме выявлены фиброз, мелкоочаговые лимфогистиоцитарные инфильтраты, кальцификаты,. Кальцификаты аналогичного строения также обнаружены в гранях, расположенных параллельно поверхности кожи. По остальному периметру имплантатов в дерме воспалительная реакция, фиброз отсутствуют (Рис. 7).
Отмечается наличие тонких васкуляризованных соединительнотканных прослоек между волокнами имплантата, а также — артерии среднего калибра.
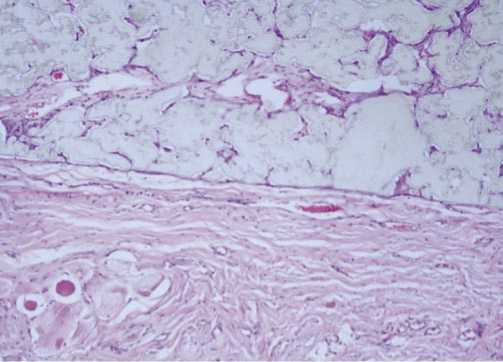
Рис. 7. Эксперимент. Гистологический срез. отсутствие в дерме воспалительной реакции, фиброза по периметру имплантата.
Инкина А.В.
КЛИНИКО-ЭКСПЕРИМЕНТАЛЬНОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ БИОПЛАСТИЧЕСКОГО МАТЕРИАЛА «ЭКОФЛОН» В РЕКОНСТРУКТИВНОЙ ХИРУРГИИ ГОРТАНИ И ТРАХЕИ
Таким образом, при гистологическом исследовании тканей, выявлено образование тонкой фиброзной капсулы вокруг импланта, с прорастанием сосудов между его волокнами. Воспалительная реакция окружающих тканей отсутствует.
Выводы : выявлено, что при использование биоимпланта «Экофлон» происходит быстрое заживление раны, экссудативная фаза воспаления протекает не выраженно, перифокальный отек минимальный. Имплант надежно фиксируется к окружающим тканям прорастающей его соединительной тканью и не имеет тенденции к смещению, при этом не вызывает реакции со стороны окружающих его тканей. Данный имплантат можно рекомендовать для возмещения объема утраченной хрящевой ткани.
Клиническая часть исследования
Положительные заключения токсиколого-гигиенических и санитарно-химических испытаний, тесты на стерильность и пирогенность изделий, проведенные во Всероссийском научно-исследовательском и испытательном институте медицинской техники (ВНИИИМТ) в соответствии с требованиями ГОСТ РИСО 10993 «Оценка биологического действия медицинских изделий», а также результаты собственных экспериментальных исследований позволили перейти к внедрению имплантатов «Экофлон» в медицинскую практику.
Пластина из пористого ПТФЭ имеет белый цвет, шероховатую поверхность, обладает выраженными гидрофобными свойствами, характеризуется легкостью обработки с помощью скальпеля, без труда прошивается хирургическими иглами. В сотрудничестве с инженерами НПК «Экофлон» изготовлены импланты заданной формы: шириной 7 мм; длиной 17 мм; толщиной 2,5 мм. Импланты были выполнены в форме арочной конструкции с учетом анатомических особенностей гортани и трахеи (Рис. 8).
Мы использовали имплант «Экофлон» для формирования утраченного хрящевого каркаса гортани и трахеи на завершающем этапе лечения больных с хроническими рубцовыми стенозами гортани и трахеи при частичном и полном ушивании ларинготрахеального дефекта. Пластина из ПТФЭ применялась для придания жесткости
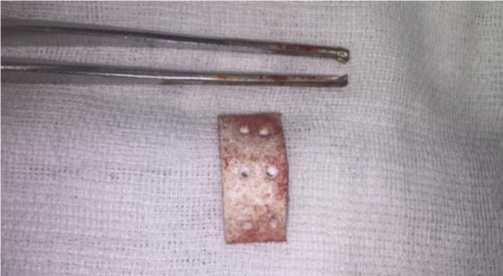
Рис. 8. Имплант арочной конструкции.
сформированной передней стенки дыхательного пути. Операции выполнены в МОНИКИ им. М.Ф. Владимирского. Перед операцией пациенты подписывали информированное согласие. Длительность послеоперационного наблюдения составила 3–12 месяцев. Контрольные осмотры включали в себя оценку субъективного состояния пациента, осмотр послеоперационной области, оценку дыхательной функции, а также эндоскопический осмотр гортани и трахеи. Дыхательная функция считалась компенсированной при отсутствии одышки, выполнении дозированной физической нагрузки (10 приседаний за 20 с) без проявлений стенотического дыхания при возвращении частоты дыхания к исходным показателям в течение первой минуты.
Результаты клинических исследований и их обсуждение
Всего в нашей клинике выполнено 12 операций по ушиванию ларинготрахеального дефекта с пластикой передней стенки гортани и трахеи имплантом «Экофлон». Группу пациентов составили 8 мужчин и 4 женщины в возрасте от 18–42 лет.
Моделирование пластины легко выполняли с помощью ножниц и скальпеля. Благодаря шероховатой поверхности имплант имел определенное сцепление с окружающими тканями, что способствовало надежной фиксации пластины в окружающих тканях.
При ушивании обширного ларинготрахеального дефекта — шириной более 1,5 см необходимо восстановить каркасность вновь сформированной передней стенки. С этой целью в начале операции выполняли разрез кожи, окаймляющий ларинготрахеальный дефект, отступя от его края не менее 0,7 см. Края образовавшего внутреннего кожного лоскута отсепаровывали, поворачивали эпидермисом внутрь и ушивали отдельными швами. Образованную таким образом переднюю стенку дыхательного пути укрепляли имплантом «Экофлон», который при необходимости обрезали до нужных размеров, перфорировали и фиксировали к оставшимся боковым стенка гортани и трахеи отдельным узловыми швами. В последующем закрывали имплант мышечным или мышечно-фасциальным лоскутом на ножке и проводили пластику дефекта кожи местным тканями.
У всех пациентов рана зажила первичным натяжением, послеоперационный период проходил гладко, без выраженных проявлений экссудации и воспаления. На протяжении всего исследования инфицирования, миграции, обнажения или отторжение имплантированного материала отмечены не были. Через 3 месяца и 1 год динамического наблюдения имплант был надежно фиксирован в нужном положении, воспалительной реакции окружающих тканей не отмечено. При эндоскопическом осмотре гортани и трахеи просвет дыхательных путей оставался достаточно широким, не было зафиксировано обнажения стенки импланта или флотации вновь созданной передней стенки дыхательных путей. Все пациенты имели компенсированное дыхание.

Таким образом, клинический опыт использования пластин из пористого ПТФЭ для замещения дефектов гортани и трахеи показал легкость их моделирования и последующей имплантации, способность выполнять опорную функцию, стабильность приданного положения за счет быстрой интеграции с окружающими тканями, а также отсутствие воспалительной реакции со стороны окружающих тканей.
Выводы:
-
1. Благодаря своим химическим и физико-механическим свойствам имплант из ПТФЭ создает благоприятные условия для врастания соединительной ткани в его поры, в результате чего происходит его прочное сращение с окружающими анатомическими структурами.
-
2. Имплант из пористого ПТФЭ надежно выполняет опорную функцию взамен утраченных хрящевых структур.
-
3. При практическом использовании имплантатов из ПТФЭ можно отметить легкость их моделирования, простоту имплантации, устойчивость к инфекции, отсутствие миграции и отторжения, что выгодно отличает его от других искусственных материалов при выполнении пластических операций.
-
4. Эластичность, возможность изготовления из пористого ПТФЭ имплантов заданной формы, способность к моделированию и быстрая интеграция с окружающими тканями позволяют рекомендовать использование имплантов «Экофлон» для пластики передней стенки гортани и трахеи.
Автор заявляет об отсутствии конфликта интересов (The author declare no conflict of interest).
364 р. (In Russ).]
157 р. (In Russ).]
Список литературы Клинико-экспериментальное обоснование применения биопластического материала "Экофлон" в реконструктивной хирургии гортани и трахеи
- Зенгер В.Г., Наседкин А.Н. Повреждения гортани и трахеи. — М.: Медицина, 1991. 240 с. [Zenger VG, Nasedkin AN. Povrezhdeniya gortani i trahei. M.: Medicina; 1991. 240 р. (In Russ).]
- Юнина А.И. Травмы органов шеи и их осложнения. — М.: Медицина, 1972. 208 с. [YUnina AI. Travmy organov shei i ih oslozhneniya. M.: Medicina; 1972. 208 р. (In Russ).]
- Зенгер В.Г., Наседкин А.Н., Паршин В.Д. Хирургия повреждений гортани и трахеи. — М.: Медкнига, 2007. 364 с. [Zenger VG, Nasedkin AN, Parshin VD. Hirurgiya povrezhdenij gortani i trahei. M.: Medkniga; 2007. 364 р. (In Russ).]
- Sautter NV, Krakovitz PR, Solares CA, Koltai PJ. Closure of persistent trac-heocutaneous fistula following «starplasty» tracheostomy in children // Int. Pediatr Otorhinolaryngol. 2006; 70(1): 99-105.
- Татур А.А., Леонович С.И., Чайковский В.В. и др. Пластика дефектов передней и боковых стенок трахеи // Медицинская панорама. — 2008. — №10. — С. 14—17. [Tatur AA, Leonovich SI, CHajkovskij VV, et al. Plastika defektov perednej i bokovyh stenok trahei. Medicinskaya panorama. 2008; (10):14-17. (In Russ).]
- Решульский С.С., Клочихин А.Л., Виноградов В.В. Пластика гортани и трахеи при стенозах / Сборник материалов Национального конгресса «Пластическая хирургия». М.: Бионика, 2011. С. 95. [Reshul'skij SS, Klochihin AL, Vinogradov VV. Plastika gortani i trahei pri stenozah / Sbo-rnik materialov Nacional'nogo kongressa «Plasticheskaya hirurgiya». M.: Bionika; 2011. Р. 95. (In Russ).]
- Хачак А.Х., Абаев В.К. и др. Применение конструкций из пористого нике-лида титана на этапах ларинготрахеопластики / Материалы XVIII съезда оториноларингологов России. М.: Регистр, 2011. Т. 3. С. 410-412. [Ha-chak AH., Abaev VK, et al. Primenenie konstrukcij iz poristogo nikelida titana na etapah laringotraheoplastiki / Materialy XVIII s"ezda otorinolaringologov Rossii. M.: Registr; 2011. T. 3. рр. 410-412. (In Russ).]
- Горбунов В.А., Вахмянин А.П., Викторова Т.И. и др. Новые материалы в реконструктивной ларинготрахеопластике / 16-й съезд оториноларингологов России: тезисы докладов. Минск, 2000. С. 464-466. [Gorbunov VA, Vahmyanin AP, Viktorova TI, et al. Novye materialy v rekonstruktivnoj laringotraheoplastike / 16 s"ezd otorinolaringologov Rossii: tezisy doklad-ov. Minsk; 2000. Р. 464-466. (In Russ).]
- Grillo H.C. Surgery of the Trachea and Bronchi. BC Decker Inc. Hamilton-London. 2004. 882 p.
- De Jong AL, Park AH, Raveh E. et al. Comparsion of thyroid, auricular, and costal cartilage donor sites for laryngotracheal reconstruction in an animal model. Arch. Otolaryngol. Head Neck Surg. 2000; 126(1): 49-53.
- Амиров Ф.Ф., Фурманов А.Ю., Симонов А.А. Аллопластика трахеи и бронхов (экспериментальное исследование). Ташкент: Медицина, 1973. 157 с. [Amirov FF, Furmanov AYU, Simonov AA. Alloplastika trahei i bronhov (eksperimental'noe issledovanie). Tashkent: Medicina; 1973. 157 р. (In Russ).]
- Ягудин Р.К., Ягудин К.Ф. Отдаленные результаты применения полипропиленовой сетки для пластики обширных ларинготрахеостом//Вестник оториноларингологии. 2016. №1. С. 67-69. [YAgudin RK, YAgudin KF. Otdalennye rezul'taty primeneniya polipropilenovoj setki dlya plastiki ob-shirnyh laringotraheostom. Vestnik otorinolaringologii. 2016; (1): 67-69. (In Russ).]
- Klinge U. et al. Foreign body reaction to mesh used for repair of abdominal wall hernias. Eur. J. Surg. 1999; 165(7): 665-673.
- Scierski W., Lisowska G., Namyslowski G., Misiolek M., Pilch J., Menaszek E., Gawlik R., Blahewicz M. Reconstruction of Ovine Trachea with a Bio-mimetic Composite Biomaterial. BioMed Research International. Volume 2018, Article ID 2610637, p. 9. doi: 10.1155/2018/2610637.
- Розанова И. Б. Биодеструкция имплантатов. В кн.: Биосовместимость. — М., 1999. — С. 212-245. [Rozanova IB. Biodestrukciya implantatov. In.: Biosovmestimost'. M.; 1999. Р. 212-245. (In Russ).]


