Клипирование створок митрального клапана у пациентов с ранее имплантированными устройствами для коррекции сердечной недостаточности
Автор: Карамова Я.Ш., Имаев Т.Э., Ускач Т.М., Терещенко С.Н.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2024 года.
Бесплатный доступ
Введение. Современные клинические рекомендации по сердечной недостаточности рассматривают комплексный подход в лечении с использованием имплантации различных устройств (кардиоресинхронизирующая терапия (CRT), имплантация кардиовертера-дефибриллятора (ИКД), установка электрокардиостимуляторов (ЭКС)), а также коррекцию клапанных пороков. Так, для лечения тяжелой недостаточности митрального клапана применяется методика клипирования его створок с помощью системы MitraClip.
Митральная регургитация, хроническая сердечная недостаточность, пластика митрального клапана, имплантируемые устройства
Короткий адрес: https://sciup.org/143183346
IDR: 143183346 | УДК: 616-089 | DOI: 10.38109/2225-1685-2024-3-28-34
Mitral valve leaflet clipping in patients with previously implanted heart failure devices
Introduction. Modern clinical guidelines for heart failure consider a comprehensive approach to treatment using implantation of various devices (cardiac resynchronisation therapy CRT, implantation of cardioverter-defibrillator (ICD), installation of pacemakers (ECS) as well as correction of valve defects. For example, for treatment of severe mitral valve insufficiency the technique of clipping its flaps using MitraClip system is used.
Текст научной статьи Клипирование створок митрального клапана у пациентов с ранее имплантированными устройствами для коррекции сердечной недостаточности
Данная статья распространяется на условиях «открытого доступа», в соответствии с лицензией CC BY-NC-SA 4.0 («Attribution-NonCommercial-ShareAlike»/ «Атрибуция-Не-коммерчески-СохранениеУсловий» 4.0), которая разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии указания автора и источника. Чтобы ознакомиться с полными условиями данной лицензии на русском языке, посетите сайт: by-nc-sa/4.0/
This is an open access article distributed under the terms of the Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International (CC BY-NC-SA 4.0) License , which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Появление новых лекарственных препаратов в составе оптимальной медикаментозной терапии (ОМТ) хронической сердечной недостаточности (ХСН) способствует кардинальному улучшению течения заболевания. Тем не менее у отдельных групп пациентов, к которым относятся больные с развитием клапанных пороков, ОМТ не способна в полной мере решить проблему высокой смертности и низкого качества жизни. В современном алгоритме лечения ХСН значимое место занимает коррекция митральной регургитации [1].
Митральная регургитация (МР) – достаточно распространенное осложнение сердечной недостаточности (СН) и бывает первичной (ПМР) и вторичной (ВМР). ПМР чаще всего возникает либо вследствие дисфункции створок митрального клапана (фиброэластический дефицит, болезнь Барлоу), либо вследствие иных причин, таких как отрыв хорд или сосочковых мышц [2]. Однако у пациентов с ХСН чаще всего развивается ВМР, частота которого напрямую зависит от возраста пациентов, а также от длительности течения ХСН и степени поражения сердечной мышцы [3]. Длительно существующая МР отрицательно влияет на процессы ремоделирования миокарда вследствие вовлечения в этот процесс левого желудочка (ЛЖ) и расширения левого предсердия, ухудшения сократительной способности ЛЖ и возникновения миокардиального фиброза в результате длительной перегрузки объемом [4].
Около трети пациентов с ХСН страдают блокадой левой ножки пучка Гиса (БЛНПГ). Примерно у трети пациентов с показаниями к кардиоресинхронизирующей терапии (CRT) наблюдается вторичная митральная регургитация (ВМР) от умеренной до тяжелой степени. Она может возникать либо вследствие систолической дисфункции, либо из-за диссинхронии. Согласно рекомендациям Европейского общества кардиологов по клапанным порокам, коррекция МР и сердечной диссинхронии являются основными терапевтическими подходами у таких пациентов [5]. Количество пациентов с ХСН и имплантированными устройствами во всем мире растет. С увеличением продолжительности жизни все большему числу таких пациентов требуется проведение хирургических вмешательств, в том числе и коррекция МР [6]. Актуальным является вопрос возможности и безопасности клипирования створок митрального клапана пациентам с устройствами.
В связи с этим целью данной работы явилась оценка влияния вмешательства на митральном клапане с помощью клипирования створок на течение ХСН у пациентов с имплантированными устройствами.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включено 73 пациента с умеренно-тяжелой и тяжелой степенью МР, которым была выполнена имплантация системы MitraClip (Abbott, США) на створки митрального клапана на базе ФГБУ «НМИЦК им. ак. Е.И. Чазова» Минздрава России.
Показанием для имплантации системы служили МР 3-4 степени и наличие клинически выраженной ХСН с фракцией выброса левого желудочка (ФВЛЖ) >20%. После оперативного вмешательства пациенты наблюдались в течение шести месяцев. Для определения процессов ремоделирования миокарда оценивалась динамика показателей ЭхоКГ и толерантность к физической нагрузке.
Среди пациентов с показаниями для коррекции МР была выделена группа больных, которым ранее были имплантированы устройства по различным показаниям. Пациентам ранее были установлены ЭКС, ИКД, CRT. Из 18 пациентов с имплантированными устройствами 6 имели ЭКС, 7 пациентам были имплантированы ИКД и 5 пациентам – CRT (рис. 1).
55 пациентов без ранее имплантированных устройств
73 пациента с MitraClip
18 пациентов с ранее имплантированными устройствами
6 пациентов 7 пациентов 5 пациентов с ЭКС с ИКД с CRT
Рисунок 1. Пациенты, включенные в исследование [составлено авторами]
-
Figure 1. Patients included in the study [compiled by the authors]
Оперативные вмешательства были выполнены в условиях гибридной рентген-операционной и проходили под контролем чреспищеводной ЭхоКГ и рентгеноскопии. ЭхоКГ проводилась на аппарате экспертного уровня Vivid E9, (GE, Норвегия) исходно и через 6 месяцев наблюдения.
Статистическая обработка полученных результатов включала методы двухсторонний F-критерий Фишера, U-критерий Манна-Уитни. Выборочные параметры, представлены в виде Me [Lq; Uq], где Me – медиана, Lq; Uq – межквартильный интервал. За минимальный уровень значимости принято p<0,05. Анализ статистики данных производился с помощью программ: Excel 2016 (Microsoft, США), статистической программы IBM SPSS Statistics 26.0 (StatSoft Inc., США). Качественные величины представлены как абсолютные значения и проценты.
Исследование было одобрено комитетом по этике при ФГБУ «НМИЦК им. ак. Е. И. Чазова» Минздрава России, протокол №273 заседания Комитета от 22 ноября 2021 года.
РЕЗУЛЬТАТЫ
В ходе наблюдения проводилось сравнение клинических, инструментальных и лабораторных показателей группы пациентов с имплантированными ранее устройствами (группа А) и группы, включившей в себя остальных пациентов (группа В). Исходная характеристика групп представлена в таблице 1.
Таблица 1. Исходная клинико-демографическая характеристика пациентов [составлено авторами]
Table 1. Initial clinical and demographic characteristics of patients [compiled by the authors]
|
Показатель |
Группа А (n=18) |
Группа В (n=55) |
р |
|
Возраст, лет |
70,5±10,95 |
71,1±9,73 |
0,7 |
|
Мужчины, % |
69 |
57 |
0,2 |
|
ФК ХСН (NYHA) II/III/IV, % |
38,9/61,1/0 |
30,9/65,5/3,6 |
1/0,9/0,4 |
|
ХСНнФВ/ХСНун/ХСНсФВ, % |
38,9/16,7/44,4 |
34,5/25,5/60 |
0,4/0,7/0,4 |
|
ПМР/ВМР, % |
27,8/72,2 |
54,5/45,5 |
0,05/0,05 |
|
ИБС, % |
77,8 |
72,7 |
0,7 |
|
ФП, % |
88,9 |
63,6 |
0,04 |
|
МР 3/4, % |
41,7/58,4 |
30,9/69,1 |
0,6/0,2 |
Примечание/Note: ФК – функциональный класс (FC – functional class), ХСН – хроническая сердечная недостаточность (CHF – chronic heart failure), ПМР – первичная митральная регургитация (PMR – primary mitral regurgitation), ВМР – вторичная митральная регургитация (SMR – secondary mitral regurgitation), ИБС – ишемическая болезнь сердца (IHD – ischemic heart disease), ФП – фибрилляция предсердий (AF – atrial fibrillation), МР – митральная регургитация (MR – mitral regurgitation), нФВ – нормальная фракция выброса (nEF – normal ejection fraction), унФВ – умеренно-низкая фракция выброса (mEF – moderate-low ejection fraction), сФВ – сниженная фракция выброса (rEF – reduced ejection fraction)
При анализе исходных клинико-демографических характеристик обращает на себя внимание, что в группе пациентов с имплантированными ранее устройствами было больше случаев развития первичной МР, процент пациентов с наличием фибрилляции предсердий в анамнезе был выше, чем в группе без имплантированных устройств (р=0,04). В остальном характеристики, показанные в таблице 1, не имеют значимых отличий.
На момент включения в исследование все пациенты получали медикаментозную терапию ХСН в максимально возможных дозировках как минимум в течение 3 месяцев (табл. 2).
По ЭхоКГ параметрам до включения в исследование не наблюдалось значимых различий между группами (табл. 3).
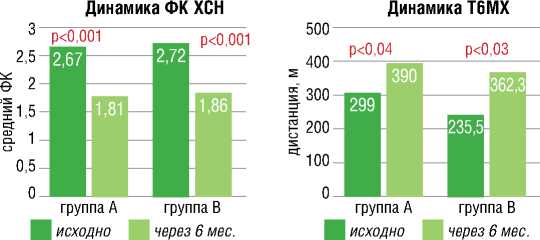
В течение полугода наблюдения получено значительное улучшение клинического течения ХСН в обеих группах. Средний функ- циональный класс (ФК) ХСН снизился в группе А с 2,67±0,8 до 1,81±0,7 (р<0,001) и в группе В с 2,72±1,97 (р<0,001) до 1,86±0,6, толерантность к физической нагрузке значительно увеличилась (средние значения дистанции теста с 6-минутной ходьбой (Т6МХ) повысились с 299 [178; 340] м до 390 [231,3; 420] м и 235,5 [182,8; 370,3] (р=0,04) м до 362,3 [270; 412.7] м (р=0,03) соответственно (рис. 2). В динамике наблюдалось снижение потребности в диуретической терапии в пересчете на фуросемид, однако в группе А снижение дозы диуретиков не достигло статистической значимости (группа А с 56,7±27,7 мг до 35±17,3 мг, р=0,07, группа В – с 39,4±18,8 мг до 26,7±15,3 мг, р=0,04 (рис. 3). Однако при оценке динамики NT-proBNP значимой динамики зарегистрировано не было (с 1042,5 [856,1; 3195,8] до 1395 [278,6; 1875], р=0,6 vs с 1386 [689,3; 3333] до 1001 [462,6; 2106], р=0,5).
Динамика диуретической терапии
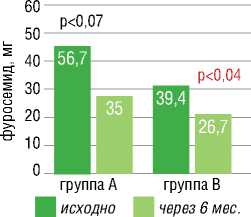
Рисунок 3. Показатели диуретической терапии в динамике [составлено авторами]
Figure 3. Diuretic therapy indicators in dynamics [compiled by the authors]
Рисунок 2. Показатели ФК и Т6МХ в динамике [составлено авторами]
-
Figure 2. FC and T6MW indicators in dynamics [compiled by the authors]
Таблица 2. Медикаментозная терапия пациентов при включении в исследование [составлено авторами]
|
Table 2. Drug therapy of patients at inclusion in the study [compiled by the authors] |
|||
|
Препарат |
Группа А, n=18 |
Группа В, n=55 |
р^^м |
|
ИАПФ/АРНИ/БРА, % |
38,9/44,4/16,7 |
34,5/30,8/29,1 |
0,7/0,3/0,3 |
|
Бета-блокаторы, % |
92,1 |
93,6 |
0,4 |
|
АМКР, % |
83,3 |
85,5 |
0,9 |
|
иНГЛТ2, % |
43,9 |
49,4 |
0,1 |
|
Диуретики, % |
100 |
89,5 |
0,1 |
|
Примечание/Note: иАПФ – ингибиторы ангиотензинпревращющего фермента (ACE – angiotensin-converting enzyme inhibitors), АРНИ – ангиотензиновых рецепторов и неприлизина ингибитор (ARNI – angiotensin receptor and niprilysin inhibitor), АМКР – антагонисты минералкортикоидных рецепторов (MRA – mineralocorticoid receptor antagonists), иНГЛТ2 – ингибиторы натрий-глюкозного котранспортера 2 (SGLT2 – sodium-glucose cotransporter 2 inhibitors) |
|||
|
Таблица 3. Исходные ЭхоКГ характеристики пациентов [составлено авторами] |
|||
|
Table 3. Baseline echocardiographic characteristics of patients [compiled by the authors] |
|||
|
Показатель |
Группа А, n=18 |
Группа В, n=55 |
■p^^м |
|
Размер ЛП, см |
5,0 [4,5; 5,7] |
4,8 [4,5; 5,2] |
0,1 |
|
КДР ЛЖ, см |
6,0 [5,8; 6,4] |
6 [5,6; 6,5] |
0,1 |
|
КСР ЛЖ, см |
4,4 [3,6; 5,1] |
4,5 [3,9; 5,3] |
0,4 |
|
Объем ЛП, мл |
144 [104,5; 195] |
127 [106; 154] |
0,2 |
|
КДО ЛЖ, мл |
168 [125; 211,3] |
156 [115; 218] |
0,7 |
|
КСО ЛЖ, мл |
88 [48; 135] |
74 [55,3; 130] |
0,3 |
|
ФВ ЛЖ, % |
44,5 [33,8; 59,3] |
47 [38; 60] |
0,3 |
|
УО, мл |
44 [37; 63] |
57,5 [48,8; 65,3] |
0,08 |
|
СВ, л/мин |
3,5 [2,6; 4,8] |
4 [3,3; 4,8] |
0,7 |
|
СДЛА, мм рт. ст. |
44 [35; 62,5] |
45 [36,5; 59,3] |
0,8 |
Примечание/Note: ЛП – левое предсердие (LA – left atrium), ЛЖ – левый желудочек (LV – left ventricle), КДР – конечнодиастолический размер (EDD – end-diastolic dimension), КСР – конечно-систолический размер (ESR – end-systolic dimension), КДО ЛЖ – конечно-диастолический объем левого желудочка (EDV – end-diastolic volume), КСО ЛЖ – конечно-систолический объем левого желудочка (ESV – end-systolic volume), ФВ ЛЖ – фракция выброса (EF – ejection fraction), УО – ударный объем (SV – stroke volume), СВ – сердечный выброс (CO – cardiac output), СДЛА – систолическое давление легочной артерии (PASP – pulmonary artery systolic pressure)
В таблицах 4 и 5 представлена динамика ЭхоКГ показателей обеих групп. Выявлено, что у пациентов группы B клипирование створок митрального клапана оказало большее положительное влияние.
В группе пациентов, которым до клипирования створок ми-триального клапана имплантировались устройства, в отличие от остальных пациентов, значимая динамика наблюдалась в увеличении УО (р=0,03) и снижении СДЛА (р=0,02), в остальном значимого улучшения показателей не зарегистрировано, однако прослеживалась тенденция к снижению.
Нами проведено сравнение ЭхоКГ показателей двух групп пациентов. Результаты показаны в таблице 6.
|
Таблица 4. Динамика показателей ЭхоКГ в группе с имплантированными ранее устройствами (А), n=18 [составлено авторами] |
|||
|
Table 4. Dynamics of EchoCG parameters in the group with previously implanted devices (A), n=18 [compiled by the authors] |
|||
|
Показатель |
Исходные данные |
Через 6 мес. после вмешательства |
р |
|
Размер ЛП, см |
5,0 [4,5; 5,7] |
5,0 [4,6; 5,4] |
0,2 |
|
КДР ЛЖ, см |
6,0 [5,8; 6,4] |
5,9 [5,2 6,9] |
0,2 |
|
КСР ЛЖ, см |
4,4 [3,6; 5,1] |
4,45 [3,7; 5,6] |
0,2 |
|
Объем ЛП, мл |
144 [104,5; 195] |
140 [101,8; 190] |
0,5 |
|
КДО, мл |
168 [125; 211,3] |
137 [105,8; 240,3] |
0,2 |
|
КСО, мл |
88 [48; 135] |
70 [54; 149,3] |
0,4 |
|
ФВ ЛЖ, % |
44,5 [33,8; 59,3] |
43,5 [36,8; 50,5] |
0,7 |
|
УО, мл |
44 [37; 63] |
58,5 [49,5; 84,3] |
0,03 |
|
СВ, л/мин |
3,5 [2,6; 4,8] |
4,3 [3,3; 5,6] |
0,3 |
|
СДЛА, мм рт. ст. |
44 [35; 62,5] |
39 [29,8; 45] |
0,02 |
Примечание/Note: ЛП – левое предсердие (LA – left atrium), ЛЖ – левый желудочек (LV – left ventricle), КДР – конечно-диастолический размер (EDD – end-diastolic dimension), КСР – конечно-систолический размер (ESR – end-systolic dimension), КДО – конечнодиастолический объем (EDV – end-diastolic volume), КСО – конечно-систолический объем (ESV – end-systolic volume), ФВ – фракция выброса (EF – ejection fraction), УО – ударный объем (SV – stroke volume), СВ – сердечный выброс (CO – cardiac output), СДЛА – систолическое давление легочной артерии (PASP – pulmonary artery systolic pressure)
Таблица 5. Динамика показателей ЭхоКГ у пациентов без имплантированных ранее устройств (В), n=55 [составлено авторами]
Table 5. Dynamics of EchoCG parameters in the group with previously implanted devices (B), n=55 [compiled by the authors]
|
Показатель |
Исходные данные |
Через 6 мес. после вмешательства |
■1 р ^^м |
|
Размер ЛП, см |
4,8 [4,5; 5,2] |
4,6 [4,4; 5,1] |
0,02 |
|
КДР ЛЖ, см |
6 [5,6; 6,5] |
5,5 [5,0; 6,3] |
0,04 |
|
КСР ЛЖ, см |
4,5 [3,9; 5,3] |
4,2 [3,3; 5,1] |
0,02 |
|
Объем ЛП, мл |
127 [106; 154] |
111 [88,5; 152,3] |
0,03 |
|
КДО, мл |
156 [115; 218] |
130 [108; 193] |
0,01 |
|
КСО, мл |
74 [55,3; 130] |
75 [41; 130] |
0,09 |
|
ФВ ЛЖ, % |
47 [38; 60] |
44 [39,5; 58,5] |
0,5 |
|
УО, мл |
57,5 [48,8; 65,3] |
61 [52; 74,5] |
0,03 |
|
СВ, л/мин |
4 [3,3; 4,8] |
4,5 [3,6; 5,3] |
0,04 |
|
СДЛА, мм.рт.ст |
45 [36,5; 59,3] |
32 [27,3; 43,5] |
0,001 |
Примечание/Note: ЛП – левое предсердие (LA – left atrium), ЛЖ – левый желудочек (LV – left ventricle), КДР – конечно-диастолический размер (EDD – end-diastolic dimension), КСР – конечно-систолический размер (ESR – end-systolic dimension), КДО – конечнодиастолический объем (EDV – end-diastolic volume), КСО – конечно-систолический объем (ESV – end-systolic volume), ФВ – фракция выброса (EF – ejection fraction), УО – ударный объем (SV – stroke volume), СВ – сердечный выброс (CO – cardiac output), СДЛА – систолическое давление легочной артерии (PASP – pulmonary artery systolic pressure)
|
Таблица 6. Показатели ЭхоКГ через 6 месяцев наблюдения в группах [составлено авторами] Table 6: EchoCG parameters after 6 months of follow-up in the groups [compiled by the authors] |
|||
|
Показатель |
Пациенты с ранее имплантированными устройствами (n=18) |
Пациенты без имплантированных ранее устройств (n=55) |
р |
|
Размер ЛП, см |
5 [4,6; 5,4] |
4,6 [4,4; 5,1] |
0,6 |
|
КДР ЛЖ, см |
5,9 [5,2; 6,8] |
5,5 [5,0; 6,3] |
0,2 |
|
КСР ЛЖ, см |
4,5 [3,7; 5,6] |
4,2 [3,3; 5,1] |
0,4 |
|
Объем ЛП, мл |
140 [99,25; 180] |
111 [88,5; 152,3] |
0,6 |
|
КДО, мл |
137 [95,3; 246,8] |
130 [108; 193] |
0,2 |
|
КСО, мл |
67,5 [50; 148,8] |
75 [41; 130] |
0,2 |
|
ФВ ЛЖ, % |
44 [36,5; 51,5] |
44 [39,5; 58,5] |
0,5 |
|
УО, мл |
60 [51,5; 84,8] |
61 [52; 74,5] |
0,07 |
|
СВ, л/мин |
4,3 [3,4; 6,1] |
4,5 [3,6; 5,3] |
0,1 |
|
СДЛА, мм рт. ст. |
40 [35,5; 45] |
32 [27,3; 43,5] |
0,8 |
Примечание/Note: ЛП – левое предсердие (LA – left atrium), ЛЖ – левый желудочек (LV – left ventricle), КДР – конечно-диастолический размер (EDD – end-diastolic dimension), КСР – конечно-систолический размер (ESR – end-systolic dimension), КДО – конечнодиастолический объем (EDV – end-diastolic volume), КСО – конечно-систолический объем (ESV – end-systolic volume), ФВ – фракция выброса (EF – ejection fraction), УО – ударный объем (SV – stroke volume), СВ – сердечный выброс (CO – cardiac output), СДЛА – систолическое давление легочной артерии (PASP – pulmonary artery systolic pressure)
Таким образом, при анализе данных обеих групп (пациентов с ранее имплантированными устройствами и без них) различий в ЭхоКГ показателях через 6 месяцев наблюдения не получено.
В течение 6 месяцев скончались 4 пациента (2 в группе А и 2 в группе В).
Клинический пример
Пациент Л. 76 лет, в анамнезе ишемическая болезнь сердца: постинфарктный кардиосклероз (инфаркт миокарда нижней локализации от 1992 г., 2012 г.), множественные чрескожные коронарные вмешательства. В феврале 2019 года отметил появление одышки при физической нагрузке, снижение толерантности к физическим нагрузкам, появление отеков ног. Был госпитализирован в ФГБУ «НМИЦК им. ак. Е. И. Чазова» Минздрава России в связи декомпенсацией ХСН по обоим кругам кровообращения. Тогда же впервые был диагностирован тахи-систолический вариант фибрилляции предсердий. По данным ЭхоКГ отмечено снижение ФВ до 30%, гипокинез всех сегментов боковой, задней и нижней стенок, митральная регургитация 3-4 степени, трикуспидальная регургитация 1-2 степени, значительная легочная гипертензия. В декабре 2021 года пациенту имплантирован КВД. В июне 2022 г. произошло срабатывание КВД (пароксизм желудочковой тахикардии), повторное срабатывание произошло через 2 недели. В августе 2022 г. проведена радиочастотная аблация аритмогенных зон нижней стенки левого желудочка и межжелудочковой перегородки. Однако 02.10.2022 г. вновь отмечал срабатывание КВД. В октябре 2022 г. находился на лечении в НМИЦК в связи с декомпенсацией ХСН. Учитывая наличие тяжелой функциональной митральной регургитации, решено выполнить транскатетерную пластику митрального клапана с имплантацией устройства MitraClip, которая была проведена в октябре 2022 года. Оперативное вмешательство прошло успешно. Через 6 месяцев наблюдения госпитализаций по поводу декомпенсаций не было. Повторных срабатываний КВД за 6 мес. не зарегистрировано, по результатам интеррогирования КВД желудочковых нарушений ритма не выявлено. Дозировка диуретиков в перерасчете на фуросемид снизилась с 40 мг до 20 мг, ФК ХСН уменьшился с 3 до 2, уровень NT-proBNP без динамики (1351 пг/мл – 1160 пг/мл). В таблице 7 указана динамика показателей ЭхоКГ за 6 месяцев наблюдения.
На рисунке 4 показан интраоперационный снимок, на котором отчетливо видны электроды от ИКД, система доставки клипсы и непосредственно сами клипсы. Данный пример демонстрирует клиническое улучшение течения ХСН и положительную динамику ЭхоКГ показателей у пациента с имлантиро-ванным ранее ИКД.
ОБСУЖДЕНИЕ
В проведенном сравнении результатов наблюдения пациентов после коррекции митральной регургитации с помощью системы клипирования створок митрального клапана в зависимости от наличия имплантированных ранее устройств получены данные об улучшении течения ХСН в виде увеличения дистанции Т6МХ, уменьшения ФК и повышения качества жизни, а также положительная динамика ЭхоКГ показателей. В литературных источниках у пациентов с имплантированными устройствами изучалась в основном выживаемость [7,8], изменения которой при наличии имплантированных ранее устройств получено не было. В проведенном нами исследовании оценить влияние имплантированных ранее устройств на прогноз не представляется возможным в виду небольшого количества летальных исходов.
В нашей работе среди пациентов с показаниями к коррекции МР больных с имплантированными ранее устройствами оказалось чуть более 20%. В наиболее значимом исследовании коррекции МР с помощью клипирования створок (COAPT), при отдельном анализе в зависимости от CRT, из 614 пациентов 224 (36,5%) имели предшествующую ресинхронизирующую те-
Таблица 7. Динамика ЭхоКГ у пациента Л. через 6 месяцев наблюдения [составлено авторами]
Table 7. EchoCG dynamics in patient L. after 6 months of follow-up
[compiled by the authors]
|
Показатель |
Исходно |
Через 6 месяцев |
|
Размер ЛП, см |
6,2 |
5,4 |
|
КДР ЛЖ, см |
8,2 |
7,2 |
|
КСР ЛЖ, см |
7,2 |
5,9 |
|
Объем ЛП, мл |
152 |
140 |
|
КДО, мл |
296 |
262 |
|
КСО, мл |
208 |
182 |
|
ФВ ЛЖ, % |
30 |
32 |
|
УО, мл |
65 |
85 |
|
СВ, л/мин |
4,2 |
6,5 |
|
СДЛА, мм рт. ст. |
81 |
47 |
Примечание/Note: ЛП – левое предсердие (LA – left atrium), ЛЖ – левый желудочек (LV – left ventricle), КДР – конечнодиастолический размер (EDD – end-diastolic dimension), КСР – конечно-систолический размер (ESR – end-systolic dimension), КДО – конечно-диастолический объем (EDV – end-diastolic volume), КСО – конечно-систолический объем (ESV – end-systolic volume), ФВ – фракция выброса (EF – ejection fraction), УО – ударный объем (SV – stroke volume), СВ – сердечный выброс (CO – cardiac output), СДЛА – систолическое давление легочной артерии (PASP – pulmonary artery systolic pressure)
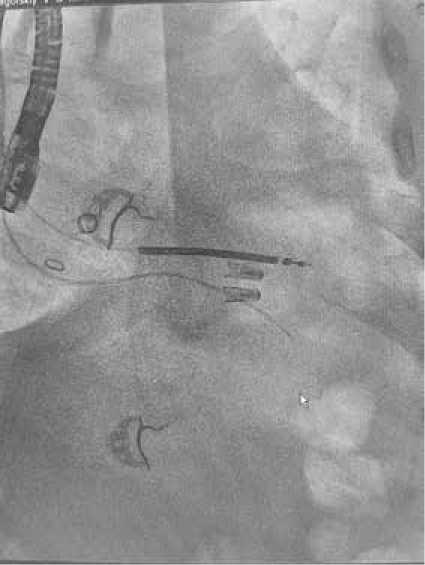
Рисунок 4. Рентгеновское изображение электродов и системы
MitraClip во время операции [составлено авторами]
Figure 4. X-ray image of the electrodes and MitraClip system during surgery [compiled by the authors]
EURASIAN HEART JOURNAL, 3, 2024 33
рапию и 390 (63,5%) не имели CRT. Пациенты с CRT имели аналогичные 2-летние показатели смертности или госпитализации по поводу декомпенсации ХСН по сравнению с пациентами без CRT (57,6% vs 55%, P=0,32). Смертность или госпитализация по поводу СН через 2 года были ниже при применении клипирования створок митрального клапана по сравнению с контрольной группой у пациентов с предшествующей ресинхронизирующей терапии (48,6% vs 67,2) и без CRT (42,5% vs 66,9%), p=0,23 [7].
В опубликованном в 2019 году исследовании по поводу влияния ранней имплантации CRT и ИКД перед применением системы клипирования створок митрального клапана с помощью MitraClip [8] изучалась когорта пациентов с ХСН с низкой ФВЛЖ – n=235. 54 пациента (23%) имели в анамнезе имплантацию CRT, 86 пациентов (36,6%) – ИКД и 95 (40,4%) пациентов были без ранее установленных устройств. Через 12 месяцев оценивалась выживаемость, которая оказалась сопоставимой – CRT 75,7%, ИКД 75,8% и пациенты без устройств – 78% (р=0,94).
В нашем исследовании не наблюдалось значимых отличий в динамике клинического состояния, показателей толерантности к физической нагрузке и лабораторных показателей в зависимости от наличия или отсутствия имплантированных устройств. Клиническое улучшение после проведенной коррекции митральной регургитации наблюдалось в обеих группах.
В динамике ЭхоКГ показателей лучшие результаты достигнуты у пациентов без имплантированных устройств, однако следует учитывать малочисленность группы с устройствами, что не позволило получить значимые результаты.
ЗАКЛЮЧЕНИЕ
Наряду с успехами в применении медикаментозной терапии в лечении ХСН, применение различных устройств значительно улучшает прогноз и качество жизни. При наличии МР применение системы клипирования створок митрального клапана оказывает положительное влияние на течение СН в виде улучшения клинического состояния и уменьшения потребности в диуретической терапии и может быть рекомендована пациентам вне зависимости от наличия имплантированных устройств в анамнезе. Отсутствие значимой динамики размеров и объемов камер сердца по данным ЭхоКГ у пациентов с имплантированными устройствами связано, вероятнее всего, с малым объемом выборки.
Список литературы Клипирование створок митрального клапана у пациентов с ранее имплантированными устройствами для коррекции сердечной недостаточности
- McDonagh, T. A., Metra, M., Adamo, M., Gardner, R. S., Baumbach, A., Böhm, M., Burri, H., Butler, J., Čelutkienė, J., Chioncel, O., Cleland, J. G. F., Coats, A. J. S., Crespo-Leiro, M. G., Farmakis, D., Gilard, M., Heymans, S., Hoes, A. W., Jaarsma, T., Jankowska, E. A., Lainscak, M., … ESC Scientific Document Group (2021). 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European heart journal, 42(36), 3599-3726. DOI: 10.1093/eurheartj/ehab368 EDN: JMLXGH
- Asgar, A. W., Mack, M. J., & Stone, G. W. (2015). Secondary mitral regurgitation in heart failure: Pathophysiology, prognosis, and therapeutic considerations. Journal of the American College of Cardiology, 65(12), 1231-1248. DOI: 10.1016/j.jacc.2015.02.009
- Iung, B., & Vahanian, A. (2014). Epidemiology of acquired valvular heart disease. The Canadian journal of cardiology, 30(9), 962-970. DOI: 10.1016/j.cjca.2014.03.022
- Geis, N.A.; Göbbel, A.; Kreusser, M.M.; Täger, T.; Katus, H.A.; Frey, N.; Schlegel, P.; Raake, P.W. Impact of Percutaneous Mitral Valve Repair Using the MitraClipTM System on Ventricular Arrhythmias and ICD Therapies. Life 2022, 12, 344. DOI: 10.3390/life12030344 EDN: WJRZES
- Cahill, T. J., Prothero, A., Wilson, J., Kennedy, A., Brubert, J., Masters, M., Newton, J. D., Dawkins, S., Enriquez-Sarano, M., Prendergast, B. D., & Myerson, S. G. (2021). Community prevalence, mechanisms and outcome of mitral or tricuspid regurgitation. Heart (British Cardiac Society), heartjnl-2020-318482. DOI: 10.1136/heartjnl-2020-318482
- Kienemund, J., Kuck, K. H., & Frerker, C. (2014). Cardiac Resynchronisation Therapy or MitraClip® Implantation for Patients with Severe Mitral Regurgitation and Left Bundle Branch Block. Arrhythmia & electrophysiology review, 3(3), 190-193. DOI: 10.15420/aer.2014.3.3.190
- Kosmidou, I., Lindenfeld, J., Abraham, W. T., Kar, S., Lim, D. S., Mishell, J. M., Whisenant, B. K., Kipperman, R. M., Boudoulas, K. D., Redfors, B., Shahim, B., Zhang, Z., Mack, M. J., & Stone, G. W. (2020). Transcatheter Mitral Valve Repair in Patients With and Without Cardiac Resynchronization Therapy: The COAPT Trial. Circulation. Heart failure, 13(11), e007293. DOI: 10.1161/CIRCHEARTFAILURE.120.007293
- D'Ancona, G., Ince, H., Schillinger, W., Senges, J., Ouarrak, T., Butter, C., Seifert, M., Schau, T., Lubos, E., Boekstegers, P., von Bardeleben, R. S., & Safak, E. (2019). Percutaneous treatment of mitral regurgitation in patients with impaired ventricular function: Impact of intracardiac electronic devices (from the German Transcatheter Mitral Valve Interventions Registry). Catheterization and cardiovascular interventions: official journal of the Society for Cardiac Angiography & Interventions, 94(5), 755-763. DOI: 10.1002/ccd.28127


