Коэффициент термоэлектрической ЭДС коллоидного раствора канифоли
Автор: Сидоров А.В., Кузнецов Д.В.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Физико-математические науки
Статья в выпуске: 3-1 (42), 2020 года.
Бесплатный доступ
В работе приведены результаты исследования термоэлектрического эффекта истинного раствора, коллоидного и их смеси. Проведены серийные измерения коэффициента термоэлектрической ЭДС растворов в зависимости от их разбавления. На основании полученных результатов можно сделать вывод, что коллоидные частицы, которые имеют высокие значения теплоты переноса и низкие значения подвижности, начинают вносить заметный вклда в итоговую величину термоЭДС смеси золя и истинного раствора, только при низких концентрациях ионного электролита. С другой стороны, в области высоких концентраций электролита термоЭДС смеси определяется ионами, имеющими высокие значения подвижности.
Термоэлектрический эффект, коэффициент соре, коэффициент термоэдс, коллоидная частица
Короткий адрес: https://sciup.org/170190751
IDR: 170190751 | DOI: 10.24411/2500-1000-2020-10244
Coefficient of thermoelectric EMF of colloidal solution of rosin
The paper presents the results of a study of the thermoelectric effect of a true solution, colloidal and their mixtures. Serial measurements of the coefficient of thermoelectric EMF of solutions are carried out depending on their dilution. Based on the results obtained, it can be concluded that colloidal particles, which have high values of heat of transfer and low mobility values, begin to make a significant contribution to the final value of the thermoEMF of a mixture of sol and true solution only at low concentrations of ionic electrolyte. On the other hand, in the region of high electrolyte concentrations, the thermoEMF of the mixture is determined by ions having high mobility values.
Текст научной статьи Коэффициент термоэлектрической ЭДС коллоидного раствора канифоли
Явление термодфиффузии, приводящее к изменению концентраций веществ в смеси под воздействием градиента температуры, известно более полутора веков. Количественно оно характеризуется коэффициентом Соре s который, например в жидкости, пропорционален градиенту концентрации растворенного вещества, возникшего при наложении единичного температурного градиента в соответствии с урав- gradm)=^ • grad(T)
нением m [1]. Здесь m – молярность растворенного вещества, T -абсолютная температура. Данное явление исследовалось в широком классе веществ: газах, жидкостях, растворах электролитов. Протекание данного явления в растворах электролитов сопровождается формированием в жидкости разнос и электрических потенциалов Δφ ~ grad(T), обусловленной различием в транспортных характеристиках катионов и анионов диссоциирующего вещества их подвижностей μ± и теплоты переноса Q±.
Величина коэффициентов Соре в водных растворах неорганических ионных электролитов по порядку величины равна 10-3 К-1 и в подавляющем большинстве случаев отрицательна по знаку [2]. Отри- цательный знак коэффициента Соре s означает, что неорганические ионные электролиты перемещаются в более горячие области, где их концентрация возрастает по сравнению с более холодными областями. Коэффициент их термоэлектрической силы α = Δφ/ΔT составляет десятки и сотни мкВ/К [3] и сравним с таковым для металлов и полупроводников, применяющихся в качестве материалов для термоэлектрических преобразователей [4].
Сравнительно недавно, в конце прошлого века, было обнаружено, что коэффициент Соре жидких дисперсных растворов может превышать коэффициент Соре ионных электролитов на два, три порядка [5]. В связи с этим началось бурное исследование таких систем. Данное явление для коллоидных растворов получило свое название – термофорез. Оно изучалось в широком классе систем водных и неводных растворителях [6, 7], в присутствии различных растворенных веществ [8], при различных значениях pH и концентрации коллоидных частиц и их размера [9].
Агрегативная устойчивость таких растворов обусловлена электрическими взаимодействиями между коллоидными частицами в растворе, которые должны быть обязательно заряженными, вследствие ад- сорбции на их поверхности ионов одного знака. В результате заряженное ядро коллоидной частицы окружается динамической оболочкой из ионов противоположного знака. Образованные таким образом мицеллы являются заряженными частицами, поэтому явление термодиффузии в коллоидных растворах всегда сопровождается возникновением термоэлектродвижущей разности потенциалов, как и в растворах ионных электролитов.
Термоэлектрические явления в отличие от термодиффузионных изучаются в коллоидных растворах в настоящее время сравнительно редко. Однако как было по- казано в [10] возникающие в них термоэлектрические разности потенциалов могут существенно влиять на термофорети-ческий транспорт коллоидных частиц. В данной работе исследуются термоэлектрические свойства коллоидного раствора сосновой канифоли в дистиллированной воде. Для исследования термоэлектрического эффекта использовалась установка, показанная на рисунке 1 [11]. Хлорсеребряные электроды и термодатчики подключались к иономеру ИПЛ-113, по полученным данным строились экспериментальные зависимости.
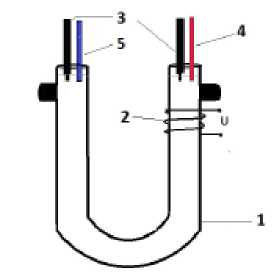
Рис. 1. Схема экспериментальной установки.
1 – U-образная трубка, 2 – нагреватель, 3 – хлорсеребряные электроды, 3,4 – термодатчики.
Для получения коллоидного раствора 2% спиртовой раствор канифоли добавлялся к дистиллированной воде, при этом получался молочно-белый, довольно устойчивый золь.
О
0,5
1,0
1,5 m,%
2,0

—■— смесь золя канифоли с водным раствором NaOH -•- водный раствор NaOH

m, %
2,0
Рис. 2. Зависимость коэффициента термоЭДС золя канифоли от массового содержания канифоли.
Рис. 3. Зависимости коэффициента термо-ЭДС водного раствора NaOH и его смеси с зо лем канифоли постоянной концентрации от массового содержания NaOH.
Исследования термоэлектрического эффекта проводились с золем канифоли при различных концентрациях 2% спиртового раствора канифоли в дистилирован-ной воде (рис. 2), с водным раствором NaOH и их смеси (рис. 3).
Как видно из графика (рис. 2) коэффициент термоЭДС водного раствора канифоли по порядку величины составляет несколько десятков мкВ/К. Зависимость имеет четко выраженный максимум при массовом содержании канифоли около 1%.
При исследовании смеси канифоли с раствором гидроксида натрия, (рис. 3) в области высоких концентраций электролита до 0.5%, коэффициент термоэлектрической силы смеси определяется ионным электролитом, анионы которого OH- имеют высокие значения подвижности. Однако при уменьшении содержания щелочи наблюдается все более и более увеличивающееся различие между коэффициентом термоЭДС чистого электролита и коэффициентом термоЭДС смеси с коллоидным раствором. Причем коэффициент термо-ЭДС смеси, при малых концентрациях щелочи, приближается к коэффициенту для чистого раствора канифоли. Таким образом, вклад коллоидных частиц, имеющих высокие значения теплоты переноса и низкие значения подвижности, в итоговую величину термоэлектродвижущей силы смеси становится заметным только при низких содержаниях электролита.
Рост интереса к термоэлектрическим свойствам коллоидных растворов со стороны исследователей обусловлен перспективами применения жидких дисперсных систем в качестве электролитов термоэлектрохимических источников тока [12], предназначенных для прямого преобразования низкопотенциальных тепловых потоков от промышленных установок в электрическую энергию. В связи с этим широкое экспериментальное и теоретическое исследование термоэлектрических явлений в коллоидных растворах является важной задачей.
Список литературы Коэффициент термоэлектрической ЭДС коллоидного раствора канифоли
- Хаазе. Р. Термодинамика необратимых процессов. - М.: Мир, 1967. - 544 с.
- Payton A.D. Soret coefficients and heats of transport of some salts of alkaline earth metals in water at 25°C / Payton A.D. Turner J.C.R. // Trans. Faraday Soc. - 1962. - Vol. 58. - P. 55-59.
- T.I. Quickenden and Y. Mua, J. Electrochem. Soc. 142, 3985 (1995) and references therein.
- R. Hu, B.A. Cola, N. Haram, J.N. Barisci, S. Lee, S. Stoughton, G. Wallace, C. Too, M. Thomas, A. Gestos, M.-E. dela Cruz, J.P Ferraris, A.A. Zakhidov, and R.H. Baughman, Nanoletters 10, 838 (2010).
- J. Lenglet et al., Phys. Rev. E 65, 031408 (2002)


