Количественное определение соединения РУ-1205 в биологических пробах
Автор: Смирнова Л.А., Ращенко А.И., Рябуха А.ф, Кузнецов К.А., Сучков Е.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Фармакология токсикология
Статья в выпуске: 2 (34), 2012 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/142148973
IDR: 142148973
Assay of compound RU-1205 in biological samples
Текст статьи Количественное определение соединения РУ-1205 в биологических пробах
Фармакокинетические показатели имеют большое значение при изучении новых высокоактивных соединений, так как они определяют тактику разработки лекарственных форм и изучение фармакодинамики данных веществ [3]. Актуальной задачей является создание новых эффективных опиоидных анальгетиков, с отсутствующими серьезными побочными эффектами [4]. В данной области каппа-селективные агонисты представляют одну из наиболее перспективных групп соединений для создания новых отечественных препаратов [2]. Результаты предварительных исследований показывают, что производные бензимидазола могут считаться потенциальными обезболивающими средствами с каппа-опиоидной активностью [1].
В ходе настоящего исследования разработан метод высокоэффективной жидкостной хроматографии (ВЭЖХ) с диодноматричным детектированием для проведения фармакокинетических исследований соединения РУ-1205, позволяющий определять изучаемое вещество в биологическом материале.
ЦЕЛЬ РАБОТЫ
Разработка метода количественного определения производного бензимидазола соединения РУ-1205 c использованием ВЭЖХ.
МЕТОДИКА ИССЛЕДОВАНИЯ
В работе использовался жидкостной хроматограф (Shimadzu, Япония). Определение соеди- нения РУ-1205 осуществлялось при помощи диодноматричного ультрафиолетового детектора при длине волны 205 нм, на колонке SUPELCOSIL LC-18 (5 мкм; 100 x 4,6 мм). Мобильная фаза включала ацетонитрил (УФ210) (Россия) и буферную систему, состоящую из однозамещенного фосфата калия 50 mМоль.
В качестве модификаторов мобильной фазы рассматривались следующие соединения: гептансульфоновая кислота, тетрагидрофуран, триэтила-мин и додецилсульфат в различных процентных концентрациях.
Извлечение соединения РУ-1205 из биологического материала осуществлялось ацетонитрилом в соотношении 1:1.
Для количественного определения вещества применялся метод абсолютной калибровки. Зависимость площадей пиков от концентрации РУ-1205 анализировалась методом регрессионного анализа. Статистическая обработка результатов проводилась при помощи компьютерной программы Exel.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
При разработке метода использовались буферные системы с диапазоном рН от 2,5 до 7,0. При отклонении рН в кислую сторону было отмечено снижение времени удерживания вещества на хроматографической колонке. При рН = 3,0 время удерживания составило 3,5—4,0 мин. Значе- ния рН выше 5,5—6 вызывали увеличение времени удерживания и снижение стабильности определения.
Температурный режим подбирался в диапазоне 30—75 оС. Уменьшение температуры приводило к резкому снижению чувствительности. В диапазоне 60—75 оС не выявлено значительных колебаний, соответственно окончательный выбор остановлен на значении 60 оС.
Соотношения водной и органической фаз: 30 % : 70 % v/v; 35 % : 65 % v/v; 40 % : 60 % v/v; 50 % : 50 % v/v и 55 % : 45 % v/v соответственно. Увеличение процента водной фазы приводило к значительному увеличению времени удерживания и снижению чувствительности. Увеличение доли органической фазы свыше 60 % вызывало уменьшение времени удерживания до 3—5 мин, неоправданно увеличивая риск интерференции эндогенными пиками биоматериала.
Модификаторы мобильной фазы не оказали положительного влияния на количественное определение соединения. Так, например, применение додецилсульфата приводило к резкому снижению высоты пика и увеличению его основания. При добавлении тетрагидрофурана происходило значительное снижение времени удерживания.
При разработке метода извлечения соединения РУ-1205 из биологического материала в качестве возможных экстрагентов рассматривались спирт этиловый, ацетонитрил, смесь спирт этиловый : ацетонитрил в соотношении 1 : 1, а также спирт этиловый, подкисленный 0,1н соляной кислотой.
Образцы встряхивались в течение десяти минут в ультразвуковой ванне для преципитации белков и центрифугировали в течение 15 минут при 3000 об/мин на центрифуге Eppendorf, после чего надосадочная жидкость отбиралась и вводилась в инжектор с объемом петли 20 мкл.
В результате в качестве экстрагента был выбран ацетонитрил, обеспечивающий достаточную степень экстракции и удовлетворительную очистку пробы. Степень экстракции соединения РУ-1205 составила не менее 90 %.
Таким образом, оптимальными условиями количественного определения субстанции РУ-1205 являются следующие: буферная система, состоящая из 50 мМ однозамещенного фосфата калия, рН = 5; соотношение водной и органической фазы 50 % : 50 % v/v; температурный режим 60 оС; длина волны детекции 205 нм; скорость потока 1мл/мин. При данных условиях время удерживания составило 8—8,5 мин (рис. 1, 2).
Количественное определение проводилось в диапазоне концентраций от 0,5 до 25 мкг/мл. В результате было установлено, что калибровочные кривые носят линейный характер, с коэффициентом регрессии (R2) равным 0,998 (рис. 3).
Были определены внутридневные процентные колебания (повторяемость метода), которые не превышали 20 % в изучаемых диапазонах концентраций. Междневные процентные колебания (воспроизводимость метода) для изучаемого соединения не превышали в основном 15 % (табл.).
При повторном проведении анализа, после 72 часов хранения водных растворов соединения при комнатной температуре, средние абсолютные процентные колебания находились в тех же пределах, показывая стабильность изучаемого вещества.
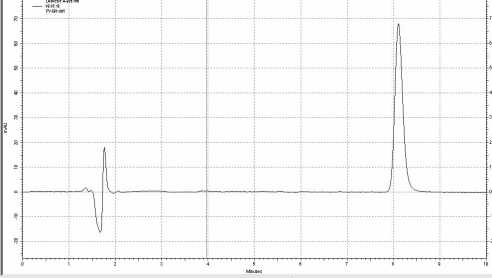
Рис. 1. Хроматограмма соединения РУ-1205 в водном растворе
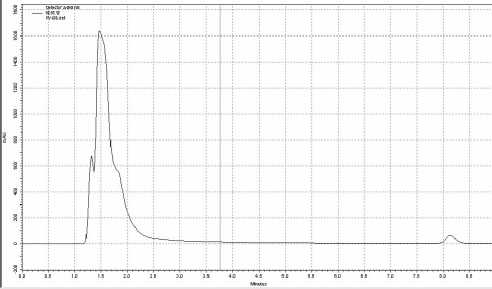
Рис. 2. Хроматограмма соединения РУ-1205 в биологическом материале
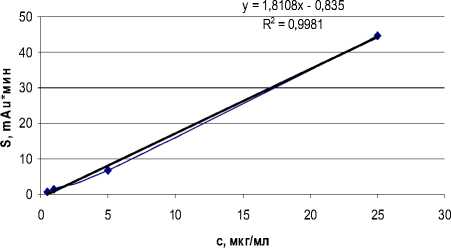
Рис. 3. Зависимость площади под хроматографическим пиком от концентрации вещества РУ-1205
Чувствительность метода для изучаемого соединения составляет 1 мкг/мл. Средняя ошибка измерения не превышает 15 %.
Показатели воспроизводимости и повторяемости метода количественного определения соединения РУ-1205 в диапазоне линейной зависимости площади хроматографического пика от концентрации растворов (M ± m)
|
Концентрация, мкг/мл |
Внутридневные колебания концентрации, мкг/мл |
Повторяемость, ± А % |
Воспроизводимость (средняя ошибка измерения), % |
||||
|
день 1 |
день 2 |
день 3 |
день 1 |
день 2 |
день 3 |
||
|
0,5 |
0,89 ± 0,07 |
0,81 ± 0,08 |
1,06 ± 0,08 |
77,42 |
62,98 |
111,36 |
83,92 |
|
1 |
1,20 ± 0,06 |
1,18 ± 0,24 |
1,24 ± 0,12 |
20,4 |
18,04 |
24,31 |
20,91667 |
|
5 |
4,24 ± 0,51 |
4,25 ± 0,53 |
3,91 ± 0,21 |
-15,27 |
-14,99 |
-21,73 |
17,33 |
|
25 |
25,13 ± 6,24 |
21,6 ± 3,51 |
30,05 ± 5,10 |
0,54 |
-13,41 |
20,19 |
2,44 |
ЗАКЛЮЧЕНИЕ
В результате проведенных исследований разработан хроматографический метод количественного определения соединения РУ-1205, обладающий достаточной чувствительностью и селективностью. Чувствительность метода составляет 1 мкг/мл, воспроизводимость 15 %.
Таким образом, разработанный метод количественного определения является высокоселективным и высокочувствительным, что позволяет эффективно использовать его для проведения фармакокинетических исследований соединения РУ-1205.


