Количественные изменения популяции стволовых клеток рака шейки матки линии HeLa под влиянием фракционированного G-облучения in vitro
Бесплатный доступ
Радиорезистентность опухолевых стволовых клеток (ОСК) рассматривается в качестве одной из возможных причин рецидивирования онкологических заболеваний после лучевой терапии. Однако, закономерности и механизмы фракционированного радиационного воздействия на эту популяцию клеток изучены недостаточно, особенно мало данных представлено для ОСК рака шейки матки (РШМ). Поэтому целью данной работы является выяснение количественных изменений ОСК после g-облучения культуры РШМ линии HeLa в режиме стандартного фракционирования дозы (по 2 Гр ежедневно в течение 5 дней). ОСК идентифицировали с помощью проточной цитометрии по способности исключать флуоресцентный краситель Хёхст 33342 и формировать так называемую боковую популяцию (side population - SP) через 24 ч после каждой фракции дозы до достижения суммарной дозы 10 Гр. Относительное и абсолютное количество ОСК увеличивалось после облучения в суммарных дозах до 6 Гр, но при дальнейшем повышении дозы уменьшалось или сохранялось на достигнутом уровне соответственно. В то же время, как и следовало ожидать, с повышением дозы радиационного воздействия происходило торможение роста общего числа клеток по сравнению с контролем. Полученные результаты сопоставлены с ранее опубликованными данными о влиянии на ОСК однократного острого облучения в диапазоне доз до 10 Гр. Обсуждены возможные причины наблюдаемых эффектов, основными среди которых являются более высокая радиорезистентность ОСК по сравнению с остальной массой опухолевых клеток, выход жизнеспособных ОСК из состояния пролиферативного покоя в процессе пострадиационной репопуляции опухолевых клеток, а также дедифференцировка сохранившихся после облучения не стволовых клеток и их переход в ОСК.
Опухолевые стволовые клетки, рак шейки матки, радиорезистентность, дедифференцировка, редкоионизирующее излучение, фракционированное облучение, однократное облучение, проточная цитометрия
Короткий адрес: https://sciup.org/170171482
IDR: 170171482 | УДК: 618.146-006.6-018.1:612.014.482.4]-076.5 | DOI: 10.21870/0131-3878-2019-28-2-112-123
Quantitative changes in the stem cell population of cervical cancer cell line HeLa under the influence of fractionated G-irradiation in vitro
Radioresistance of cancer stem cells (CSCs) is considered as one of the possible causes of cancer recurrence after radiation therapy. However, the regularities and mechanisms of the effect of fractionated irradiation on this cell population have been insufficiently studied, particularly, there is little evidence of mechanisms of fractionated irradiation effects on cervical cancer stem cells. Therefore, the goal of this work is elucidating quantitative changes in stem cells of cervical cancer cell line HeLa following γ-irradiation in the standard dose fractionation mode (2 Gy daily for 5 days). CSCs were identified by flow cytometry by their ability to exclude the fluorescent dye Hoechst 33342 (SP method) 24 hours after each dose fraction in the cumulative dose range up to 10 Gy. The relative and absolute number of CSCs increased after irradiation at cumulative doses up to 6 Gy. However, further dose increasing resulted in reduction of the number of CSC, and absolute number of the cells remained unchanged. At the same time, increasing radiation exposure caused inhibition of the cells growth as compared to the control, as expected. The obtained results were compared with previously published data on effects of single acute irradiation in the dose range up to 10 Gy on CSCs. Possible mechanisms of the observed effects seem to include the higher radioresistance of CSCs in comparison with the other tumor cells, CSC proliferation during the postradiation repopulation of cancer cells, and dedifferentiation of non-stem cells that survived irradiation and their transition to CSCs pool.
Текст научной статьи Количественные изменения популяции стволовых клеток рака шейки матки линии HeLa под влиянием фракционированного G-облучения in vitro
Гетерогенность опухолевых клеток по морфологическим и функциональным признакам (в том числе по чувствительности к радиационным и химическим воздействиям) является фундаментальным свойством злокачественных опухолей. Поскольку такая гетерогенность во многом определяет эффективность лечения онкологических больных, выяснение разнообразных механизмов её формирования не теряет своей актуальности уже многие годы. В последнее время активно развивается представление о том, что в злокачественных новообразованиях имеются особые клетки, которые являются родоначальниками гетерогенных клонов, составляющих опухоль. Они отличаются от остальных опухолевых клеток по туморогенной активности (способности восстанавливать рост исходной опухоли при трансплантации в организм иммунодефицитных мышей) и сходны со стволовыми клетками нормальных тканей по ряду молекулярнобиологических и структурно-функциональных особенностей (профиль генной экспрессии, набор белковых маркеров на поверхности клеток, интенсивное удаление лекарственных препаратов и липофильных красителей и т.д.). Эти клетки получили название опухолевых стволовых клеток (ОСК); в различных литературных источниках их называют также стволоподобными (stem-like)
Матчук О.Н.* – ст. научн. сотр., к.б.н.; Замулаева И.А. – зав. отд., д.б.н., проф. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
или опухоль-инициирующими клетками (tumor initiating cells). С помощью различных методов продемонстрировано существование ОСК в злокачественных новообразованиях практически всех локализаций и стабильных линиях опухолевых клеток человека и животных.
Результаты собственных исследований и данные литературы, полученные, главным образом, в условиях in vitro , указывают на более высокую резистентность ОСК к острому однократному воздействию редкоионизирующего излучения по сравнению с остальными опухолевыми клетками, поэтому предполагают, что именно ОСК определяют неблагоприятные отдалённые результаты радиотерапии [1-10]. При этом важно отметить, что в литературе представлено значительно меньше данных о влиянии фракционированного радиационного воздействия на ОСК в культурах опухолевых клеток различного происхождения, а в отношении ОСК рака шейки матки (РШМ) имеются лишь единичные публикации [11]. Выяснение закономерностей ответа ОСК РШМ на фракционированное облучение представляется весьма актуальным, учитывая рост заболеваемости раком этой локализации в РФ [12] и использование радиотерапии в качестве одного из основных методов лечения инвазивного РШМ [13]. Поэтому целью данной работы является выяснение количественных изменений ОСК после γ-облучения культуры рака шейки матки линии HeLa в режиме стандартного фракционирования дозы. Обнаруженные эффекты сравнивали с ранее полученными данными об изменении размера этой популяции после однократного γ-облучения in vitro [14].
Материалы и методы
В работе использован один из основных методов идентификации ОСК, основанный на оценке эффективности исключения из клеток флуоресцентного красителя Хёхст 33342. ОСК (в отличие от остальных клеток) обладают способностью исключать указанный краситель вследствие высокой экспрессии на плазматической мембране различных АТФ-связывающих транспортёров [15]. Благодаря этой способности ОСК могут быть выявлены с помощью проточной цитометрии как «боковая популяция» (side population – SP) в ряде стабильных линий опухолевых клеток, включая использованную в данной работе линию HeLa [16, 17]. При этом для обозначения остальных клеток часто применяется термин non SP (NSP), который принят в данной работе ввиду его распространённости в зарубежных публикациях.
Клетки РШМ человека линии HeLa культивировали в стандартных условиях: в полной питательной среде DMEM (ПанЭко, РФ), содержащей 10% эмбриональной сыворотки крупного рогатого скота (Biosera, Франция), пенициллин (50 ед/мл), стрептомицин (50 мкг/мл) и глютамин (292 мкг/мл), в CO 2 инкубаторе Shellab (США) в увлажнённой атмосфере с 5% содержанием CO 2 при температуре +37 оС. Для опыта клетки рассевали в пластиковые флаконы (Corning, США, площадь поверхности 25 см2). По достижении 30-40% конфлюэнтности клетки подвергали воздействию γ-излучения 60Со на установке «Агат-Р» (Россия) в разовой дозе 2 Гр ежедневно до достижения суммарной дозы 10 Гр (мощность дозы 0,5 Гр/мин). Относительное и абсолютное количество клеток SP оценивали через 24 ч после облучения в суммарных дозах 2, 4, 6, 8 и 10 Гр; одновременно эти же показатели анализировали в контрольных (не облучённых) образцах. Определяли общее количество клеток в каждом флаконе с помощью камеры Горяева и проводили стандартное окрашивание с применением флуоресцентного красителя Хёхст 33342
(Sigma, США) для определения доли клеток SP в изучаемых культурах, как подробно описано в работе [3]. Концентрация Хёхста составляла 5 мкг/мл, время инкубации – 90 мин при 37 оС и периодическом перемешивании. Для исключения из анализа мёртвых и погибающих клеток в образцы добавляли раствор йодистого пропидия до конечной концентрации 2 мкг/мл за 10-15 мин до анализа. Окрашенные образцы анализировали с помощью проточного цитофлуориметра FACS Vantage (Becton Dickinson Immunocytometry Systems, BDIS, США), оборудованного двумя лазерами с длинами волн 364 и 488 нм. Флуоресценцию Хёхста измеряли в синей (424±20 нм) и красной (675±20 нм) областях спектра (при λ возб =364 нм), а также регистрировали флуоресценцию йодистого пропидия при длине волны 585±20 нм (λ возб =488 нм). Для контроля окрашивания использовали параллельные образцы клеток, инкубированных с Хёхстом в присутствии верапамила – блокатора кальциевых каналов I класса, препятствующего выведению Хёхста 33342 из клеток. Данные собирали в файл, который затем обрабатывали с помощью программы CellQuestPro (BDIS, США). Регион SP выделяли графически таким образом, чтобы в образцах с верапамилом в этот регион попадало минимальное количество клеток. Вычисляли относительное количество (процент) клеток SP и NSP, а затем их абсолютное количество в каждом флаконе. Проведено 3 независимых эксперимента, результаты которых были объединены. В каждом эксперименте использовано по 4-5 флаконов на каждую суммарную дозу облучения и соответствующий необлучённый контроль.
Для описательной статистики использовали среднее значение и стандартную ошибку (SE), вычисленные с помощью программы «Statistica 6.0» (StatSoft., Inc.). Групповое сравнение полученных данных проводили по критерию Манна-Уитни в той же программе. Различия считали статистически значимыми при р<0,05. Построение графиков выполняли с помощью программы «Origin 6.0» (Microcal Software, Inc.).
Результаты и обсуждение
Фракционированное радиационное воздействие существенно тормозило рост клеточной культуры, и после облучения в суммарной дозе 10 Гр наблюдали уменьшение общего количества клеток в 2,4 раза по сравнению с контролем (рис. 1).
Доля клеток SP в контрольных образцах исследуемой линии не изменялась значимо в течение всего эксперимента, составляя в среднем (±SE) 5,5±0,3%. Но в облучённых культурах этот показатель увеличивался после каждой фракции до суммарной дозы 6 Гр, после чего происходило уменьшение этого показателя (рис. 2).
В ходе эксперимента происходило повышение абсолютного количества клеток SP в контроле (рис. 3), что обусловлено быстрым увеличением общего числа культивируемых клеток в экспоненциальной фазе роста (рис. 1). Повышение абсолютного количества клеток SP в облучённых культурах наблюдалось до дозы 6 Гр, а затем (при дальнейшем облучении) этот показатель статистически значимо не менялся (рис. 3). Важно, что после облучения в дозах 4 и 6 Гр абсолютное количество клеток SP превышало контрольный уровень, несмотря на уменьшение общего количества облучённых клеток по сравнению с контролем. Как видно на рис. 3, под влиянием радиационного воздействия абсолютное содержание клеток SP максимально возрастало в среднем в 15 раз (в диапазоне 6-10 Гр) по сравнению с исходным уровнем до облучения (точка «0»).
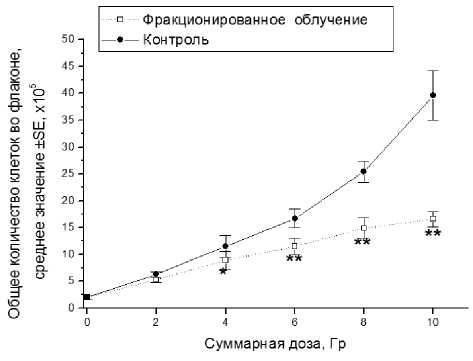
Рис. 1. Влияние фракционированного γ-облучения на общее количество опухолевых клеток линии HeLa в сравнении с необлучённым контролем.
* p<0,05 по сравнению с контролем; ** p<0,01 по сравнению с контролем.
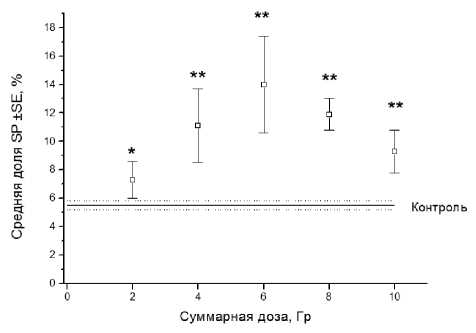
Рис. 2. Изменение относительного количества (доли) клеток SP после фракционированного γ-облучения в разных суммарных дозах.
* p<0,05 по сравнению с контролем; ** p<0,01 по сравнению с контролем.
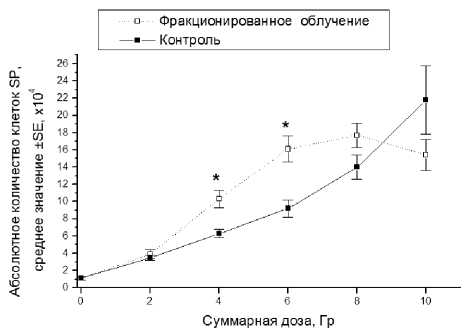
Рис. 3. Изменение абсолютного количества клеток SP в контроле и после фракционированного облучения в разных суммарных дозах. * p<0,05 по сравнению с контролем.
Представляло интерес сопоставить эффекты однократного и фракционированного воздействия на размер популяции ОСК. Данные по абсолютному количеству SP после однократного острого γ-облучения были опубликованы нами ранее [14] и пересчитаны по отношению к контролю, принятому за 100% для удобства сопоставления с эффектами фракционированного облучения. Таким же образом были рассчитаны данные по фракционированному облучению в каждой временно́й точке (после каждой накопленной дозы). Полученные результаты представлены на рис. 4. Видно, что при таком подходе абсолютное количество клеток SP изменяется одинаковым образом по сравнению с временны́ м контролем при однократном и фракционированном облучении, хотя общее количество клеток уменьшается при однократном облучении (10 Гр) в 4 раза, а при фракционированном облучении (10 Гр) – в 2,4 раза по сравнению с контролем. Следует также отметить, что однократное облучение максимально повышало абсолютное количество клеток SP примерно в 2,6 раза по сравнению с исходным уровнем (данные не показаны), а фракционированное – в 15 раз, как отмечалось выше. Таким образом, как и ожидалось, фракционированное облучение (по сравнению с однократным) оказывало менее эффективное действие на общую популяцию опухолевых клеток, но при этом примерно одинаково влияло на размер популяции ОСК, если сравнивать этот показатель с временны́ м контролем, т.е. тем самым учитывать рост контрольной культуры и увеличение абсолютного количества клеток SP в контроле. Однако при сравнении с исходным количеством ОСК (SP) фракционированное облучение приводило к более выраженному эффекту, чем однократное острое воздействие в тех же дозах.
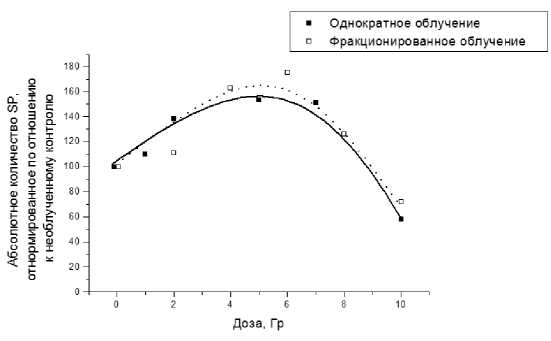
Рис. 4. Сравнение эффектов острого однократного и фракционированного облучения по критерию абсолютного количества клеток SP, принятого в соответствующих контрольных образцах за 100%. Данные по абсолютному количеству клеток SP после однократного облучения получены нами ранее [14].
Резистентность ОСК к однократному острому воздействию редкоионизирующего излучения является широко известным фактом, обнаруженным в культурах опухолевых клеток различного происхождения in vitro, опухолях экспериментальных животных и ксенографтах опухолевой ткани человека в организме иммунодефицитных мышей. Культура РШМ линии HeLa не является исключением: резистентность ОСК к однократному облучению была продемонстрирована по многим критериям, включая увеличение доли ОСК (выявляемых по иммунофенотипу и/или SP), экспрессии генов, вовлечённых в формирование и поддержание стволовых свойств, количества сфероидов после такого воздействия, а также включая более высокую клоногенную выживаемость облучённых ОСК по сравнению с остальными клетками [16-19]. Значительно меньше данных представлено в литературе о влиянии фракционированного облучения на ОСК, причём они касаются, в основном, рака молочной железы, рака предстательной железы и глиомы [20-25], в то время как для РШМ данных крайне мало [11]. В последнем исследовании продемонстрировано более чем 20-кратное повышение доли ОСК в культуре РШМ линии SiHa после фракционированного облучения в суммарной дозе 30 Гр. На примере рака предстательной железы, головы и шеи показано, что длительное фракционированное облучение в суммарных дозах, соответствующих клиническому диапазону (50-70 Гр) и выше него (90 Гр), с успехом может быть использовано для получения радиорезистентных клеточных линий, обогащённых ОСК [26, 27]. Вместе взятые данные литературы и результаты наших исследований свидетельствуют о резистентности ОСК разных локализаций не только к однократному, но и фракционированному воздействию редкоионизирующего излучения.
Интересно, что в ряде исследований проводилось сопоставление эффектов острого однократного и фракционированного облучения in vitro по критерию изменения доли ОСК, выявляемых по иммунофенотипу в клеточных культурах глиомы [22, 23], или по критерию количества маммосфер, образующихся после облучения стабильных культур рака молочной железы [20]. В этих исследованиях показаны более выраженные эффекты фракционированного облучения по сравнению с однократным. Так, например, в работе Kim et al., 2011 [23] установлено, что доля CD133+ ОСК (в клеточных культурах глиомы линий U87 и U373) повышается по сравнению с контролем примерно в 3 раза при однократном облучении в дозе 6 Гр, и в 6 раз при фракционированном облучении в режиме 3x2 Гр. Кроме того, именно после фракционированного облучения авторы показали наибольшее увеличение экспрессии генов Sox2, Notch2, р-катенина и др., связанных со стволовым состоянием клеток.
Наблюдаемое нами и другими авторами повышение количества ОСК (SP) после острого однократного и фракционированного облучения может объясняться целым рядом причин, в том числе:
-
- более высокая радиорезистентность ОСК по сравнению с остальной массой опухолевых клеток,
-
- выход ОСК из состояния пролиферативного покоя в процессе пострадиационной репопуляции опухолевых клеток, которая, вероятно, начинается с пула ОСК (SP),
-
- дедифференцировка сохранившихся после облучения не стволовых клеток и их переход в ОСК (SP). В последнее время появляется всё больше данных о пластичности ОСК и возможности дедифференцировки не стволовых опухолевых клеток [28-33]. Такой переход является, по-видимому, редким событием в интактных клеточных культурах/опухолях, но может происходить чаще под влиянием различных факторов, включая ионизирующее излучение.
Что касается различий в эффектах фракционированного и однократного воздействия на популяцию ОСК, то так же можно предложить несколько объяснений. К числу возможных причин более выраженного повышения количества ОСК при фракционированном облучении по сравнению с однократным относятся: дополнительная индукция радиорезистентности ОСК между фракциями дозы, многократный пострадиационный отбор наиболее резистентных клеток, многократная индукция дедифференцировки не стволовых клеток после каждой фракции дозы. Вклад этих механизмов в увеличение относительного и абсолютного количества ОСК после разных режимов облучения пока не точно выяснен и будет изучен в дальнейшем.
Работа выполнена на базе МРНЦ им. А.Ф. Цыба – филиала ФГБУ «НМИЦ радиологии Минздрава России, на протяжении многих лет успешно сочетающего в своей работе экспериментальные исследования и их клиническое применение [34].
Заключение
Показано значительное повышение относительного и абсолютного количества ОСК, выявленных методом SP в культуре РШМ линии HeLa после фракционированного облучения in vitro в стандартном режиме (2 Гр на фракцию, ежедневно); при этом общее количество клеток многократно снижалось по сравнению с необлучённым контролем. Относительное количество ОСК постепенно увеличивалось до достижения суммарной дозы 6 Гр, но при дальнейшем накоплении дозы этот показатель снижался. Абсолютное количество ОСК увеличивалось до дозы 6 Гр и при дальнейшем облучении до суммарной дозы 10 Гр не менялось. Наблюдаемое повышение количества ОСК (SP) после фракционированного облучения может объясняться целым рядом причин. Среди них не только более высокая радиорезистентность ОСК по сравнению с остальной массой опухолевых клеток, но и выход жизнеспособных ОСК из состояния пролиферативного покоя в процессе пострадиационной репопуляции опухолевых клеток, а также дедифференцировка сохранившихся после облучения не стволовых клеток и их переход в ОСК. Точный вклад каждого из этих механизмов в радиационно-индуцированное повышение количества ОСК представляет значительный интерес и требует дальнейших исследований.
Исследование выполнено за счёт гранта Российского научного фонда (проект № 1875-10025).
Список литературы Количественные изменения популяции стволовых клеток рака шейки матки линии HeLa под влиянием фракционированного G-облучения in vitro
- Dubrovska A. Report on the International Workshop «Cancer stem cells: The mechanisms of radioresistance and biomarker discovery» //Int. J. Radiat. Biol. 2014. V. 90, N 8. P. 607-614.
- Rycaj K., Tang D.G. Cancer stem cells and radioresistance //Int. J. Radiat. Biol. 2014. V. 90, N 8. P. 615-621.
- Матчук О.Н., Замулаева И.А., Селиванова Е.И., Липунов Н.М., Пронюшкина К.А., Ульяненко С.Е., Лычагин А.А., Смирнова С.Г., Орлова Н.В., Саенко А.С. Чувствительность клеток SP линии мела-номы В16 к действию редко- и плотноионизирующего излучений //Радиационная биология. Радиоэкология. 2012. № 3. P. 261-267.
- Матчук О.Н., Замулаева И.А., Ковалёв О.А., Саенко А.С. Механизмы радиорезистентности клеток SP культуры мышиной меланомы В16 //Цитология. 2013. Т. 55, № 8. С. 553-559.
- Матчук О.Н., Саенко А.С. Влияние редкоионизирующего излучения и химиопрепаратов на опухолевые стволовые клетки (SP) меланомы B16 и аденокарциномы молочной железы MCF-7 //Радиация и риск. 2013. Т. 22, № 2. С. 67-76.
- Проскуряков С.Я., Матчук О.Н., Замулаева И.А. Современное состояние и перспективы разработки новых подходов к лечению меланомы //Вестник РОНЦ им. Н.Н. Блохина. 2011. Т. 22, № 2. С. 31-40.
- Chang L., Graham P., Hao J., Ni J., Deng J., Bucci J., Malouf D., Gillatt D., Li Y. Cancer stem cells and signaling pathways in radioresistance //Oncotarget. 2016. V. 7, N 10. P. 11002-11017.
- Qi X.S., Pajonk F., McCloskey S., Low D.A., Kupelian P., Steinberg M., Sheng K. Radioresistance of the breast tumor is highly correlated to its level of cancer stem cell and its clinical implication for breast irradiation //Radiother Oncol. 2017. V. 124, N 3. P. 455-461.
- Yang F., Xu J., Tang L., Guan X. Breast cancer stem cell: the roles and therapeutic implications //Cell Mol. Life Sci. 2017. V. 74, N 6. P. 951-966.
- Krause M., Dubrovska A., Linge A., Baumann M. Cancer stem cells: radioresistance, prediction of radiotherapy outcome and specific targets for combined treatments //Adv. Drug Deliv. Rev. 2017. V. 109. P. 63-73.
- Liu H., Wang Y.J., Bian L., Fang Z.H., Zhang Q.Y., Cheng J.X. CD44+/CD24+ cervical cancer cells resist radiotherapy and exhibit properties of cancer stem cells //Eur. Rev. Med. Pharmacol. Sci. 2016. V. 20, N 9. P. 1745-1754.
- Злокачественные новообразования в России в 2015 году (заболеваемость и смертность) /Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИРЦ» Минздрава России, 2017. 250 с.
- Крикунова Л.И., Сыченкова Н.И., Шентерева Н.И., Мкртчян Л.С. Лучевая терапия в онкогинеколо-гии //Терапевтическая радиология: Руководство для врачей /Под ред. акад. РАМН, проф. А.Ф. Цыба, чл.-корр. РАМН, проф. Ю.С. Мардынского. М.: Медицинская книга, 2010. С. 347-383.
- Замулаева И.А., Матчук О.Н., Селиванова Е.И., Андреев В.Г., Липунов Н.М., Макаренко С.А., Жаворонков Л.П., Саенко А.С. Увеличение количества опухолевых стволовых клеток под воздействием редкоионизирующего излучения //Радиационная биология. Радиоэкология. 2014. Т. 54, № 3. С. 256-264.
- Hirschmann-Jax C., Foster A.E., Wulf G.G., Nuchtern J.G., Jax T.W., Gobel U., Goodell M.A., Brenner M.K. A distinct "side population" of cells with high drug efflux capacity in human tumor cells //Proc. Natl. Acad. Sci. USA. 2004. V. 101, N 39. P. 14228-14233.
- Qi W., Zhao C., Zhao L., Liu N., Li X., Yu W., Wei L. Sorting and identification of side population cells in the human cervical cancer cell line HeLa //Cancer Cell Int. 2014. V. 14, N 1. Article 3.
- Wang K., Zeng J., Luo L., Yang J., Chen J., Li B., Shen K. Identification of a cancer stem cell-like side population in the HeLa human cervical carcinoma cell line //Oncol. Lett. 2013. V. 6, N 6. P. 1673-1680.
- López J., Poitevin A., Mendoza-Martínez V., Pérez-Plasencia C., García-Carrancá A. Cancer-initiating cells derived from established cervical cell lines exhibit stem-cell markers and increased radioresistance //BMC Cancer. 2012. V. 12, N 48. P. 1-14.
- Chhabra R. Cervical cancer stem cells: opportunities and challenges //J. Cancer Res. Clin. Oncol. 2015. V. 141, N 11. P. 1889-1897.
- Phillips T.M., McBride W.H., Pajonk F. The response of CD24(-/low)/CD44+ breast cancer-initiating cells to radiation //J. Natl. Cancer Inst. 2006. V. 98, N 24. P. 1777-1785.
- Lagadec C., Vlashi E., Della Donna L., Meng Y., Dekmezian C., Kim K., Pajonk F. Survival and self-renewing capacity of breast cancer initiating cells during fractionated radiation treatment //Breast Cancer Res. 2010. V. 12, N 1. Article R13.
- Gao X., McDonald J.T., Hlatky L., Enderling H. Acute and fractionated irradiation differentially modulate glioma stem cell division kinetics //Cancer Res. 2013. V. 73, N 5. P. 1481-1490.
- Kim M.J., Kim R.K., Yoon C.H., An S., Hwang S.G., Suh Y., Park M.J., Chung H.Y., Kim I.G., Lee S.J. Importance of PKC6 signaling in fractionated-radiation-induced expansion of glioma-initiating cells and resistance to cancer treatment //J Cell Sci. 2011. V. 124, N 18. P. 3084-3094.
- Kim R.K., Suh Y., Cui Y.H., Hwang E., Lim E.J., Yoo K.C., Lee G.H., Yi J.M., Kang S.G., Lee S.J. Fractionated radiation-induced nitric oxide promotes expansion of glioma stem-like cells //Cancer Sci. 2013. V. 104, N 9. P. 1172-1177.
- Cojoc M., Peitzsch C., Kurth I., Trautmann F., Kunz-Schughart L.A., Telegeev G.D., Stakhovsky E.A., Walker J.R., Simin K., Lyle S., Fuessel S., Erdmann K., Wirth M.P., Krause M., Baumann M., Dubrovska A. Aldehyde dehydrogenase is regulated by ß-catenin/TCF and promotes radioresistance in prostate cancer progenitor cells //Cancer Res. 2015. V. 75, N 7. P. 1482-1494.
- Cho K.J., Park E.J., Kim M.S., Joo Y.H. Characterization of FaDu-R, a radioresistant head and neck cancer cell line, and cancer stem cells //Auris. Nasus. Larynx. 2018. V. 45, N 3. P. 566-573.
- Skvortsov S., Skvortsova I.I., Tang D.G., Dubrovska A. Prostate cancer stem cells: current understanding //Stem Cells. 2018. V. 36, N 10, P. 1457-1474.
- Chaffer C.L., Brueckmann I., Scheel C., Kaestli A.J., Wiggins P.A., Rodrigues L.O., Brooks M., Reinhardt F., Su Y., Polyak K., Arendt L.M., Kuperwasser C., Bierie B., Weinberg R.A. Normal and neoplastic nonstem cells can spontaneously convert to a stem-like state //Proc. Natl. Acad. Sci. USA. 2011. V. 108, N 19. P. 7950-7955.
- Iliopoulos D., Hirsch H.A., Wang G., Struhl K. Inducible formation of breast cancer stem cells and their dynamic equilibrium with non-stem cancer cells via IL6 secretion //Proc. Natl. Acad. Sci. USA. 2011. V. 108, N 4. P. 1397-1402.
- Cabrera M.C., Hollingsworth R.E., Hurt E.M. Cancer stem cell plasticity and tumor hierarchy //World J. Stem Cells. 2015. V. 7, N 1. P. 27-36.
- Li F., Zhou K., Gao L., Zhang B., Li W., Yan W., Song X., Yu H., Wang S., Yu N., Jiang Q. Radiation induces the generation of cancer stem cells: a novel mechanism for cancer radioresistance //Oncol. Lett. 2016. V. 12, N 5. P. 3059-3065.
- Gao X., Sishc B.J., Nelson C.B., Hahnfeldt P., Bailey S.M., Hlatky L. Radiation-induced reprogramming of pre-senescent mammary epithelial cells enriches putative CD44(+)/CD24(-/low) stem cell phenotype //Front Oncol. 2016. N 6. Article 138.
- Lee S.Y., Jeong E.K., Ju M.K., Jeon H.M., Kim M.Y., Kim C.H., Park H.G., Han S.I., Kang H.S. Induction of metastasis, cancer stem cell phenotype and oncogenic metabolism in cancer cells by ionizing radiation //Mol. Cancer. 2017. V. 16, N 1. Article 10.
- Каприн А.Д., Галкин В.Н., Жаворонков Л.П., Иванов В.К., Иванов С.А., Романко Ю.С. Синтез фундаментальных и прикладных исследований - основа обеспечения высокого уровня научных результатов и внедрения их в медицинскую практику //Радиация и риск. 2017. Т. 26, № 2. С. 26-40.


