Комбинированное лечение местнораспространенного рака гортани и гортаноглотки с применением локальной гипертермии
Автор: Чойнзонов Евгений Лхамацыренович, Мухамедов Марат Рафкатович, Старцева Жанна Александровна, Спивакова Ирина Олеговна, Черемисина Ольга Владимировна, Васильев Николай Вольтович, Грибова Ольга Вячеславовна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 6 (72), 2015 года.
Бесплатный доступ
Представлены 2-летние результаты комбинированного лечения 24 больных раком гортани и гортаноглотки III-IV (T3N0-1M0) стадий. На первом этапе всем пациентам проводилась дистанционная лучевая терапия на фоне локальной гипертермии (ЛГ) в качестве радиомодификатора. При выраженной регрессии опухолевого процесса, которая оценивалась на дозе 40,0 Гр, лучевая терапия продолжалась по радикальной программе до СОД 66,0 Гр в сочетании с локальной гипертермией (всего 12 сеансов). Наличие трахеостомы у больных не препятствовало проведению ЛГ. Больным с частичной регрессией или стабилизацией опухолевого процесса (n=19)выполнялся хирургический этап комбинированного лечения, в 36,8 % осуществлены органосохраняющие операции. Морфологическое исследование операционного материала показало, что у 10 (53 %) больных отмечался лечебный патоморфоз IV степени, у 4 (21 %) - III степени. Все больные, включенные в исследование, живы и находятся под динамическим наблюдением от 6 до 29 мес., медиана выживаемости - 13,5 мес. Таким образом, применение локальной гипертермии в качестве радиомодификации лучевой терапии у больных раком гортани и гортаноглотки позволяет улучшить непосредственные результаты лечения, не увеличивая лучевую нагрузку на организм больного.
Рак гортани и гортаноглотки, локальная гипертермия, комбинированное лечение, лечебный патоморфоз, выживаемость
Короткий адрес: https://sciup.org/14056783
IDR: 14056783 | УДК: 616.22+616.321]-006.6-059:615.832
Combined modality treatment including local hyperthermia in patients with locally-advanced laryngeal and laryngopharyngeal cancer
The paper presents two-year results of combined modality treatment of patients with stage III-IV (T3N0-1M0) locally advanced laryngeal and laryngopharyngeal cancer. In the first phase of the treatment, all 24 patients included into the study, received preoperative RT with local hyperthermia. Preventive tracheostoma was not an obstacle for the treatment. Patients who achieved partial response or stable disease underwent surgery. In case of complete tumor regression (n=5), radiotherapy was continued up to the total dose of 66 Gy. Histological examination of surgical specimens revealed complete pathological response in all patients who received combined modality treatment. Regional metastases were revealed in 2 patients, and they subsequently underwent lymph node dissection. The overall 2-year survival rate was 100 % and 2-year metastasis-free survival was 91.7 %.
Текст научной статьи Комбинированное лечение местнораспространенного рака гортани и гортаноглотки с применением локальной гипертермии
Рак гортани и гортаноглотки – социально значимые заболевания, этиологический фактор которых находится в непосредственной связи с табакокурением, употреблением алкоголя, профессиональными вредностями, а также с хроническими воспалительными процессами [7, 10]. В общей структуре заболеваемости злокачественными опухолями рак гортани составляет 1,8–5 %, рак гор-таноглотки – 0,4–1,3 % [1, 2]. При госпитализации более 70 % больных имеют распространенный процесс, что обусловливает трудности лечения данной категории пациентов [4, 6, 7, 12]. Существующие методы лечения имеют низкую эффективность, а расширенные операции зачастую приводят к нарушению питания и дыхания с наличием трахеостомы, к стойкой утрате трудоспособности и оказывают негативное влияние на качество жизни [5, 6, 11].
Все вышеизложенное обосновывает актуальность совершенствования методов лечения местнораспространенного рака гортани и гортаноглотки
[3, 4, 9]. При комбинированном лечении применяются различные модификаторы лучевой терапии, в частности, активно изучаются возможности клинического использования локальной гипертермии (физический модификатор), которая обеспечивает высокую эффективность в сочетании с низкой токсичностью, свойственной цитостатикам, которые в последнее время часто применяются не только при системной химиотерапии, но и в качестве радиосенсибилизаторов. Особый интерес вызывают исследования по применению дистанционной лучевой терапии (ДЛТ) в сочетании с гипертермией, результаты которых свидетельствуют об увеличении радиационного ответа и выраженной регрессии опухоли, а также длительном безреци-дивном периоде [3, 8, 12].
Целью исследования явилось изучение влияния локальной гипертермии на регрессию опухоли при неоадъювантной лучевой терапии у больных местнораспространенным раком гортани и гортаноглотки.
Материал и методы
В исследование включено 24 больных с морфологически верифицированным раком гортани и гортаноглотки III–IV (T3N0–1M0) стадий, получавших лечение в отделении опухолей головы и шеи Томского НИИ онкологии за период с 2012 по 2015 г. Критерием включения в исследование являлись рак гортани/гортаноглотки у пациентов, давших информированное согласие на участие в проспективном контролируемом наблюдении. Стадия заболевания оценивалась согласно международной классификации по системе TNM (7-е издание AJCC, 2009 г.). Критерии исключения: стеноз гортани III–IV степени, хондроперихондрит и деструкция хрящей гортани.
У 5 (21 %) больных был диагностирован рак гортаноглотки, у 19 (79 %) – рак гортани. Распределение по полу: мужчины – 22 (91,6 %), женщины – 2 (8,4 %) больных. Возраст пациентов – 39–70 лет, в среднем – 57,83 ± 1,39 года. Высокодифференцированный плоскоклеточный рак был верифицирован у 3 (12,5 %), умереннодифференцированный – у 17 (70,8 %), низкодифференцированный – у 4 (16,7 %) пациентов. До начала лечения всем больным проводилось комплексное клиническое обследование, которое включало: общеклинические анализы, видеоларингоскопию с биопсией, СКТ с контрастированием, рентгенографию легких, УЗИ шеи, щитовидной железы и органов брюшной полости, цитологическое и гистологическое исследование биопсийного материала.
Больные получали курс ДЛТ до СОД 40 Гр в стандартном режиме фракционирования дозы (РОД 2,0 Гр 5 раз в нед), на фоне радиосенсибилизации локальной гипертермией (ЛГ). Сеансы проводились на гипертермической системе Celsius TCS, 2 раза в нед, продолжительностью 60 мин, при температуре 42–44°С, количество сеансов – 8, начиная с первого дня лучевой терапии.
До начала лечения и при наборе больными СОД 40 Гр всем пациентам выполнялось эндоскопическое исследование гортани с видеозаписью видеоэндоскопами фирмы «Olympus». Оценивались границы опухолевого процесса, сосудистый рисунок, площадь и объем экзофита, характер поражения (тип роста опухоли), распространение опухоли на структуры гортани и сопутствующие хронические изменения слизистых оболочек. В 14 случаях процесс имел экзофитную, в 7 – смешанную, в 3 – инфильтративную форму роста. Эффект от лечения лучевой терапии в сочетании с локальной гипертермией оценивался согласно критериям RECIST. Больным, эффект лечения которых оценен как «частичная регрессия» и «стабилизация», проводился второй этап комбинированного лечения – оперативное вмешательство. Пациентам, у которых наблюдалась полная регрессия опухолевого процесса на дозе 40 Гр, была продолжена дистанционная лучевая терапия до СОД 66 Гр, с локальной гипертермии – 12 сеансов.
Результаты и обсуждение
Исследование показало хорошую переносимость физического радиосенсибилизатора лучевой терапии при фактическом отсутствии побочных эффектов. Ни в одном случае не было отмечено дискомфорта или непереносимости при локальной гипертермии. Наличие превентивной трахеостомы у 2 больных раком гортани T3N0–1M0 стадии не препятствовало проведению сеансов ЛГ.
При контрольном обследовании, при наборе больными СОД 40 Гр и 8 сеансов локальной гипертермии, по данным видеоларингоскопии у 6 (25 %) пациентов наблюдалась полная клиническая регрессия опухоли, им была продолжена лучевая терапия по радикальной программе до СОД 60–66 Гр и дополнительно проведено еще 4 сеанса ЛГ.
В группе больных, эффект лечения которых оценен как «частичная регрессия», – 15 (62,5 ± 5,8 %) и «стабилизация процесса» – 4 (16,7 ± 4,2 %), вторым этапом комбинированного лечения выполнено хирургическое вмешательство, из них у 12 (63 ± 5,1 %) – в объеме органосохраняющих операций, из них 5 больным выполнена фронтолатеральная резекция гортани, 6 пациентам – гемиларингэктомия, в 1 случае – резекция грушевидного синуса. Операции большего объема выполнены 7 (37 ± 5,8 %) пациентам, в том числе комбинированные ларингэктомии с формированием трахео-глоточного шунта – 4, ларингэктомии – 3 больным. Необходимо заметить, что хирургический этап комбинированного лечения не сопровождался какими-либо техническими трудностями, связанными с предыдущей термолучевой терапией.
Весьма показательными оказались результаты морфологического изучения операционного материала у больных, получивших комбинированное лечение. Так, по результатам морфологического исследования в 10 (53 %) случаях отмечался лечебный патоморфоз IV степени, в 4 (21 %) – лечебный патоморфоз III степени. У 6 (25 %) больных, получавших радикальный курс лучевой терапии на фоне 12 сеансов ЛГ, при контрольном обследовании зарегистрирована полная, морфологически подтвержденная регрессия опухоли.
Все больные, включенные в исследование, живы и находятся под динамическим наблюдением от 6 до 29 мес, медиана – 13,5 мес. При контрольном обследовании, проведенном через 6 мес после завершения комбинированного лечения, у 2 больных раком гортани T3N0–1M0 стадии, получивших в одном случае органосохраняющее лечение в объеме гемиларингэктомии и в другом случае – ларингэктомии, наблюдалось прогрессирование заболевания в виде метастатического поражения регионарных лимфоузлов. Этим пациентам была выполнена лимфодиссекция шеи. При контроле через 12 и 24 мес данных за прогрессирование или рецидив заболевания не получено. Общая кумулятивная 2-летняя выживаемость составила 100 %, безрецидивная кумулятивная 2-летняя выживаемость – 91,7 ± 5,9 %.
Заключение
Анализируя результаты лечения больных, получивших комбинированное лечение, мы отметили, что сочетание локальной гипертермии с лучевой терапией на предоперационном этапе не вызывает существенных осложнений ни во время выполнения оперативного вмешательства, ни в послеоперационном периоде.
Разработанная оригинальная методика радикального и предоперационного курсов лучевой терапии на фоне локальной гипертермии у больных раком гортани и гортаноглотки позволяет улучшить непосредственные результаты лечения, не увеличивая лучевую нагрузку. При этом удалось значимо увеличить количество случаев с выраженными явлениями терапевтического патоморфоза (III–IV степени), что является достаточно объективной оценкой предложенной методики лечения. Клинические исследования по применению локальной гипертермии в сочетании с лучевой терапией при лечении больных раком гортани и гортаноглотки продолжаются.
Для подтверждения эффективности разработанной методики комбинированного лечения, с применением предоперационной лучевой терапии на фоне локальной гипертермии у больных местнораспространенным раком гортани и гортаноглотки T1–3N0–1M0 и выполнения органосохраняющих операций приводим следующее клиническое наблюдение.
Больная Б., 39 лет, диагноз: Рак гортаноглот-ки T3N0M0 стадии (гистологическое заключение (№ 32555–59, от 10.12.2013): плоскоклеточный рак умеренной степени дифференцировки), обратилась с жалобами на комок в горле при глотании в декабре 2013 г.
При обследовании, по данным ультразвукового исследования шеи признаков метастатического поражения лимфатических узлов не получено. По данным видеоларингоскопии выявлено, что голосовая щель симметрична, при фонации полностью смыкается. На правой черпало-надгортанной связке визуализируется бугристая, тугоэластическая ткань. Аналогичные участки определяются в правом грушевидном синусе. Подскладочный отдел свободен (рис. 1). По данным СКТ отмечается утолщение и деформация правой черпалонадгортанной складки с признаками накопления контрастного вещества, кроме того, изменения аналогичного характера имеются в передней и латеральной стенках правого грушевидного синуса, вплоть до его вершины, просвет синуса сужен (рис. 2).
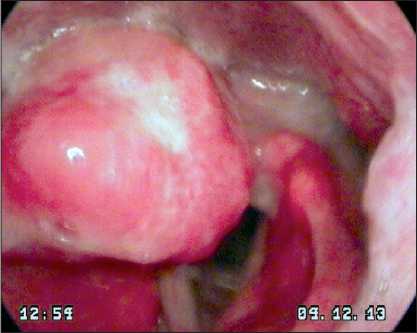
Рис. 1. Эндофото. Видеоларингоскопия до начала лечения. Определяется экзофитная опухоль, замещающая правую черпало-надгортанную связку
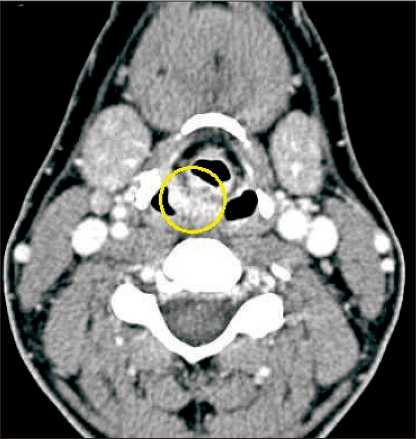
Рис. 2. СКТ-скан до начала лечения. Объемное образование в проекции правой черпало-надгортанной связки
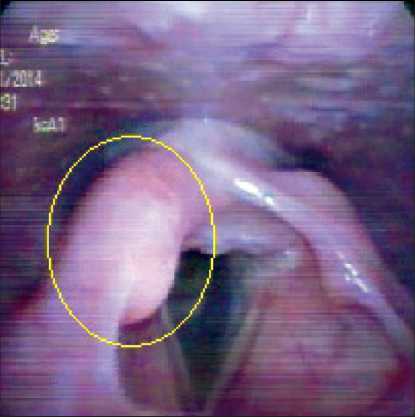
Рис. 3. Эндофото. Контрольная видеоларингоскопия после проведения дистанционной гамма-терапии СОД 40 Гр и 8 сеансов локальной гипертермии. Частичная регрессия опухоли
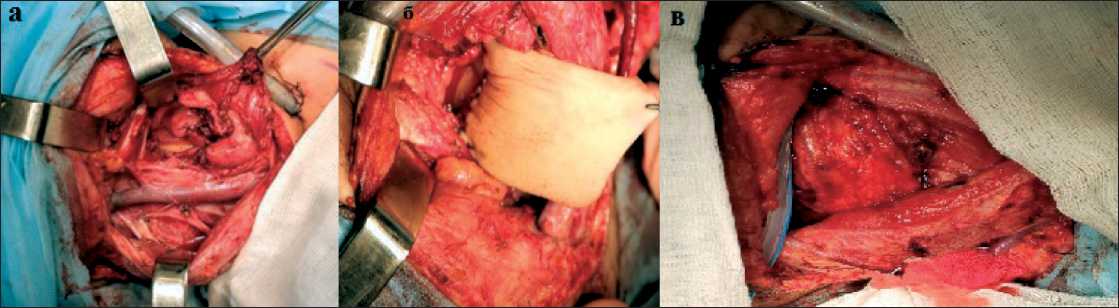
Рис. 4. Этапы оперативного вмешательства: а – лимфодиссекция шеи и резекция гортаноглотки справа, б – пластика грушевидного синуса, в – укрытие дефекта мышцами
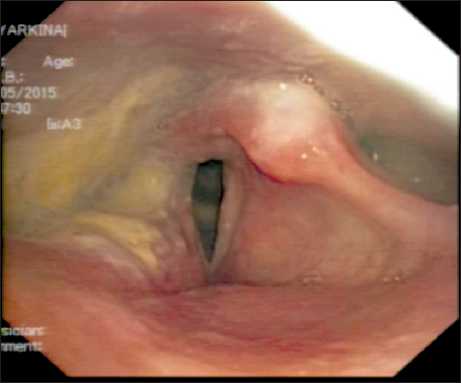
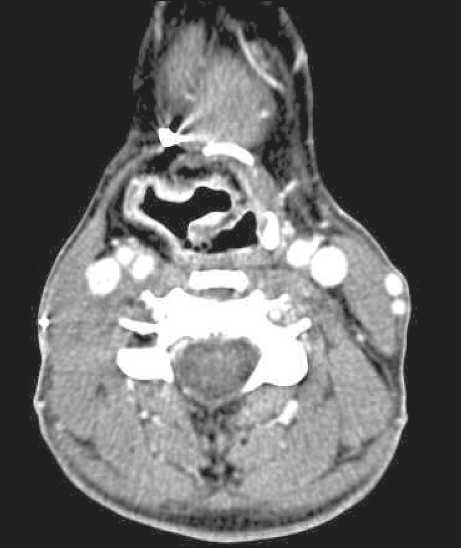
Рис. 6. СКТ-скан, контрольное обследование через 18 мес после завершения лечения. Признаков рецидива нет
Рис. 5 . Эндофото. Видеоларингоскопия через 18 мес после завершения лечения. Признаков рецидива нет
При контрольном обследовании, по достижении СОД 40 Гр и 8 сеансов ЛГ, эффект проводимого лечения расценен как частичная регрессия опухоли (рис. 3). Согласно дизайну исследования, больной был проведен второй этап комбинированного лечения – выполнена операция в объеме трахеостомии, лимфодиссекции шеи справа, резекции гортаноглотки справа, пластики дефекта луче- вым лоскутом (рис. 4). Послеоперационный период протекал без осложнений.
Пациентка находится под динамическим наблюдением, сохранена полная социальная и трудовая адаптация. По данным контрольного обследования через 18 мес после завершения комбинированного лечения признаков прогрессирования заболевания не выявлено (рис. 5, 6).
Список литературы Комбинированное лечение местнораспространенного рака гортани и гортаноглотки с применением локальной гипертермии
- Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2012 году (заболеваемость и смертность). М., 2014. 250 с.
- Кицманюк З.Д., Чойнзонов Е.Л., Мусабаева Л.И., Новиков В.А. Тактика лечения рака гортани на современном этапе//Сибирский онкологический журнал. 2003. № 2. С. 3-11.
- Мухамедов М.Р., Чойнзонов Е.Л., Гюнтер В.Э., Черемисина О.В., Лукьянов В.Д., Мядзель А.А., Шинкарев С.А., Коренев А.А., Васильев Н.В., Цветаев В.А., Кульбакин Д.Е. Использование биоадаптированных имплантатов на основе никелида титана в хирургической реабилитации больных раком гортани (результаты десятилетнего кооперированного исследования//Вестник РОНЦ им. Н. Н. Блохина РАМН. 2010. Т. 21, № 1. С. 65-70.
- Подвязников С.О., Чойнзонов Е.Л., Кропотов М.А., Кожанов Л.Г., Пустынский И.Н., Письменный В.И., Алиева С.Б., Акетова Т.А., Таболиновская Т.Д. Диагностика и лечение рака гортаноглотки. Клинические рекомендации//Сибирский онкологический журнал. 2014. № 6. С. 71-75.
- Чижевская С.Ю., Чойнзонов Е.Л., Балацкая Л.Н. Качество жизни больных раком гортани и гортаноглотки на этапах комбинированного лечения и в отдаленные сроки//Сибирский онкологический журнал. 2015. № 2. С. 15-22.
- Чижевская С.Ю., Чойнзонов Е.Л. Современные возможности и перспективы комбинированного лечения рака гортани и гортаноглотки//Сибирский онкологический журнал. 2007. № 4. С. 127-132.
- Чойнзонов Е.Л., Старцева Ж.А., Мухамедов М.Р., Спивакова И.О., Черемисина О.В., Грибова О.В., Кульбакин Д.Е., Суркова П.В. Локальная гипертермия в комбинированном лечении рака гортани и гортаноглотки//Сибирский онкологический журнал. 2014. № 5. С. 5-12.
- Чойнзонов Е.Л., Балацкая Л.Н., Мухамедов М.Р. Рак гортани. Современные аспекты лечения и реабилитации. Томск, 2006. 280 с.
- Чойнзонов Е.Л., Балацкая Л.Н. Качество жизни онкологических больных. Томск, 2011. 152 с.
- Genden E.M., Ferlito A., Rinaldo A., Silver C.E., Fagan J.J., Suárez C., Langendijk J.A., Lefebvre J.L., Bradley P.J., Leemans C.R., Chen A.Y., Jose J., Wolf G.T. Recent changes in the treatment of patients with advanced laryngeal cancer//Head Neck. 2008. Vol. 30 (1). P. 103-110.
- Nakahara R., Kodaira T., Furutani K., Tachibana H., Tomita N., Inokuchi H., Mizoguchi N., Goto Y., Ito Y., Naganawa S. Treatment outcomes of definitive chemoradiotherapy for patients with hypopharyngeal cancer//J. Radiat. Res. 2012. Vol. 53 (6). P. 906-915 DOI: 10.1093/jrr/rrs052


