Компьютерное предсказание патогенных свойств мутантов белка SOD1, ассоциированных с боковым амиотрофическим склерозом
Автор: Алемасов Н.А., Иванисенко Н.В., Иванисенко В.А.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Биологические науки
Статья в выпуске: 10-1 (25), 2018 года.
Бесплатный доступ
Внутриклеточная агрегация белков является одной из причин многих нейродегенеративных заболеваний. В частности, мутации в гене SOD1 связаны с наследственной формой бокового амиотрофического склероза (БАС). Ранее нами была предложена регрессионная модель, предсказывающая дожитие пациентов с БАС, которые являются носителями мутаций в белке SOD1. Эта модель была построена на основе анализа стабильности водородных связей, возникающих в мутантах SOD1 при моделировании методом молекулярной динамики (МД). В настоящей работе данная регрессионная модель была улучшена с помощью учёта новой характеристики водородных связей, отражающей показатель консервативности водородной связи в пространстве конформационных состояний белка. Расчёт конформационной консервативности водородных связей, осуществлённый с помощью эластичных сетевых (ЭС) моделей позволил увеличить коэффициент корреляции между предсказанными с помощью новой модели и наблюдаемыми значениями дожития пациентов с мутациями в SOD1 (R = 0.92).
Боковой амиотрофический склероз, водородные связи, регрессионные модели, молекулярная динамика, эластичные сетевые модели
Короткий адрес: https://sciup.org/170184758
IDR: 170184758 | DOI: 10.24411/2500-1000-2018-10053
Computational prediction of pathogenic properties of SOD1 mutants which are associated with amyotrophic lateral sclerosis
Intracellular protein aggregation is one of the causes of many neurodegenerative diseases. In particular, mutations in the SOD1 gene are associated with the familial form of amyotrophic lateral sclerosis (ALS). We have previously proposed a regression model that predicts the survival of patients with ALS who are carriers of mutations in the SOD1 protein. This model was built on the basis of the analysis of the stability of hydrogen bonds forming in SOD1 mutants when simulated by the molecular dynamics (MD). In the present work, this regression model has been improved by taking into account the new characteristic of hydrogen bonds, reflecting the conservativeness index of the hydrogen bond in the space of conformational states of the protein. The calculation of conformational conservatism of hydrogen bonds, carried out using elastic network (EN) models, made it possible to increase the correlation coefficient between the predicted using the new model and the observed survival values of patients with mutations in SOD1 (R = 0.92).
Текст научной статьи Компьютерное предсказание патогенных свойств мутантов белка SOD1, ассоциированных с боковым амиотрофическим склерозом
Боковой амиотрофический склероз (БАС) – неизлечимое нейродегенеративное заболевание. Выделяется две его формы: наследственная и спорадическая [1]. Известно, что второй по распространённости и наиболее изученной причиной наследственной формы БАС являются мутации в гене SOD1, кодирующем фермент супер-оксиддисмутазу-1 [2]. Одной из гипотез относительно механизма возникновения заболевания на молекулярном уровне является агрегация белка SOD1, вызванная его неверной укладкой в результате мутаций [2].
Известно, что водородные связи играют важную роль, в частности, в поддержании структуры белков [3]. В одном из in silico исследований структуры и динамики SOD1 уже анализировались водородные связи и сеть, которую они образуют в этом белке [4]. Ранее нами с помощью метода молекулярной динамики (МД) было исследовано 39 мутаций в белке SOD1 [5]. Были обнаружены водородные связи, доля времени существования которых в траектории МД (или стабильность) достоверно коррелирует с дожитием пациентов с БАС. На основе найденных водородных связей была построена регрессионная модель, позволяющая предсказать дожитие пациентов с мутациями в SOD1.
Настоящее исследование направлено на расширение ранее созданной модели с учётом крупномасштабной динамики белка SOD1. Для этого проведено моделирование динамики структуры белка с использованием эластичных сетевых моделей (ЭС) [6]. На основе результатов анализа структуры и динамики мутантов SOD1 предложена комплексная регрессионная модель, учитывающая как конформации, полученные с помощью МД, так и конформации, полученных в данной работе с помощью ЭС. Для построения регрессионной модели проводился расчёт конформационной консервативности водородных связей, как отношение числа конформаций, в которых связь присутствовала, к общему числу полученных в ЭС конформаций. Анализ конформационной консервативности водородных связей, позволил улучшить точность расширенной модели по сравнению с ранее созданной моделью. Коэффициент корреляции между предсказанными и наблюдаемыми значениями дожития пациентов, носителей мутаций в SOD1, составил R = 0.92.
Материалы и методы
В работе исследована структура белка SOD1 дикого типа и 35 его мутантных форм, взятые из базы данных ALSOD . Получение пространственных структур мутантных белков SOD1 производилось с помощью моделирования мутаций в структуре PDBID 2V0A с использованием FoldX [7]. Проверка и исправление полученных структур мутантов, включая удаление клэшей и исправление неоптимальных конформаций также проводилась с использованием FoldX.
Построение ЭС для белка дикого типа и его мутантов проводилось с помощью системы ElNemo с параметрами по- умолчанию [8]. В рамках каждой такой модели был получен ансамбль из 11 конформаций для каждой из 5 нетривиальных мод колебаний с наивысшим показателем коллективности. Таким образом, для белка дикого типа и каждого из изучаемых мутантов были рассчитаны 55 конформаций, представляющих крупномасштабные флуктуации структуры этих молекул. С помощью пакета программ AMBER [9] структура, соответствующая каждой конформации впоследствии минимизировалась с целью избежать физически недостижимых торсионных углов, длин связей и других параметров SOD1.
Водородные связи в каждой из 55 конформаций белка находились с помощью утилиты cpptraj из пакета программ AMBER. Статистический анализ стабильности водородных связей проводился с помощью библиотек numpy, scipy и sklearn для языка Python.
Результаты и обсуждение
Следует заметить, что характер движений атомов молекул в моделях ЭС и МД различается. Различия состоят в том, что в моделировании ЭС все конформации молекулы отличаются и соответствуют позициям атомов вдоль выбранной моды колебаний в некоторый промежуток времени. В МД атомы движутся неподалёку от некоторого локального минимума и могут принимать одну и ту же конформацию не один раз. По этой причине доля существования водородной связи среди конформаций белка в ЭС названа конформационной консервативностью, в то время как в нашей предыдущей работе [5] доля конформаций белка в траектории МД, в которых связь была сформирована называлась стабильностью.
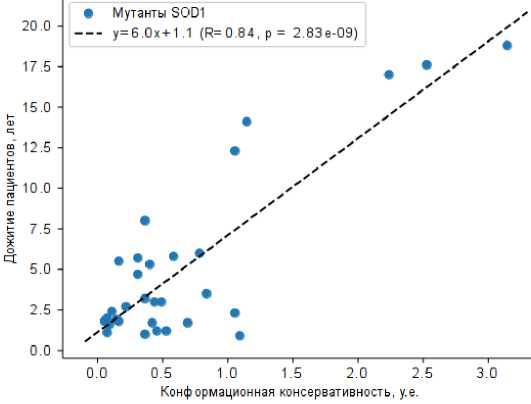
Рис. 1. Корреляция между функцией конформационной консервативности водородных связей, найденных в рамках моделирования эластичных сетей для мутантов SOD1 и дожитием пациентов с БАС – носителей соответствующих мутациями в белке.
Показатель, характеризующий патогенность водородных связей в МД рассчитывался с помощью суммарной стабильности Om,K, описанной нами ранее в работе [5]. Для оценки патогенности водородных связей в ЭС применялась суммарная конформационная консервативность Cu,N, которая рассчитывается на основе
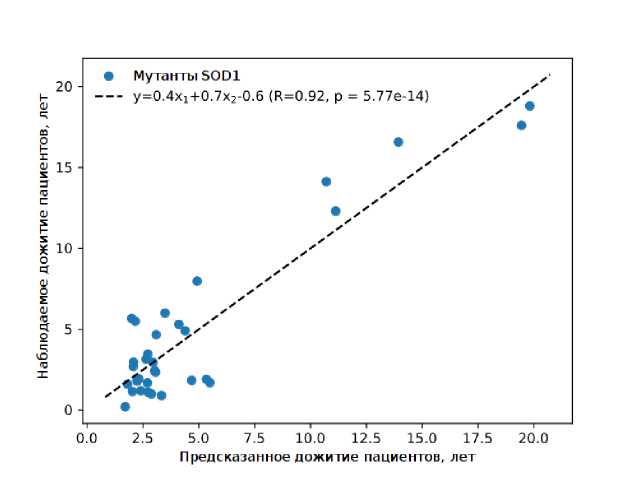
Рис. 2. Корреляция между предсказанным временем жизни пациентов с БАС с мутациями в SOD1, полученным с помощью двухфакторной линейной регрессии на основе конформационной консервативности патологичных водородных связей в ЭС и стабильностей патологичных водородных связей в МД
конформационной консервативности отдельных водородных связей аналогично Om,K. Регрессионная модель включала два независимых фактора – Om,K и Cu,N.
Коэффициент корреляции между функцией конформационной консервативности Cu,N и дожитием пациентов с мутациями в SOD1 составил R = 0.84 (p = 2.8*10-9) (см. рис. 1).
Конформационная консервативность и стабильность водородных связей, соответственно, в ЭС и МД являются различными по своей природе. Поэтому на основе данных двух независимых характеристик была построена множественная регрессия. Коэффициент корреляции для данной регрессии оказался выше (R = 0.92, p = 5.8*10-14), чем для регрессий на основе каждого из параметров в отдельности (см. рис. 2). Таким образом, комбинация результатов моделирования ЭС и МД позволила получить более точную регрессионную модель для предсказания дожития пациентов с мутациями в SOD1, страдающих БАС.
Заключение
Учёт показателя консервативности водородных связей в пространстве конформационных состояний белка SOD1
позволил улучшить созданную ранее модель, которая была построена на использовании информации о стабильности водородных связей. Коэффициент корреляции между предсказанными с помощью новой модели и наблюдаемыми значениями дожития пациентов с мутациями в SOD1 составил R = 0.92, что позволяет объяснить более 84% (R2 = 0,846) дисперсии в дожитии пациентов, носителей рассматриваемых мутаций в SOD1.
Список литературы Компьютерное предсказание патогенных свойств мутантов белка SOD1, ассоциированных с боковым амиотрофическим склерозом
- Kiernan M.C. et al. Amyotrophic lateral sclerosis // Lancet. 2011. Vol. 377. №9769. P. 942-955.
- Tokuda E., Furukawa Y. Copper Homeostasis as a Therapeutic Target in Amyotrophic Lateral Sclerosis with SOD1 Mutations // Int. J. Mol. Sci. Multidisciplinary Digital Publishing Institute, 2016. Vol. 17, № 5. P. 636.
- Fernández A., Scheraga H.A. Insufficiently dehydrated hydrogen bonds as determinants of protein interactions. // Proc. Natl. Acad. Sci. U. S. A. 2003. Vol. 100, № 1. P. 113-118.
- Khare S.D., Dokholyan N. V. Common dynamical signatures of familial amyotrophic lateral sclerosis-associated structurally diverse Cu, Zn superoxide dismutase mutants. // Proc. Natl. Acad. Sci. U. S. A. 2006. Vol. 103, № 9. P. 3147-3152.
- Alemasov N.A. et al. Dynamic properties of SOD1 mutants can predict survival time of patients carrying familial amyotrophic lateral sclerosis // J. Biomol. Struct. Dyn. Taylor & Francis, 2017. Vol. 35, № 3. P. 645-656.
- Tirion M. Large Amplitude Elastic Motions in Proteins from a Single-Parameter, Atomic Analysis. // Phys. Rev. Lett. American Physical Society, 1996. Vol. 77, № 9. P. 1905-1908.
- Guerois R., Nielsen J.E., Serrano L. Predicting Changes in the Stability of Proteins and Protein Complexes: A Study of More Than 1000 Mutations // J. Mol. Biol. 2002. Vol. 320, № 2. P. 369-387.
- Suhre K., Sanejouand Y.-H. ElNemo: a normal mode web server for protein movement analysis and the generation of templates for molecular replacement. // Nucleic Acids Res. Oxford University Press, 2004. Vol. 32, № Web Server issue. P. W610-4.
- Salomon-Ferrer R., Case D.A., Walker R.C. An overview of the Amber biomolecular simulation package // Wiley Interdiscip. Rev. Comput. Mol. Sci. 2013. Vol. 3, № 2. P. 198-210.


