Комплексная иммуно-гормональная оценка риска возникновения рака молочной железы у женщин в постменопаузе
Автор: Глушков А.Н., Поленок Е.Г., Гуров Е.А., Гордеева Л.А., Мун С.А., Костянко М.В., Студенников А.Е., Елисейкин А.М., Захаров В.Н., Антонов А.В., Байрамов П.В., Вержбицкая Н.Е., Колпинский Г.И.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 6 т.24, 2025 года.
Бесплатный доступ
Цель исследования – определение индивидуальных комбинаций содержания в сыворотке крови эстрадиола и прогестерона (Е2 и Pg), антител классов А и G против Bp, E2 и Pg, и антиидиотипических антител класса G к E2 и Pg, значимо ассоциированных с возникновением рака молочной железы (РМЖ) у женщин в постменопаузе. Материал и методы. Обследовались 763 некурящие женщины: 206 здоровых и 557 больных РМЖ І стадии до начала лечения. Содержание в сыворотке гормонов и антител определяли с помощью конкурентного и неконкурентного иммуноферментных методов соответственно. CART-анализ (Classification and Regression Trees) полученных результатов выполняли с помощью программы Statistica 13.0. Результаты. Определены 7 групп в дереве решений по индивидуальным комбинациям IgG2-E2, E2, IgA1-E2, Pg и IgG1-Bp, значимо ассоциированным с риском РМЖ. Высокие уровни E2 в комбинации с высокими уровнями IgG1-Bp чаще обнаруживали у больных РМЖ, чем у здоровых женщин (54,2 vs 26,7 %; p<0,001; OR=3,3 [2,3–4,7]), так же как и низкие уровни Pg в комбинации с низкими уровнями IgG1-Bp и со средними уровнями IgG2-E2 (9,9 vs 3,9 %; p=0,01; OR=2,7 [1,3–5,8]). В остальных 5 группах различные комбинации высоких и низких уровней исследованных факторов встречались чаще (72,4 %) у здоровых женщин, чем у больных РМЖ (36,4%). Содержание в сыворотке E2 и Pg не связано с уровнями исследованных антител и анти-антител. Уровни антиидиотипических антител не коррелировали с уровнями соответствующих идиотипических антител. Заключение. Влияние E2 и Pg на возникновение РМЖ проявлялось только в комбинациях с IgG2-E2, IgA1-E2 и IgG1-Bp. Анализ антител против E2, Pg и Bp и соответствующих анти-антител рекомендуется для исследования иммунологических механизмов возникновения химически индуцированных гормонозависимых опухолей у человека.
Антитела, эстрадиол, прогестерон, бензо[а]пирен, рак молочной железы
Короткий адрес: https://sciup.org/140313327
IDR: 140313327 | УДК: 618.19-006:616-097.3:577.17 | DOI: 10.21294/1814-4861-2025-24-6-70-81
Comprehensive immuno-hormonal assessment of the risk of breast cancer in postmenopauseal women
The study aimed to determine the personal combinations of blood serum estradiol and progesterone (E2 and Pg), classes A and G antibodies against E2, Pg and Benzo[a]pyrene (IgA1-E2, IgA1-Pg, IgA1-Bp; IgG1-E2, IgG1-Pg, IgG1-Bp), class G antiidiotypic antibodies to E2 and Pg (IgG2-E2, IgG2-Pg) levels associated with breast cancer in postmenopausal women. Material and Methods. There were investigated 763 nonsmoking women: 206 healthy and 557 breast cancer patients (BCP) with I stage BC before treatment. The blood serum levels of hormones and antibodies were studied using competitive and non-competitive enzyme immunoassay, respectively. Statistical analysis of the results was performed using Statistica 13.0 Software, Classification and Regression Trees (CART-analysis). Results. There were revealed 7 groups according to personal combinations of IgG2-E2, E2, IgA1-E2, Pg, and IgG1-Bp associated with BC risk. High E2 levels in combination with high IgG1-Bp levels were revealed in 54.2 % of BCP vs 26.7 % of healthy women (p<0.001; OR=3.3 [2.3–4.7]). Low Pg levels in combination with low IgG1-Bp levels and average IgG2-E2 levels were more often found in BCP than in healthy women (9.9 % vs 3.9 %; p=0.01; OR=2.7 [1.3–5.8]. The various combinations of high and low levels of studied factors in others 5 groups were found in 72.4 % of healthy women and in 36.4 % of BCP. Concentrations of E2 and Pg were not correlated with studied antibodies and anti-antibodies levels. Levels of antiidiotypic antibodies were not associated with corresponding idiotypic antibodies. Conclusion. The effect of E2 and Pg on breast cancer development was demonstrated only in combination with IgG2-E2, IgA1-E2, and IgG1-Bp. Immunoassay of antibodies and antiantibodies to E2, Pg and Bp is recommended for research of chemical induced hormone-depended human carcinogenesis.
Текст научной статьи Комплексная иммуно-гормональная оценка риска возникновения рака молочной железы у женщин в постменопаузе
Рак молочной железы (РМЖ) остается основной онкологической патологией женского населения РФ и других стран [1, 2]. Несмотря на рост заболеваемости, смертность от РМЖ снижается благодаря ее раннему выявлению и повышению эффективности лечения. Для снижения заболеваемости продолжается поиск медикаментозных средств профилактики РМЖ, в частности среди селективных модуляторов эстрогеновых рецепторов и ингибиторов ароматазы [3–6]. Одной из основных проблем, сдерживающих развитие этого направления, является отсутствие надежных показаний для их применения у здоровых женщин – информативных критериев риска возникновения РМЖ. Использование таких критериев позволило бы повысить эффективность раннего выявления РМЖ и снизить заболеваемость благодаря на- значению химиопрофилактических средств при минимизации осложнений. В случаях семейного РМЖ рекомендуется анализ мутаций в генах BRCA1, BRCA2, PLB2, CHEK2, ATM [7] наряду с оценкой образа жизни, гормонального статуса, денситометрией молочной железы и других факторов. Для мультифакторных РМЖ необходимы дополнительные фенотипические предикторы.
Основанием для поиска таких предикторов являлись хорошо известные данные о ключевом значении в канцерогенезе молочной железы генотоксических метаболитов химических канцерогенов окружающей среды, в частности бензо[а] пирена (Bp) и эндогенного эстрадиола (E2). Обнаружены ассоциации образования ДНК-аддуктов этих низкомолекулярных соединений с риском возникновения РМЖ [8–12]. Будучи ковалентно связанными с макромолекулярными носителями, метаболиты Bp и E2 становятся гаптенами, способными индуцировать синтез соответствующих специфических антител. У больных РМЖ обнаружены повышенные уровни антител против Bp и E2 по сравнению со здоровыми женщинами [13].
Вместе с тем, известны взаимоусиливающие эффекты Bp и E2 на клетки молочной железы. Некоторые метаболиты Bp проявляли эстрогеновую или антиэстрогеновую активность, в частности, индуцировали или угнетали активность β-галактозидазы, связываясь с ER [14]. E2 стимулировал образование Bp-ДНК аддуктов в ER экспрессирующих клетках линии MCF-7 при их обработке совместно с Bp [15]. Нами обнаружены прямые корреляции между уровнями антител против Bp и E2 в сыворотке здоровых женщин и больных РМЖ, однако одновременно высокие их уровни встречались чаще у больных РМЖ, чем у здоровых лиц [16]. Очевидно, совместные специфичные иммунные реакции на указанные соединения отражают их участие в канцерогенезе молочной железы и одновременное образование ДНК-аддуктов с Bp и E2.
В сыворотке больных РМЖ выявлены антитела против рецепторов ERα в больших количествах, чем у здоровых женщин [17], а также антиидиоти-пические антитела, специфичные к моноклональным антителам против E2 и Pg, модулирующие содержание этих гормонов у здоровых женщин больше, чем у больных РМЖ [18].
Таким образом, в работах показано потенциальное значение антител против Bp, E2 и Pg, а также антиидиотипических анти-антител к E2 и Pg в определении риска возникновения РМЖ. Однако при этом антитела разных классов иммуноглобулинов описаны по отдельности; не учитывалось участие самих гормонов в совокупности с антителами в индукции РМЖ; проводилось сравнение здоровых женщин со всей когортой больных РМЖ, а не с больными в начальных стадиях опухолевого роста, что было не совсем корректно в поисках информативных предикторов РМЖ. Очевидно, что результирующая оценка взаимосвязей перечисленных факторов с риском возникновения РМЖ зависит от индивидуальных комбинаций их содержания в сыворотке крови здоровых женщин. При одновременном участии в канцерогенезе молочной железы стимулирующее или угнетающее действие одних может нивелироваться или усиливаться влиянием других. В итоге комбинации только некоторых из исследуемых факторов могут оказаться значимо ассоциированными с риском РМЖ.
Для оценки комбинированного влияния стероидных гормонов, идиотипических и антиидиотипи-ческих гормон-специфических антител и антител против химических канцерогенов окружающей среды целесообразно обследовать здоровых и больных РМЖ в постменопаузе, чтобы исключить циклические колебания гормонального статуса, и использовать CART-анализ (Classification and Regression Trees Analysis), применяемый в онкологии для решения подобных диагностических задач [19].
Цель исследования – определение индивидуальных комбинаций содержания в сыворотке крови E2 и Pg; антител классов A и G против Bp, E2 и Pg; антиидиотипических антител класса G к E2 и P, значимо ассоциированных с возникновением РМЖ у женщин в постменопаузе.
Материал и методы
Исследовали сыворотку крови 763 некурящих женщин в постменопаузе. Из них 206 условно здоровых женщин, составивших группу сравнения (возраст – 57,7 ± 5,8 года), и 557 женщин, больных РМЖ I стадии (возраст – 65,6 ± 8,0 лет). Все женщины исследуемой группы поступали в Кузбасский онкологический диспансер, г. Кемерово, с первично установленным диагнозом: Инвазивная карцинома молочной железы неспецифического типа. При дальнейшем обследовании у них были выявлены следующие молекулярно-биологические подтипы РМЖ: люминальный А – 48,7 %, люминальный В HER2 отрицательный – 40,9 %, люминальный В HER2 положительный – 1,4 %, HER2 положительный нелюминальный – 0,7 %, трижды негативный фенотип – 7,4 %. Все больные ранее не получали специального противоопухолевого лечения, в том числе гормонотерапию. В группу сравнения были отобраны женщины по следующим критериям: отсутствие какого-либо злокачественного новообразования, патологии молочной железы, некурящие, проживающие на территории Кемеровской области.
Содержание в сыворотке стероидных гормонов определяли с помощью коммерческих наборов «ИммуноФА-Эстрадиол», «ИммуноФА-ПГ» («Иммунотех», г. Москва) согласно инструкциям. Идиотипические антитела классов A и G против Bp, E2 и Pg (IgА1-Bp, IgА1-E2, IgА1-Pg, IgG1-Bp, IgG1-E2, IgG1-Pg) исследовали с помощью ELISA [20], используя адсорбированные на пластике конъюгаты указанных гаптенов с бычьим сывороточным альбумином и проявляя связавшиеся иммуноглобулины козьими антителами против IgА и IgG человека, меченными пероксидазой хрена (Invitrogen, США). Антиидиотипические антитела класса G, специфичные к E2 и Pg (IgG2-E2, IgG2-Pg), определяли с помощью ELISA [20], используя адсорбированные на пластике моноклональные антитела против E2 и Pg в наборах «ИммуноФА-Эстрадиол», «ИммуноФА-ПГ» («Иммунотех», г. Москва) в качестве антигенов и пероксидазные конъюгаты козьих антител против IgG человека. В представленной работе не исследовали содержание в сыворотке крови других иммунологических факторов, потенциально участвующих в канцерогенезе молочной железы: антиидиотипических антител к Вр (IgА2-Bp и IgG2-Bp) и антиидиотипических антител класса А к E2 и Pg (IgА2-E2 и IgА2-Pg).
Полученные результаты обрабатывали с помощью программы Statistica 13.0 (StatSoft Inc., USA). В базу данных были внесены показатели уровней исследованных антител (условные единицы, у.е.) и содержание гормонов (pmol/L) от здоровых женщин и больных РМЖ. Наблюдаемый дисбаланс выборок (соотношение 1:2,7) потребовал стратифицированного разделения данных на обучающую (608 наблюдений: 164 здоровые женщины и 444 больных РМЖ) и тестовую (154 наблюдения: 41 здоровая женщина и 113 больных РМЖ) выборки в пропорции 80:20 %. Для коррекции дисбаланса исключительно к обучающим данным применена техника SMOTE (Synthetic Minority Over-sampling Technique) с использованием библиотеки imbalanced-learn (Python 3.11) при параметре k_neighbors=5, что позволило синтезировать 280 дополнительных образцов миноритарного класса и сформировать сбалансированную обучающую выборку объемом 890 наблюдений (445 здоровых лиц и 445 больных РМЖ), тогда как тестовая выборка (n=154) сохранила исходный дисбаланс. На обработанных обучающих данных с использованием 10 потенциальных предикторов (8 иммунологических и 2 гормональных показателя) построено CART-дерево (Classification and Regression Trees) в программной среде Statistica 13.0 (модуль «Многомерные деревья классификации») со следующими параметрами: критерий ветвления – индекс Джини, минимальное число объектов в терминальном узле – 15, максимальная глубина дерева – 7 уровней. Для оценки различий между исследуемыми группами использовали непараметрический критерий χ2 с поправкой Йейтса на непрерывность вариации, т.к. распределение полученных показателей носило ненормальный характер согласно W-критерию Шапиро–Уилка. Критический уровень значимости – p<0,05. Ассоциации исследуемых показателей с риском возникновения РМЖ оценивали с помощью величины отношения шансов (ОR) с доверительным интервалом (CI) при 95 % уровне значимости.
Результаты
Результаты моделирования распределения здоровых женщин и больных РМЖ в соответствии с определенными параметрами исследованных 10 факторов сыворотки крови («дерево решений» по CART-анализу) представлены на рис. 1. Построенное CART-дерево достигло глубины 5 уровней с образованием 7 терминальных узлов, демонстрируя сложную иерархию иммунологических и гормональных маркеров. Анализ ветвления показал, что начальное разделение в корневом узле определялось уровнем IgG1-Bp с пороговым значением 7,6 у.е. Одна часть когорты с IgG1-Bp≤7,6 у.е. (n=409) направлялась в левую ветвь, а другая с IgG1-Bp>7,6 у.е. (n=481) – в правую ветвь дерева. Последующие уровни ветвления последовательно
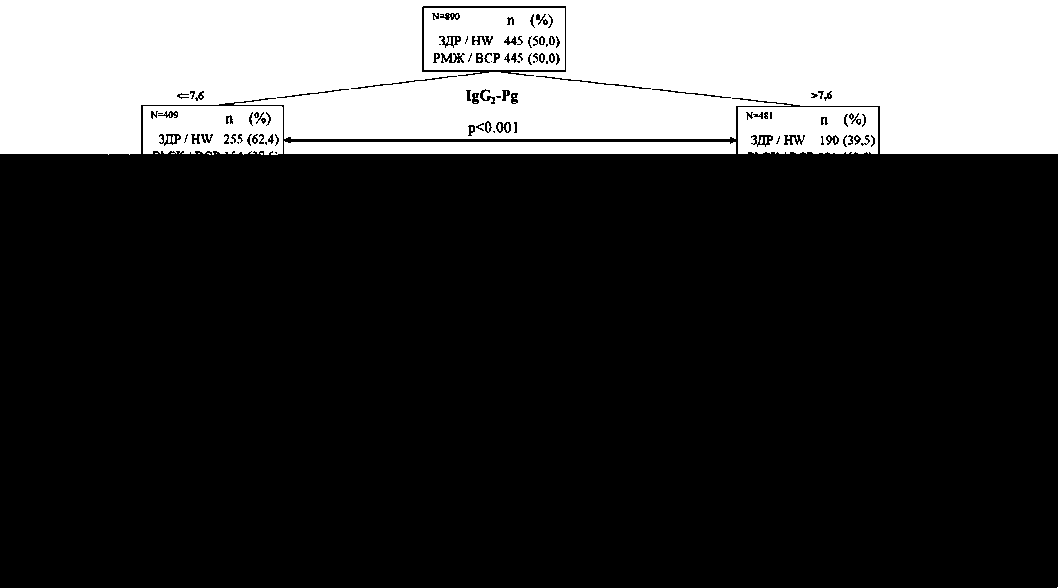
Рис. 1. CART-анализ исследуемых антител и гормонов в сбалансированной обучающей выборке 445 здоровых женщин (ЗДР) и 445 больных раком молочной железы (РМЖ). Примечание: рисунок выполнен авторами
Fig. 1. CART-analysis of studied antibodies and hormones in balanced training sampling of 445 healthy women (HW) and 445 breast cancer patients (BCP). Note: created by the authors
вовлекали остальные параметры, учитываемые при построении модели.
Среди 409 женщин с низкими уровнями IgG1-Bp (≤7,6 у.е.) 62,4 % были здоровыми, а 37,6 % – больными. Дальнейшее их разделение зафиксировано по уровням IgG2-E2. Среди 162 женщин с низкими уровнями IgG2-E2≤3,4 у.е. здоровых было 75,9 %, а больных – 24,1 %. Из 247 женщин с высокими уровнями IgG2-E2>3,4 у.е. 53,4 % было здоровых и 46,6 % – больных. В свою очередь, эта группа разделилась на две с более высокими уровнями IgG2-E2>5,4 у.е. (61 человек: 73,8 % здоровых и 26,2 % больных) и с IgG2-E2 в интервале 3,4 – 5,4 у.е. (186 человек: 46,8 % здоровых и 53,2 % больных). Последняя группа состояла из 2 подгрупп, различающихся по содержанию Pg: из 62 человек с низкими Pg≤645 pmol/L здоровых было 27,4 %, а больных – 72,6 %; из 124 человек с высокими Pg>645 pmol/L –56,5 и 43,5 % соответственно.
Правая ветвь дерева решений с высокими уровнями IgG1-Bp>7,6 у.е. сначала разделилась по содержанию E2. У 344 человек оно было высоким, >79 pmol/L. Среди них здоровых оказалось 30,8 %, а больных – 69,2 %. Группа с низким содержанием E2≤79 pmol/L разделилась на две подгруппы: с низкими уровнями IgA1-E2≤2,6 у.е. (80 человек – 77,5 и 22,5 % соответственно) и с высокими уров- нями IgA1-E2>2,6 у.е. (57 человек – 38,6 и 61,4 % соответственно).
Таким образом, с помощью CART-анализа выявлены значимые различия между здоровыми женщинами и больными РМЖ по частоте индивидуальных комбинаций 5 из 10 исследованных факторов сыворотки: IgG1-Bp, IgG2-E2, E2, Pg и IgA1-E2. Остальные факторы (IgA1-Bp, IgG1-E2, IgA1-Pg, IgG1-Pg и IgG2-Pg) не участвовали в формировании этих различий или их участие было незначительным. Используя этот алгоритм CART-анализа, построили модель распределения здоровых женщин и больных РМЖ с учетом 5 значимых факторов. В результате получили точно такое же распределение (дерево решений), как на рис. 1, а именно: 7 различных индивидуальных комбинаций 5 значимых факторов, по-разному представленных в модели у здоровых лиц и больных РМЖ.
В таблице 1 показано представительство каждой из этих комбинаций в сравниваемых группах. Удельный вес здоровых женщин был выше, чем больных РМЖ (p<0,001, OR=0,3), при наличии в сыворотке крови следующих комбинаций уровней анализированных факторов: IgG1-Bp≤7,6 у.е. + + IgG2-E2≤3,4 у.е. (позиция 1); IgG1-Bp≤7,6 у.е. + + IgG2-E2>5,4 у.е. (позиция 4); IgG1-Bp>7,6 у.е. + + E2≤79 pmol/L + IgA1-E2≤2,6 у.е. (позиция 5).
Таблица 1/table 1
Число и частота индивидуальных комбинаций исследованных антител и гормонов по сбалансированной обучающей выборке в CaRt-анализе у здоровых женщин и больных РМЖ number and frequency of revealed personal combinations of studied antibodies and hormones according to balanced training sampling in CaRt-analysis of healthy women and breast cancer patients
|
Комбинации антител и гормонов/ Combinations of hormones and antibodies |
Здоровые женщины/ Healthy women (n=206) |
РМЖ I стадии/ Stage I BC (n=557) |
χ2 (р) OR (95 %CI) |
|
1. IgG1-Bp≤7,6 + IgG2-E2≤3,4 |
123 (27,6 %) |
39 (8,8 %) |
51,9 (<0,001) 0,3 (0,2–0,4) |
|
2. IgG1-Bp≤7,6 + IgG2-E2 3,4–5,4 + Pg ≤645 |
17 (3,8 %) |
45 (10,1 %) |
12,6 (<0,001) 2,8 (1,6–5,0) |
|
3. IgG1-Bp≤7,6 + IgG2-E2 3,4–5,4 + Pg>645 |
70 (15,7 %) |
54 (12,1 %) |
2,1 (0,15) 0,7 (0,5–1,1) |
|
4. IgG1-Bp≤7,6 + IgG2-E2>5,4 |
45 (10,1 %) |
16 (3,6 %) |
13,8 (<0,001) 0,3 (0,2–0,6) |
|
5. IgG1-Bp>7,6 + E2≤79 + IgA1-E2≤2,6 |
62 (14,0 %) |
18 (4,0 %) |
25,4 (<0,001) 0,3 (0,2–0,4) |
|
6. IgG1-Bp>7,6 + E2≤79 + IgA1-E2>2,6 |
22 (5,0 %) |
35 (7,9 %) |
2,7 (0,10) 1,6 (0,9–2,8) |
|
7. IgG1-Bp>7,6 + E2>79 |
106 (23,8 %) |
238 (53,5 %) |
81,3 (<0,001) 3,7 (2,8–4,9) |
|
χ2 (р) 1–2 |
42,9 (<0,001) |
||
|
1–3 |
11,3 (<0,001) |
||
|
1–4 |
0,03 (0,87) |
||
|
2–3 |
12,9 (<0,001) |
||
|
2–4 |
24,6 (<0,001) |
||
|
3–4 |
4,5 (0,03) |
||
|
5–6 |
19,6 (<0,001) |
Примечание: таблица составлена авторами.
Note: created by the authors.
Таблица 2/table 2
Число и частота индивидуальных комбинаций исследованных антител и гормонов в фактической выборке у здоровых женщин и больных раком молочной железы number and frequency of revealed personal combinations of studied antibodies and hormones in real sampling of healthy women and breast cancer patients
|
Комбинации антител и гормонов/ Combinations of hormones and antibodies |
Здоровые женщины/ РМЖ I стадии/ Healthy women Hea(ltnh=y2w06o)men Stage I BC (n=557) |
χ2 (р) OR (95 %CI) |
|
|
1. IgG1-Bp≤7,6 + IgG2-E2≤3,4 |
55 (26,7 %) |
49 (8,8 %) |
39,4 (<0,001) 0,3 (0,2–0,4) |
|
2. IgG1-Bp≤7,6 + IgG2-E2 3,4–5,4 + Pg ≤645 |
8 (3,9 %) |
55 (9,9 %) |
6,4 (0,01) 2,7 (1,3–5,8) |
|
3. IgG1-Bp≤7,6 + IgG2-E2 3,4–5,4 + Pg>645 |
26 (12,6 %) |
62 (11,1 %) |
0,19 (0,66) 0,9 (0,5–1,4) |
|
4. IgG1-Bp≤7,6 + IgG2-E2>5,4 |
19 (9,2 %) |
21 (3,8 %) |
7,9 (0,005) 0,4 (0,2–0,7) |
|
5. IgG1-Bp>7,6 + E2≤79 + IgA1-E2≤2,6 |
29 (14,1 %) |
25 (4,5 %) |
19,6 (<0,001) 0,3 (0,2–0,5) |
|
6. IgG1-Bp>7,6 + E2≤79 + IgA1-E2>2,6 |
14 (6,8 %) |
43 (7,7 %) |
0,1 (0,78) 1,1 (0,6–2,1) |
|
7. IgG1-Bp>7,6 + E2>79 |
55 (26,7 %) |
302 (54,2 %) |
46,3 (<0,001) 3,3 (2,3–4,7) |
|
χ2 (р) 1–2 |
25,3 (<0,001) |
||
|
1–3 |
9,7 (0,002) |
||
|
1–4 |
0,15 (0,69) |
||
|
2–3 |
5,0 (0,02) |
||
|
2–4 |
13,6 (<0,001) |
||
|
3–4 |
3,1 (0,08) |
||
|
5–6 |
8,7 (0,003) |
||
Примечание: таблица составлена авторами.
Note: created by the authors.
Не было различий по представительству здоровых и больных РМЖ (p>0,05, OR≈1) при наличии комбинаций: IgG1-Bp≤7,6 у.е. + IgG2-E2 в интервале 3,4 – 5,4 у.е. + Pg>645 pmol/L (позиция 3) и IgG1-Bp>7,6 у.е. + E2≤79 pmol/L + IgA1-E2>2,6 у.е. (позиция 6). Значительно чаще (в 2,2 раза) были представлены больные РМЖ (53,5 %), чем здоровые женщины (23,8 %; p<0,001, OR=3,7), при высоких уровнях IgG1-Bp>7,6 у.е. в комбинации с высоким содержанием E2>79 pmol/L (позиция 7).
Различия по представительству здоровых и больных женщин между выделенными в модельном CART-анализе 7 вариантами индивидуальных комбинаций анализируемых факторов, приведенные в табл. 1, позволят обсудить их потенциальную роль в канцерогенезе молочной железы.
Далее исследовали представительство этих 7 вариантов индивидуальных комбинаций 5 значимых факторов сыворотки, выявленных CART-анализом, в когорте из 206 здоровых женщин и 557 больных РМЖ, участвующих в данном исследовании. Выяснилось, что и те, и другие разделяются на такие же 7 комбинаций антител и гормонов (табл. 2). Ни в одном случае не обнаружено какого-либо другого индивидуального сочетания исследованных факторов. Более того, различия между фактически обследованными женщинами по представительству каждой из этих комбинаций почти полностью совпадали с рассчитанными по CART-анализу. Корреляции между фактическими и расчетными данными были значимыми (p<0,001) с rs=0,99 для здоровых и rs=0,97 для больных женщин. Различия между представительством каждой из 7 комбинаций исследованных факторов между здоровыми и больными по табл. 2 тоже полностью совпадали с приведенными в табл. 1. При этом комбинация высоких уровней IgG1-Bp>7,6 у.е. и Е2>79 pmol/L у больных РМЖ встречалась в 2 раза чаще, чем у здоровых женщин (54,2 vs 26,7 %, p<0,001).
Исследование значимости выделенных в CART-анализе 5 факторов, по которым здоровые женщины и больные РМЖ имели статистически значимые различия, показало, что, несмотря на определяющую роль IgG1-Bp в начальном разделении CART-дерева, анализ общей важности признаков (Gini Importance) выявил доминирование E2-ассоциированных факторов (рис. 2).. Наибольшую значимость проявили IgG2-E2 (100 %), E2 (90 %), IgA1-E2 (68 %). На 4-м месте оказался Pg (59 %), а исходный разделитель IgG1-Bp занял седьмую позицию (51 %). Вместе с тем, выяснилось, что уровни этих факторов коррелируют между собой и с уровнями других исследованных факторов сыворотки крови у здоровых лиц значимо (p<0,01), но с разной степенью:
– IgG2-E2 с IgG1-Bp (rs=0,43);
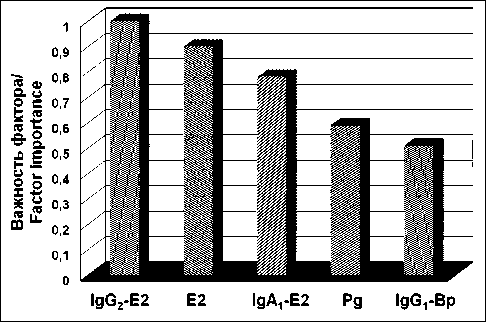
Рис. 2. Важность значимых факторов, выделенных в дереве решений по CART-анализу.
Примечание: рисунок выполнен авторами
Fig. 2. Importance of significant factors identified in the decision tree based on CART analysis. Note: created by the authors
– E2 с IgA1-E2 (rs=0,33);
– IgA1-E2 с IgA1-Bp (rs=0,61), с IgA1-Pg (rs=0,67);
– IgG1-Bp с IgA1-Bp (rs=0,31), с IgG1-E2 (rs=0,81), с IgG1-Pg (rs=0,66).
Содержание Pg не было взаимосвязано ни с одним из исследованных факторов.
Следует отметить хорошую воспроизводимость полученной CART-модели на независимой тестовой выборке. На обучающей выборке (164 здоровые женщины и 444 больных РМЖ) точность составляла 69,4 %, чувствительность – 71,5 %, специфичность – 67,4 %, F1 мера – 0,700. На тестовой выборке (41 здоровая женщина и 113 больных РМЖ) получены схожие результаты: 66,2; 65,5; 68,3 % и 0,740 соответственно.
Обсуждение
У здоровых женщин и больных РМЖ I стадии исследовали содержание в сыворотке 10 факторов: 2 стероидных гормонов, 6 идиотипических антител против классов A и G против Bp, E2 и Pg, а также 2 антиидиотипических антител класса G к E2 и Pg и с помощью CART-анализа определили наиболее значимые индивидуальные комбинации – потенциальные предикторы РМЖ.
Почти полное совпадение данных о представительстве выделенных комбинаций и у здоровых, и у больных в фактической когорте обследованных женщин с расчетными данными свидетельствовало об адекватности построенной модели ассоциаций указанных факторов по CART-анализу. Высокие значения коэффициентов корреляции между ними (rs=0,97, p<0,001) подтверждают это утверждение.
Сопоставление представительства каждой из 7 комбинаций у здоровых и больных РМЖ (табл. 2) позволяет сделать предположения о роли исследованных факторов в возникновении РМЖ. Среди женщин с одновременно низкими уровнями
IgG1-Bp≤7,6 у.е. и IgG2-E2≤3,4 у.е. (комбинация 1) удельный вес здоровых (26,7 %) был больше, чем больных (8,8 %), а при повышении уровня IgG2-E2 до значений 3,4–5,4 у.е. при тех же низких уровнях IgG1-Bp эти показатели составили 3,9 и 9,9 % соответственно, в комбинации с низким содержанием Pg≤645 pmol/L (комбинация 2); 12,6 и 11,1 % соответственно, в комбинации с высоким содержанием Pg>645 pmol/L (комбинация 3). Различия между ними были значимыми (1–2, p<0,001; 1–3, p=0,002; 2–3, p=0,02). У женщин с низкими уровнями IgG1-Bp≤7,6 у.е. в комбинации с более высокими уровнями IgG2-E2>5,4 у.е. (комбинация 4) доля больных РМЖ оказалась меньше, чем здоровых (3,8 vs 9,2 %). Это означало, что при низких значениях IgG1-Bp возрастание уровня IgG2-E2 с 3,4 до 5,4 у.е. было ассоциировано с повышением риска РМЖ (OR с 0,3 до 2,7), а дальнейшее возрастание уровня IgG2-E2 выше 5,4 у.е. – с понижением риска РМЖ (OR=0,4). То есть влияние IgG2-E2 на возникновение РМЖ у женщин с низкими уровнями IgG1-Bp было двухфазным – стимулирующим при возрастании с 3,4 до 5,4 у.е. и тормозящим при возрастании более 5,4 у.е.
Сопоставление комбинаций 2 и 3 с одинаковыми уровнями IgG1-Bp и IgG2-E2, но с разными уровнями Pg свидетельствовало о тормозящей возникновение РМЖ роли Pg: при низком его содержании (Pg≤645 pmol/L) OR=2,7, а при высоком OR=0,9. В 5 и 6-й комбинациях уровни IgG1-Bp были высокими – 7,6 у.е., а E2 – низкими ≤79 pmol/L. Среди женщин с одновременно низкими уровнями IgA1-E2≤2,6 у.е. доля здоровых была больше, чем больных (14,1 vs 4,5 %; OR=0,3), а с одновременно высокими уровнями IgA1-E2>2,6 у.е. они были равными (6,8 vs 7,7 %; OR=1,1). Различия по этим комбинациям оказались значимыми (p=0,003), что свидетельствовало о стимулирующей роли IgA1-E2 у женщин с низким содержанием в сыворотке E2 в комбинации с высокими уровнями IgG1-Bp. Одновременное повышение уровней IgG1-Bp и E2 (комбинация 7) встречалось у 26,7 % здоровых женщин и у 54,2 % больных РМЖ (OR=3,3; 2,3–4,7).
Полученные результаты соответствуют известным представлениям о стимулирующих канцерогенез молочной железы функциях E2 и тормозящих – Pg. Вместе с тем, выяснилось, что стимулирующее действие E2 проявлялось у женщин с высокими уровнями IgG1-Bp. Это не противоречило данным, полученным нами ранее, о повышении риска РМЖ при одновременно повышенных уровнях антител против Bp и E2 [16], поскольку содержание E2 в сыворотке здоровых женщин коррелировало с уровнем IgA1-E2, а IgA1-E2 – с IgA1-Bp (p<0,01). По-видимому, антитела против Bp, циркулирующие в сыворотке, действительно усиливают транспорт Bp из окружающей среды в кровь, как было показано в экспериментах in vitro (из апикального пространства монослоя эпителиальных клеток в базальное) [21], и способствуют накоплению Bp в органах-мишенях in vivo [22]. Таким образом, достигается двойное, взаимоусиливающее канцерогенное действие Bp и E2 [14, 15].
У женщин с низким содержанием E2 в комбинации с одновременно высокими уровнями антител против Bp и E2 (позиция 6) значение OR было выше (1,1), чем у женщин с высокими уровнями антител против Bp и низкими – против E2 (позиция 5), у которых OR=0,3 (p=0,003). То есть при «недостатке» E2 и антител против E2 повышение уровней антител против Bp не приводило к повышению риска возникновения РМЖ. Тормозящее канцерогенез действие повышенного содержания Pg проявлялось только у женщин с низкими уровнями IgG1-Bp и средними уровнями IgG2-E2 в интервале 3,4–5,4 у.е. (комбинация 3).
Интересно, что наиболее важными факторами в разделении исследованной когорты женщин на здоровых и больных по CART-анализу являлись не E2 и Pg, а антиидиотипические антитела IgG2-E2. Индукторами их образования у здоровых женщин могут быть соответствующие идиотипические антитела против E2, согласно классической теории об иммунологических сетях Йерне [23]. Однако нам не удалось найти корреляционные взаимосвязи между уровнями IgG2-E2 и антител против E2. Появление IgG2-E2 может быть ответом на соматические мутации ER, характерные для злокачественной трансформации клеток при РМЖ [24]. В этом случае антитела портив ER теоретически могут проявлять себя как антиидиотипические. In vitro установлено, что антиидиотипические антитела, реагирующие с моноклональными антителами против E2, демонстрировали E2-подобные эффекты [25]. Из сыворотки больных РМЖ выделены антитела против ER, стимулирующие пролиферацию ER-экспрессирующих клеток РМЖ [17], и этот эффект блокировался селективным модулятором ER [26]. По-видимому, анализ антиидиотипиче-ских антител к E2 или антител к ER, действительно, не менее важен, чем определение E2 в качестве фактора риска возникновения РМЖ.
Таким образом, установлено, что из 8 исследованных иммунологических факторов только IgG1-Bp, IgG2-E2 и IgA1-E2 проявили себя как предикторы РМЖ совместно с E2 и Pg. Однако в настоящей работе не было учтено потенциальное участие в иммуно-гормональной регуляции зло- качественной трансформации клеток молочной железы: антиидиотипических антител IgA2-Bp и IgG2-Bp, способных модулировать эффекты IgA1-Bp и IgG1-Bp; антиидиотипических IgA2-E2 и IgA2-Pg, способных модулировать действие соответствующих идиотипических антител против E2 и Pg и связываться с ER и PR, проявляемых с помощью ER и PR (в том числе мутантных форм) в качестве антигенов. Кроме того, дисбаланс между сравниваемыми группами (206 здоровых женщин и 557 больных РМЖ) мог вносить ошибку в CART-анализ используемой базы гормональных и иммунологических данных. Поэтому в дальнейших исследованиях целесообразно нивелировать этот дисбаланс и дополнить имеющуюся базу данных недостающими показателями других потенциальных участников канцерогенеза молочной железы.


