Комплексное лечение больных с хроническим генерализованным пародонтитом средней степени тяжести с использованием методов остеогингивопластики биокомпозиционными материалами и направленной тканевой регенерации
Автор: Иманалиева Ализа Жекшеновна, Абасканова Перизат Дуйшеновна, Турсуналиев Откурбек Эсенбекович, Бакиев Бахтияр Абдуллаевич, Куттубаева Клара Бейшеновна
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 4 т.7, 2021 года.
Бесплатный доступ
Совершенствование методов комплексного лечения заболеваний пародонта продолжает оставаться насущной проблемой стоматологии и требует междисциплинарного подхода. Тяжесть течения пародонтита и выраженность деструктивных явлений диктуют необходимость применения остеопластических средств для восстановления поврежденных тканей пародонта. Доказано, что эффективность мембранной техники значительно повышается при совместном использовании мембран и подсадочных материалов. Подтверждено позитивное влияние комбинированного применения обогащенной тромбоцитами и фибрином плазмы крови (ОТПК - аутогенные факторы роста, остеопластических материалов и метода направленной тканевой регенерации (НТР). Цель - повышение эффективности реконструктивного лечения больных с генерализованным пародонтитом путем сочетанного использования аллопластики, обогащенной тромбоцитами плазмы крови и метода направленной тканевой регенерации. Методы исследования: клинический, рентгенологический. За период 2018-2019 гг. под наблюдением находились 34 больных с хроническим генерализованным пародонтитом средней степени тяжести. Всем пациентам проводили профессиональную гигиену полости рта, лазеротерапию и антибактериальную терапии ровамицином. 6 пациентам в комплексной терапии были произведены хирургические вмешательства: остеогингивопластика биокомпозиционными материалами с применением НТР ауто-аллогенными мембранами. Костные дефекты заполнялась биокомпозиционным материалом: гранулами гидроксилаппатита (Полистом, РФ) в сочетании с ОТПК, сверху аутоплазменная мембрана, выделенная из ОТПК и коллагеновая мембрана (Полистом, РФ). Ближайшие и отдаленные сроки лечения протекали вполне благоприятно. При контрольной рентгенографии через 12 месяцев у больных наблюдалось восстановление костного дефекта с органотипичным строением.
Пародонтит, остеогингивопластика, отпк, мембрана, аутоплазма, регенерация
Короткий адрес: https://sciup.org/14121056
IDR: 14121056 | УДК: 616.31-089.23 | DOI: 10.33619/2414-2948/65/19
Complex treatment of patients with chronic generalized periodontitis of a medium degree of severity using the methods of osteogygivoplasty with biocomposite materials and guided tissue regeneration
Improvement of methods of complex treatment of periodontium diseases continues to be an urgent problem of dentistry and requires an interdisciplinary approach. The severity of the course of periodontitis and the severity of destructive phenomena dictates the need to use osteoplastic agents to restore damaged periodontium tissues. It has been proven that the efficiency of membrane technology is significantly increased when membranes and substitute materials are used together. The positive effect of the combined use of Platelet Rich Plasma (PRP - autogenous growth factors), osteoplastic materials and the method of Guided Tissue Regeneration (GTR) has been confirmed. To increase the efficiency of reconstructive treatment of patients with generalized periodontitis through the combined use of alloplasty, Platelet Rich Plasma and the method of Guided Tissue Regeneration. Method of testing: clinical, X-ray. For the period 2018-2019, 34 patients with chronic generalized periodontal atrophy of moderate severity were under observation. All patients underwent professional oral hygiene, laser therapy, and antibacterial therapy with rovamycin. 6 patients in complex therapy underwent surgical interventions: osteogingivoplasty with biocomposite materials using GTR auto-allogenic membranes. Bone defects were filled with biocomposite material: hydroxylappatite granules (Polistom, RF) in combination with PRP, on top of an autoplasma membrane isolated from PRP and collagen membrane (Polistom, RF). The immediate and long-term periods of treatment were quite favorable. Control X-ray examination after 12 months showed restoration of a bone defect with an organotypic structure.
Текст научной статьи Комплексное лечение больных с хроническим генерализованным пародонтитом средней степени тяжести с использованием методов остеогингивопластики биокомпозиционными материалами и направленной тканевой регенерации
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 616.31-089.23
Актуальность. Заболевания пародонта являются актуальной проблемой современной стоматологии в связи с высокой распространенностью, склонностью к частому прогрессированию и трудностью лечения [1–3]. Согласно данным ВОЗ (2000 г.), пародонтит тяжелой степени встречается в 5–20% случаев, пародонтит средней степени тяжести — в 25– 45% случаев, а интактный пародонт встречается лишь в 2–10% случаев. Следовательно, можно говорить о том, что распространенность заболеваний пародонта в целом по миру составляет в среднем 94,3% [4]. В последние годы, несмотря на успехи развития медицины и повышение качества лечения пародонтита, отмечается неуклонный рост заболеваемости, особенно увеличивается число пациентов молодого и среднего возраста. Из них, в комплексной терапии заболеваний пародонта нуждается 44% пациентов и основным видом лечения остается хирургическое, которое позволяет добиться ликвидации очагов воспаления, приостановить прогрессирование деструкции альвеолярной кости и добиться длительной стабилизации процесса [5]. Однако устранение причин пародонтита, снятие зубных отложений, удаление некротизированных тканей и грануляций далеко не всегда обеспечивают оптимальные условия для регенерации поврежденных воспалительным процессом тканей. Тяжесть течения пародонтита и выраженность деструктивных явлений диктуют необходимость применения остеопластических средств, стимулирующих и оптимизирующих процессы восстановления поврежденных тканей пародонта [6]. Многочисленными экспериментальными и клиническими исследованиями было доказано, что эффективность мембранной техники значительно повышается при совместном использовании мембран и подсадочных материалов [7–10].
Исследованиями подтверждено позитивное влияние комбинированного применения обогащенной тромбоцитами и фибрином плазмы крови (ОТПК — аутогенные факторы роста) [11–13], остеопластических материалов [14–15] и метода направленной тканевой регенерации (НТР) [16–18].
В процессе биорезорбции структуры ксеноколлагена включаются в структуры кровяного сгустка и регенерирующих тканей пациента, положительно влияют на рост и организацию фибриллярных структур. Следовательно, на сегодня наиболее перспективным является создание и использование многокомпонентных биоповязок с целью оптимизации репаративного остеогенеза послеоперационных костных дефектах различного генеза.
Цель: повышение эффективности реконструктивного лечения больных c генерализованным пародонтитом путем сочетанного использования аллопластики, обогащенной тромбоцитами плазмы крови и метода направленной тканевой регенерации.
Материалы и методы исследования
Были проведены клинические обследования и лечение 34 больных с хроническим генерализованным пародонтитом средней степени тяжести. Пациентов мужского пола было 41,2% и женского — 58,8%. Для определения динамики клинической картины проведенного лечения у всех пациентов проводили индексную оценку состояния гигиены полости рта и тканей пародонта, используя индекс гигиены Грина-Вермильона, пародонтальный индекса Рассела и индекс кровоточивости зубодесневой борозды (индекс Мюлемана). Рентгенологический метод позволил определить наличие, характер, степень и распространенность патологических изменений в костной ткани челюстей, провести дифференциальную диагностику болезней пародонта.
Жалобы больных при поступлении на: кровоточивость десен при чистке зубов и во время приема пищи, болезненность десен, неприятный запах из полости рта, наличие зубного налета, образование зубного камня, подвижность зубов и затруднения при пережевывании пищи. При осмотре выявлены следующие симптомы заболевания: болезненность десневого края при пальпации, отделяемое из ПК: серозное у 8 пациентов, гнойное в 4 случаях, подвижность зубов:1 степень — у 16; 2 степень — у 13; 3 степень — 5; глубина пародонтального кармана (ПК): <3,5 мм — 13 случаев, от 3,5 до 5,5 мм — 12; >5,5 — у 9 пациентов; травматическая окклюзия — у 11, диастемы, тремы — 7, суперконтакты — 6. Укорочение уздечки верхней губы выявлено у 3 пациентов, нижней губы — 4 случая, рецессия наблюдалась у 4 больных во фронтальном отделе нижней челюсти.
Всем пациентам первоначально проводили профессиональную гигиену полости рта ультразвуковым скейлером Voodpecker, UDS-K. Далее проводили полирование коронковой части зубов с использованием полировочных щеток различной формы и полировочной пасты
Detartrein Alfa Pro, Circon. Полирование поверхности корней зубов проводили финишными борами. В качестве ремтерапии применяли глубокое фторирование поверхности зубов с использованием эмали Bifluord 12 — и дентингерметизирующего ликвида фирмы Voco. В исследуемой группе проводилось комбинированное лечение, представленное сочетанием лазеротерапии и антимикробной терапии ровамицином. Ровамицин назначали по 3 млн. ME 3 раза в сутки в течение 10 дней. В зависимости от состояния пародонтальных карманов, части пациентам назначали аппликации с химотрипсином. Всем пациентам был назначен поливитаминный комплекс (Дуовит, Алфавит, Мультитабс) и препараты Ca (Кальций-Д3, компании «Никомед»). Дополнительно для оценки эффективности проводимой антибактериальной терапии использовали классические микробиологические методы исследования. Также, до лечения, в конце лечения (10 день лечения) и спустя месяц после лечения у всех пациентов проводилась оценка клинической картины с использованием индексов Грина-Вермильона, Рассела и Мюлемана (Таблица).
Таблица.
ДИНАМИКА ИНДЕКСНОЙ ОЦЕНКИ У ПАЦИЕНТОВ С ХРОНИЧЕСКИМ ГЕНЕРАЛИЗОВАННЫМ ПАРОДОНТИТОМ СРЕДНЕЙ СТЕПЕНИ ТЯЖЕСТИ
|
Оценочные индексы |
До лечения (M±m) |
На 10 сутки лечения (M±m) |
Через месяц после лечения (M±m) |
|
Индекс Грина- Вермильона |
2,7±0,3 |
0,3±0,2 (р 1 <0,001) |
0,4±0,3 (р 2 <0,001) |
|
Индекс Рассела |
3,2±0,4 |
0,6±0,3 (р 1 <0,001) |
0,7±0,3 (р 2 <0,001) |
|
Индекс Мюлемана |
2,4±0,4 |
0,1±0,2 (р 1 <0,001) |
0,1±0,2 (р 2 <0,001) |
Примечание : р 1 , p 2 — достоверность различий по отношению к показателям до лечения.
На первые сутки лечения гиперемия десны проявилась у всех пациентов исследуемой группы, увеличилось число пациентов с отеком десны и с наличием серозного экссудата. Количество пациентов с гнойным содержимым пародонтальных карманов значительно уменьшилось. На пятые сутки гиперемия сохранялась у большинства пациентов, отек наблюдался у 4-х пациентов, а гнойный экссудат отсутствовал. На десятые сутки лечения только у одного пациента из обследуемой группы определялась гиперемия десны. Через 1 месяц после проведенного курса лечения клиническая картина у пациентов данной группы оставалась стабильной, только у двух пациентов была выявлена гиперемия десны и у одного отек десны. Микробиологическое исследование содержимого пародонтальных карманов пациентов выявило значительное (р<0,05) снижение содержания бактероидов в пародонтальных карманах. Количество выделений энтерококков из пародонтальных карманов уменьшилось на 48,7%, а стрептококков на 61,6% (р<0,001). Положительный эффект от сочетания двух вышеуказанных методов лечения заключался в антимикробном действии ровамицина и стимулирующим действием лазерного излучения.
Каждые шесть месяцев всем пациентам проводили профессиональную гигиену полости рта и поддерживающую терапию в соответствии с распределением пациентов по исследуемым группам. Анализ индексной оценки эффективности проведенного нами лечения хронического генерализованного пародонтита в исследуемой группе осуществляли через 6 и 12 месяцев. Динамика изменений индекса Грина-Вермильона и пародонтального индекса Рассела и индекса кровоточивости Мюлемана показала самые минимальные значения.
Таким образом, в результате проведенных исследований и оценки ближайших и отдаленных результатов лечения хронического генерализованного пародонтита средней степени тяжести, была выявлена эффективность метода лазеротерапии в сочетании с антимикробной терапией ровамицином.
6 пациентам с генерализованным хроническим пародонтитом средней степени тяжести в комплексной терапии были показаны и произведены хирургические вмешательства по репаративной реконструкции альвеолярного отростка с сочетанным использованием биокомпозиционных материалов и метода направленной тканевой регенерации (НТР). В качестве средства стимулирующего репаративный остеогенез в костных дефектах использовали биокерамические аллопласты гидроксиапатит (ГАП 99, «Полистом», РФ) размером 0,25–1,0 мм, ОТПК, коллагеновую мембрану «Парадонкол» или «Гапкол» («Полистом», РФ). При выборе подсадочного материала и коллагеновой мембраны мы исходили из позитивных, достаточно серьезных исследований ряда авторов. При подсадке ГА проявляет высокую биологическую совместимость с тканями реципиента: практически отсутствуют воспалительная реакция, а также системная и местная токсичность. При имплантации биодеградирующегося ГА в сыворотке крови сохраняется нормальное содержание кальция и фосфатов за счет поступления ионов кальция из ГА в специализированный костный пул. Кроме того, резорбция гидроксиапатита проходит без образования фиброзной капсулы вокруг имплантата. Результаты клинических исследований [19] показали, что использование ГА для заполнения костных дефектов приводило к росту костной ткани в области оперативного вмешательства в среднем на 2,0±0,5 мм. Исследования [20] в аналогичной ситуации показали результат свыше З мм. Российские исследователи продемонстрировали еще более высокую активность препаратов ГА. Так, по данным [21], прирост кости при использовании препаратов на основе ГА в ряде случаев достигал 4,5 мм. Сопоставляя мембраны между собой, необходимо отметить, что рассасывающиеся мембраны имеют ряд преимуществ перед нерезорбирующимися мембранами. Они позволяют избежать проведения повторных операций с целью удаления мембран и исключить дополнительную хирургическую травму. Однако рассасывающиеся мембраны в ране должны сохранять стабильные свойства достаточно длительное время для того, чтобы у подлежащих тканей была возможность регенерировать.
В качестве иллюстрации приводим клиническое наблюдение:
Больной И-в Ф. А., 32 лет обратился на кафедру хирургической стоматологии и челюстно-лицевой хирургии Киргизской государственной медицинской академии им. И. К. Ахунбаева 13.04.19 г. с жалобами на: подвижность передних зубов верхней челюсти и затруднения при пережевывании пищи, кровоточивость десен при чистке зубов и во время приема пищи, болезненность десен, неприятный запах из полости рта и наличие зубного налета. Больным себя считает 1,5–2,0 года. При объективном исследовании выявлены следующие признаки заболевания: отек и болезненность десневого края в области 11, 12 и 21, 22 зубов, серозное отделяемое из пародонтальных карманов, подвижность зубов:1 степень — у 22; 2 степень — у 12, 3 степень — 21 и 12 зубов; глубина пародонтального кармана (ПК): <3,5 мм — у 22 зуба, от 3,5 до 5,5 мм — в области 12 зуба; >6,5 — на проекции 11 и 12 зубов; травматическая окклюзия и диастема между 11 и 12 зубами, перкуссия указанных зубов болезненна. На дентальной рентгенограмме определяется тень деструкции альвеолярной кости в области 11 и 21 зубов, включая прикорневую зону 11 зуба, межзубная костная пластинка резорбирована (Рисунок 1). Поставлен клинический диагноз: Хронический генерализованный пародонтит средней степени тяжести, подвижность 11 и 12 зубов 3 степени. Травматическая окклюзия и диастема. Предварительная санация полости рта, депульпирование и эндодонтическое лечение 11 и 21 зубов, шинирование фронтальных зубов нижней челюсти.
15.04.2019 г. Операция — остеогингивопластика фронтального сегмента верхней челюсти биокомпозиционными материалами с применением НТР ауто-аллогенными мембранами. Под местной анестезией Sol. Articaini 4% — 3,4 мл произведены разрезы по схеме лоскутных операций. После отслаивания слизисто-надкостничного лоскута, механической и медикаментозной обработки пародонтального дефекта определяли его размеры и форму (Рисунок 2).
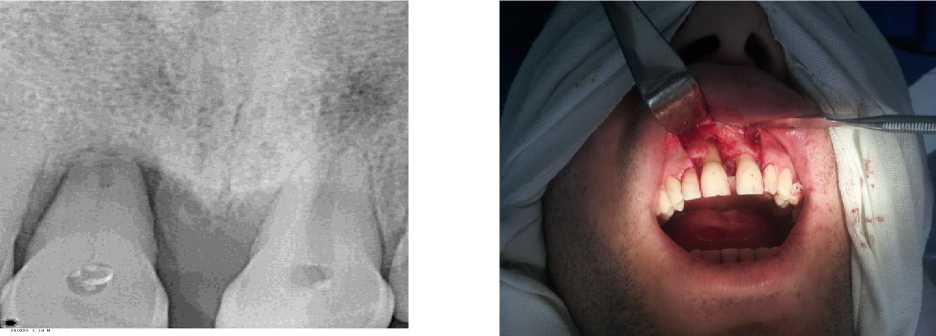
Рисунок 1. Рентгенограмма больного до операции: деструкция альвеолярной кости в области 11 и 21 зубов. Пародонтит локализованная форма тяжелая степень подвижность зубов 3–4 степени
Рисунок 2. Этап операции: трапециевидный лоскут выкроен, откинут, кость скелетирована, определяется значительная деструкция альвеолярной кости в области 11 и 21 зубов с обнажением корней
Подбирали соответствующую мембрану, используя одну из стерильных оболочек упаковки в качестве шаблона, перенося размеры дефекта на мембрану. Края мембраны формировали с учетом того, чтобы они перекрывали края костного дефекта не менее чем на 2–3 мм. Мелкодисперсный (0,25 мм) гидроксиапатит (ГАП 99, «Полистом», РФ) смешивали с приготовленной плазмой и тромбоцитарной массой, предварительно удалив аутоплазменную мембрану и подготовив последнею к использованию (Рисунок 3). Биокомпозицию укладывали на область костного дефекта вестибулярно и орально (Рисунок 4).
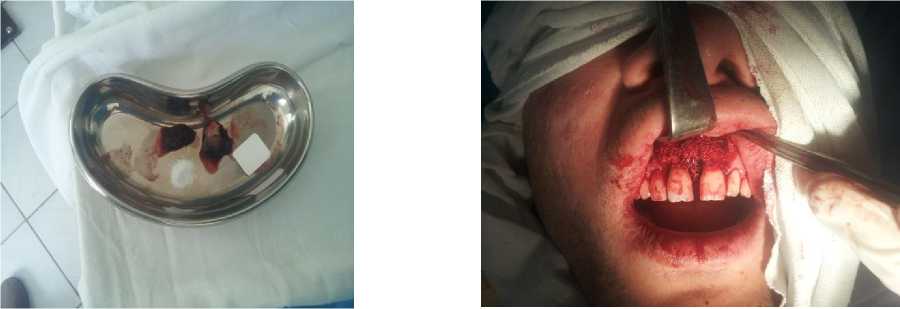
Рисунок 3. Приготовление биокомпозиционного материала: гидросилапатит (ГАП-99), обогащенная тромбоцитами плазма крови (О.Т.П.К), аутоплазменная и коллагеновая мембрана
Рисунок 4. Биокомпозиционный материал уложен на область дефектов альвеолярного отростка
Учитывали тот факт, что рассасывающиеся мембраны в ране должны сохранять стабильные свойства достаточно длительное время для того, чтобы у подлежащих тканей была возможность регенерировать. Для этих целей мы использовали методику послойного наложения мембран (аутоплазменная, затем коллагеновая) одна на другую и таким образом увеличиваются сроки резорбции (Рисунок 5). Кроме того, мы наблюдали хорошую адгезию коллагеновой мембраны на аутоплазменную, что исключало дополнительную фиксацию. Лоскуты после небольшой мобилизации возвращены на место и ушиты проленом (Рисунок 6).
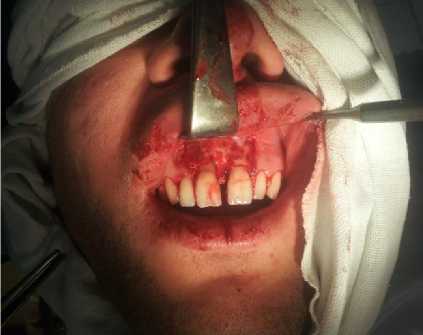
Рисунок 5. Раневая поверхность с биокомпозиционным материалом прикрыта аутоплазменной и коллагеновой мембранами
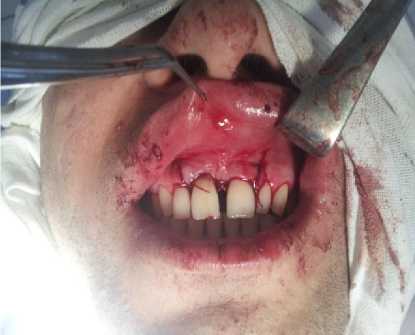
Рисунок 6. Наложение швов из пролена
Послеоперационное течение гладкое, швы удалены через 7 суток. Больной явился на осмотр 12 месяцев, уезжал на заработки за границу, через полгода поставил металлокерамические протезы. состояние хорошее. Жалоб не предъявляет. Протезная конструкция стабильная, устойчивая (Рисунок 7). При пальпации определяется плотная безболезненная альвеолярная кость. Десневая манжетка и сосочки хорошо контурирует, слизистая бледно-розового цвета. На одонтопантомограмме через 12 месяцев определяется репаративная регенерация кости альвеолярного отростка во фронтальном сегменте верхней челюсти (Рисунок 8).
Рисунок 7. Через 12 месяцев после операции и протезирования металлокерамическим протезом
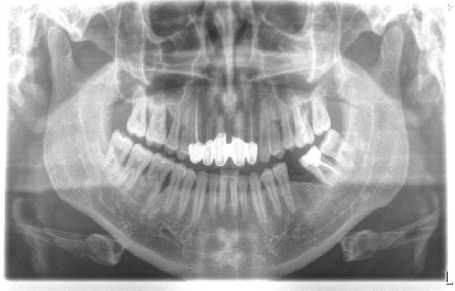
Рисунок 8. Одонтопантомограмма через 12 месяцев: определяется репаративная регенерация фронтального сегмента верхней челюсти
Заключение
Эффективным методом комплексного курса лечения хронического генерализованного пародонтита средней степени тяжести является лазеротерапия в сочетании с антимикробной терапией ровамицином. В случаях значительной потери костной ткани альвеолярного отростка оптимальной является проведение оперативных вмешательств по репаративной реконструкции альвеолярного отростка с сочетанным использованием биокомпозиционных материалов и метода направленной тканевой регенерации, результатом которой является частичное или полное восстановление утраченной костной ткани и структур пародонта.
Список литературы Комплексное лечение больных с хроническим генерализованным пародонтитом средней степени тяжести с использованием методов остеогингивопластики биокомпозиционными материалами и направленной тканевой регенерации
- Барер Г. М., Немецкая Т. И. Болезни пародонта. Клиника, диагностика и лечение. М., 1996. 85 с.
- Безрукова И. В., Грудянов А. И. Агрессивные формы пародонтита. М., 2002. 126 с.
- Цепов Л. М., Николаев А. И. Диагностика и лечение заболеваний пародонта. М., 2002. С. 34-60.
- Лепеева Н. А., Ермолаева Л. А., Шишкин А. Н. Состояние тканей пародонта у больных метаболическим синдромом // Вестник Санкт-Петербургского университета. 2012. №3. С. 145-152.
- Грудянов А. И. Заболевания пародонта. М.: Медицинское информационное агентство, 2009. 336 с.
- Орехова Л. Ю. Заболевания пародонта. М., 2004. 432 с.
- Грудянов А. И., Чупахин П. В. Методика направленной регенерации тканей. Подсадочные материалы. М.: Медицинское информационное агентство, 2007. 64 с.
- Cordioli G., Majzoub Z., Riachi F. Postloading behavior of regenerated tissues in GBR-treated implant sites // Int. J. Periodontics. Restorative Dent. 1999. V. 19. №1. P. 44-55.
- Eickholz P., Hausmann E. Evidence for healing of class II and class III furcations 24 months after guided tissue regeneration therapy: digital subtraction and clinical measurements // J. Periodontol. 1999. Vol. 70. №12. P. 1490-1500. https://doi.org/10.1902/jop.1999.70.12.1490
- Becker W. Periodontal regeneration: myth or reality? // Calif. Dent. Assoc. 1999. V. 27. №2. P. 118-121.
- Робустова Т. Г. Гребенникова И. П. Плазма, обогащенная тромбоцитами, при костно-восстановительных операциях на челюстях // Российский стоматологический журнал. 2005. №2. С. 19-22.
- Модина Т. Н. Применение комплекса «Cerasorb» - богатая тромбоцитами плазма -бедная тромбоцитами плазма» в пародонтальной хирургии // Dental Market. 2004. №4. P. 2224.
- Адда Ф. Тромбоциты с высоким содержанием фибрина // Институт стоматологии. 2003. №1 (18). С. 67-69.
- Яременко А. И., Галецкий В. Д., Королев В. О. Современные остеопластические и остеоиндуктивные материалы. Состояние проблемы. Перспективы применения в стоматологии и челюстно-лицевой хирургии // Ин-т стоматологии. 2011. №2 (51). С. 70-71.
- Lecovic V., Kenney F. Guided tissue regeneration using calcium phosphate implants together with 4 different membranes. A study on furcation in dogs // J. of Periodonlology. 1993. V. 64. №11. P. 1154-1156. https://doi.org/10.1902/jop.1993.64.11s.1154
- Schek R. K., Buser D., Hardwick W. R. et al. Healing pattern born regeneration in membrane-protected defects: a histologic study in the canine mandible // Int Oral Maxilofak Implants. 1994. V. 9. P. 13-29.
- Sculean A., Donos N. Chiantella С. еt al. GTR with bioresorbable membranes in the treatment of intra-bony defects: a clinical and histologic study // Int. J. Periodontics Restorative Dent. 1999. V.19. №5. P. 501-509.
- Casati M. Z., Sallum E. A., Caffesse R. G., Nociti F. H., Sallum A. W., & da Silva Pereira, S. L. Guided Tissue Regeneration With a Bioabsorbable Polylactic Acid Membrane in Gingival Recessions. A Histometric Study in Dogs // Journal of Periodontology. 2000. V. 71. №2. P. 238-248. https://doi.org/10.1902/jop.2000.7L2.238
- Yukna C. N., Yukna R. A. Multi-center evaluation of bioabsorbable collagen membrane for guided tissue regeneration in human class II furcation // J. Periodontol. 1996. V. 67. №7. P. 650657.
- Suzuki M., Shionome, Sakata J. Clinical use of porous hydroxyapatite in the periodontal vertical bone defects // Jap. J. Conservative Dent. 1993. V. 36. №6. P. 140.
- Воробьев Ю. И., Воложин А. И., Богдашевская В. Б. и др. Клинико-рентгенологическая оценка эффективности ГА с коллагеном при лечении пародонтита и радикулярных кист // Стоматология. 1995. №2. С. 30-34.


