Комплексное лечение тяжелого абдоминального сепсиса у пациента, оперированного по поводу рака желудка
Автор: Стойко Ю.М., Левчук А.Л., Рябов А.Л., Кудрявцев А.Н., Чернова Н.А., Чижов А.Г., Кулабухов В.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4 т.5, 2010 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140187858
IDR: 140187858 | УДК: 616.33-006.6-089:617.55:616.94
Complex treatment of severe abdominal sepsis in patients who underwent surgery due to stomach cancer
Текст статьи Комплексное лечение тяжелого абдоминального сепсиса у пациента, оперированного по поводу рака желудка
УДК: 616.33-006.6-089:617.55:616.94
COMPLEX TREATMENT OF SEVERE ABDOMINAL SEPSIS IN PATIENTS WHO UNDERWENT SURGERY DUE TO STOMACH CANCER
Stoiko Yu.M. Levchuk, A.L., Ryabov A.L., Kulabukhov V.V., Kudryavtsev A.N., Chernova N.A., Chizhov A.G.
Рак желудка занимает ведущее место среди новообразований органов пищеварения. Частота рака желудка в России, по-прежнему, остается высокой, что определяет социально-экономическую и медицинскую значимость этой проблемы.
Увеличение продолжительности жизни и успехи в лечении рака на современном этапе развития медицины связаны не только с расширяющимися возможностями диагностики и профилактики онкологических заболеваний, но и с развитием многомодальной агрессивной хирургии, основные принципы которой базируются на циторедуктивной технике оперативного вмешательства и интраоперационной химиотерапии.
Вместе с тем, сохраняется высокая летальность, составляющая среди мужчин 14,9%, а среди женщин – 13,4%.
Специфичность, обширность и травматичность проводимых хирургических вмешательств, определяют общие проблемы послеоперационного периода – несостоятельность анастомозов, кишечную перфорацию, абсцессы брюшной полости, внутрибрюшные кровотечения, развитие послеоперационного острого панкреатита.
Онкологические больные весьма подвержены к развитию сепсиса в силу особенностей течения злокачественного процесса с формированием специфического интоксикационного синдрома, иммунологической дезинтеграции, трофических и регуляторных расстройств, часто вне зависимости от локализации опухоли.
Циркуляция в кровотоке высоких концентраций эффекторного цитокина – фактора некроза опухоли - приводит к апоптозу злокачественных клеток через систему рецепторов Fas-Fasl. Продукты клеточного распада являются универсальными молекулярными паттернами, способными через механизм структурных рецепторов привести к развитию системного воспалительного ответа неинфекционного генеза.
Аналогичный механизм характерен и для взаимодействия липополисахарида грамотрицательных бактерий с клетками врождённого иммунитета человека и является одним из ключевых в формировании избыточной системной воспалительной реакции при генерализованной инфекции. У онкологического больного эти механизмы, потенцируют друг друга. Лечение таких пациентов является сложной клинической задачей, успех решения которой зависит от усилий большого количества специалистов и требует нетривиальных диагностических и терапевтических подходов.
У Больного Д., 51 год, в феврале 2008 года диагностирован рак антрального отдела желудка Т2N0M0 (высокодифференцированная аденокарцинома). 01.03.08 выполнена лапаротомия: субтотальная резекция желудка по Ру, холецистэктомия, дренирование подпечёночного пространства.
Течение вторых послеоперационных суток осложнилось развитием острого отечного панкреатита. Проводилась патогенетическая терапия. Однако через 12 часов у пациента развилась
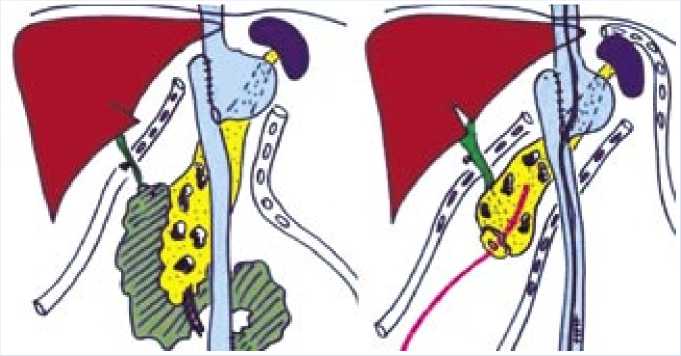
Рис. 1. Схема операции: исходное состояние (слева) и результат операции (справа)
клиническая картина ферментативного перитонита. 03.04.08 выполнена экстренная операция в объеме: релапаротомия, санация и дренирование брюшной области, назоинтестинальное дренирование. Интраоперационно отмечалось наличие в брюшной полости до 1000 мл свободного серозно-геморрагического выпота, обнаружены бляшки стеатонекроза. Особенностью макроскопической картины явилось равномерное увеличение приводящей кишки до энтеро-энтероанастомоза до 4 см в диаметре с явлениями венозного стаза. Дефектов серозного покрова, фибрина обнаружено не было.
На следующий день 04.04.08 нарастали явления интоксикации, отмечено одномоментное поступление отделяемого с примесью желчи из подпеченочного пространства. Выполнена экстренная операция. Интраоперационно выявлен некроз культи 12-перстной кишки и участка приводящей петли тощей кишки. Произведена дуоденэктомия, резекция некротизированного участка тощей кишки, дренирование панкреатического и общего желчного протоков (рис. 1).
Интраоперационно развился септический шок. В течение последующих 12 часов прогрессировали признаки по-лиорганной недостаточности: олигурия < 0,5 мл кг/ч; тканевая гипоперфузия – лактат более 2 ммоль/л; снижение индекса оксигенации < 150; прокальцитониновый тест ≥ 10 нг/мл.
Интегральная оценка по SAPS3 составила 88 баллов, прогноз летальности – 92%.
В течение первого часа выполнены все необходимые лабораторно-диагностические мероприятия (взятие бактериологического материала до начала антибактериальной терапии, инвазивный

мониторинг гемодинамики и т.д) для определения тяжести состояния и выработки дальнейшей тактики терапии.
Антибактериальная терапия по де-эскалационной схеме (Меронем 3 г/сут), антисекреторная, антикоагулянтная терапия, инотропная и вазопрессорная поддержка, парентеральное питание. С целью экстракорпоральной детоксикации и почечно-заместительной терапии начат сеанс продленной (72 часа) вено-венозной гемофильтрации с высокими объемами замещения (70 мл/кг/час).
На фоне проводимого лечения отмечена стабилизация состояния: значительное снижение инотропной поддержки, отмена вазопрессоров, улучшение кислородно-транспортной функции, снизился показатель прокальцитонина до уровня менее 0,5 нг/мл. При интегральной оценке тяжести состояния больного отмечено снижение баллов по SAPS3. Снизился риск летального исхода с 92% до 62%.
Несмотря на достигнутую стабилизацию состояния сохранялись признаки полиорганной дисфункции, эндогенной интоксикации, что позволило предположить формирование вторичных гнойных очагов.
По алгоритму комплексной терапии абдоминального сепсиса (рис. 2) своевременно выявлены и устранены следующие вторичные гнойные очаги:
– 18.04.2008 г. – абсцесс малого таза, тотальное нагноение лапаротом-ной раны, частичная эвентрация петель тонкой кишки.
– 22.04.2008 г. – формирование панкреатического и желчного свищей.
– 26.05.2008 г. – абсцесс в проекции головки поджелудочной железы.

Хирургическая обработка Синдром Системной
(первичная и повторные) Воспалительной Реакции
Рис. 2. Алгоритм комплексной терапии абдоминального сепсиса
– 31.05.2008 г. – межпетельный абсцесс.
Поиск и санация гнойных очагов проводилась в условиях интенсивного наблюдения за больным, компоненты которого определяли динамику и особенности органопротективной терапии. Так, при определении стадии повреждения почек по шкале RIFLE и 5 баллов по шкале SOFA, был проведен 48-часовой сеанс почечнозаместительной терапии (вено-венозная гемофильтрация). Сохраняющийся высокий показатель (более 7 баллов) шкалы клинической оценки инфекции легких (CPIS) требовал длительного проведения (ИВЛ) в течение 23 суток. При этом с целью профилактики внутрибольничной инфекции у больного в полном объеме использованы элементы концепции «изолированный пациент». Значительные потребности пациента в энергетических и пластических субстратах вследствие выраженного синдрома гиперметаболизма и больших потерь из панкреатического и желчного свищей на фоне интестинальной недостаточности, компенсировались проведением парентерального питания «три в одном» с дополнительным добавлением незаменимых аминокислот. Так же обязательной добавкой были макро- и микроэлементы, витамины. Длительное применение, в течение 55 суток, полного парентерального питания весомых осложнений не вызвало.
Вследствие проводимой консервативной терапии вновь достигнута стабилизация состояния. На 44 сутки, на (КТ) грудной клетки отмечена положительная динамика в виде уменьшения размеров инфильтрации легочной ткани и повышение воздушности легких, уменьшение количества жидкости в плевральных по- лостях. Сохранялись большие потери из панкреатического и желчного свищей (более 700 мл/сут), синдром гиперкатаболизма в период реконвалесценции сепсиса. С целью определения объемного и качественного состава парентерального питания и инфузионной терапии проводился еженедельный подсчет энергетических потребностей и ежедневная оценка кислотно-щелочного и электролитного состава крови. В среднем потери превышали в 3 раза базовые уровни.
Через 59 суток лечения в отделении реанимации состояние пациента позволило перевести его в хирургическое отделение.
К июлю 2008 года состояние больного стабилизировалось, улучшилась функция пищеварения. В относительно удовлетворительном состоянии пациент выписан под наблюдение хирурга и гастроэнтеролога по месту жительства.
Через 5 месяцев пациент повторно госпитализирован в Пироговский Центр с ухудшением состояния, которое было обусловлено эндогенной интоксикацией и гипотрофией 2 степени (Индекс массы тела составлял 16,37). Со слов пациента с сентября 2008 года отмечалось увеличение отделяемого по дренажу, гиперемия в области свища, снижение массы тела, нарастание общей слабости. С первой декады декабря 2008 года появились тянущие боли в поясничной области, учащенное болезненное мочеиспускание, периоды гипертермии до 37,5° С с ознобом, боли в области установленного дренажа брюшной полости.
При обследовании (КТ живота и малого таза) в правом латеральном кармане между нижним краем печени, задней стенкой восходящей кишки и листком брюшины выявлена многокамерная полость, заполненная жидкостью с пузырьками газа. Полость имела толстые стенки. Её нижняя граница находилась на уровне головки бедренной кости. По ходу восходящей кишки деструктивные изменения распространялись в правую половину малого таза, а по ходу петли подвздошной кишки – в межпетельное пространство брыжейки тонкой кишки. Суммарный объем жидкости составлял 200–300 мл.
Возникла неоднозначная клиническая ситуация: с одной стороны наличие гнойного очага требовало срочной санации, с другой стороны операция на фоне выраженного истощения заведомо привела бы к неблагоприятному исходу.
Пациент консультирован Президентом НМХЦ, академиком РАМН Ю.Л. Шев-
ченко – показана реконструктивная операция, направленная на восстановление целостности ЖКТ, в плановом порядке, после компенсации водно-электролитных, белково-энергетических нарушений.
В период интенсивной предоперационной подготовки, направленной на переключение метаболических реакций в сторону повышения основного обмена, состояние пациента оставалось тяжелым. Наличие гнойного очага ограничивало возможности консервативной терапии, сохранялся риск развития хирургических осложнений (аррозивное кровотечение и т.д.) и распространения гнойного очага.
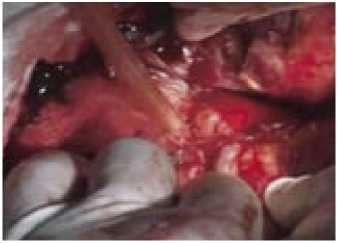
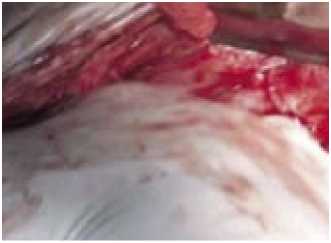
Учитывая все возможные риски оперативного вмешательства, 30.12.08 выполнена плановая операция: лапаротомия, рассечение спаек, выделение наружного холедохо-панкреатического свища, вскрытие, санация и дренирование ограниченного забрюшинного затека, наложение папилло-еюнального анастомоза на наружном управляемом дренаже по Фенкеру с межпетельным тонкокишечным анастомозом по Брауну. Дренирование подпеченочного пространства (рис. 3).
-
a) Выделение наружного холедохопанкреатического свища.
-
b) Вскрытие, санация ограниченного забрюшинного затека.
-
c) Формирование папилло-еюналь-ного анастомоза.
10.02.09 по стабилизации состояния, пациент переведён в хирургическое отделение, в дальнейшем на 76 сутки выписан на амбулаторное лечение.
Послеоперационный период протекал относительно гладко – пациент не лихорадил, прогрессивно снижались показатели нейтрофильного лейкоцитоза (рис. 4).
Адекватность дренирования подтверждена при МРТ брюшной полости от 13.01.2009 года: внутрипеченочные протоки не расширены, просвет однородный. Общий желчный проток 7 мм, в нем дренажная трубка. Проток поджелудочной железы до 3 мм, дистальный конец обрывается на расстоянии 9 мм от места слияния с желчным протоком.
В период наблюдения с 13.01.09 по 26.01.09 на фоне проводимой плановой терапии состояние оставалось тяжёлым. Электролитные нарушения, связанные со значительными потерями кишечного содержимого, панкреатического сока, желчи при аспирационном дренировании зоны холедохоеюноанастомоза корригировались за счёт внутривенного введения электролитных растворов. Суточные энергетические и пластические потребности покрывались за счёт парентерального питания.
В настоящий момент пациент чувствует себя хорошо, увеличил массу тела на 20 кг. При контрольном осмотре дан- ных за прогрессирование онкологического процесса нет, клинико-лабораторные показатели в пределах нормы.
Заключение: врач в случае курации пациента со злокачественным заболеванием в периоперационном периоде должен быть бдительным, учитывая, что грань, отделяющая системное воспаление от полиорганной недостаточности у данной категории пациентов весьма эфемерная. Присоединение инфекционного компонента может протекать в виде различных клинических масок и манифестировать септическим шоком уже в операционной, в ходе одного из этапов оперативного вмешательства. В послеоперационном периоде необходимо применять весь спектр возможностей современной интенсивной терапии для купирования проявлений полиорганной недостаточности, замещения жизненно-важных функций для обеспечения, при необходимости, дальнейших оперативных вмешательств. Только своевременная и последовательная оценка состояния пациента, полное взаимодействие хирургов и реаниматологов позволяют успешно бороться с недугом и определяет оптимальное качество жизни пациента в дальнейшем.
Данное клиническое наблюдение демонстрирует уникальные возможности лечебно-диагностической инфраструктуры Пироговского Центра в проведении
комплексного лечения онкологического
пациента с тяжелым абдоминальным сепсисом, тесное и созидательное взаимодействие хирургов и реаниматологов, явившееся залогом успешного лечения.
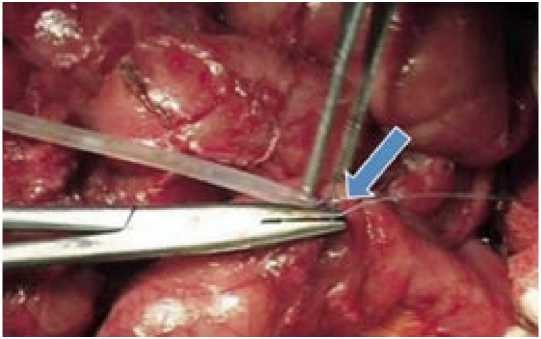
Рис. 3. Основные моменты реконструктивно-восстановительной операции
Стойко Ю.М.
Национальный медико-хирургический Центр им.
20 18
" 12
° 10
х 8
4 2 О
Операция 30.12.2008
Нейтрофильный лейкоцитоз
Рис. 4. Динамика нейтрофильного лейкоцитоза в до- и послеоперационном периоде


