Комплексообразование палладия (II) с бромидом триоктилпропаргиламмония
Автор: Букин Вячеслав Иванович, Андреев Владимир Петрович, Соболев Павел Сергеевич
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Физико-химическая биология
Статья в выпуске: 8 (161), 2016 года.
Бесплатный доступ
Рассматривается комплексообразование палладия (II) с бромидом триоктилпропаргиламмония. Методами электронной и инфракрасной спектроскопии показано, что комплексы состава 1:1 и 1:2 в водно-толуольных смесях образуются с участием тройной связи. Предполагается, что как ацетиленовые четвертичные аммониевые соли, так и их комплексы с солями палладия могут проявлять противомикробное и противоопухолевое действие. Описаны условия очистки, выделения и концентрирования палладия экстракционным методом, которые защищены патентом.
Координация, комплексообразование, апоптоз, экстракция, палладий, нуклеофильность, четвертичные аммониевые соли
Короткий адрес: https://sciup.org/14751117
IDR: 14751117 | УДК: 577.1+547
Palladium (II) complexation with bromide of trioctylpropargylammonium
The complexation of palladium (II) with bromide of trioctylpropargylylammonium is examined. The methods of electron and infrared spectroscopy demonstrated that the complexes of compositions 1:1 and 1:2 in water-toluene mixtures are formed with the help of the triple bond. It is assumed that both acetylenic Quaternary ammonium salts and their complexes with palladium salts can exhibit antimicrobial and antitumor activity. Protected by a patent, conditions of purification, separation and concentration of palladium by method of extraction are described.
Текст научной статьи Комплексообразование палладия (II) с бромидом триоктилпропаргиламмония
В основе физиологической активности аминов [4] лежит их способность образовывать водородные, ковалентные и ионные связи, которые определяют способность аминов приближаться к рецепторному сайту в организме, реагировать с ним и образовывать, нарушать или модифицировать химические связи. Даже проницаемость клеточной мембраны зависит от того, в каком виде находится аминогруппа. Например, для четвертичных аммониевых оснований она понижена (ацетилхолин не проникает через гематоэнцефалический барьер), при наличии же в равновесной смеси даже небольшого количества свободного амина проникновение через мембрану может иметь место [4]. Все это должно быть справедливо (с некоторыми особенностями) и по отношению к ацетиленовым аминам и четвертичным аммониевым солям (ЧАС).
В последнее время металлы платиновой группы находят все более широкое применение в
биологии и медицине, например в качестве противоопухолевых (цисплатин (цис-диаминдихлор-платина), карбплатин), иммуномодулирующих (эфазол) и других препаратов. Однако, несмотря на значительный терапевтический эффект, лекарственные препараты на основе цис-платины обладают побочным действием (вызывают тошноту, рвоту, расстройство функций костного мозга, являются причиной различных нервных заболеваний). Кроме того, существенным недостатком таких препаратов является их низкая растворимость в воде [5]. Поэтому проводится огромная работа по поиску аналогов этих комплексов, обладающих меньшей токсичностью и более широким спектром противоопухолевой активности. Например, автором работы [6] показано, что соединения палладия оказывают противоопухолевое действие и не обладают выраженным цитотоксическим действием, причем наибольшим противоопухолевым действием на клетки миеломы SP-2X обладает соединение цис-Pd(NH3)2Cl2, при инкубации с которым число клеток миеломы снижается на 67 %.
В 2009 году группой исследователей были опубликованы результаты, касающиеся взаимосвязи структуры ЧАС с их апоптогенными свойствами [7]. Выяснилось, что аналогично бактерицидным апоптозиндуцирующие свойства ЧАС зависят от длины цепи вещества: в частности, эффективным соединением является цетримониум бромид. В связи с этим в настоящей работе исследуется комплексообразование палладия с ацетиленовой четвертичной аммониевой солью – бромидом проп-2-инилтриоктиламмония – методом экстракции 0,025 М раствором ЧАС в толуоле из растворов, содержащих 1 мг/мл палладия с различным содержанием HCl. Полученные данные приведены в табл. 1.
Как видно из представленных данных, с ростом концентрации соляной кислоты в растворе наблюдается понижение коэффициента распределения палладия. При росте концентрации соляной кислоты от 0,67 до 5,72 М D Pd падает с 46,74 до 0,63. Максимальное извлечение палладия (Е Pd = 98 %) наблюдается при экстракции палладия из раствора, содержащего 0,67 М соляной кислоты.
Для определения состава экстрагируемого комплекса палладия была изучена экстракция (метод сдвига равновесия) палладия бромидом проп-2-инилтриоктиламмония в толуоле в диапазоне концентраций экстрагента от 0,025 до 0,050 моль/л. Исходный раствор содержал 1,09 мг/ мл палладия и 2,9 М HCl. Полученные данные приведены в табл. 2.
Как видно из представленных данных, по мере роста концентрации экстрагента коэффициент распределения палладия возрастает. По тангенсу угла наклона зависимости lg D Pd = f (lg C Э ) можно узнать о соотношении металл/экстрагент в экстрагируемом комплексе.
Ввиду того что tgα = 1,46, можно предположить, что палладий переходит в органическую фазу с образованием двух комплексов состава палладий/экстрагент 1:1 и 1:2. Похожие данные были получены при изучении экстракции цинка и меди ацетиленовыми ЧАС [1], [2].
В электронных спектрах поглощения экстракта не наблюдается полос, отвечающих иону [PdCl 4 ]2–, – полосы переноса заряда с максимумом λ = 279 нм (ε = 10500 моль–1см–1) и широкой полосы λ = 473 нм (ε = 161 моль–1см–1), отвечающей спинразрешенному d–d-переходу. Это исключает существование в органической фазе аниона [PdCl4]2- и говорит о том, что экстракция не идет по механизму анионного обмена, типичного при экстракции аминами.
Наиболее важное изменение при комлексооб-разовании Pd(II) c бромидом проп-2-инилтриок-тиламмония затрагивает полосу поглощения в области 2115 см1, отвечающую за валентные колебания связи C≡C, а также полосу поглощения в области 3311 см-1, отвечающую за валентные колебания связи C–H, прилегающей к тройной связи. При образовании комплекса эти полосы исчезают, что может говорить о координации Pd(II) по тройной связи.
В работах [1], [2], посвященных экстракции цинка и меди ацетиленовыми четвертичными аммониевыми солями, предполагается, что исследуемый экстрагент способен к образованию
Таблица 1
Зависимость коэффициента распределения палладия от концентрации соляной кислоты в растворе. С Э = 0,025 моль/л
|
C Pd исх, мг/мл |
X Pd , мг/мл |
Y Pd , мг/мл |
D |
lgD |
E |
C HCl исх, М |
C HCl равн, М |
|
1,079 |
0,023 |
1,056 |
46,74 |
1,670 |
97,91 % |
0,670 |
0,642 |
|
1,157 |
0,116 |
1,041 |
9,009 |
0,955 |
90,01 % |
1,367 |
1,311 |
|
1,111 |
0,138 |
0,973 |
7,057 |
0,849 |
87,59 % |
2,697 |
2,604 |
|
1,094 |
0,250 |
0,845 |
3,385 |
0,530 |
77,19 % |
4,418 |
4,185 |
|
1,111 |
0,683 |
0,428 |
0,626 |
–0,203 |
38,51 % |
5,720 |
5,348 |
Таблица 2
Зависимость коэффициента распределения палладия от концентрации экстрагента
|
CЭисх, моль/л |
CЭсвоб, моль/л |
lgCЭ своб |
XPd, мг/мл |
YPd, мг/мл |
D |
lgD |
|
0,025 |
0,009 |
–2,036 |
0,250 |
0,840 |
3,360 |
0,526 |
|
0,030 |
0,013 |
–1,886 |
0,186 |
0,904 |
4,860 |
0,687 |
|
0,035 |
0,017 |
–1,770 |
0,131 |
0,959 |
7,302 |
0,863 |
|
0,040 |
0,021 |
–1,672 |
0,093 |
0,997 |
10,68 |
1,029 |
|
0,045 |
0,026 |
–1,583 |
0,084 |
1,006 |
11,96 |
1,078 |
|
0,050 |
0,030 |
–1,517 |
0,049 |
1,041 |
21,20 |
1,326 |
Таблица 3
Реэкстракция палладия различными реэкстрагентами
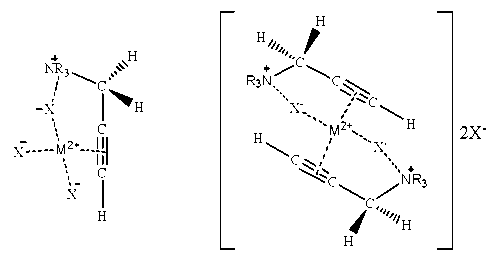
Предполагаемая структура комплексов ацетиленовых ЧАС с ионами палладия, где X – Br, Cl
Таким образом, электронные спектры поглощения, ИК-спектры, а также известные литературные данные [1], [2] позволяют сделать предположение, что палладий образует подобные комплексы с бромидом проп-2-инилтриоктилам-мония в органической фазе.
С целью выбора эффективного реэкстрагента для реэкстракции палладия из фазы ЧАС была изучена реэкстракция палладия раствором 8 М соляной кислоты, смесью 12,5 % NH4OH и 50 г/л NH4Cl и 10 % раствором тиомочевины в 1 М HCl. Реэкстракцию проводили из органических растворов после экстракции, содержащих 1 мг/мл палладия (соотношение водной и органической фаз 1:1, время контактирования 5 мин.). Полученные данные представлены в табл. 3.
Как видно из полученных данных, наиболее полная реэкстракция палладия осуществляется 10%-ным раствором тиомочевины в 1 М HCl (степень реэкстракции 98 %). Кроме того, для реэкстракции палладия можно использовать соляную кислоту: 8 М HCl реэкстрагирует палладий на 93 %. Использование аммиака для реэкстракции палладия нецелесообразно, так как степень его реэкстракции составляет всего лишь 10 %.
Для промышленного использования экстрагента необходимо было подтвердить возможность его повторного использования. Для этого экстрагент после реэкстракции палладия тиомочевиной отмывали раствором 1 М NaCl за 4 стадии (время контактирования составляло 5 мин.), после чего проводили повторную экстракцию по методике, описанной ранее, из раствора, содержащего 1 мг/мл Pd и 0,5 М HCl. Степень извлечения палладия при использовании регенерированного экстрагента составляет 98 %, то есть практически такая же, как в первом случае (см. табл. 3). Это говорит о том, что экстрагент не разрушается в процессах экстракции и реэкстракции и его можно использовать многократно. Описанные выше условия очистки, выделения и концентрирования палладия экстракционным методом защищены патентом [6].
Таким образом, экстракционным методом показано, что ацетиленовые ЧАС образуют комплексы с солями платины. В дальнейшем нами предполагается исследовать их апоптозстимули-рующие свойства.
PALLADIUM (II) COMPLEXATION WITH BROMIDE OF TRIOCTYLPROPARGYLAMMONIUM
Список литературы Комплексообразование палладия (II) с бромидом триоктилпропаргиламмония
- Андреев В. П., Тунина С. Г., Усов В. В., Ремизова Л. А. Экстракция цинка бромидом гепт-2-инилтриокти-ламмония//Журнал общей химии. 2003. Т. 73. № 7. С. 10941098.
- Андреев В. П., Тунина С. Г., Ремизова Л. А. Экстракция цинка и меди ацетиленовыми четвертичными аммониевыми солями//Журнал общей химии. 2005. Т. 75. № 5. С. 712718.
- Букин В. И., Андреев В. П., Соболев П. С., Шестаков Д. С. Способ извлечения палладия из водных растворов солей металлов. Патент РФ № 2574266, 2016.
- Общая органическая химия: В 12 т./Под ред. Д. Бартона и У Д. Оллиса. Т. 3. Азотсодержащие соединения/Под ред. И. О. Сазерленда. М.: Химия, 1982. 736 с.
- Желиговская Н. Н., Мельников М. Я., Силаев В. Г., Трофимов В. А. Способ получения цисдиаминхлопрокаинатплатины (II) хлорида. Патент РФ № 2151740, 2000.
- Фомина Н. Ю. Биохимические основы действия соединений палладия на белково-нуклеиновый обмен эукариотических и прокариотических клеток in vivo и in vitro: Дис.. канд биол. наук. Краснодар, 2004. 142 с.
- Ito E., Yip K. W., Katz D. et al. Potential Use of Cetrimonium Bromide as an Apoptosis-Promoting Anticancer Agent for Head and Neck Cancer//Molecular Pharmacology. 2009. Vol. 76. P. 969-983.


