Контроль безопасности продукции, предназначенной для детей: химико-аналитическое обеспечение
Автор: Ларькина М.В., Горячева Л.В., Егорченкова О.Е., Фейсханов М.Р.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Гигиена
Статья в выпуске: 2 т.15, 2019 года.
Бесплатный доступ
Цель: разработка метода измерения концентраций диметилдитиокарбамата цинка (цимата) и диэтилдитиокарбамата цинка (этилцимата) в водных вытяжках, обеспечивающего контроль уровня миграции этих веществ в водную среду и отвечающего требованиям ТР ТС 008 / 2011 «О безопасности игрушек», на основе газохроматографического метода анализа. Материал и методы. Объекты исследования: образцы водной вытяжки из резинолатексных композиций, составляющих основы детских игрушек; стандартные образцы цимата, этилцимата, сероуглерода. Проведены экспериментальные исследования по разработке газохроматографического метода с использованием пламенно-фотометрического детектора, капиллярной колонки и проведением анализа равновесной парогазовой фазы. Результаты. Установлено, что количественное определение цимата и этилцимата в водных вытяжках возможно при сочетании хроматографирования растворов сероуглерода в бензоле и автоматического дозирования парогазовой фазы (сероуглерода, выделившегося в результате кислотного гидролиза в присутствии хлорида олова (II)). Показана эффективность выбранных условий проведения газохроматографического анализа. Рассчитан коэффициент пересчета К, характеризующий поправку значений, полученных путем анализа прямого ввода сероуглерода в бензоле и парофазного анализа. Заключение. Для контроля безопасности продукции, предназначенной для детей, разработан метод измерения концентраций цимата и этилцимата в водных вытяжках из резинолатексных изделий. Метод оформлен в виде методических указаний и обеспечивает нижний предел количественного определения: 0,1 мг / дм3.
Водная вытяжка, детские игрушки, хроматографические методы, цимат, этилцимат
Короткий адрес: https://sciup.org/149135298
IDR: 149135298 | УДК: 614.37(045)
Control of safety of products intended for children: chemical and analytical support
Objective: to develop a method for measuring the concentrations of zinc dimethyldithiocarbamate (cimate) and zinc diethyldithiocarbamate (ethylcymate) in aqueous extracts, which provides control of the level of migration of these substances into the aquatic environment and meets the requirements of TR CU 008 / 2011 «On the safety of toys», based on the gas chromatographic analysis method. Material and Methods. The object of the study included samples of the aqueous extract of rubber latex compositions that form the basis of children»s toys, standard samples of cymate, of ethylcymate, of carbon disulphide. Experimental studies have been carried out to develop a gas chromatographic method using a fame photometric detector, a capillary column and an analysis of the equilibrium vapor-gas phase. Results. It was found out that the quantitative determination of cymate and ethylcymate in aqueous extracts is possible with the combination of chromatography of solutions of carbon disulfde in benzene and automatic dosing of the vapor phase (carbon disulfde released as a result of acid hydrolysis in the presence of tin chloride (II)). The efciency of the selected conditions of gas chromatographic analysis is shown. The conversion factor K, which characterizes the correction of the values obtained by analyzing the direct input of carbon disulfde in benzene and vapor phase analysis, is calculated. Conclusion. To control the safety of products intended for children, developed a method of measuring concentrations of cymate and ethylcymate the aqueous extracts of rubber latex products. The method is designed in the determination: 0,1 mg / dm3.
Текст научной статьи Контроль безопасности продукции, предназначенной для детей: химико-аналитическое обеспечение
1Введение. В современном мире решающим фактором экономического, политического и социального развития является сохранение здоровья людей, и прежде всего здоровья подрастающего поколения. Дети относятся к уязвимым группам населения с точки зрения влияния внешних факторов природной среды. В связи с этим предъявляются высокие требования к материалам, входящим в состав товаров, предназначенных для использования детьми, в том числе игрушек [1].
Среди ассортимента игрушек, представленных на рынке, большое распространение получили изделия на основе резинолатексных композиций. В процессе их производства в качестве вулканизаторов применяют цимат и этилцимат, относящиеся к классу дитиокарбаматов. Цимат и этилцимат являются веществами, обладающими сенсибилизирующим действием.
Миграция цимата и этилциматаиз резиновых игрушек в водную среду в случае превышения установленных значений приводит к проявлению токсического действия [2–3].
Проблема формирования нормативов общей химической нагрузки на детей, достоверной оценки уровней веществ-загрязнителей, присутствующих в объектах среды обитания, характеристика их поступления в организм человека не может быть решена без современных методологий аналитической идентификации ксенобиотиков [4–5].
В целях защиты здоровья детей и лиц, присматривающих за ними, снижения риска воздействия вредных веществ, используемых в производстве товаров детского ассортимента, в принимаемых в Российской Федерации законодательных и нормативных документах повышенное внимание уделяется качеству такой продукции, с тем чтобы обеспечить безопасность реализуемых товаров [1, 4, 5].
Продукты питания и товары, предназначенные для детей, должны проходить тщательный контроль на безопасность, это, в частности, относится и к детским игрушкам, изготавливаемых из различных материалов. Согласно требованиям гигиенической безопасности, изложенным в Техническом регламенте Таможенного союза «О безопасности игрушек» (ТР ТС 008/2011) [1], установленными допустимыми значениями уровней миграции этих веществ в водную среду (ДКМ) являются 0,5 мг/дм3 для этилцимата и 0,6 мг/дм3для цимата [1].
Современные товары детского ассортимента, на которые распространяется действие технического регламента, характеризуются многообразием как по функциональному назначению (изделия для ухода за детьми, одежда, изделия из текстиля, трикотажа, кожи и меха, обувь и кожгалантерейные изделия, коляски и велосипеды, книги, журналы, школьно-письменные принадлежности), так и по качеству используемых для их изготовления материалов (дерево, резина, бумага, картон, различные виды пластмасс, ткань, мех, керамика, кожа и ее заменители) [6].
Перечень контролируемых веществ определяется в зависимости от состава материала и вида изделия.
Таким образом, технологии производства товаров, предназначенных для детей, достаточно разно-
образны, и изготовление товаров из резинового сырья занимает большое место в этом списке.
Процесс производства резиновых изделий включает этап вулканизации, в качестве ускорителей которого используются вещества, относящиеся к классу дитиокарбаматов.
Дитиокарбаматы — вещества с низкой летучестью, в связи с этим наиболее возможный путь загрязнения — миграция их в воду (водно-миграционный путь).
Данные вещества обладают ингаляционной токсичностью, оказывают раздражающее действие на кожу, на слизистую оболочку глаз (вызывают слезотечение, отек) [7].
Дитиокарбаматы — сверхбыстрые ускорители, которые практически не обладают временем индукции. В связи с этим при применении их в качестве первичных ускорителей обычно используются замедлители во избежание ожогов материала, а также инициаторы активации, такие как оксид цинка или жирные кислоты.
Наиболее распространенные дитиокарбаматы, используемые в качестве вулканизаторов в производстве резин: диметилдитиокарбамат цинка (ци-мат), диэтилдитиокарбамат цинка (этилцимат) и дибутилдитиокарбамат. Возможность воспламенения этих соединений уменьшается с увеличением длины алкильной группы: цимат<этилцимат<дибутилдит иокарбамат. Все вещества имеют схожую высокую реакционную способность. Высокая полярность Zn-сульфидных связей приводит к низкой растворимости вулканизаторов в резиновой смеси и снижению ее гомогенности [8–10].
Дитиокарбаматы часто используются для отверждения изделий с низким содержанием серы и низкотемпературного отверждения для белых/прозрачных или ярко окрашенных резиновых изделий и в качестве вторичных ускорителей вулканизации для сокращения времени отверждения.
Фунгицидные препараты на основе дитиокарбаматов, в частности цимат (цирам), получили широкое применение в сельском хозяйстве для борьбы с различными заболеваниями растений [11–12].
Цель: разработка чувствительного, с высокой избирательностью метода определения дитиокарбаматов в водных вытяжках с использованием газохроматографических подходов, который позволял бы контролировать безопасность продукции, предназначенной для детей.
Материал и методы. Объектом исследования были образцы водной вытяжки из резинолатексных композиций, составляющих основы детских игрушек; стандартные образцы цимата, этилцимата, сероуглерода.
Исследование проводили методом газожидкостной хроматографии (ГЖХ) на газовом хроматографе «Кристалл 5000.2» с пламенно-фотометрическим детектором, специфичным на серу (ПФД-S), и малополярной капиллярной колонкой VF-5ms 15 м * 0,53 мм * 0,25 мкм.
В работе использовались образцы аналитических стандартов сероуглерода с содержанием основного компонента не менее 99,9%; цимата с содержанием основного компонента не менее 42,9%; этилцима-та с содержанием основного компонента не менее 97,0%.
Количественную оценку дитиокарбаматов в пробе проводили по градуировочной характеристике, построенной по градуировочным растворам сероуглерода в бензоле различной концентрации.
Исходные и рабочие растворы дитиокарбаматов для внесения с концентрацией готовили растворением каждого из веществ в 0,1 М раствора гидроксида натрия (тщательно перемешивая и помещая в ультразвуковую ванну на 30 минут при температуре 35–37°С).
При подготовке пробы водной вытяжки для анализа исследуемый образец измельчали на кусочки размером приблизительно 1х1 см, взвешивали, помещали в стеклянную емкость с притертой пробкой, заливали дистиллированной водой из расчета 1:10 и выдерживали в течение 3 часов при температуре 37±2°С. Водные вытяжки готовились непосредственно перед анализом.
Для выполнения определения пробу водной вытяжки объемом 5 см3 помещали в стеклянную виалу вместимостью 20 см3. Вносили 5,0 см3 солянокисло-вого раствора двухлористого олова с массовой долей 1,5%. Виалы закрывали герметичными алюминиевыми крышками с фторопластовыми самоуплотняющимися прокладками способом обжима и помещали на 1 час в термостат дозатора равновесного пара (температура 80°С). По завершении процесса вводили в испаритель хроматографа аликвоту парогазовой фазы объемом 2 см3 и анализировали в описанных выше условиях хроматографирования.
Результаты. В рамках наших исследований установлено, что наиболее приемлемым для идентификации диметилдитиокарбамата цинка (цимата) и диэтилдитиокарбамата цинка (этилцимата) в водных вытяжках является метод газожидкостной хроматографии с пламенно-фотометрическим детектором, при котором идентификация веществ проведена по количеству сероуглерода, выделившегося в парогазовую фазу после кислотного гидролиза исследуемой пробы.
Гидролиз дитиокарбаматов до сероуглерода при определении веществ выполнен с использованием дозатора равновесной паровой фазы с применением подкисленного соляной кислотой раствора двухлористого олова (восстановитель). Создание термодинамического равновесия между конденсированной и парогазовой фазами было достигнуто термостатированием герметически закрытых образцов в течение 30 минут при температурах: термостата дозатора равновесного пара 80°С; крана-дозатора 120°С (рис. 1).
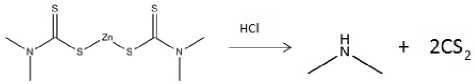
Рис. 1. Схема кислотного гидролиза цимата с образованием сероуглерода
Количественная оценка дитиокарбаматав пробе проведена по градуировочной характеристике, построенной по градуировочным растворам сероуглерода в бензоле.
Градуировочная характеристика, выражающая линейную (с угловым коэффициентом) зависимость десятичного логарифма концентрации сероуглерода в бензоле от десятичного логарифма площади пика построена в диапазоне 0,1-1,0 мкг/см3.
LgС = А*LgS — В (коэффициент корреляции 0,96).
В формулу расчета содержания дитиокарбамата в пробе был введен коэффициент пересчета (К) кон-
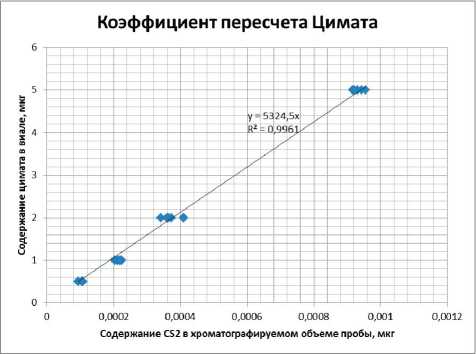
Рис. 2. Зависимость внесенного количества цимата в пробу от содержания сероуглерода в хроматографируемом объеме пробы (мкг в 1 мм3)
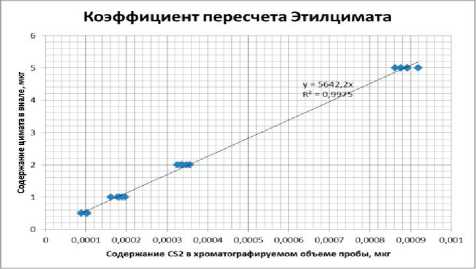
Рис. 3. Зависимость внесенного количества этилцимата в пробу от содержания сероуглерода в хроматографируемом объеме пробы (мкг в 1 мм3)
центрации сероуглерода, найденной по градуировочной характеристике (мкг/см3), построенной на основе анализа градуировочных растворов сероуглерода в бензоле, на содержание цимата/этилцимата (рис. 2, 3) в пробе при парофазном анализе (мкг в виале, в 5 см3 пробы).
Методом наименьших квадратов построено уравнение линейной регрессии зависимости внесенного количества дитиокарбамата в пробу от наблюдаемой концентрации сероуглерода в хроматографируемом объеме пробы, рассчитанной по градуировочной характеристике.
На основе выведенной зависимости коэффициент пересчета содержания сероуглерода, найденный по градуировочной характеристике (мкг), на содержание цимата в пробе при парофазном анализе (мкг в виале, в 5 см3 пробы) составил 5324,5; этилцимата 5642,2.
Исследование зависимости отклика дитиокарбаматов от газовых потоков показало, что пик сероуглерода формируется отчетливо при скорости потока водорода 90,0см3/мин; воздуха 40см3/мин.
Деление потока газа-носителя 10:1 позволило установить одинаковые условия газохроматографического анализа как при детектировании раствора сероуглерода в бензоле (при установлении гра-дуировоной зависимости), так и при анализе проб с внесением (идентификация сероуглерода, выделя- ющегося в результате кислотного гидролиза в равновесную фазу).
Достигнутый нижний предел количественного определения анализируемых дитиокарбаматов в водной вытяжке составил 0,1 мг/дм3, что обеспечивает контроль цимата и этилцимата в соответствии с ТР ТС О08/2011, который регламентирует допустимые уровни миграции в водную среду на уровне 0,5 мг/дм3 (цимат) и 0,6 мг/дм3 (этилцимат). Приготовление водных вытяжек для определения цимата и этилцима-та проводили из пяти видов детских игрушек, приобретенных на потребительском рынке.
В соответствии с Планом разработки методических документов по вопросам организации федерального государственного санитарно-эпидемиологического надзора и обеспечения санитарно-эпидемиологического благополучия населения на 2017–2019 гг. (приказ Роспотребнадзора от 18.08.2017 г. №671) на основании проведенных исследований, обобщения и статистической обработки результатов сформированы Методические указания по измерению концентраций диметилдитиокарбамата цинка (цимата) и диэтилдитиокарбамата цинка (этилцимата) в водных вытяжках для контроля ДКМ указанных веществ в водной среде. Методические указания представлены на утверждение в установленном порядке по разделу «4.1. Методы контроля. Химические факторы».
Обсуждение. Анализ методической базы определения цимата и этилцимата показал, что существует множество подходов измерения веществ: атомноабсорбционная спектроскопия, высокоэффективная жидкостная, газожидкостная хроматография, колориметрическое определение и др.
Жидкостная хроматография является методом, широко используемым для определения остаточных количеств дитиокарбаматов. Однако некоторые комплексы «металл — дитиокарбамат» (например, Zn, Cd, Pb) нестабильны, и их анализ очень затруднен [13]. Реакции замены металла могут происходить между этими комплексами и металлическими компонентами хроматографической системы (например, стальная хроматографическая колонка). Использование свободной от металла колонки или добавление ион-парного агента (например, ЭДТА или дитиокарбамат-кислоты) уменьшает этот обмен для Pb- Cd-комплексов. С другой стороны, анализ дитиокарбаматов цинка напрямую с применением ВЭЖХ невозможен. Поэтому дитиокарбаматы цинка не могут быть проанализированы методом ВЭЖХ с использованием колонки из нержавеющей стали, замена на колонку с PEEK-покрытием не избавляет от образования остаточного металла, в результате чего на хроматограмме присутствуют многочисленные мешающие пики [10].
Существует аналитический метод [14] разделения и количественного определения девяти дитиокарбаматов, в том числе цирама (цимата) в овощах и фруктах с использованием LC-MS/MS. К достоинствам данного подхода можно отнести селективность метода, низкий предел обнаружения, к недостаткам — дорогостоящее оборудование, времязатратную пробо-подготовку, плохую стабильность аналитов.
Колориметрический метод [15–16], основанный на способности производных дитиокарбаминовой кислоты (цимат и этилцимат) разлагаться под действием минеральных кислот, переводя их в интенсивно окрашенный диметил- или диэтилдитиокарбамат меди, не дает возможности одновременного определения перечисленных веществ в одной пробе, т. е. обладает низкой чувствительностью, недостаточной точностью и малой селективностью.
Вольтамперометрический метод [10] требует экстракции органическими растворителями, которая является времязатратной (кропотливой) и недостоверной из-за неполной экстракции диссоциированных комплексов «металл — лиганд».
Методы спектрофотометрии [17–18] и атомно-абсорбционной спектроскопии [19], основанные на количественном обнаружении Zn (II), делают точность определения сомнительной из-за загрязнения образцов этим металлом. Чувствительность определения меньше, чем при газохроматографическом определении CS2.
Достаточно широко используемым методом является метод газожидкостной хроматографии с детекторами электронного захвата (ДЭЗ) и масс-селективным (МСД), основанными на кислотном гидролизе с разложением дитиокарбаматов до сероуглерода, последующей количественной идентификацией (анализом равновесного пара), на хроматографических колонках насадочного или капиллярного типа.
Применение масс-селективного детектирования для анализа сероуглерода затруднительно из-за его малой молекулярной массы — 76.
Продуктами гидролиза дитиокарбаматов наряду с сероуглеродом являются вторичные амины. Особенностью методики определения диметиламина в водных объектах (питьевой воде и воде водоемов) является силанизирование всех контактирующих с газовой фазой поверхностей, что не позволяет применять автоматические и полуавтоматические отборники газовой фазы. Анализ подкисленных водных растворов может привести к разрушению неподвижной фазы капиллярных колонок, что ограничивает применение колонок такого типа в этом методе.
Имеется большой опыт разработанных подходов к определению дитиокарбаматов, основанных на определении дитиокарбаматов путем детектирования сероуглерода, выделившегося в парогазовую фазу в результате гидролиза, анализом равновесного пара (АРП) [22–24]. Отличительная особенность техники АРП состоит в том, что химическая информация, содержащаяся в газовой фазе, используется для заключения о составе контактирующей с ней конденсированной фазы [2–3, 20–21].
Правомерность использования методического подхода определения остаточных количеств цима-та или этилцимата, включающего их разложение до дисульфида углерода (CS2) в кислой среде с последующей его количественной идентификацией газовой хроматографией (анализ равновесного пара), явилась обоснованной.
Особенностью пламенно-фотометрического детектора (ПФД) является наличие экспоненциальной зависимости интенсивности сигнала детектора от концентрации вещества, что приводит к тому, что в области низких концентраций сигналы малы и линейность градуировочной характеристики не всегда соблюдается даже в пределах одного порядка измеряемых концентраций. В этой связи при применении ПФД особое внимание было сосредоточено на подборе условий хроматографирования веществ.
Метод парофазного анализа не позволяет определить уровни извлечения компонентов. В ходе лабораторных экспериментов установлено, что имеет значение только воспроизводимость анализа, которая определяется путем повторного анализа градуировочных растворов сероуглерода в бензоле с последующим их анализом и установлением градуировочных характеристик.
Выбор в качестве растворителя бензола обоснован данными по растворимости в нем сероуглерода.
Количественная оценка вещества реализована на основе построения градуировочной характеристики, выражающей зависимость площади хроматографического пика сероуглерода от его концентрации в растворе бензола с учетом коэффициента пересчета К, характеризующего поправку значений, полученных путем анализа прямого ввода сероуглерода в бензоле и парофазного анализа, и демонстрирующих хорошую сходимость и воспроизводимость результатов.
Применение методических подходов, определенных в настоящем исследовании, может быть приемлемым для идентификации цимата и этилцимата в других объектах окружающей среды и растительной продукции.
Выводы:
-
1. Разработанный метод измерения диметилдитиокарбамата цинка (цимата) и диэтилдитиокарбамата цинка (этилцимата) в водных вытяжках является оптимальным, быстроисполнимым и недорогим для воспроизведения.
-
2. Сравнение полученных данных после прямого ввода растворов сероуглерода в бензоле и автоматического дозирования парогазовой фазы (сероуглерода, выделившегося в результате кислотного гидролиза в присутствии хлорида олова (II)) позволило провести количественное определение диметилдитиокарбамата цинка (цимата) и диэтилдитиокарбамата цинка (этилцимата) в водных вытяжках.
-
3. Созданный метод обеспечивает контроль диметилдитиокарбамата цинка (цимата) и диэтилдитиокарбамата цинка (этилцимата) в водных вытяжках в соответствии с установленными нормативами. Метод оформлен в виде Методических указаний по разделу «4.1. Методы контроля. Химические факторы».
Список литературы Контроль безопасности продукции, предназначенной для детей: химико-аналитическое обеспечение
- Технический регламент Таможенного союза ТР ТС 008 / 2-11 "О безопасности игрушек". M., 2011
- Ракитский В. Н., Юдина Т. В., Федорова Н. Е. Методические проблемы химико-аналитического обеспечения безопасности продукции, выращенной с применением дитиокарбаматов. Международный научно-исследовательский журнал 2014; 4: 21-2
- Юдина Т. В., Федорова Н. Е., Волкова В. Н., Ларькина М. В. Химико-аналитическое обеспечение безопасности продукции, выращенной с применением дитиокарбаматов. В кн.: Современные проблемы гигиены и эпидемиологии и пути их решения: сборник научных трудов ФНЦГ им. Ф. Ф. Эрисмана. Воронеж, 2008; с. 341-5
- Дитиокарбаматные пестициды, этилентиомочевина и пропилентиомочевина: общее введение. Всемирная Организация Здравоохранения, 1991; c. 143
- Концепция долгосрочного социально-экономического развития Российской Федерации на период до 2020 года от 17.11.2008 г. №1662-p (в ред. от 10.02.2017 г. №172). URL: http://www.consultant.ru / document / cons_doc_ LAW_82134 / 28c7f9e359e8af09d7244d8033c66928fa27e527
- ГОСТ 25779-90 "Игрушки. Общие требования безопасности и методы контроля". М.: ИПК Издательство Стандартов, 2008
- Joseph AM, George B, Madhusoodanan KN, Alex R. Current status of sulphur vulcanization and devulcanization chemistry: Process of vulcanization. Rubber Science 2015; 28 (1); 82-121. URL: https://www.researchgate.net / publication / 275519885_ current_status_of_sulphur_vulcanization_ and_devulcanization_ chemistry_process_of_vulcanization (25.09.2018)
- Kaniwa MA. High-performance liquid chromatographic identifcation and determination of dithiocarbamates in vulcanized rubber products. Journal of Chromatography A 1987; 405: 263-71
- Weissmahr KW, Houghton CL, Sedlak DL. Analysis of the Dithiocarbamate Fungicides Ziram, Maneb, and Zineb and the Flotation Agent Ethylxanthogenate by Ion-Pair Reversed-Phase HPLC. Analytical Chemistry 1998; 70 (22): 4800-4
- Mathieu C, Herbreteau B, Lafosse M, et al. Liquid Chromatography of Unstable Zinc Dithiocarbamates: Application to Rubber Gloves Analysis. Journal of High Resolution Chromatography 2000; 23 (9): 565-6
- Каспаров В. А., Промоненков В. К. Применение пестицидов за рубежом. М.: Агропромиздат, 1990; 224 с.
- Directory of pesticides and agrochemicals approved for use in the Russian Federation. Moscow: Agrorus 2018; 771 p. Russian (Справочник пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации. М.: Агрорус, 2018; 771 с.
- Depree GJ, Bledsoe TA, Siegel PD. Determination of Zinc Dialkyldithiocarbamates in Latex Condoms. Journal of Chromatographic Science 2002; 42: 80-4
- Gustafsson KH, Fahlgren CH. Determination of dithiocarbamate fungicides in vegetable food stufs by high-performance liquid chromatography. Journal of Agricultural and Food Chemistry 1983; 31 (2): 461-3
- Методические указания по санитарно-гигиенической оценке резиновых и латексных изделий медицинского назначения. М., 1988; 25 с.
- Колориметрическое определение купроцина-II, манеба, марцина, полимарцина, поликарбацина, тиазона, ТМТД, цинеба, цирама и эдитона в воздухе, продуктах питания растительного происхождения и биологических средах. В кн.: Методы определения микроколичеств пестицидов: сборник методических указаний. М.: Колос, 1977; c. 238-41
- Mathew L. Spectrophotometric determination of ziram (dithiocarbamate fungicide) by thiocyanate and rhodamine 6G method. Talanta 1995; 42 (1): 41-3
- Kaur M, Kaur V, Malik AK, et al. Developmant of a Derivative Spectrophotometric Method for the Determination of Fungicide Zinc Ethylenebisthiocarbamate using Sodium Molibdate. Journal of the Brazilian Chemical Society 2009; 20 (5): 993-8
- Al-Alam J, Bom L, Chbani A, et al. Analysis of Dithiocarbamate Fungicides in Vegetable Matrices using HPLC- UV followed by Atomic Absorption Spectrometry. Journal of Chromatographic Science 2016; 12: 1-7
- Методические указания по газохроматографическому парофазному определению дитиокарбаматов в растительном материале: МУК 4.1.2016-05. М.: ФЦиГ Роспотребнадзора, 2009; с. 84-90
- Измерение концентраций тирама в воздухе рабочей зоны и атмосферном воздухе населенных мест методом газожидкостной хроматографии: МУК 4.1.1418-03. В кн.: Определение остаточных количеств пестицидов в пищевых продуктах, сельскохозяйственном сырье и объектах окружающей среды: сборник методических указаний. М.: ФЦГиЭ Роспотребнадзора, 2007; с. 15-23
- Методические указания по измерению концентраций манкоцеба в атмосферном воздухе населенных мест методом газожидкостной хроматографии: МУК 4.1.2141-06. В кн.: Определение остаточных количеств пестицидов в пищевых продуктах, сельскохозяйственном сырье и объектах окружающей среды: сборник методических указаний. М.: ФЦГиЭ Роспотребнадзора, 2009; с. 34-44
- Определение остаточных количеств тирама методом газохроматографического парофазного анализа: МУК 4.1.2708-10. В кн.: Сборник МУК 4.1.2668-10, 4.1.2675- 4.1.2679-10, 4.1.2683-4.1.2684-10, 4.1.2687-10, 4.1.2690-10, 4.1.2706-4.1.2709-10, 4.1.2768-10. М.: ФЦиГ Роспотребнадзора, 2011; 191 c.
- Измерение концентраций пропинеба в воздухе рабочей зоны и смывах с кожных покровов операторов методом газохроматографического парофазного анализа МУК 4.1.3194-14. М.: ФЦГиЭ Роспотребнадзора, 2015; 25 c.


