Коррекция лекарственно-индуцированной гепатотоксичности новыми тритерпеновыми производными (экспериментальные исследования)
Автор: Бессергенева Е.П., Жукова Н.А., Толстикова Т.Г., Сорокина И.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 6 (48), 2011 года.
Бесплатный доступ
Проведено морфологическое исследование влияния новых тритерпеновых производных - 3β,28-ди-О-никотинат бетулина (of 3) и метилового эфира 3,20-диоксимино-29-норлуп-28-овой кислоты (of 15) на печень мышей СВА/Lac с перевитой лимфомой RLS на фоне и без полихимиотерапии. Установлено, что введение агентов of 3 и of 15 животным-опухоленосителям на фоне по- лихимиотерапии уменьшает объем и степень токсического поражения печени, митотическую активность опухолевых клеток в первичном узле как на фоне полихимиотерапии, так и без нее и оказывает умеренное противоопухолевое действие. Эти свойства наиболее выражены у агента of 15. Введение агентов of 3 и of 15 животным с перевитой лимфомой RLS уменьшает выраженность альтеративных изменений, связанных с общим и местным влиянием неопластического процесса.
Метастазирование в печень мышей лимфомы rls, полихимиотерапия, гепатопротективный эффект, 28-ди-о-никотинат бетулина (of 3), метиловый эфир 3, 20-диоксимино-29-норлуп-28-овой кислоты (of 15)
Короткий адрес: https://sciup.org/14055964
IDR: 14055964 | УДК: 616.36-099:615.244]-092.9
Correction of drug-induced hepatotoxicity with the new triterpene derivatives (experimental research)
A morphological study of influence of new triterpene derivatives - 3β,28-di-O-nikotinate of betuline (of 3) and methyl ether 3, 20-dioximino-29-norlup-28-oic acid (of 15) on liver of mice CBA/Lac with transplanted lymphoma RLS against polychemotherapy background and without it was carried out. It was shown that administration of the agents of 3 and of 15 to the tumor-bearing mice against polychemotherapy background reduces volume and extent of toxic liver injury, mitotic activity of cancer cells in the primary tumor nodule against polychemotherapy background and without it and displays moderate antineoplastic activity. Of 15 agent has more expressed such characteristics. Administration of the agents of 3 and of 15 to the animals with transplanted lymphoma RLS results in a decrease of intensity of alterative changes associated with general and local influence of neoplastic process.
Текст научной статьи Коррекция лекарственно-индуцированной гепатотоксичности новыми тритерпеновыми производными (экспериментальные исследования)
Гепатотоксичность является одним из серьезных осложнений интенсивной лекарственной терапии многих заболеваний, в том числе и злокачественных новообразований. Известно, что токсические реакции при проведении химиотерапии реализуются через химические и иммунологические механизмы, нередко носят кумулятивный характер, препятствуют проведению курсового лечения в установленные сроки, сопровождаются снижением эффективности цитостатической терапии и требуют постоянной коррекции гепатотропными средствами в межкурсовой период [2]. В связи с этим поиск новых эффективных и экономически доступных веществ, обладающих протективными свойствами, по–прежнему является актуальным. В последние годы внимание фармакологов и специалистов в области меди- цинской химии привлекают природные тритерпеноиды лупанового ряда, сочетающие широкий спектр биологической активности c экономической доступностью. Так, у производных бетулиновой и бетулоновой кислот выявлены противоопухолевая, противовирусная, бактериостатическая, антиоксидантная, гепатопротекторная и противовоспалительная активности [9–13].
Цель работы – изучение протективных свойств новых производных бетулина у животных с перевитой лимфомой RLS на фоне и без полихимиотерапии.
Материал и методы
Для исследования взяты новые производные бетулина: 3β,28-ди-О-никотинат бетулина (of 3) и метиловый эфир 3,20-диоксимино-29-норлуп-28-овой кислоты (of 15), синтезированные в Институте органической химии
УНЦ РАН (проф. О.Б. Казакова). Эксперименты проведены на 60 мышах-самцах линии СВА/Lac с исходной массой тела 22–25 г, содержавшихся в условиях стандартного вивария. Всем животным перевивали внутримышечно в бедро задней лапы мышиную лимфому RLS в виде суспензии опухолевых клеток в физиологическом растворе (0,1 мл, 2×105 клеток/мл). Перевивочный материал был получен из банка опухолей лаборатории регуляции экспрессии генов Института цитологии и генетики СО РАН (к.б.н. В.И. Каледин, к.м.н. В.П. Николин, к.б.н. Н.А. Попова).
На 5-й день после перевивки опухоли мышей делили на 6 групп (по 10 особей в каждой). Всем животным, за исключением I, IV и VI группы, вводили однократно внутрибрюшинно комплекс цитостатических препаратов, моделирующих полихимиотерапию (ПХТ) [3]: доксорубицин («Лэнс-Фарм», Москва) – 4 мг/кг, цикло-фосфан («Биохимик», Саранск) – 50 мг/кг, винкристин («Гедеон Рихтер», Венгрия) – 0,1 мг/кг и преднизолон («Гедеон Рихтер», Венгрия) – 5 мг/кг массы тела. В последующие 7 дней двум группам мышей (III и IV) вводили внутрижелудочно через зонд of 3, а V и VI группам – of 15, трижды через день в дозе 100 мг/кг в водно-твиновом растворе из расчета по 0,2 мл/10 г массы. Группа сравнения (II) и контроль (I группа) получали водно-твиновую смесь.
На 2, 4, 6-е сут после введения of 3 и of 15 на фоне и без ПХТ определяли объём опухоли путём измерений первичного узла по трём взаимоперпендикулярным направлениям. На 7-е сут после введения ПХТ животных выводили из опыта декапитацией под эфирным наркозом и определяли массу тела, массу опухоли (по разнице в массе лапы с опухолью и здоровой коллатеральной лапы). Подсчитывали индекс торможения роста опухоли (ТРО %): отношение разности массы опухоли в контрольной (mk) и опытных (mo) группах к массе опухоли в контроле: mk – mo/mk.
Печень, первичный опухолевый узел фиксировали в 10 % параформальдегиде на 0,1 М фосфатном буфере Зёренсена (pH 7,4) в течение 4 сут с последующей стандартной обработкой на гистологическом комплексе MICROM («Карл Цейс» Германия). Срезы толщиной 4 мкм окрашивали гематоксилином и эозином, ставили ШИК-реакцию с докраской гематоксилином и оранжевым G. Препараты исследовали методом световой микроскопии в проходящем свете на микроскопе Axioskop 40.
Морфометрический анализ срезов проводили с использованием окулярной сетки на 289 точек [1]. В печени подсчитывали объемную плотность гепатоцитов с дистрофическими и некротическими повреждениями, объемную плотность синусоидов со свободным просветом, с фибрином и метастазами. В первичном опухолевом узле подсчитывали количество митозов на 1000 клеток с расчетом митотического индекса: МИ = Nm./N; где Nm – число митозов, N – общее количество клеток. Изменение данных параметров в группах подопытных животных выражали в процентах относительно контроля (I) и референс–группы с ПХТ (II), показатели которых приняты за 100 %. Статистическую обработку данных проводили методами параметрической статистики с использованием пакета программ «Microsoft Excel». Результаты считали достоверными при значении критерия Стьюдента p<0,05.
Результаты и обсуждение
Лимфома RLS, резистентная к циклофосфану, получена путем многократных перевивок из лимфомы LS, растет в виде солидного узла, метастазирует гематогенно в печень, почки, селезенку [4, 5]. Противоопухолевое действие агентов оценивалось по средним размерам опухоли. Показано, что на 2-е сут в опытных группах размеры опухоли не отличались от контроля. При применении агентов of 3 и of 15 на фоне ПХТ на 4-е и 6-е сут отмечалось выраженное уменьшение средних размеров опухоли (табл. 1). Так, после введения of 15 ингибирование роста опухоли на 4-е и 6-е сут составило 31 % и 47 % соответственно, а введение of 3 приводило к торможению роста опухоли на 35 % на 6-е сут. В группе животных на фоне ПХТ индекс ТРО составил лишь 27 % (табл. 1). На 7-е сут тенденция к уменьшению роста опухоли сохранялась только у животных, получавших of 15 на фоне ПХТ. При подсчете митозов в первичном узле опухоли было установлено, что торможение роста опухоли происходит за счет угнетения митотической активности. Наибольший положительный эффект отмечается в группе животных, получавших of 15. Как на фоне ПХТ, так и при индивидуальном введении агента of 15 митотический индекс уменьшается на 28 % и 40 % соответственно. Введение агента of 3 в сочетании с ПХТ приводит к снижению митотического индекса на 32 %, а при индивидуальном введении митотическая активность так же, как и в группе с ПХТ, повышается на 32 % (табл.2). В референсной группе (ПХТ) митотический индекс увеличился на 33 % по сравнению с контролем, что связано с устойчивостью данного штамма опухоли к циклофосфану. Таким образом, агент of 15 проявляет умеренно выраженное противоопухолевое действие при индивидуальном применении и обладает способностью усиливать
Таблица 1
Средние размеры и индекс торможения роста опухоли в период введения агентов
Митозы в первичном узле перевитой опухоли RLS
|
Группы |
2-е сут |
4-е сут |
6-е сут |
7-е сут |
||||
|
Размеры опухоли, см3 |
ТРО |
Размеры опухоли, см3 |
ТРО |
Размеры опухоли, см3 |
ТРО |
Размеры опухоли, см3 |
ТРО |
|
|
I (контроль) |
0,14 ± 0,02 |
0,55 ± 0,05 |
1,42 ± 0,18 |
2,39 ± 0,25 |
||||
|
II (ПХТ) |
0,14 ± 0,01 |
0 |
0,49 ± 0,04 |
10 |
1,03 ± 0,08 |
27 % |
2,12 ± 0,16 |
11,3 % |
|
III (ПХТ + of 3) |
0,13 ± 0,01 |
7,4 % |
0,47 ± 0,05 |
14,5 % |
0,92 ± 0,09* |
35 % |
2,27 ± 0,28 |
5 % |
|
IV (of 3) |
0,14 ± 0,01 |
0 |
0,53 ± 0,07 |
3,6 % |
0,98 ± 0,16 |
31 % |
1,79 ± 0,35 |
25 % |
|
V (ПХТ + of 15) |
0,14 ± 0,01 |
0 |
0,38 ± 0,05* |
31 % |
0,75 ± 0,07** |
47 % |
1,84 ± 0,19 |
23 % |
|
VI (of 15) |
0,13 ± 0,01 |
7,4 % |
0,53 ± 0,05 |
3,6 % |
1,04 ± 0,10 |
28 % |
2,12 ± 0,29 |
11 % |
Примечание: * – различия, статистически значимые по сравнению с I группой (р<0,05); ** – различия, статистически значимые по сравнению с I группой (р<0,01).
Таблица 2
|
Группы |
Кол-во митозов |
Митотический индекс |
Эффективность |
|
I (контроль) |
34,5 ± 2,71 |
0,0345 (3,45 %) |
100 % |
|
II (ПХТ) |
45,89 ± 1,36 ** |
0,0489 (4,89 %) |
141 % |
|
III (ПХТ + of 3) |
34,9 ± 1,13 ### |
0,0349 (3,49 %) |
71 % |
|
IV (of 3) |
45,63 ± 1,15 ** |
0,0456 (4,57 %) |
132 % |
|
V (ПХТ + of 15) |
25,13 ± 1,16 ### |
0,0251(2,51%) |
51 % |
|
VI (of 15) |
21 ± 0,91 *** |
0,021 (2,1 %) |
60 % |
Примечание: ** – различия, статистически значимые по сравнению с контрольной группой (p≤0,01); *** – различия, статистически значимые по сравнению с контрольной группой (p≤0,001); ###– различия, статистически значимые по сравнению с группой с ПХТ (p≤0,001).
цитостатическое действие полихимиотерапии.
В ходе микроскопического анализа печени были выявлены типичные морфологические изменения, связанные с общим и местным влиянием опухоли. Установлено, что у мышей всех групп типичные изменения наблюдались в виде обширных перипортальных и диффузных клеточных метастазов в просвете сину-соидов с активным делением в них опухолевых клеток, развитием внутрипеченочного холестаза с локальной перестройкой печеночных балок. У животных контрольной группы ведущим признаком поражения гепатоцитов были мелковезикулярная липидная инфильтрация, гидропическая дистрофия, мелкоочаговые некрозы гепатоцитов с признаками поражения синусоидального русла (утолщение стенок синусоидов и заполнение их просветов фибрином).
Показано, что однократное введение животным ПХТ приводит к развитию токсического повреждения печени. Альтеративные изменения в ткани печени проявляются выраженным синдромом регенераторно-пластического дефицита (дистрофия, атрофия и некроз). Так, в парен- химе выявлялись множественные фокальные сливные и мелкоочаговые некрозы печеночных клеток. В гепатоцитах преобладает гидропическая и баллонная дистрофия. Мелковезикулярная липидная инфильтрация выявляется лишь в виде мелких очагов в центролобулярных зонах. В синусоидальном русле преобладает диффузная опухолевая инфильтрация (рис. 1).
Морфометрический анализ подтвердил, что введение комплекса цитостатиков сопровождается увеличением доли некробиотических процессов над дистрофическими. На 500 % увеличился объем некрозов (табл. 3). Объемная плотность гепатоцитов с тяжелыми видами дистрофий увеличилась на 81 %, а доля гепатоцитов с липидной инфильтрацией уменьшилась на 37 %. Рост объемной плотности метастазов в просвете синусоидов составил 200 %. Таким образом, у животных с лимфомой RLS, после введения ПХТ развился тяжелый лекарственный гепатит, сопровождающийся увеличением доли деструктивно-некротических поражений гепатоцитов.
Введение производных бетулина of 3 и of 15 на фоне химиотерапии приводит к уменьшению объёмной
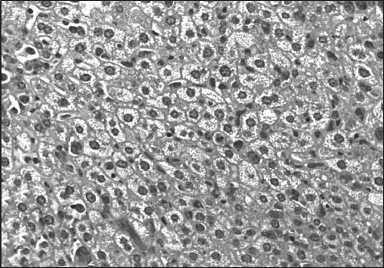
Рис. 1. Микрофото. Печень мыши с перевитой лимфомой RLS на фоне полихимиотерапии. Тотальная жировая инфильтрация гепатоцитов, в синусоидах – метастазы опухоли.
Окраска гематоксилином и эозином. ×400
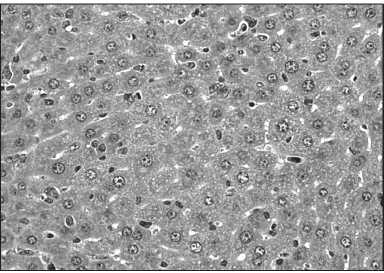
Рис. 2. Микрофото. Печень мыши с перевитой лимфомой RLS после введения агента of 15 на фоне полихимиотерапии. Очаговая мелковезикулярная липидная инфильтрация гепатоцитов, в синусоидах – метастазы опухоли. Окраска гематоксилином и эозином. ×400
плотности некрозов в паренхиме печени, способствует появлению двуядерных гепатоцитов и частичному купированию признаков холестаза. В гепатоцитах выявляется мелковезикулярная липидная инфильтрация и очаговая гидропическая дистрофия (рис. 2). Морфометрический анализ подтвердил, что введение тестируемых агентов привело к уменьшению доли некробиотических поражений в печени. Под влиянием агентов of 3 и of 15 объем некрозов уменьшился в среднем на 80 % по сравнению с референсной группой. Однако введение агента of 3 привело к уменьшению доли гепатоцитов с мелковезикулярной липидной инфильтрацией на 33 % и не оказало положительного влияния на состояние синусоидального русла: доля синусоидов с фибрином и метастазами увеличилась на 78 % и, напротив, введение агента of 15 привело к уменьшению этого показателя на 40 % (табл. 3).
При введении агентов of 3 и of 15 животным без полихимиотерапии в гепатоцитах выявляются признаки как тяжелых деструктивных изменений (в виде гидропической, баллонной дистрофии), так и менее выраженных (в виде мелковезикулярной липидной инфильтрации). В просвете синусоидов видны нити фибрина, увеличенные синусоидальные клетки. Признаки внутрипеченочного холестаза менее выражены, чем у контрольных животных. При морфометрическом анализе выявлено, что введение агентов of 3 и of 15 сопровождается уменьшением объемной плотности некрозов на 83 % и доли синусоидов с фибрином на 20 % (табл. 4). Таким образом, введение исследуемых агентов уменьшает выраженность типичных морфологических изменений, связанных с общим и местным влиянием неопластического процесса.
Полученные результаты коррелируют с данными, полученными ранее у мышей с перевитой лимфомой RLS после введения бетулоновой кислоты и ее аланинамидного производного на фоне и без ПХТ [5]. Обращает внимание точная воспроизводимость типичных патологических процессов после введения производных бетулина и бетулоновой кислоты, сопровождающихся
Таблица 3
Показатели морфометрического исследования печени животных с перевитой лимфомой RLS на фоне ПХТс введением агентов of 3 и of 15
|
Группы |
Дистрофия гепатоцитов |
Некрозы гепатоцитов |
Просвет синусоидов |
|||
|
Мелковезикулярная жировая |
Гидропическая баллонная |
Свободный |
Фибрин |
Метастазы |
||
|
I (контроль) |
0,49 ± 0,038 |
0,11 ± 0,015 |
0,018 ± 0,005 |
0,06 ± 0,001 |
0,24 ± 0,03 |
0,08 ± 0,023 |
|
II (ПХТ) |
0,31 ± 0,013** |
0,20 ± 0,025* |
0,11 ± 0,02** |
0,053 ± 0,004 |
0,18 ± 0,01 |
0,16 ± 0,01* |
|
III (ПХТ + of 3) |
0,24 ± 0,01# |
0,21 ± 0,015 |
0,014 ± 0,005# |
0,06 ± 0,009 |
0,31 ± 0,02# |
0,16 ± 0,02 |
|
V (ПХТ + of 15) |
0,47 ± 0,08 |
0,19 ± 0,07 |
0,01 ± 0,001# |
0,06 ± 0,008 |
0,11 ± 0,024# |
0,15 ± 0,01 |
Примечание: ** – различия, статистически значимые по сравнению с контрольной группой (p≤0,01); # – различия, статистически значимые по сравнению с группой с ПХТ (p≤0,01).
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2011. №6 (48)
Таблица 4
|
Группы |
Дистрофия гепатоцитов |
Некрозы гепатоцитов |
Просвет синусоидов |
|||
|
Мелковезикулярная жировая |
Гидропическая баллонная |
Свободный |
Фибрин |
Метастазы |
||
|
I (контроль) |
0,49 ± 0,038 |
0,11 ± 0,015 |
0,018 ± 0,005 |
0,06 ± 0,001 |
0,24 ± 0,03 |
0,08 ± 0,023 |
|
IV (of 3) |
0,46 ± 0,05 |
0,14 ± 0,035 |
0,003 ± 0,002* |
0,07 ± 0,008 |
0,19 ± 0,02 |
0,13 ± 0,019 |
|
VI (of 15) |
0,46 ± 0,05 |
0,14 ± 0,035 |
0,003 ± 0,002* |
0,07 ± 0,008 |
0,19 ± 0,02** |
0,13 ± 0,02 |
Показатели морфометрического исследования печени животных с перевитой лимфомой RLS после введения агентов of 3 и of 15
Примечание: * – различия, статистически значимые по сравнению с контрольной группой (p≤0,05); ** – различия, статистически значимые по сравнению с контрольной группой (p≤0,01).
улучшением структуры печени. Выявленное положительное влияние агентов of 3 и of 15 на состояние синусоидального русла приводит к улучшению процессов транссинусоидального обмена [6–8]. На основании этих фактов можно предположить, что выявленное гепато-протективное действие новых производных бетулина также реализуется посредством стабилизации клеточных мембран.
Выводы
-
1. Проведение полихимиотерапии животным с перевитой лимфомой RLS приводит к развитию токсического повреждения печени.
-
2. Введение 3β,28-ди-О-никотината бетулина (of 3) и метилового эфира 3,20-диоксимино-29-норлуп-28-овой кислоты (of 15) животным-опухоленосителям на фоне полихимиотерапии уменьшает объем и степень токсического поражения печени. Эти свойства наиболее выражены у метилового эфира 3,20-диоксимино-29-норлуп-28-овой кислоты (of 15).
-
3. Введение агентов of 3 и of 15 животным с перевитой лимфомой RLS уменьшает выраженность альте-ративных изменений, связанных с общим и местным влиянием неопластического процесса.
-
4. Метиловый эфир 3,20-диоксимино-29-норлуп-28-овой кислоты (of 15) в сочетании с полихимиотерапией и без нее уменьшает митотическую активность опухолевых клеток в первичном узле и вызывает задержку роста опухоли.
-
5. Сочетание выявленных свойств у 3β,28-ди-О-никотината бетулина (of 3) и метилового эфира 3,20-диоксимино-29-норлуп-28-овой кислоты (of 15) позволяет рекомендовать их для дальнейшего изучения в качестве высокоэффективных корректоров гепатоток-сического действия цитостатиков.
Работа выполнена в рамках Интеграционной программы СО РАН (N 93) «Развитие исследований в области медицинской химии и фармакологии как научной основы разработки отечественных лекарственных препаратов».


