Краткий обзор по итогам VI Всемирного симпозиума по лёгочной гипертензии 2018 г. в Ницце: взгляд молодого учёного
Автор: Таран Ирина Николаевна
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Обзор мероприятий
Статья в выпуске: 2, 2018 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/143165115
IDR: 143165115
A brief summary of the results of the 6th World symposium on pulmonary hypertension in Nice in 2018: view of a young scientist
Текст обзорной статьи Краткий обзор по итогам VI Всемирного симпозиума по лёгочной гипертензии 2018 г. в Ницце: взгляд молодого учёного
Впервые Всемирный Симпозиум по проблеме легочной гипертензии (ЛГ) состоялся в Женеве в 1973 году и в дальнейшем, после издания «Эвианской классификации» легочной артериальной гипертензии (ЛАГ) в 1998 г в рамках второго всемирного симпозиума, проводился традиционно каждые 5 лет (Венеция 2003, Дана Поинт 2008, Ницца 2013). В 2018 году местом проведения симпозиума была выбрана Ницца, завораживающая шумом морского прибоя и мартовским снегопадом.
Основной целью данного симпозиума явился обзор главных научных достижений в сфере ЛГ за прошедшие 5 лет и обсуждение возможности проведения совместных исследовательских программ для пополнения доказательной базы.
В начале симпозиума было уделено внимание патофизиологии ЛГ. В докладе Guignabert С. обсуждался вклад воспаления в процесс ремоделирования легочного сосудистого русла, возможность выделения провоспалительного фенотипа эндотелиальных клеток легочных артерий (ЛА).
В сфере генетики обсуждалась перспектива создания биобанков для пациентов с ЛАГ и разработка новой генетической панели для данной когорты пациентов.
В своем докладе Morrel N.W. представил новые генетические мутации при ЛАГ, имеющие высокий уровень доказанности: P-тип АТФазы (ATP13A3), фактор роста и дифференциации 9 (GDF2) (BMP9), SRY (Sex determining region Y) Box 17 (SOX17); мутацию гена Аквапорина 1 (AQP1) с более низким уровнем доказанности.
Известно, что у пациентов с ИЛГ и различными формами ЛАГ нарушена регуляция сигнальной системы белка костного морфогенеза. Ведутся разработки в создании манипуляций, непосредственно влияющих на генетическую мутацию рецептора 2-го типа белка костного морфогенеза (BMPR 2), как у пациентов с наследуемой ЛАГ, так и у пациентов с ИЛГ.
В настоящий момент является актуальным фенотипирование пациентов с ЛГ для дальнейшей индивидуализации тактики лечения и определения прогноза.
За последние годы фенотип пациентов с ЛАГ значимо изменился. Данное заболевание верифицируется у пациентов более старшего возраста (45-60 лет), с более высоким индексом массы тела и обширным спектром коморбидных состояний.
В докладе Rabinovitch M. были продемонстрированы данные о выделении новых фенотипов ЛАГ, представленных в виде 4 иммунных кластеров во время проведения протеомики цитокинов.
Также представляет интерес вклад генетических мутаций в клинический фенотип и прогноз пациентов с ЛАГ.
В разделе диагностики впервые за прошедшие 20 лет обсуждался вопрос об изменении диагностического критерия ЛГ в виде снижения порога среднего давления в легочной артерии (срДЛА) до 20 мм рт. ст. согласно данным катетеризации правых отделов сердца (КПОС). При этом данные изменения касаются пациентов Группы 1 и 3. Однако эксперты предлагают оставить прежний порог срДЛА >25 мм рт. ст. у пациентов с хронической тромбоэмболической ЛГ (ХТЭЛГ).
Для пациентов Группы 2 для верификации диагноза также было предложено снижение порога срДЛА до 20 мм рт. ст. Однако при определении изолированной или смешанной пост- и прекапиллярной ЛГ было предложено исключить значение диастолического градиента давления. Преобразованные критерии для установления изолированной посткапиллярной ЛГ выглядят следующим образом: уровень давления заклинивания ЛА (ДЗЛА) >15 мм рт. ст., срДЛА >20 мм рт. ст и легочное сосудистое сопротивление (ЛСС) <3 ед Вуда. Тогда как критерии смешанной пост- и прекапиллярной ЛГ: ДЗЛА >15 мм рт. ст., срДЛА >20 мм рт. ст и ЛСС >3 ед Вуда.
У пациентов со значением ДЗЛА 13-15 мм рт. ст. и высокой/про-межуточной вероятностью наличия ЛГ ввиду сердечной недостаточности (СН) с сохранной фракцией выброса (ФВ) предполагается рассмотрение нагрузочного теста с внутривенной инфузией 500 мл физиологического раствора во время КПОС в течение 5 минут. При повышении ДЗЛА >18 мм рт. ст. после пробы очевидно превалирование посткапиллярного компонента.
При этом назначение различной специфической терапии в рамках РКИ с целью оценки ее безопасности и переносимости у пациентов с ЛГ на фоне СН с сохранной ФВ оказалось безуспешным и даже небезопасным.
В разделе относительно новых и перспективных диагностических методик, позволяющих оценить функцию правого желудочка (ПЖ), был представлен эхокардиографический (ЭхоКг) метод – двумерный стрейн (2D strain). Оценка деформации ПЖ позволяет выявить субклиническое ухудшение функции ПЖ до момента развития более выраженных изменений. Продольный стрейн свободной стенки ПЖ отражает функцию миокарда ПЖ и является сильным прогностическим фактором.
Требуется проведение многоцентровых проспективных клинических исследований с включением различных групп пациентов с ЛГ для определения роли метода ЭхоКг и магнитно-резонансной томографии (МРТ) в оценке стрейна ПЖ в клинической практике.
Акцентировалось внимание на оценке взаимодействия ПЖ и ЛА, адаптации ПЖ к постнагрузке с помощью определения сопряжения ПЖ – ЛА.
В настоящий момент предложено несколько вариантов оценки сопряжения ПЖ – ЛА. Первым методом является оценка функции ПЖ с помощью анализа Pressure-Volume loops (Петли Давления – Объема). Этот метод заключается в инвазивной оценке давления и объема желудочков, что отражается на диаграммах и в дальнейшем используется для расчета сердечно-сосудистого (СС) сопряжения.
СС сопряжение представлено в виде отношения эффективной артериальной жесткости (Ea) к конечно-систолической жесткости желудочка (Es). Для малого круга кровообращения расчет эффективной артериальной жесткости проводится по формуле: Ea = (срДЛА – ДЗЛА)/УО, где УО –ударный объем ПЖ; расчет конечной систолической жесткости ПЖ проводится по формуле : Emax = срДЛА/КСО, где КСО – конечно-систолический объем.
Второй методикой оценки СС сопряжения является использование двумерной (2D) и трехмерной (3D) трансторакальной ЭхоКг. C помощью 2D-ЭхоКг оцениваются срДЛА, ДЗЛА, УО, тогда как 3D-ЭхоКг позволяет оценить КСО ПЖ. И по соответствующим формулам рассчитывается сопряжение ПЖ-ЛА.
На базе отдела легочной гипертензии и заболеваний сердца, отдела ультразвуковой диагностики ФГБУ НМИЦ кардиологии Минздрава России проводится научная работа по изучению динамических изменений СС сопряжения ПЖ – ЛА у пациентов с ИЛГ и неоперабельной ХТЭЛГ на фоне различной специфической терапии. Было выявлено, что параметры СС ПЖ – ЛА имеют прямые взаимосвязи с параметрами шкалы стратификации риска летального исхода пациентов с ЛАГ, что говорит о возможности их применения в оценке тяжести состояния пациента. Так же представляет интерес использование данного метода при фенотипировании пациентов с ИЛГ и ХТЭЛГ. Результаты работы были представлены в рамках данного симпозиума в виде постерного доклада (рис. 1).
В докладе Noodredegraaf A.V. и в ряде пилотных работ, представленных в качестве постеров на симпозиуме, для расчета сопряжения ПЖ – ЛА использовалось отношение систолической экскурсии кольца трикуспидального клапана к систолическому давлению в ПЖ. Данное отношение может иметь прогностическое значение, но не отражает сопряжения ПЖ -ЛА.
В разделе диагностики и стратификации риска пациентов с ЛГ обсуждалось использование метода спировелоэргометрии (СВЭМ) и его роль в клинической практике. Данная методика нашла свое применение в оценке тяжести, риска и прогноза пациентов с ЛГ. Так же проведение СВЭМ в динамике необходимо при оценке эффективности проводимой специфической терапии и проводимых реабилитационных программ.
В рамках симпозиума был продемонстрирован опыт отдела легочной гипертензии и заболеваний сердца ФГБУ НМИЦ кардиологии Минздрава России. В постерном докладе был освещен вклад СВЭМ в оценку риска пациентов с ЛАГ. Согласно результатам ис-

На фотографии представлена часть делегации из Москвы, кото-
рая принимала участие в данном симпозиуме.
Слева направо: Таран Ирина Николаевна – аспирант отдела легочной гипертензии и заболеваний сердца, ФГБУ «НМИЦ Кардиологии» Минздрава Росссии;
Царева Наталья Анатольевна – к.м.н., доцент кафедры пульмонологии ФГАОУ Первый МГМУ им. И.М. Сеченова Минздрава России; Авдеев Сергей Николаевич – член-корр. РАН, д.м.н., заведующий кафедрой пульмонологии ФГАОУ Первый МГМУ им. И.М. Сеченова Минздрава России, главный внештатный специалист-пульмонолог Минздрава России;
Горбачевский Сергей Валерьевич – д.м.н., профессор, сердечно-сосудистый хирург, заведующий отделением хирургического заболевания сердца с прогрессирующей легочной гипертензией НМИЦ Сердечно-сосудистой хирургии имени А.Н. Бакулева Минздрава России;
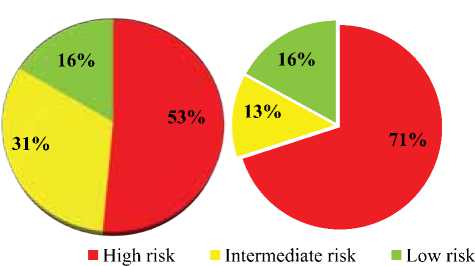
следования до проведения СВЭМ в когорте 55 пациентов с ЛАГ было выявлено, что 53% были в зоне высокого риска развития летального исхода в течение года. При этом после проведения СВЭМ было выявлено, что дополнительно у 18% был высокий риск, что в дальнейшем повлияло на выбор более агрессивной тактики специфической терапии (рис. 2).
Перспективным методом, позволяющим детально оценить трехмерную конструкцию легочного сосудистого русла, является проведение МРТ с последующей печатью древа легочных артерий в трехмерном формате. Основными преимуществами данного метода является безопасность и более низкая стоимость по сравнению с инвазивной оценкой. У пациентов с ХТЭЛГ данная методика позволит более детально оценить уровень и характер тромботического поражения легочных артерий и быть опорой для рентгенэндоваску-лярных хирургов и сердечно-сосудистых хирургов в выборе тактики ведения данных пациентов.
При обсуждении пациентов с ХТЭЛГ была предложена новая интраоперационная классификация, основанная на уровне тромботического поражения легочных артерий.
Уровень 0 (Бывший Тип IV)
Уровень I (Бывший тип I или II)
Уровнь IC
Уровень II (Бывший I или II тип)
Уровень III (Бывший тип III)
Уровень IV (Бывший тип III)
Нет данных за ХТЭЛГ
Поражены главные ветви ЛА
Полная окклюзия целого легкого
Поражение на уровне долевых артерий или в главных нисходящих ветвях ЛА
Поражение на сегментарном уровне
Поражение на субсегментарном уровне
ВЛИЯНИЕ НАЧАЛЬНОЙ ТЕРАПИИ РИОЦИГУАТОМ И ПЕРЕХОДА С ТЕРАПИИ СИЛДЕНАФИЛОМ НА РИОЦИГУАТ У ПАЦИЕНТОВ ИДИОПАТИЧЕСКОЙ ЛЕГОЧНОЙ ГИПЕРТЕНЗИЕЙ НА РЕМОДЕЛИРОВАНИЕ ПРАВЫХ ОТДЕЛОВ СЕРДЦА И СОПРЯЖЕНИЕ ПРАВОГО ЖЕЛУДОЧКА – ЛЕГОЧНОЙ АРТЕРИИ
Таран И.Н., Белевская А.А., Саидова М.А., Мартынюк Т.В., Чазова И.Е.
Национальный Медицинский Исследовательский Центр кардиологии, Отдел легочной гипертензии и заболеваний сердца,Москва, Россия
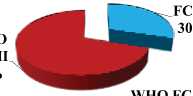
Цель: Оценить влияние риоцигуата на функциональный класс (ФК) (ВОЗ), параметры трансторакальной ЭхоКГ у ранее нелеченных пациентов с идиопатической легочной гипертензией (ИЛГ) и у пациентов, ранее нс достигших целей лечения на фоне терапии силденафилом.
Материалы и методы: В исследование были включены 22 пациента с ИЛГ: 14 - ранее нс принимающих терапию и 8 - не достигших целей лечения на фоне терапии силденафилом. В таблице 1 представлена исходная характеристика подгрупп. Исходно всем пациентам был инициирован риоцигуат с постепенным увеличением дозы
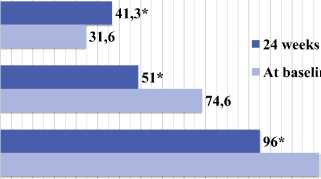
согласно алгоритму титрации препарата. Исходно 24 недели лечения проводилась оценка ФК параметров ремоделирования правых отделов межжелулочкого взаимодействия и сопряжения
и через (ВОЗ), сердца, правого
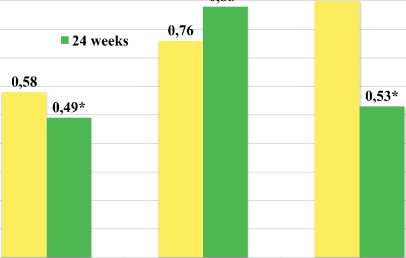
желудочка (ПЖ)- легочной артерии (ЛА) с помощью 2D и 3D ЭхоКГ. Расчет сопряжения ПЖ-ЛА проводился по формуле Еа/Етах. где Еа эффективная артериальной жесткость и Emax конечно - систолическая жесткость ПЖ. Результаты представлены на диаграмме 1-6 и в Таблице 2. Диаграмма 1.
Динамика дистанции в Т6МХ после 24 недель лечения .
ФК
Исимио
ФК (ВОЗ)
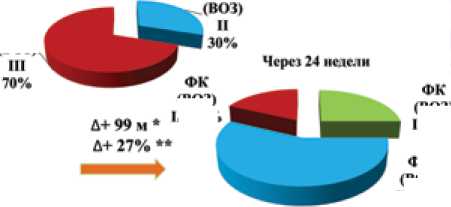
(ВОЗ)
III 18%
Таблица 1. Исходная характеристика подгрупп пациентов с ИЛ Г.
|
Исканные параметры |
Обтай iруина И. II (п -22) |
llvpctiK'.iiMNc с (Гранин се.11сиафм.1ом 1 п~К) |
|
|
Ранее ис-мчснныс пацие-шм (п- 14) |
|||
|
Вофаст.лст |
423 1343: 54| |
42|343: 4331 |
42 [33; 50 | |
|
Фу и кив mi |
альвый статус |
||
|
ФК MI/IIMV(B |
0-7 ISD |
ОАУЮ |
М/М |
|
Дастаммжа в Т6МХ. м |
■МИ) |320;444| |
400 [340; 4Т*| |
371 |329;439| |
|
X О. peak, мл/кг/мни |
1.1 |8;14) |
1|?3;12.15| |
II Ц:14| |
|
МАСО, ilope* |
38[32: 41| |
42 [36; 55| |
33 [30-39.91 |
|
2D и 3D ТхаКГ |
|||
|
ILK>wa.ib ПП. см1 |
20114; 13Л| |
ЮД| 163;25| |
24 |173: 23| |
|
КД ПЖ. см |
М [4; 4.6| |
4Д5 (4.1; 435| |
43 |ЗА 4,6| |
|
TAPSE.cn |
1.7 |М»; 1 Л| |
1,5(1.34; 1.7| |
1311,7; 131 |
|
АНЭЛЖ |
U 11.41; 1Л| |
1.7(1* Ml |
1,46[М;137| |
|
ГАСПЖ.% |
27 |23г 32| |
27,7[21* 32| |
26 |24; 2131 |
|
СДЛА. мм р!.ст. |
78 [75: 105| |
78 [75; |10| |
78 |65; 1531 |
|
срДЛА. мм ркст. |
$7147: 6*1 |
563 [47; 73| |
57143:6331 |
|
КДО ПЖ. мл |
118 105,7; 14531 |
120|188; 142| |
1161»4; 144| |
|
КСО ПЖ, мл |
74>|64.5:86Д| |
77 |67.0; 8531 |
74,6 [62: 142,7| |
|
ФВ ПЖ. % |
313122:361 |
31[22:361 |
32 [23; 3631 |
|
Еа ЛА* мм рт-стУмл* |
0.72 [036; 1Л2| |
0.9 10.7; 1Л7| |
437 [435; 4,63| |
|
EanatIDK. мм pi.cvJM;i |
03 [0,63; 037| |
а. 8|033:034| |
0.78 |0Л7:1| |
|
Сенржжгшес ПЖ - ЛА ♦ |
0.1[0.7; IJ2) |
1.1 |036;138| |
0,61 [4,47; 036| |
*• р < 0.05 <6cxw пн мне uiw"ui ли псчгругпы. pww грннимммша <жлмн»ф*.1 к. ФК (ВО)Ь бутиком», чеадй маге во
(ВОЗ) KiMjufhua. Vt/V«>2 enniewiNWHU» «мипт во >ne»«c.iew> rely. ЦП прем* пуееявеее. М ПЖ бавегышй лммегр [ 25% ••^r TAPSI: - скстшчостме эемэрлм wmu трмкуслмжмога сажми дЮ ЛЖ - лмескммчесхМ вмкк -шпюорвгимктм
Исходно
24 недели
(ВОЗ) И
Диаграмма 23,4. Динамика TAPSE, FAC ПЖ и дИЭ ЛЖ через 24 недели лечения рноцнгуатом.
леем* ее-еухпе». FAC ПЖ - фрежиэеоевеос *»ee*e«w ilmnmum ПЖ, СДЛА- сгнтсчжмесюде weemioe в ЛА. срДЛА срелже .иакиж » ЛА. КДО - вмкч*» ,и«мкмн*ееасМ обич. К<1) «знечмо снстти-мскяй обмч. ФК ПЖ фумнця выброса
Таблица 2. Динамика VO2 peak и VE/Vco2 после 24 недель лечения.
11.5110Д;12|
33.6129.5:42.71
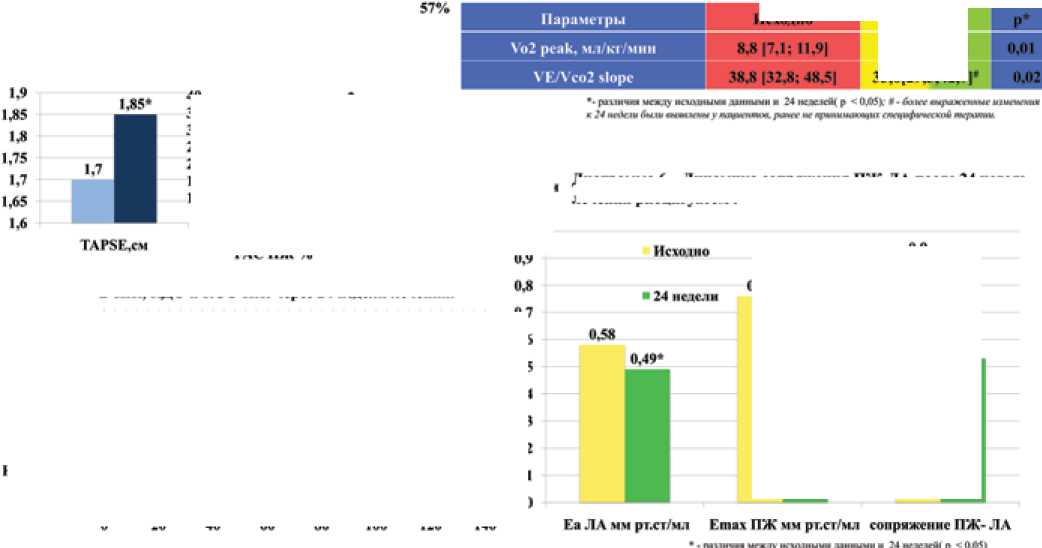
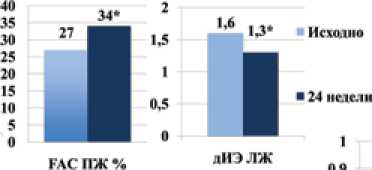
Дня1ряммя 6 . ДНН1МНК1 сопряжения МА-ЛА после 24 недель лечения рноцн1у»юм.
Диаграмма 5.
Динамика ФВ ПЖ, КДО и КСО ПЖ через 24 недели лечения.
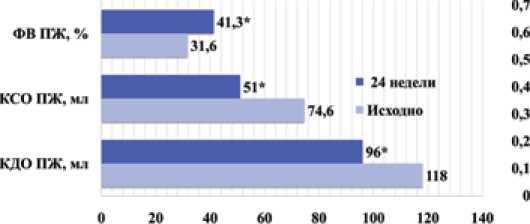
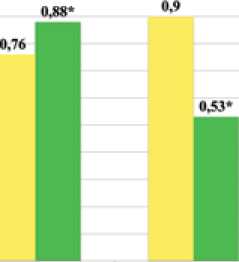
Выводы: Ионотерапия рноцнгуатом н переход с терапии силденафилом на риоцигуат оказались одинаково эффективными для пациентов с ИЛГ, что отражалось в выраженном обратном ремоделировании правых отделов сердца и улучшении сопряжения ПЖ-ЛА.
Рисунок 1. Влияние терапии риоцигуатом на ремоделирование правых отделов сердца и сопряжение ПЖ-ЛА
РОЛЬ СПИРОВЕЛОЭРГОМЕТРИИ В ОЦЕНКЕ ТЯЖЕСТИ ПАЦИЕНТОВ С ЛЕГОЧНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ
Таран И.Н., Валиева З.С., Мартынюк Т.В, Чазова И.Е.Национальный Медицинский Исследовательский Центр кардиологии, Отдел легочной гипертензии и заболеваний сердца,Москва, Россия
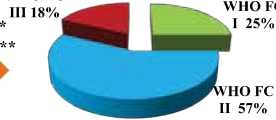
Цель: Оценить вклад спировелоэргометрии (СВЭМ) в стратификацию риска летального исхода у пациентов с легочной артериальной гипертензией (ЛАГ).
Материалы и методы: 55 пациентам с ЛАГ (ср. возраст 43,4+10.73 лет) была проведена СВЭМ. Потребление кислорода (VO2), выделение углекислого газа (VCO2), минутная вентиляция легких (VE) измерялась в режиме breath-by -breath.
Стратификация риска до проведения СВЭМ
Стратификация после проведения
риска СВЭМ
Таблица 1. Характеристика пациентов с ЛАГ.
|
| Параметры |
ЛАГ. зссоннттронаиияя с || |
|||
|
илг (п=48) |
впе <п-5) |
СЗСТ Декарспи! |
||
|
(п-1) |
н токсины (п-1) |
|||
|
Во траст, лет |
43,1+ 11 |
36+1 |
61 |
41 |
|
Пол ( п - женский) |
42 |
3 |
1 |
1 |
|
Дистанция Т6МХ. м |
411^+120 |
485+117,9 |
320 |
433 |
|
ФК( BO3)l4l(n) |
9/22 |
2/1 |
1/1 |
1/0 |
|
ФК(ВОЗ)Ш/1У(п) |
п/е |
20 |
0/0 |
00 |
|
Плошал ь ПП. см2 |
23Л+7.7 |
163+6 |
12 |
32 |
|
БД ПЖ. ем |
3.7+0,61 |
3.1+0,98 |
23 |
5 |
|
НИВ. см |
2.1+0,29 |
2.O+O.2 |
IJ1 |
2.0 |
|
Жидкость в перикарде: Следовое? небольшое (и) |
6'2 |
00 |
0/1 |
0/0 |
|
Х о2 peak. мл/кг/мнн |
10,9+5.1 |
13,5+5.9 |
9.6 |
8.5 |
|
VE/Vco2 slope |
46+19.7 |
43.2+8Д |
40.9 |
73 |
|
K*teiq>H»»H. правых oi.ie.TOB сердца |
||||
|
СрДЛА, мм рт.ст. |
54.2 +.11 |
48,5 +17,6 |
30 |
46 |
|
срДПП. мм рт.ст. |
8+5.5 |
5,6+5 |
1 |
1 |
|
SVo2. % |
58.6*8,8 |
783+6.3 |
65 |
74 |
|
СИ. л/мнн/м2 |
1.96+0.6 |
2.9 |
2.1 |
1,7 |
|
ЛСС д■■♦ceclr, |
1270+625 |
1330+723 |
594 |
1025 |
.с
ИЛ Г - и.пюпатн'кеки Л Г, ВИС - врожденные пороки сердца. СЭСТ системные юболсваиня сосдмиитслмеой ткани, Т6МХ тест 6 минутной ходьбы, ФК (ВОЗ) - функциональный класс
Всемирной Орсаникшин
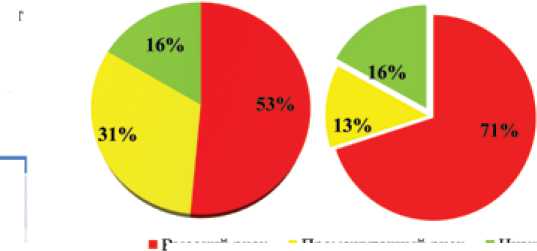
Высоким риск
Промежуточный риск
Низкий риск
Результант: У большинства пациентов был высокий риск легального исхода в течение 1 гада (53%) (п-29), у 17 пациентов (31%) был промежуточный риск. После выполнения СВЭМ было выявлено, что дополнительно 10 пациентов, ранее находящихся в промежуточном риске, имеют высокий риск летального исхода. 9 пациентов (16%) были в низком риск,что также было подтверждено с помощью СВЭМ.
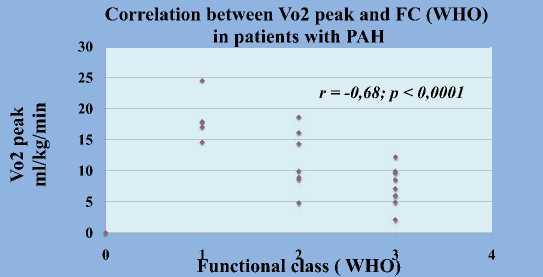
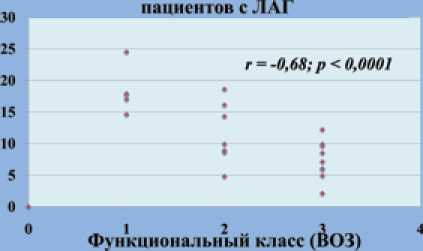
Взаимосвязь между Vo2 peak и ФК (ВОЗ) у
Зцижх>\р«1К,1И, пп - правое прслсерляс. М ПЖ - /иииии» люмстр правого желудочка. HI IB - нижняя полая вена. VbVco2 - вентиляционный эквивалент по Со2, срДЛА среднее давление я легочной артерии, срДПП среднее давление ■ ПП, Sw2 • сатурация смешанной встеотной крови кислородом. СИ -сердечный индекс, ЛСС легочное сосуд|»стое сопротивление.
|
Параметры, отражающие прогноз |
Низкий риск <5% |
Пром ежугоч нын риск 5-10% |
Высокий риск >10% |
|
СВЭМ |
VO2peak >15 мл/мин/кг VE/VCO2 slope < 36 |
VO2peak 11-15 мл/мнн/кг VE/VCO2 slope 36-44,9 |
\O2pcak <11 мл 'мин/кт V 1 \ СО2 slope >45 |
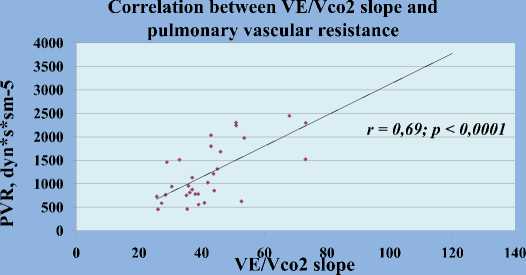
Взаимосвязь между VE/Vco2 slope и ЛСС
ш
*
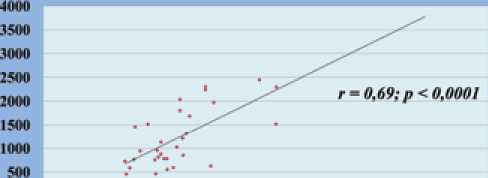
О
D
40 . 64) 80 100 120 140
V ЕЛ со2 slope
Была выявлена значимая отрицательная корреляционная связь между Vo2pcak и ФК (ВОЗ) (г=-0,68;р<0,0001) и положительная взаимосвязь между Vo2pcak и дистанцией в Т6МХ (г=О,68;р <0.0001); значимая положительная корреляционная связь между VE/Vco2 slope и ЛСС (r=0,69;p<0.0001). S ПИ (г=0,5;р<0,003), срДПП (r=O,57;p Выводы: При оценке достижения целей терапии результаты СВЭМ являются надежными маркерами, отражающими прогрессирование ЛАГ. Следует подчеркнуть роль СВЭМ в стратификации риска пациентов с ЛАГ. У авторов отсутствует конфликт интересов. Рисунок 2. Роль метода спировелоэргометрии в оценке тяжести пациентов с ЛА Согласно полученным данным в исследовании RACE был предложен новый алгоритм по тактике ведения пациентов с неоперабельной ХТЭЛГ, где было обозначено, что метод транслюминальной балонной ангиопластики легочных артерий может быть рассмотрен у данной когорты пациентов только совместно с медикаментозным лечением. Тактика медикаментозного лечения пациентов с ЛАГ, группы 2 и 3 не претерпела значимых изменений. Более детально были описа- ны перспективы начальной комбинированной терапии у пациентов с промежуточным и высоким риском развития летального исхода. Вопрос о методе оптимизации терапии за счет замены препаратов из одного класса на другой при плохой переносимости, неадекватном ответе или не достижении целей лечения требует дальнейшего изучения. Taran I.N. A BRIEF SUMMARY OF THE RESULTS OF THE 6TH WORLDSYMPOSIUM ON PULMONARY HYPERTENSIONIN NICE IN 2018: VIEW OF A YOUNG SCIENTIST «National Medical Research Center of cardiology» Ministry of Healthcare of Russian Federation, Moscow, Russia Information about authors: Taran Irina Nikolaevna Postgraduate student of department of pulmonary hypertension and heart diseases of Federal State Budget Organization «National Medical Research Center of cardiology» Ministry of Healthcare of Russian Federation, Moscow. И zaviirina@mail.ru The 1st World Symposium on the Problem of Pulmonary Hypertension (PH) was held in Geneva in 1973 and following the publication of the Evian Classification of PH in 1998 after the Second World Symposium, was traditionally held every 5 years (Venice 2003, Dana Point 2008, Nice 2013). In 2018, the venue of the symposium was Nice with amazing sea views and March snowfall. The main objective of this symposium was to review the main scientific achievements in the field of PH in the past 5 years and discuss the possibility of conducting joint research programs to replenish the evidence base. At the beginning of the symposium, attention was paid to the pathophysiology of PH. According to the Guignabert’s report the contribution of inflammation in the process of remodeling of the pulmonary vascular bed, the possibility of identification the proinflammatory phenotype of the pulmonary arteries (PA) endothelial cells were discussed. The creating of biobank and developing a new genetic panel for PAH patients are the perspective in the field of genetics. In the report of Morrel N.W. the new genetic mutations in PAH with a high level of evidence such as P-type ATPase (ATP13A3), growth and differentiation factor 9 (GDF2) (BMP9), SRY (Sex determining region Y) Box 17 (SOX17) and Aquaporin 1 (AQP1) with a lower level of evidence were presented. Pullamsetti S.S. was demonstrated the novel channelopathies in PAH – calcium activated chloride (TMEM16A) channels, that have been identified in many epithelial and endothelial cells as well as in smooth muscle cells. Upregulated chloride channels cause depolarization in IPAH and increased PA contraction and remodeling that is important in disease pathogenesis. It indicates the discovery of new mechanisms that induce the IPAH and the possibility of creating specific drug therapies that effect on this pathway. Better understanding the bidirectional regulatory mechanisms between metabolic remodeling and the epigenome in PH are also the future directions. It is known that bone morphogenetic protein receptor type 2 (BMPR2) is frequently downregulated in IPAH and some PAH associated forms. Intervention targeting BMPR2 in IPAH and PAH patients are under development. It has been supposed, that phenotyping of PH patients for further determination of treatment strategy and prognosis is necessary. PAH phenotype has changed: patients become older at the time of diagnosis verification, with higher body mass index and multiple comorbidities. With cytokine proteomics the new PAH phenotypes which presented as 4 immune clusters were established, that was demonstrated in report of Rabinovitch M. The one of the future direction is to assess the impact of genetic mutations on clinical phenotypes and outcomes in patients with PH. For the first time in the past 20 years the issue of changing the diagnostic criteria in PH was discussed. It has been supposed to reduce the threshold of mean PA pressure (mPAP) to 20 mm Hg according to right heart catheterization data (RHC). However, these changes may be applicable only in PH Group 1 and 3. Whereas the previous threshold >25 mm Hg was proposed to leave in patients with chronic thromboembolic PH (CTEPH). It has been supposed to reduce the threshold of mPAP to 20 mm Hg in PH Group 2 patients also. However, it was suggested to exclude the value of the diastolic pressure gradient in evaluation the isolated or mixed post- and precapillary PH. The modified criteria for an isolated post-capillary PH are: the PA wedge pressure (PAWP) >15 mm Hg, mPAP >20 mm Hg and the pulmonary vascular resistance (PVR) <3 Wood Units. While the criteria for mixed post- and precapillary PH are: PAWP >15 mm Hg, mPAP >20 mm Hg and PVR >3 Wood Units. In patients with PAWP between 13-15 mm Hg and high/ intermediate probability of PH and heart failure (HF) with preserved ejection fraction (EF), a fluid loading challenge should be considered with 500 ml of saline over 5 minutes during RHC. A PAWP >18 mm Hg immediately after fluid administration is considered abnormal. At the same time, the initiation of various specific drugs in patients with PH and HF with a preserved EF was unsuccessful and even unsafe according to the randomized clinical trials results. The assessment of right ventricular (RV) two-dimensional (2D) strain by Echo or cardiac magnetic resonance imaging (MRI) were demonstrated as the method, that estimates subclinical RV impairment before the development of the more conventional abnormalities of RV performance. RV free wall longitudinal strain is an index of RV myocardial function and is a powerful predictor of outcome. The photos show some Russian delegators from Moscow, who participated in 6th World Symposium on PH 2018. From left to right:: Taran Irina Nikolaevna – postgraduate student of Department of Pulmonary Hypertension and Heart Diseases, National Medical Research Center of cardiology Ministry of Healthcare of Russian Federation; Careva Natal'ja Anatol'evna – PhD, assistant professor of department of pulmonology, Federal State Autonomous Educational Institution of Higher Education I.M. Sechenov First Moscow State Medical University of the Ministry of Healthcare of the Russian Federation; Avdeev Sergej Nikolaevich – Corresponding member of the Russian Academy of Sciences, head of department of pulmonology, Federal State Autonomous Educational Institution of Higher Education I.M. Sechenov First Moscow State Medical University of the Ministry of Healthcare of the Russian Federation, chief specialist-pulmonologist of the Ministry of Health of Russia; Nakonechnikov Sergej Nikolaevich – Dr. Med. Sci., Prof., Deputy director general for Telemedicine Technologies and Public Communications, National Medical Research Center of cardiology Ministry of Healthcare of Russian Federation; Gorbachevskij Sergej Valer'evich – Dr. Med. Sci., Prof., cardiovascular surgeon, head of department of Surgical Heart Diseases with Progressive Pulmonary Hypertension, National Medical Research Center of Cardiovascular surgery of Bakulev A.N. Ministry of Healthcare of Russian Federation; Volkov Aleksandr Vital'evich – PhD., head of department of functional and ultrasound methods, Federal State Budget Research Organization Scientific Institute of Rheumatology of VA. Nasonovoj. The conduction of multicenter prospective clinical trials with inclusion of different groups of patients with PH to determine the role of the Echo and MRI in assessment of the RV strain in clinical practice is required. The attention was also focused on the evaluation of the RV – PA coupling. There are several approaches for evaluation of RV – PA coupling. The first method is the Pressure-Volume loops analysis. It consists of invasive assessment of the pressure and volume of the ventricles, which is reflected in the diagrams and is subsequently used to calculate cardiovascular coupling. The RV–PA coupling is calculated as Ea:Emax ratio, where Ea is the effective arterial elastance and Emax is the ventricular end-systolic elastance. Effective arterial elastance was calculated as follows: Ea = (mPAP – PAWP)/SV, where SV is the stroke volume and ventricular end-systolic elastance was calculated by the formula: Emax = mPAP/ESV, where ESV is the RV end-systolic volume. The second technique for assessing RV – PA coupling is the use of 2D and three-dimensional (3D) transthoracic Echo with the evaluation of mPAP, PWAP and SV by 2D Echo and RV ESV by 3D with subsequent calculation of RV – PA coupling according to the formulas. In the National Medical Research Center of Cardiology in department of pulmonary hypertension and heart diseases and department of ultrasound techniques a scientific work on dynamics of RV – PA coupling in patients with IPAH and inoperable CTEPH with various specific therapies is carried out. The close associations between RV – PA coupling and parameters from risk stratification scale were revealed, that reflected the usefulness of RV – PA coupling in assessment of severity in PH patients. Furthermore, it is interesting to use this method in phenotyping of IPAH and CTEPH patients. The results of the study were presented on the symposium during the poster session (Picture 1). The evaluation of the ratio between tricuspid annular plane systolic excursion (TAPSE) and systolic PAP (SPAP) was the third method of RV – PA coupling determination as was demonstrated in Noodredegraaf’s report. However, the TAPSE/SPAP ratio may have prognostic information, but may not represent coupling. In the section on diagnosis and risk stratification of PH patients, the use of cardiopulmonary exercise testing (CPET) and its role in clinical practice were discussed. CPET data provide information about severity, risk and prognosis of patients with PH. The conduction of CPET in dynamics is necessary in assessing the efficacy of specific therapy and rehabilitation programs. The experience of department of pulmonary hypertension and heart diseases of National Medical Research Center of cardiology about the value of CPET in assessment of severity in patients with PAH was also presented during the poster session. The study included 55 patients and before CPET performing the majority of patients (53%) had a high risk of mortality during 1 year. After CPET performing we revealed, that an additional 18% of patients, who had been earlier in intermediate risk, had a high risk of mortality during 1 year, that influenced on a decision about more aggressive specific therapy for these patients (Picture 2). It is possible to make a detailed evaluation of the 3D structure of the pulmonary vascular bed by MRI with subsequent printing of the PA tree in a 3D format. The main advantages of this method are safety and lower cost in comparison with invasive methods. This technique may be helpful in detailed assessment of the level and character of thrombotic lesions of the PA’s both for endovascular and cardiovascular surgeons in CTEPH patients’ management. In the field of CTEPH patients the new intra – operative classification was proposed (level of anatomical disease rather than type of clot). Level 0 (Old type IV) No evidence of CTEPH in either lung Level I (Old type I or II) Disease in the main PA's Level IC Complete occlusion of the entire lung Level II (Old type I or II) Disease starting at the level of lobal arteries, or in the main descending PA's Level III (Old type III) Disease starting in the segmental levels Level IV (Old type III) Disease starting at the level of sub-segmental arteries According to the results of RACE study a new algorithm for management of patients with inoperable CTEPH was proposed. It was indicated that the method of transluminal balloon angioplasty of PA’s could be considered in this cohort of patients only with specific drugs treatment. The strategy of treatment in patients with PAH, groups 2 and 3, did not undergo significant changes. The attention was focused on prospects of initial combination therapy in patients with intermediate and high risk of mortality. The method of therapy optimization by switching from one class of specific drug to another due to intolerability, inadequate response or failure to achieve the treatment goals requires further study. INFLUENCE OF INITIAL RIOCIGUAT MONOTHERAPY AND TRANSITION FROM SILDENAFIL TO RIOCIGUAT THERAPY IN PATIENTSWITH IDIOPATHIC PULMONARY ARTERIAL HYPERTENSION ON RIGHT HEART REMODELINGAND RIGHT VENTRICULAR – PULMONARY ARTERIAL COUPLING Taran I.N., Belevskaya A.A., Saidova M.A., Ma tynyuk TV, Chazova IE National Medical Research Center of cardiology,Department of pulmonary hyprtension and heart diseases,Moscow, Russia Objective: To evaluate the influence of riociguat on WHO functional class (FC), parameters of transthoracic Echo in na ive patients (pts) with idiopathic pulmonary arterial hypertension (IPAH) and in those who have failed to achieve treatment goals with sildenafil. Materials and methods: The study included 22 IPAH pts: 14 -treatment-na'ive pts and 8 pts, who failed to achieve treatment goals with sildenafil. The baseline characteristics of subgroups are presented in the Table 1. Riociguat was initiated for all pts at baseline with a gradual dose increase according to the dose titration algorithm. At baseline and after 24 weeks of riociguat treatment all pts were assessed for WHO FC, right heart remodeling parameters, interventricular interaction, and right ventricular - pulmonary arterial coupling (RVPAC) by 2D and 3D Echo. The RVPAC was calculated as Ea/Emax ratio, where Ea is the effective arterial elastance and Emax is the ventricular end-systolic elastance. Results are demonstrated in Figures 1-6 and Table 2. Figure 1. The dynamics of 6MWT after 24 weeks of treatment. Table 1. Characteristics of IPAH pts subgroups at baseline. Baseline parameters Overall IPAH group (n=22) Treatment- naive subgroup (n= 14) Treatment - switch subgroup ( n=8) Age, years 42,5 [34,5; 50] 42 [34,5; 43,5] 42 [33; 50 ] Functional status FC I/II/III/IV (WHO) 0/7/15/0 0/4/10/0 0/3/5/0 6MWT, m 400 [320;440] 400 [300; 478] 371 [329;439] VO2 peak, ml/kg/min 9,9 [8; 14] 9 [7,8;12,95] 11 [8;14] VE/VCO2 slope* 38 [32; 49] 42 [36; 55] 33 [30;39,9] WHO II At baseline FC II 70°/, 2D and 3D echocardiography RA area, cm2 20 [16; 23,5] 19,2 [16,6; 25] 20 [17,0; 23] RVBD, cm 4,4 [4; 4,6] 4,45 [4,1; 4,65] 4,5 [3,8; 4,6] TAPSE, cm 1,7 [1,49; 1,8] 1,5(1,34; 1,7] 1,8 [1,7; 1,9[ LVdEI 1,6 [1,48; 1,8] 1,7 [1,6; 1,8] 1,46 [1,4; 1,57] RV FAC, % 27 [23; 32] 27,7 [21,5; 32] 26 [24; 29,5] SPAP, mmHg 78 [75; 105] 78 [75; 110] 78 [65; 95,5] mean PAP, mmHg 57 [47; 68] 56,5 [47; 73] 57 [43; 63,5] RV EDV, ml 118 [95,7; 145,6] 120 [108; 142] 116 [94; 140] RV ESV, ml 74,6 [64,5; 86,2] 77 [67,9; 85,6] 74,6 [62; 102,7] RV EF, % 31,6 [22; 36] 31 [22; 36] 32 [23; 36,5] PA Ea, mm Hg/ml* 0,72 [0,56; 1,02] 0,9 [0,7; 1,07] 0,57 [0,39; 0,63] RV Emax, mm Hg/ml 0,8 [0,63; 0,87] 0, 8[0,53; 0,84] 0,78 [0,67; 1] RVPAC* 0,9 [0,7; 1,32] 1,1 [0,86;l,48] 0,69 [0,47; 0,86] All data are presented as mediana ± 1QR; *- p value < 0,05 (lower values for treatment - switch subgroup);FC (WHO)- functional class according to the World Health Organization classification, 6MWT- 6-minute walking test, Vo2 peak- peak oxygen uptake, VE/Vco2 - ventilation equivalents for Co2 . RA- right atrium. RVBD- right ventricular basal diameter, TAPSE- tricuspid annular plane systolic excursion, dEI- diastolic index eccentricity of left ventricular, FAC RV - RV fractional area change, SPAP- systolic pulmonary arterial pressure, RV EDV - end diastolic volume of RV, RV ESV - end systolic volume of RV, RV EF- RV ejection fraction. △+ 99 m △+ 27% After 24 weeks Figure 2,3,4. The dynamics of TAPSE, RV FAC and dIE after 24 weeks of riociguat treatment. Table 2. The dynamics of VO2 peak and VE/Vco2 after 24 weeks of treatment. Parameters At baseline Vo2 peak, ml/kg/min VE/Vco2 slope 8,8 [7,1; 11,9] 38,8 [32,8; 48,5] 24 week P* ll,5[10,2;12] 0,01 33,6[29,5;42,7]# 0,02 TAPSE,cm Conclusion: 34* RV FAC % LVdEI At baseline *- difference between baseline and week 24; # - more significant changes at week 24 in treatment -naivegroup. 24 weeks Figure 5. The dynamics of RV EF, RV EDV and ESV after 24 weeks of treatment. RV EF, % RV ESV, ml RV EDV, ml 0 20 40 60 80 100 120 140 Riociguat monotherapy and transition from sildenafil improvement in right heart remodeling and RVPAC. At baseline Figure 6. The dynamics of RVPAC after 24 weeks of riociguat treatment. RVPAC * - difference between baseline and 24 week ( p value < 0,05) PA Ea mm Hg/ml RV Emax mm Hg/ml to riociguat appeared equally effective on IPAH pts with a pronounced Picture 1. The influence of riociguat therapy on right heart remodeling and RV –PA coupling. THE VALUE OF CARDIOPULMONARY EXERCISE TEST IN ASSESMENTOF THE SEVERITY OF PULMONARY ARTERIAL HYPERTENSION PATIENTS Taran I.N., Valieva Z.S., Martynyuk T.V., Chazova I.E. National Medical Research Center of cardiology,Department of pulmonary hypertension and heart diseases,Moscow, Russia Objective: To evaluate the impact of cardiopulmonary exercise test (CPET) on fatal events risk stratification in pts with pulmonary arterial hypertension (PAH). Materials and methods: 55 pts with PAH (mean age 43,4+10,73 years) were underwent CPET on cycle ergometry. Oxygen uptake (VO2), carbon dioxide output (VCO2), minute ventilation (VE) were measured breath-by -breath. Table 1. Characteristics of the PAH patients. Risk stratification in PAH pts without CPET performing Risk stratification in PAH pts with CPET performing Parameters I PAH,; associated with I IPAH (n=48) CHD (n=5) CTD (n=D Drugs and toxins (n=l) Age, years 43,1 + 11 36+1 61 41 Sex ( n - female) 42 3 1 1 6MWT, m 411,6+120 485+117,9 320 433 FC (WHO) T/П (n) 9/22 2/1 0/1 1/0 FC ( WHO) III/1V (n) 17/0 2/0 0/0 0/0 RA area ,cm2 23,8+7,7 16,5+6 12 32 RVBD, cm 3,7+0.61 3,1+0,98 2,8 5 IVC, cm 2,1+0,29 2,0+0,2 1.8 2,0 Pericardial effusion: Minimal /small (n) 6/2 0/0 0/1 0/0 Vo2 peak, ml/kg/min 10,9+5.1 13,5+5,9 9,6 8,5 VE/Vco2 slope 46+19,7 43,2+8,3 40,9 73 Right heart catheterization mPAP, mm Hg 54,2 у 1 48,5 +17,6 30 46 mRAP. mm Hg 8+5,5 5,6+5 1 1 SVo2, % 58,6+8,8 78,5+6,3 65 74 Cl, 1/min/m2 1,96+0,6 2.9 2.1 1,7 PVR dyn*s*sm-5 1270±625 1330+723 594 1025 IPAH - idiopathic PAH, CHD - congenital heart diseases, CTD- connective tissue diseases, 6MWT- 6-minute walking test, FC (WHO)- functional class according to the World Health Organization classification, RA- right atrium, RV BD - right ventricular basal diameter, IVC -inferior vena cava, Vo2 peak- peak oxygen uptake, VE/Vco2 -ventilation equivalents for carbon dioxide, mPAP- mean pulmonary arterial pressure, mRAP- mean right atrial pressure, Svo2- mixed venous blood saturation, CI- cardiac index, PVR - pulmonary vascular resistance. Results: The majority of pts (53%) had the high-risk of fatal events during 1 year (n=29), and 17 pts ( 31 %) had the intermediate risk. After the CPET performing we found, that an additional 10 pts, who had been earlier in the intermediate risk, had a high risk of mortality during 1 year. 9 pts (16%) were belonged to the low risk , that was also confirmed by CPET data. Parameters, that reflected the prognosis Low risk <5% Intermediate risk 5-10% High risk >10% CPET VOlpeak >15 ml/min/kg VE/VCO2 slope < 36 VOlpeak 11-15 ml/min/kg VE/VCO1 slope 36-44,9 VOlpeak <11 ml/min/kg VE/VCO1 slope >45 The significant negative correlation between Volpeak and FC (WHO) was found (r=-0,68;p<0,0001). The significant positive correlation between Volpeak and distance in 6MWT was revealed (r=0,68;p <0,0001). The VE/Vcol slope value had significant positive correlation with PVR level (r=0,69;p<0,0001), RA area (r 0.5:p '0.003), inRAP (r=0,57;p<0.0012). Conclusion: For the assessment of achieving therapy goals CPET is one of the reliable markers to reflect the PAH progression. The critical role of CPET in risk stratification in PAH pts should be emphasized. Disclosure: The authors have no conflict of interests to declare. Picture 2. The value of cardiopulmonary exercise test in assessment of the severity of pulmonary arterial hypertension patients