Кристалличность ароматических полиамидинов
Автор: Холхоев Бато Чингисович, Бурдуковский Виталий Федорович, Субанаков Алексей Карпович
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Химия
Статья в выпуске: 3, 2015 года.
Бесплатный доступ
Методом РФА исследована степень кристалличности ароматических полиамидинов, полученных в расплаве, растворе ионной жидкости и реагенте Итона. Было найдено, что степень кристалличности полиамидинов зависит от способа проведения реакции.
Ароматические полиамидины, ионные жидкости, реагент итона, кристалличность
Короткий адрес: https://sciup.org/148182886
IDR: 148182886 | УДК: 541.64,
Crystallinity of aromatic polyamidines
Using XRD the crystallinity of aromatic polyamidines obtained in melt, ionic liquids and Eaton’s reagent was investigated. It was found that degree of crystallinity of the polyamidines strongly depends on the way of the reaction.
Текст научной статьи Кристалличность ароматических полиамидинов
Полиамидины (ПАД) в последнее десятилетие привлекают повышенное внимание вследствие возможности их использования в оптоэлектронике, металлорганическом катализе, медицине и др. [1]. Однако, несмотря на перспективность полимеров, они до сих пор остаются малоизученными соединениями. Так, в одной из крупнейших в мире единой реферативной базе данных Scopus® [2] имеется 77 работ, посвященных ПАД (тогда как, например, для полибензимидазолов – 1575, для полиамидов – 37756), хотя первая публикация, в которой упомянуты эти полимеры, вышла в 1947 г.
По расположению амидиновой группировки в полимерной цепи выделяют две группы ПАД:
I
H
I
I
H
II
При этом, судя по количеству работ, значительно более изученными являются ПАД-I, которые, как показано в работе [3], в зависимости от способа получения имеют различную степень кристалличности (СК), обусловленную образованием межмолекулярных водородных связей между амидиновыми группами. Пленкообразующие ПАД-II впервые были получены нами сравнительно недавно [4– 7], поэтому представлялось целесообразным изучить кристалличность полимеров, поскольку СК, как известно, определяет значительную часть свойств полимеров, в т.ч. способность к переработке в изделие [8].
Экспериментальная часть
Все ПАД получены по методикам, приведенным в работах [4–7].
РФА проводили на дифрактометре D8 Advance Bruker AXS (Cu K α -излучение). Образцы полимеров для РФА предварительно сушили в вакууме при 60–70 °С в течение 24 ч, затем тщательно перетирали в ступке. Степень кристалличности (СК) полимеров определяли из отношения площадей пиков кристаллических фаз к общей площади аморфных и кристаллических фаз.
ИК-спектры регистрировали на спектрофотометре «Excalibur FTS 3000NX» (Varian) в диапазоне волновых чисел 4000–400 см-1. Образцы снимали в виде пленки или таблеток с KBr.
Молекулярные массы полимеров определяли с помощью гель-проникающей хроматографии, которую проводили на хроматографе фирмы "Waters", насадка колонок – U-Styragel Linear, рефрактометрический детектор, растворитель - тетрагидрофуран, Т = 20 ° С, скорость потока 0.5 мл/мин. Система обработки данных "Maxima", калибровка по полистирольным стандартам.
Результаты и их обсуждение
Изучение СК ПАД, полученных в расплаве, в растворе ионной жидкости (1-бутил-3-метилимидазолия гептахлордиалюминат) и в реагенте Итона, осуществляли с помощью метода РФА и пакета программ Diffract plus Bruker AXS.
Результаты, обобщенные в таблице, показывают, что СК ароматических ПАД значительно зависит от способа получения. Так, из всего ряда исследованных ПАД (рис. 1, 2), наибольшей СК обладает полимер, полученный полиприсоединением динитрилов и диаминов в расплаве (ПАД-1) – 76.15 % . Такая высокая СК, очевидно, достигается за счет жесткоцепной природы полимера, обусловленной наличием пара -фениленовых фрагментов, низкой молекулярной массы и более эффективного образования водородных связей между макромолекулами. При синтезе такого ПАД в ионной жидкости, содержащей подвижные ионы в реакционной среде, происходит, очевидно, сольватация амидинового фрагмента, что делает невозможным образование водородных связей [9, 10] и полимер имеет аморфную структуру. Аналогичная зависимость наблюдалось в случае ПАД-3.
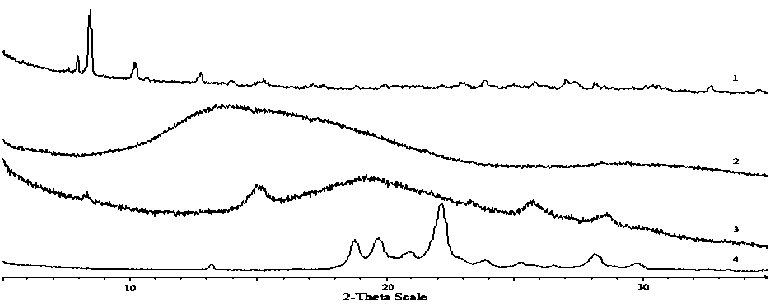
Рис. 1. Рентгенограммы ПАД-1 (1), ПАД-2 (2), ПАД-3 (3), ПАД-4 (4)
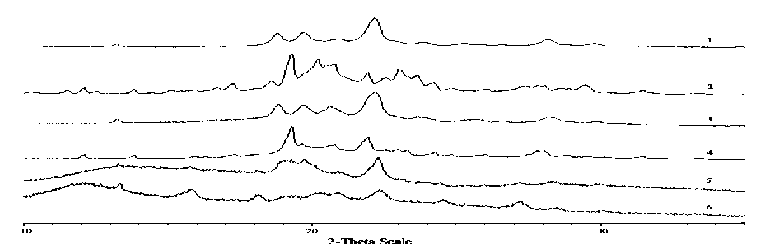
Рис. 2. Рентгенограммы ПАД-4 (1), ПАД-5 (2), ПАД-6 (3), ПАД-7 (4), ПАД-8 (5), ПАД-9 (6)
Интересные закономерности были обнаружены при исследовании СК ПАД, полученных в реагенте Итона. Несмотря на то, что реакция полимерообразования протекала в растворе, все синтезированные ПАД обладали кристалличностью. При этом СК, как видно из таблицы, зависит от жесткости полимерной цепи. Так, ПАД-4, содержащий одну мостиковую группу, обладает наибольшей СК.
Таблица
Свойства полиамидинов
|
№ |
ПАД |
Способ полу-чения1 |
M w ∙10-3 2 |
СК, % |
d3, Å |
|
1 |
NH O NH II II ∗ CN NC HH |
расплав |
8 |
76.15 |
|
|
2 |
ИЖ |
19 |
– |
5.67, 2.92 |
|
|
3 |
NH NH ∗ ∗ CN NC HH O |
ИЖ |
13 |
– |
|
|
4 |
РИ |
17 |
36.49 |
4.22 |
|
|
5 |
O O NH NH ∗ ∗ N N HH O |
РИ |
8 |
35.66 |
4.28 |
|
6 |
OSO NH NH II II • ∗ CN NC ∗ HH O |
РИ |
15 |
28.52 |
4.29 |
|
7 |
O NH NH ∗ CN NC ∗ HH O |
РИ |
20 |
20.04 |
4.32 |
|
8 |
O H NH O N C ∗ II II ∗ C NH H |
РИ |
25 |
14.07 |
6.39 4.25 3.01 |
|
9 |
РИ4 |
25 |
52.69 |
6.90 4.18 |
1 – ИЖ и РИ – полимер синтезирован в ионной жидкости и в реагенте Итона (соответственно); 2 – по данным гель-проникающей хроматографии; 3 – среднее расстояние между полимерными цепями; 4 – пленка полимера, синтезированного в реагенте Итона
При введении мостиковой сульфоновой группы (ПАД-6) СК уменьшается и составляет 28.52 % . Далее было установлено, что введение в диаминный фрагмент вместо сульфоновой группы простых эфирных групп (ПАД-7,8) приводит к еще большему снижению СК, при этом введение одной мостиковой группы (ПАД-7) приводит к снижению СК до 20.04 % , двух (ПАД-8) - до 14.07 %. Средние расстояния (d) между макромолекулярными цепями, рассчитанные по величине максимума гало [3], имели близкие значения (4.22–4.32 Å), при этом более высокие СК соответствовали меньшим расстояниям между полимерными цепями.
Известно [11], что введение в полимерную цепь объемных кардовых группировок в некоторых случаях приводит к образованию аморфных полимеров. Однако ПАД, содержащий дифенилфталид-ную кардовую группировку, обладает достаточно высокой СК, сравнимой с ПАД-4. Причинами столь высокой СК кардового ПАД являются, вероятно, образование межмолекулярных водородных связей с участием более электроноакцепторного атома кислорода карбонильной группы и ориентация ПАД по типу изотактических полимеров.
Растворение ПАД-8 в ДМФА с выдерживанием при 20 оС в течение суток с последующим осаждением водой приводит к получению полностью аморфного полимера. Однако пленка этого полимера, полученная из 10 %-ного раствора в ДМФА, обладает кристалличностью, превосходящей СК исходного полимера более чем в 3.5 раза. На рентгенограмме исходного ПАД-8 наблюдается три области гало, что соответствует значениям d 6.39, 4.25 и 3.01 Å. Тогда как на дифрактограмме пленки присутствует только две области гало, соответствующие величинам d 6.90 и 4.18 Å. Очевидно, при медленном испарении ДМФА происходит взаимная ориентация макромолекул дальнего порядка, при этом наблюдается изменение расстояния между полимерными цепями.
Образование межмолекулярных водородных связей в случаях кристаллических ПАД наглядно иллюстрируется значительным уширением полос колебания NH-групп (3500–2500 см-1) в ИК-области в сравнении с аморфными полимерами.
Таким образом, в работе показано, что ароматические ПАД в зависимости от строения элементарного звена и способа получения обладают различной степенью кристалличности, которая связана с возникающим упорядочением системы за счет образования водородных связей между амидиновыми группами.
Список литературы Кристалличность ароматических полиамидинов
- Wang Z.T., Zhang Y.S., Zhao Y.X., Zhu G.M. Recent progress of polyamidine//Polym. Mater. Sci. Eng. -2007. -Vol. 23. -P. 6-9.
- http://www.scopus.com/home.url
- Böhme F., Klinger C., Komber H., Haussler L., Jehnichen D. Synthesis and properties of polyamidines//J. Polym. Sci. Part A: Polym. Chem. -1998. -Vol. 36. -P. 929-938.
- Холхоев Б. Ч., Бурдуковский В.Ф., Могнонов Д.М. Синтез ароматических полиамидинов в реагенте Итона//Высо-комолек. соедин.Б. -2013. -Т. 55, № 12. -С. 1506-1509.
- Kholkhoev B. Ch., Burdukovskii V.F., Mognonov D.M. Preparation of aromatic polyamidines and their transformation in polybenzimidazoles//EXPRESS Polymer Letters. -2014. -Vol. 8, № 9. -С. 635-646.
- Холхоев Б. Ч., Бурдуковский В.Ф., Могнонов Д.М. Синтез полиамидинов на основе 1,4-дицианобензола и 4,4’-диаминодифенилоксида в ионных жидкостях//Изв. PÆH Серия хим. -2010. -Т. 59, № 11. -С. 2104-2105.
- Холхоев Б. Ч., Бурдуковский В.Ф., Могнонов Д.М. Полиамидины на основе динитрилов и диаминов//Журн. приклад. химии. -2011. -Т. 84, № 3. -С. 519-520.
- Аверко-Антонович И.Ю., Бикмуллин Р. Т. Методы исследования структуры и свойств полимеров. -Казань: Изд-во КГТУ, 2002. -С. 360-364.
- Wang B., Tang Y., Wen Zh., Wang H. Dissolution and regeneration of polybenzimidazoles using ionic liquids//Eur. Polym.J. -2009. -Vol. 45. -P. 2962-2965.
- Ионные жидкости и их использование для растворения природных полимеров/Н.П. Новоселов //Журн. общей химии. -2007. -Т. 77, № 8. -С. 1317-1327.
- Виноградова С.В., Васнев В.А., Выгодский Я.С. Кардовые полигетероарилены. Синтез, свойства и своеобразие//Успехи химии. -1996. -Т. 65. -С. 266-295.


