Кристаллографическое исследование ротовой жидкости в динамике местного лечения дезоксирибонуклеатом натрия пациентов с афтозным стоматитом
Автор: Македонова Ю.А., Калашникова С.А., Александрина Е.С., Боловина Я.П.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 2 т.20, 2023 года.
Бесплатный доступ
Рецидивирующий афтозный стоматит (РАС) занимает третье место по распространенности в структуре заболеваний слизистой оболочки рта. За последние 3 года, согласно данным ретроспективного анализа, произошел прирост патологии на 1,92 %. Этиология остается дискутабельной в научно-исследовательской среде, но, как правило, развитие РАС связывают с генетической предрасположенностью, а конкретно - с влиянием эпигенетики, эндокринными заболевания, заболеваниями желудочно-кишечного тракта и т. д. В литературе имеется большое число исследований, посвящённых взаимосвязи инфекции COVID-19 и РАС, вероятнее всего, это могло служить одной из причин прироста заболевания за последние 3 года. Пациенты, несмотря на проводимую терапию, страдают мучительными болями при приеме пищи и разговоре. Все это диктует необходимость поиска новых средств и методов местного лечения РАС, а также способов, позволяющих превентировать новые рецидивы. Кристаллографическое исследование один из доступных неинвазивных методов, позволяющий оценить эффективность проводимой терапии. Целью исследования стал анализ кристаллограмм пациентов с РАС в динамике лечения дезоксирибонуклеатом натрия. Результаты анализа кристаллограмм пациентов с РАС показали, что группа, использующая в местном лечении дезоксирибонуклеат натрия, имела более четкую упорядоченную кристаллическую структуру, также количественный анализ достоверно отличался от группы (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Афтозный стоматит, дезоксирибонуклеат натрия, кристалограмма, ротовая жидкость
Короткий адрес: https://sciup.org/142238790
IDR: 142238790 | УДК: 616.31-002.2
Crystallographic study of the oral fluid in the dynamics of local treatment with sodium deoxyribonucleate in patients with aphthous stomatitis
Recurrent aphthous stomatitis (RAS) is the third most common in the structure of diseases of the oral mucosa. Over the past 3 years, according to the data of a retrospective analysis, there was an increase in pathology by 1,92 %. The etiology remains debatable in the research environment, but, as a rule, the development of RAS is associated with a genetic predisposition, and specifically with the influence of epigenetics, endocrine diseases, diseases of the gastrointestinal tract, etc. There are a large number of studies in the literature on the relationship between COVID-19 infection and RAS, most likely this could be one of the reasons for the increase in the disease over the past 3 years. Patients, despite ongoing therapy, suffer from excruciating pain when eating and talking. All this dictates the need to search for new means and methods of local treatment of RAS, as well as ways to prevent new relapses. Crystallo-graphic study is one of the available non-invasive methods to evaluate the effectiveness of the therapy. The aim of the study was to analyze the crystallograms of patients with RAS in the course of treatment with sodium deoxyribonucleate. The results of the analysis of the crystallograms of patients with RAS showed that the group using sodium deoxyribonucleate in local treatment had a clearer ordered crystal structure, and the quantitative analysis was significantly different from the group (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Кристаллографическое исследование ротовой жидкости в динамике местного лечения дезоксирибонуклеатом натрия пациентов с афтозным стоматитом
Рецидивирующий афтозный стоматит (РАС) – распространенное заболевание слизистой оболочки рта, характеризующееся одиночными или множественными болезненными и рецидивирующими афтами [1]. По данным последних исследований известно, что его распространенность в разных группах населения колеблется от 5 до 50 %, при этом средний показатель распространенности составляет 20 % и выше у молодых женщин [2, 3]. Афты полости рта весьма болезненны для пациентов, вызывают боль и жжение при приеме пищи, глотании и разговоре. Эти проблемы нарушают функции пациентов и значительно снижают качество жизни как у детей, так и у взрослых [4, 5].
На сегодняшний день причины возникновения РАС связывают с некоторыми предрасполагающими факторами, такими как психологические, гематологические, генетические, травматические и аллергические. Тем не менее этиология заболевания неизвестна. Таким образом, окончательного лекарства от этого заболевания не существует [6, 7]. Пока РАС активен, основной целью лечения является минимизация симптомов и отсрочка рецидива после заживления. Предполагается, что лечение РАС облегчит боль и жжение, сократит период заболевания и превенти-рует рецидив афт [7, 8].
Для лечения РАС были исследованы различные фармацевтические препараты в форме местного и системного действия. Среди препаратов для местного применения доступны различные варианты, в том числе антисептики, противовоспалительные средства, антибиотики и кортикостероиды.
Успешной и широко используемой группой для этой цели являются местные кортикостероиды [9, 10]. Хотя краткосрочное применение кортикостероидов обычно не вызывает побочных эффектов, их длительное применение может вызывать местные и системные побочные эффекты, такие как кандидоз, угнетение функции надпочечников, истончение слизистой оболочки, лекарственная устойчивость [11].
Так, обилие средств и способов для лечения РАС говорит о том, что высокоэффективного метода так и не существует на сегодняшний день, при этом на фоне пандемии COVID-19 произошел прирост данного заболевания. Из этого возникает острая потребность в разработке новых средств терапии и диагностики РАС.
Одним из доступных, неинвазивных методов диагностики является анализ кристаллической структуры ротовой жидкости, который позволяет оценить состояние полости рта и наличие воспалительного процесса [12].
ЦЕЛЬ РАБОТЫ
Проанализировать кристаллограммы ротовой жидкости для оценки эффективности дезоксирибону-клета натрия в местном лечение пациентов с афтозным стоматитом.
МЕТОДИКА ИССЛЕДОВАНИЯ
Для реализации поставленной цели на базе кафедры стоматологии Института НМФО ФГБОУ ВО ВолгГМУ Минздрава России было проведено обследование 60 пациентов с диагнозом К12.0 рецидивирующие афты полости рта, малые (МКБ 10) и было одобрено локальным этическим комитетом ФГБОУ ВО ВолгГМУ Министерства здравоохранения РФ от 22.03.2021, справка № 2021/017. Критерием включения в исследование был клинический диагноз малый афтозный стоматит по классификации Стэнли (язвы размером менее 10 мм, расположенные на неороговевающих поверхностях слизистой оболочки, рецидивирующие с интервалом 1–4 месяца, заживление через 7–10 дней).
Критериями исключения были беременность, аллергические реакции на используемые препараты, хронические заболевания (например, гепатит, СПИД, глютеновая болезнь, дефицит IgA, диабет и т. д.) и прием лекарств (например, антибиотиков, противогрибковых препаратов, кортикостероидов, гормональной терапии и т. д.).
Всем пациентам проводили обследование до лечения, при необходимости назначали санацию полости рта, профессиональную гигиену полости рта, консультацию врача – стоматолога-ортопеда, устранение травмирующих фактор и консультацию врача-гастроэнтеролога, врача-иммунолога, врача-эндокринолога.
Пациентов распределили на 2 исследовательские группы по 30 человек. I группа получала общепринятую терапию (Национальное руководство под ред. Л. А. Дмитриевой, 2019 г.): аппликационная анестезия 10%-м раствором лидокаина; промывание слабыми антисептиками полости рта, снятие мягкого налета с поверхности слизистой оболочки рта и зубов; удаление некротических масс с применением фермента трипсина, 1 мг которого растворяют в 1 мл 0,9%-го раствора натрия хлорида; адгезивная дентальная паста солкосерила по 10 минут 2–3 раза в день; имудон (6–8 таблеток в день). II группа применяла аппликации дезоксирибонуклеата натрия с лидокаином (Колегель-ДНК-Л) 2 раза в день по 20 минут на протяжении 10 дней. Методика заключалась в нанесении на предварительно очищенную афту геля с лидокаином, дезоксиробонуклеатом натрия на основе альгината натрия и последующее покрытие саморассавыющейся пленкой. Помимо этого, было проведено обследование ротовой жидкости группы здоровых лиц (контрольная группа) с применением клиновидной дегидратации, которая используется для определения структурно-пространственной организации всех биологических жидкостей организма и является скрининговым методом широко применяемым для получения нормативных параметров исследования, выявления патологических процессов и контроля лечения [13]. Данное исследование проводили до лечения и на 7-е сутки.
В качестве материала исследовали использовали ротовую жидкость, забор которой проводили натощак из-под язычной области. Материал подвергался дегидратации на строго горизонтальной поверхности обезжиренного предметного стекла в течение 24 часов в объеме капли 20 мкл. Исследование проводилось на базе кафедры анатомии ФГБОУ ВО ВолгГМУ Минздрава России с помощью лабораторного Микроскоп Leica DM 1000. Полученные изображения фаций ротовой жидкости анализировали с использованием качественных и количественных параметров на базе программы Видеотест Мор-фо. Качественный анализ включал описание общей кристаллографической картины, описание кристаллов, выявление маркеров патологии.
Для количественного анализа с расчетом статистических показателей использовали определение ширины кристаллической структуры (ШКС, мкм), длины кристаллической структуры (ДКС, мкм), ширины краевой зоны (ШКЗ, мкм), соотношение ширины центральной и краевой зон (СКЦ, у. е.).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
Результаты анализа кристаллограмм контрольной группы пациентов продемонстрировали четкое разделение пространств фаций на центральную и периферическую зоны. В центральной зоне минеральные вещества образовывали множественные древовидные и папоротникообразные кристаллы с ответвлениями I и II порядка. В периферической зоне присутствовали преимущественно белковые компоненты, которые формировали так называемые «крылья бабочки» (рис. 1).
На кристаллограммах пациентов с РАС до лечения в ходе качественного анализа были выявлены размытые, нечеткие граница между периферической и центральной зонами, резкие нарушение с кристаллопостроением как белковой составляющей фации, так и минеральной. В центральной части кристаллы имели фрактальный характер, а в периферической зоне фации определились единичные, хаотичные, короткие трещины (рис. 2).
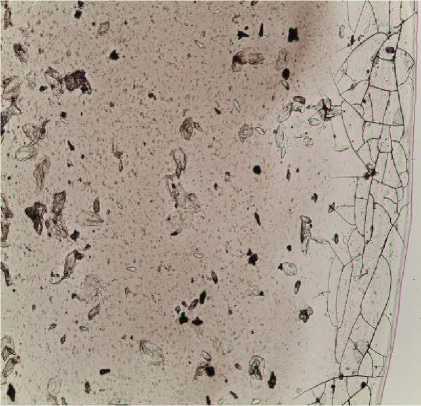
а
Рис. 1. Кристаллограмма пациента контрольной группы: а – периферическая зона фации; б – центральная зоны фации

б

Рис. 2. Кристаллограмма пациента с РАС до лечения
Через 7 дней от начала лечения в полости рта сохранялись афты на стадии эпителизации в обеих группах. В I группе, где применяли общепринятую схему лечения, граница между центральной и периферической зонами была выражена нечетко. У края фации были видны тонкие отрывистые трещины, также определились по площади фасции мелкозернистые гранулы и древовидные кристаллы (рис. 3).
Показатель ширины краевой зоны достоверно отличался от первоначального значения ( р < 0,05), но при этим, этот же параметр наряду со значениями длины кристаллической структуры, соотношения ширины центральной и краевой зон имели статистическое различие с цифрами аналогичных параметров контрольной группы ( р < 0,01).
Во II группе после 7 дней местной терапии РАС с применением геля «Колегель-ДНК-Л» также при анализе кристаллической картины наблюдались признаки воспаления. Граница между зонами была выражена слаба, в области краевой зоны наблюдались множественные трещины, местами обрывистые и хаотично направленные, также в ходе анализа фаций были обнаружены мелкозернистые гранулы, а в центральной зоне присутствовали дефектные закристаллизованные структуры (рис. 4).
Количественный анализ показал достоверно значимую разницу параметров длины кристаллической структуры и ширины краевой зоны по отношению к первоначальным значениям ( р < 0,05), помимо этого, значение ДКС [(40,92 ± 0,73) мм] были в 1,1 раз больше относительно I группы [(36,72 ± 0,67) мм].
Однако II группа имела достоверную разницу ширины краевой зоны с контрольной группой ( р < 0,01) (см. табл.).
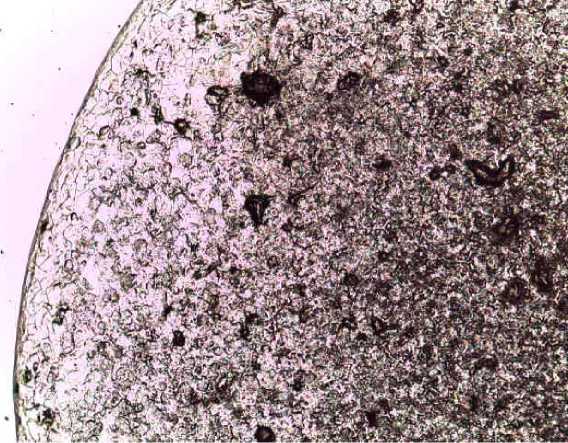
Рис. 3. Кристаллограмма пациента I группы на 7-й день лечения
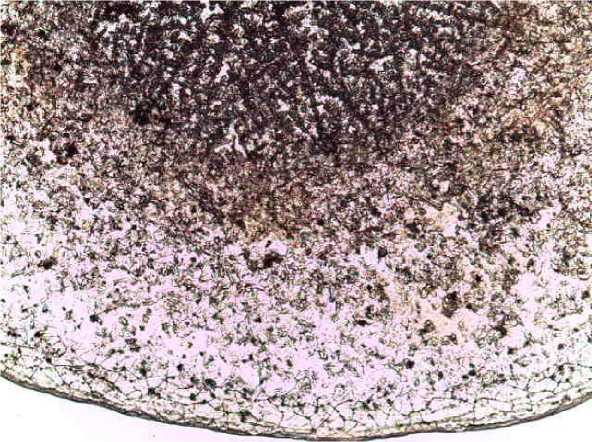
Рис. 4. Кристаллограмма пациента II группы на 7-й день лечения
Сравнительный количественный анализ фаций пациентов
|
Количественный параметр |
ШКС, мм |
ДКС, мм |
ШКЗ, мм |
СКЦ, у. е. |
|
Контроль |
2,07 ± 0,05 |
42,89 ± 0,76 |
47,26 ± 0,55 |
0,85 ± 0,01 |
|
До лечения |
1,79 ± 0,08 |
34,28 ± 1,56** |
78,32 ± 2,48** |
2,37 ± 0,27** |
|
I группа |
1,84 ± 0,05 |
36,72 ± 0,67** |
63,37 ± 1,37*,** |
2,18 ± 0,19** |
|
II группа |
1,97 ± 0,06 |
40,92 ± 0,73* |
55,38 ± 0,94*,** |
1,42 ± 0,38 |
Примечание: * – достоверность различий по отношению к показателю до лечения, р ˂ 0,05; ** – достоверность различий по отношению к показателю контроля, р ˂ 0,01.
ЗАКЛЮЧЕНИЕ
Кристаллографическое исследование пациентов с РАС позволило исследовать ротовую жидкость и выявить признаки воспаления до лечения, а также сохраняющиеся нарушения и на 7-й день терапии. На основании полученных результатов качественного анализа можно заключить, что в группе, где применяли дезоксирибонуклеат натрия, на 7-й день наблюдалось больше упорядоченных кристаллических структур относительно кристаллограмм I группы. Количественный анализ на основании параметров длины кристаллической структуры и соотношения ширины центральной и краевой зон продемонстрировал отсутствие достоверной разницы значений II группы от контрольной группы в отличии от показателей I группы.
На основании чего можно заключить, что кристаллографическое исследование позволило доказать эффективность применения дезоксирибонуклеата натрия в местной терапии РАС, но данное исследование требует необходимости изучения отдаленных сроков наблюдения при помощи метода клиновидной дегидратации.
Список литературы Кристаллографическое исследование ротовой жидкости в динамике местного лечения дезоксирибонуклеатом натрия пациентов с афтозным стоматитом
- Yang L., Zhu Q., Xie X., et al. Electrochemical behavior of CoCrMo alloy for dental applications in acidic artificial saliva containing albumin. Colloids Surf B Biointerfaces. 2019; 1(184):110–115.
- De Luca G., Cariddi A., Campochiaro C. et al. Efficacy and safety of apremilast for Behçet's syndrome: a real-life single-centre Italian experience. Rheumatology (Oxford). 2020;59(1):171–175.
- Македонова Ю. А., Александрина Е. С., Варгина С. А., Синенко Т. А. Сравнительная эффективность местного лечения афтозного стоматита. Эндодонтия today. 2021; 19(2):105–110.
- Roblegg E., Coughran A., Sirjani D. Saliva: An all-rounder of our body. Eur J Pharm Biopharm. 2019;142:133–141.
- Millsop J. W., Wang E. A., Fazel N. Etiology, evaluation, and management of xerostomia. Clin Dermatol. 2017; 35(5):468–476.
- Ghallab N. A. Diagnostic potential and future directions of biomarkers in gingival crevicular fluid and saliva of periodon-tal diseases: Review of the current evidence. Arch Oral Biol. 2018;87:115–124.
- Shouval D. S., Rufo P. A. The role of environmental factors in the pathogenesis of inflammatory bowel diseases: a re-view. JAMA Pediatr. 2017;171(10):999–1005.
- Kelly P., Connolly E. The prevalence and persistence of saliva in vehicles. Forensic Sci Int Genet. 2021;53:102–113.
- Volle G., Fraison J. B., Gobert D. et al. Dietary and non-dietary triggers of oral ulcer recurrences in Behcet's disease. Arthritis Care Res. 2017;69(9):1429–1436.
- Kaczor-Urbanowicz K. E., Martin Carreras-Presas C., Aro K. et al. Saliva diagnostics – Current views and directions. Exp Biol Med (Maywood). 2017;242(5):459–472.
- Reyes J., Fontes D., Bazzi A et al. Effect of saliva fluid properties on pathogen transmissibility. Sci Rep. 2021;11(1):16051.
- Пестов А. Ю., Крамарь В. О., Калашникова С. А., Постолов М. П. Биофизические параметры ротовой жидкости при нарушении микрофлоры полости рта. Вестник Волгоградского государственного медицинского университета. 2012;3(43):91–94.
- Калашников А. В., Калашникова С. А., Горячев А. Н. Патент № 2566719 С2 Российская Федерация, МПК G01N 33/48 (2006.01). Способ дифференциальной диагностики экссудативных плевритов туберкулезной этиологии с использованием клиновидной дегидратации плевральной жидкости: № 2013134349/15: заявл. 22.07.2013: опубл. 27.01.2015. 10 с.


