КТ-семиотика репаративных процессов в большеберцовой кости при интрамедуллярном остеосинтезе имплантатами с покрытием нитридами титана и гафния в эксперименте
Автор: Ахтямов Ильдар Фуатович, Шакирова Ф.В., Гатина Эльмира Биктемировна, Алиев Э.И., Мечов М.П.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2015 года.
Бесплатный доступ
Цель. Сравнительное изучение локального состояния костной ткани в зоне регенерации при фиксации отломков большеберцовой кости спицами из стали 12ХI8H9T с нанотехнологическим покрытием в эксперименте. Материалы и методы. В эксперименте на 40 беспородных кроликах были изучены биологические свойства нанопокрытия на основе сверхтвердых соединений нитридов титана и гафния. Результаты. Отмечено положительное влияние на формирование регенерата у животных с исследуемым покрытием. Перестроечные процессы костной ткани происходили в более ранние сроки в отличие от группы сравнения, что определялось более высокой плотностью кортикальной пластинки. Заключение. Применение имплантатов с покрытием нитридами титана и гафния, обладающих высокой прочностью, термической и химической стабильностью, сопровождалось формированием кортикальной пластинки в зоне остеоклазии с более высокими показателями плотностных характеристик.
Имплантат, компьютерная томография, нитрид титана и гафния
Короткий адрес: https://sciup.org/142121827
IDR: 142121827 | УДК: 616.718.5-001.5-003.93-089.227.843-092.9-073.756.8:[661.882 | DOI: 10.18019/1028-4427-2015-2-53-56
CT-semiotics of tibial reparative processes for intramedullary osteosynthesis using the implants coated with titanium and hafnium nitrides experimentally
Purpose. Comparative studying the local state of bone tissue in the regeneration zone for fixation of tibial fragments using wires of 12X18H9T steel with nanotech coating experimentally. Materials and Methods. Biological properties of nanocoating based on superhard compounds of titanium and hafnium nitrides studied experimentally in 40 mongrel rabbits. Results. The positive effect on the formation of regenerated bone observed in the animals with the coating studied. The processes of bone tissue reorganization occurred earlier unlike the comparison group determined by higher cortical density. Conclusion. The use of implants with the coating of titanium and hafnium nitrides having high strength, thermal and chemical stability accompanied by forming the cortical plate with higher density values in osteoclasis zone.
Текст научной статьи КТ-семиотика репаративных процессов в большеберцовой кости при интрамедуллярном остеосинтезе имплантатами с покрытием нитридами титана и гафния в эксперименте
Актуальной задачей травматологии является проблема выбора оптимального способа фиксации костных отломков и правильный выбор материалов, используемых при остеосинтезе и имплантации [12].
Металлические имплантаты имеют ряд недостатков, связанных с невысокой стойкостью к коррозии, особенно под воздействием биологически активных сред, что приводит к металлозу, несовместимости с тканями живого организма и отторжению имплантатов. Чаще это заканчивается несращением перелома, развитием гнойных процессов. В этой связи постоянно ведутся разработки по созданию оптимальных конструкций имплантатов и изыскиваются соответствующие биосовместимые материалы [9].
Одним из решений проблемы получения нового поколения имплантатов является использование схемы «металлическая основа-биопокрытие», то есть нанесение на их поверхность биосовместимых нерезорбируе-мых покрытий [2]. В настоящее время в этом качестве рассматриваются покрытия на основе нитридов титана. Они привлекательны биосовместимостью, обеспечивают низкий коэффициент трения и адекватную остеоинтеграцию [13]. Потенциально перспективными представляются также покрытия, содержащие нитрид гафния, который характеризуется химической инертностью, хорошей устойчивостью к окислению в экстремальных условиях [14], а также бактерицидностью [1]. Однако исследования этого вида покрытий единичны.
МАТЕРИАЛЫ И МЕТОДЫ
Исследования проводились на кафедре ветеринарной хирургии ФГБОУ ВПО Казанской государственной академии ветеринарной медицины имени Н.Э. Баумана. Все экспериментальные исследования, содержание, уход и эвтаназия проводились согласно требованиям «Европейской конвенции по защите позвоночных животных, используемых для экспериментов и других научных целей» (1986) [7].
Использованные в эксперименте имплантаты представляли собой спицы из стали 12ХI8H9T, диаметром 2 мм. Часть спиц была подвергнута камерному нанесению покрытий из нитридов титана и гафния методом конден- сации из плазменной фазы при ионной бомбардировке.
Эксперименты были проведены согласно ГОСТ ИСО (Р) 10993 (п. 11, 12) и одобрены Локальным Этическим Комитетом при ФГБОУ ВПО «Казанский государственный медицинский университет» Министерства здравоохранения Российской Федерации (протокол № 5 от 25 июня 2013 г.).
Экспериментальная модель использована на 40 кроликах в возрасте 6-7 месяцев с массой тела 2 526±74,4 г. Длина большеберцовой кости кроликов составила 105±3 мм. Животные были подобраны по принципу аналогов и разделены на две равные группы по 20 в каждой. Кролики содержались в одинаковых условиях, на одинаковом рационе, согласно рекомендациям по кормлению и содержанию лабораторных животных (Приказ Минздрава СССР от 12.08.1977 № 755).
При проведении опыта операцию осуществляли под общей анестезией (Rometar 2 % – 0,15-0,2 мл/кг, Золетил 100 – 10-15 мг/кг). Всем экспериментальным животным осуществлена открытая остеоклазия большеберцовой кости в области средней трети диафиза с медиальной поверхности голени с последующим ретроградным введением в костномозговую полость одной интрамедуллярной спицы [10]. В послеоперационном периоде проводилась внешняя иммобилизация оперированной конечности гипсовой повязкой до 10 суток.
При нарушении целостности большеберцовой кости путем остеоклазии у 38 кроликов (95 %) отмечался поперечный перелом, а у 2-х кроликов (5 %) оскольчатый.
Длительность эксперимента составила 180 суток. В послеоперационном периоде за животными вели ежедневные клинические наблюдения на протяжении всего периода лечения.
Компьютерную томографию проводили на муль-тиспиральном компьютерном томографе Toshiba Aquilion-16 (МСКТ) на 10, 30, 60, 90, 120,150 и 180 сутки после оперативного вмешательства (параметры – 120 кВ, 200 мАс, фильтр Bone, толщина среза 0,5 мм) [3, 11]. При проведении денситометрии определяли плотность периостальной мозоли и кортикальной пластинки в зоне остеоклазии.
Статистическую обработку полученных цифровых данных выполняли с применением пакета программ «SPSS», версия 13. Вычисляли среднеарифметическое выборочное значение показателя (М), стандартную ошибку среднеарифметического значения (m) по каждой из сравниваемых величин с определением достоверности различий (p) по методу Стьюдента-Фишера.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При проведении МСКТ костей голени интактных кроликов плотность кортикальной пластинки большеберцовой кости в зоне в средней трети диафиза составляла 2890,0±63,1 HU (табл. 1).
На 10 сутки после операции на серии рентгеновских компьютерных томограмм у животных обеих групп были получены изображения костей голени правой конечности, фиксированных интрамедуллярной конструкцией (рис. 1). В обеих группах в зоне остеоклазии наблюдалась сформировавшаяся периостальная реакция. Плотность формировавшейся периостальной мозоли у животных группы сравнения на данном сроке составляла 443,0±44,0 HU, что в 1,9 раза ниже чем у животных опытной группы (877,0±30,0 HU) (р=0,001) (табл. 1).
На 30-е сутки были выявлены достоверные различия между группами, где плотность кортикальной пластинки у животных с имплантатами из стали без покрытия была достоверно меньше на 23 % – 1163±44,8 НU, чем у животных с имплантатами, покрытыми нитридами титана и гафния (1429±6,8HU) (р=0,001) (рис. 2). Отмечалась полная консолидация отломков большеберцовой кости у животных обеих групп.
Плотность вновь сформированной кортикальной пластинки в зоне остеоклазии у животных группы сравнения на 60 сутки (имплантаты из стали 12ХI8H9T) составила 1708,0±171,6 HU и была достоверно ниже на 26 %, чем у животных опытной группы – 2159,7±80,8 HU (р=0,045) (рис. 3).
При проведении МСКТ на последующих сроках (90-х, 120-х, 150-х суток) отмечалась тенденция к увеличению плотности кортикального слоя большеберцовой кости, где показатели опытной группы были на 15,5 % выше аналогичных значений животных группы сравнения.
При проведении МСКТ костей голени на 180 сутки плотность кортикальной пластики у животных группы сравнения составила 2414,5±115,5 HU, что на 18 % ниже, чем у животных с исследуемым покрытием – 2857,5±200,5 HU (рис. 4).
Таблица 1
Денситометрические показатели кортикальной пластинки (HU)
|
Группа животных |
До операции |
10 сутки |
30 сутки |
60 сутки |
90 сутки |
120 сутки |
150 сутки |
180 сутки |
|
Группа сравнения |
2890,0±63,1 |
443,0±44,0+++ |
1163,3±44,8+++ |
1708,0±171,6+ |
2191,0±277,0 |
2247,5±38,5 |
2321,0±284,0 |
2414,5±115,5 |
|
Опытная группа |
877,0±30,0 |
1429,3±6,8 |
2159,7±80,8 |
2299,0±165,2 |
2742,5±287,5 |
2754,5±291,5 |
2857,5±200,5 |
Примечание: + – достоверные различия в отношении показателей опытной группы: + – р<0,05, +++ – р<0,001.

Рис. 2. МСКТ большеберцовой кости, зона перелома. 30-е сутки эксперимента (MPR): а – группа сравнения; б – опытная группа
Рис. 1. МСКТ большеберцовой кости в области перелома на 10-е сутки (MPR): а – группа сравнения, б – опытная группа
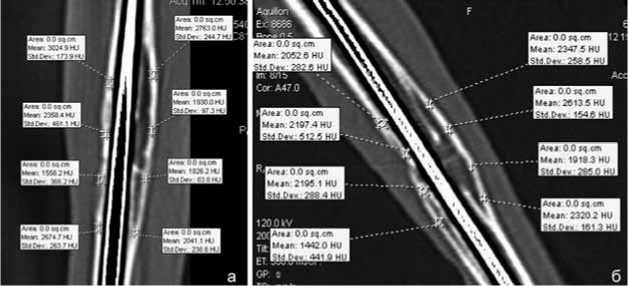
Рис. 3. МСКТ большеберцовой кости, зона перелома. 60-е сутки эксперимента (MPR): а – группа сравнения; б – опытная группа

Рис. 4. МСКТ большеберцовой кости, зона перелома. 180 сутки эксперимента (MPR): а – группа сравнения; б – опытная группа
ЗАКЛЮЧЕНИЕ
Таким образом, проведенное исследование позволяет заключить, что применение имплантатов с покрытием нитридами титана и гафния, обладающих высокой прочностью, термической и химической стабильностью, сопровождается формированием кортикальной пластинки в зоне остеоклазии с более высокими показателями плотностных характеристик. Так, на 10 сутки эксперимента плотность формировавшейся периостальной мозоли у животных опытной группы была достоверно выше в 1,9 раза. Подобные результаты отмечались на всех последующих сроках эксперимента. На 30-е сутки плотность кортикальной пластинки у животных с исследуемым покрытием была выше на 23 %, на 60-е сутки – на 26 %. На 90-е, 120-е, 150-е, 180-е сутки не было выявлено достоверных различий между группами, но плотность кортикального слоя большеберцовой кости у животных с имплантатами, покрытыми нитридами титана и гафния, была выше в среднем на 15-18 %.
Исходя из результатов исследования можно заключить, что процессы ремоделирования костной ткани в зоне остеоклазии у животных, где применялись имплантаты с покрытием нитридами титана и гафния, происходила в более ранние сроки в отличие от группы сравнения.
Применение имплантатов с покрытием нитридами титана и гафния при погружном остеосинтезе следует считать перспективным, клинически оправданным методом и позволяет рекомендовать его для широкого клинического внедрения.
Список литературы КТ-семиотика репаративных процессов в большеберцовой кости при интрамедуллярном остеосинтезе имплантатами с покрытием нитридами титана и гафния в эксперименте
- Абдуллин И. Ш., Миронов М. М., Гарипова Г. И. Бактерицидные и биологически стойкие покрытия для медицинских имплантатов и инструментов//Мед. техника. 2004. № 4. С. 20-22
- Клинические аспекты современной лучевой диагностики в травматологии и ортопедии/Г.В. Дьячкова, Ю.Л. Митина, К.А. Дьячков, Д.А. Алекберов, А.Н. Бакарджиева, Р.В. Степанов, Е.В. Скрипкин, Ю.М. Александров, А.В. Акуленко//Гений ортопедии. 2011. № 2. С. 91-97.
- Дьячков К.А., Дьячкова Г.В., Александров Ю.М. Рентгеноморфологические особенности и плотность корковой пластинки большеберцовой кости на различных этапах удлинения//Вестн. травматологии и ортопедии им. Н.Н. Приорова. 2012. № 4. С. 58-61.
- Оценка качества кости методом мультисрезовой компьютерной томографии у больных хроническим остеомиелитом/Г.В. Дьячкова, К.А. Дьячков, С.М. Александров, Т.А. Ларионов, Н.М. Клюшин//Травматология и ортопедия России. 2013. № 3. С. 88-94.
- Анализ репаративного костеобразования при лечении больных с переломами длинных трубчатых костей по данным компьютерной томографии и двухэнергетической рентгеновской абсорбциометрии/Г.В. Дьячкова, Р.В. Степанов, Л.В. Суходолова, С.П. Бойчук, Н.Д. Хубаев, Н.Ф. Обанина//Вестн. новых мед. технологий. 2006. № 3. С. 74-78.
- Завадовская В.Д. Лучевая диагностика: учеб. пособие. Ч. 1. Методы лучевой диагностики. Лучевая анатомия органов и систем. Основные патологические синдромы. М.: Видар, 2009. 375 с.
- Карлов А.В., Шахов В.П. Системы внешней фиксации и регуляторные механизмы оптимальной биомеханики. Томск: STT, 2001. 480 с.
- Кишновская Е.А. Сращение переломов//Вестн. рентгенологии и радиологии. 1980. № 3. С. 27-30.
- Корнилов Н.В., Грязнухин Э.Г. Травматология и ортопедия: рук. для врачей. Т. 1. Общие вопросы травматологии и ортопедии. СПб.: Гиппократ, 2004. 786 с.
- Лопухин Ю.М. Экспериментальная хирургия. М.: Медицина,1971. 346 с.
- Прокоп М., Галански М. Спиральная и многослойная компьютерная томография: учеб. пособие. В 2 т. Т. 2/пер. с англ.; под ред. А.В. Зубарева, Ш.Ш. Шотемора. 2-е изд. М.: МЕДпресс-информ, 2011. 712 с.
- Самошкин И.Б., Слесаренко Н.А. Реконструктивно-восстановительная хирургия опорно-двигательного аппарата у собак: рук. для ветеринарных врачей. М.: Советский спорт, 2008. 200 с.
- Sovak G., Weiss A., Gotman I. Osseointegration of Ti6Al4V alloy implants coated with titanium nitride by a new method//J. Bone Joint Surg. Br. 2000. Vol. 82, No 2. P. 290-296.
- Nanomechanical properties of hafnium nitride coating/T. Laha, Y. Chen, K. Balani, A. Agarwal//Scripta Materialia. 2008. Vol. 58. P. 1121-1124.


