Квантово-химический расчет молекул метилциклобутана и этилциклобутана методом AM1
Автор: Бабкин Владимир Александрович, Игнатов Алексей Викторович, Фомичев Валерий Тарасович, Заиков Геннадий Ефремович
Журнал: НБИ технологии @nbi-technologies
Рубрика: Технико-технологические инновации
Статья в выпуске: 1 (10), 2014 года.
Бесплатный доступ
Впервые выполнен квантово-химический расчет молекул метилциклобутана и этилциклобутана методом AM1 с оптимизацией геометрии по всем параметрам стандартным градиентным методом. Получено оптимизированное геометрическое и электронное строение этих соединений. Теоретически оценена их кислотная сила. Установлено, что молекулы метилциклобутана и этилциклобутана относятся кклассу очень слабых кислот (pKa > 14).
Квантово-химический расчет, метод am1, метилциклобутан, этилциклобутан, кислотная сила
Короткий адрес: https://sciup.org/14968306
IDR: 14968306 | УДК: 547.854.83:544.183.25
Quantum and chemical calculation of methylcyclobutane and ethylcyclobutane molecules by AM1 method
For the first time methylcyclobutan and ethylcyclobutan are polymerized in the presence of AlCl3/HBr, AlCl3/HCl and Al(OH)Cl2 catalysts to room temperature in 1953. Other systematic researches on polymerization of these monomers are practically absent. Still quantum and chemical calculations of these monomers, and, in particular, are not executed by the AM1 method, and mechanisms of elementary acts at electronic level are not studied and the nature of the active centers is not investigated. In this regard, the purpose of the real work is quantum and chemical calculation methylcyclobutan and ethylcyclobutan AM1 method with geometry optimization in all respects the standard gradient method which has been built in PC GAMESS, in approach of the isolated molecule in a gas phase and a theoretical assessment of its acid force. For visual representation of models of molecules the known MacMolPlt program was used. The optimized geometrical and electronic structure, the general energy and electronic energy methylcyclobutan and ethylcyclobutan are received by the AM1 method and shown in fig. 1-2 and in tab. 1-2. Applying a formula rKa = 47.74 - 154.949 (= +0.09 and +0.10 - the maximum charges on atoms of hydrogen, rKa - a universal indicator of acidity), we find values of acid force equal a rKa = 34 and 32. For the first time it is executed quantum chemical calculation of the molecules of methylcyclobutane and ethylcyclobutane by AM1 method with optimization of geometry on all parameters. The optimized geometrical and electronic structures of these connections are received. Acid forces of methylcyclobutane and ethylcyclobutane are theoretically appreciated. It is established, than it relates to the class of very weak H-acids.
Текст научной статьи Квантово-химический расчет молекул метилциклобутана и этилциклобутана методом AM1
Метилциклобутан и этилциклобутан впервые полимеризовали в присутствии катализаторов AlCl3/HBr, AlCl3/HCl и Al(OH)Cl2при комнатной температуре в 1953 году [3; 7]. Другие систематические исследования по полимеризации этих мономеров до настоящего времени практически отсутствуют. До сих пор не выполнены квантово-химические расчеты этих мономеров, в частности, методом AM1, не изучены механизмы элементарных актов на электронном уровне и не исследована природа активных центров. В связи с этим целью настоящей работы является квантово-химический расчет молекул метилциклобутана и этилциклобутана методом AM1 с оптимизацией геометрии по всем параметрам стандартным градиентным методом, встроенным в PC GAMESS [5], в приближении изолированной молекулы в газовой фазе и теоретическая оценка его кислотной силы. Для визуального представления моделей молекул использовалась известная программа MacMolPlt [6].
Результаты расчетов
Оптимизированное геометрическое и электронное строение, общая энергия и электронная энергия молекул метилциклобутана и этилциклобутана получены методом AM1 и показаны на рисунках 1 и 2 и в таблицах 1 и 2. Применяя формулу рКа = 47.74 –154.949 q m H + ax [1; 2; 4] (= +0.09 и +0.10 – максимальные заряды на атомах водорода, рКа – универсальный показатель кислотности: см. табл. 3), находим значения кислотной силы, равные рКа =34 и 32.
Таким образом, нами впервые выполнен квантово-химический расчет молекул метилциклобутана и этилциклобутана методом AM1. Получено оптимизированное геометрическое и электронное строение этих соеди- нений. Теоретически оценены их кислотные силы рКа, равные 34 и 32.
Установлено, что метилциклобутан и этилциклобутан относятся к классу очень слабых Н-кислот (pKa > 14).
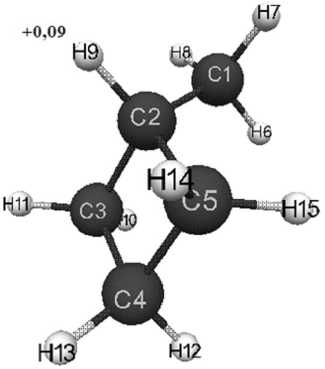
Рис. 1. Геометрическое и электронное строение молекулы метилциклобутана
( Е 0 = -28.590 кДж/моль, Е эл = -117.931кДж/моль)
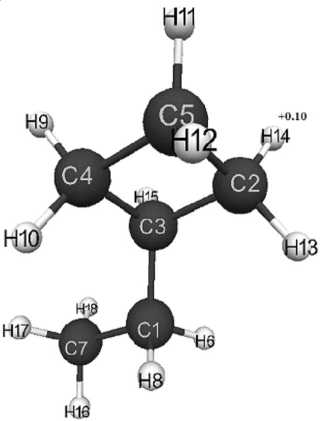
Рис. 2. Геометрическое и электронное строение молекулы этилциклобутана
( Е 0 = -34.316 кДж/моль, Е эл = -155.325 кДж/моль)
Таблица 1
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы метилциклобутана
|
Длины связей |
R, A |
Валентные углы |
Град. |
|
C(2)-C(1) |
1.5 |
C(1)-C(2)-C(3) |
115 |
|
C(3)-C(2) |
1.55 |
C(2)-C(3)-C(4) |
90 |
|
C(4)-C(3) |
1.54 |
C(1)-C(2)-C(5) |
115 |
|
C(5)-C(4) |
1.54 |
C(2)-C(1)-H(6) |
110 |
|
H(6)-C(1) |
1.12 |
C(2)-C(1)-H(7) |
110 |
|
H(7)-C(1) |
1.12 |
C(2)-C(1)-H(8) |
110 |
|
H(8)-C(1) |
1.12 |
C(1)-C(2)-H(9) |
110 |
|
H(9)-C(2) |
1.15 |
C(2)-C(3)-H(10) |
113 |
|
H(10)-C(3) |
1.11 |
C(2)-C(3)-H(11) |
113 |
|
H(11)-C(3) |
1.11 |
C(3)-C(4)-H(12) |
114 |
|
H(12)-C(4) |
1.11 |
C(3)-C(4)-H(13) |
114 |
|
H(13)-C(4) |
1.11 |
C(2)-C(5)-H(14) |
114 |
|
H(14)-C(5) |
1.11 |
C(2)-C(5)-H(15) |
114 |
|
H(15)-C(5) |
1.11 |
– |
– |
Таблица 2
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы этилциклобутана
|
Длины связей |
R, A |
Валентные углы |
Град. |
|
C(3)-C(1) |
1.50 |
C(5)-C(2)-C(3) |
90 |
|
C(3)-C(2) |
1.55 |
C(2)-C(3)-C(4) |
90 |
|
C(5)-C(2) |
1.54 |
C(3)-C(4)-C(5) |
90 |
|
C(5)-C(4) |
1.54 |
C(2)-C(5)-C(4) |
90 |
|
C(4)-C(3) |
1.55 |
C(2)-C(3)-C(1) |
114 |
|
C(7)-C(1) |
1.51 |
C(3)-C(1)-H(6) |
113 |
|
H(6)-C(1) |
1.12 |
C(3)-C(1)-H(8) |
110 |
|
H(8)-C(1) |
1.12 |
C(3)-C(4)-H(9) |
114 |
|
H(9)-C(4) |
1.11 |
C(3)-C(4)-H(10) |
114 |
|
H(10)-C(4) |
1.10 |
C(2)-C(5)-H(11) |
114 |
|
H(11)-C(5) |
1.10 |
C(2)-C(5)-H(12) |
114 |
|
H(12)-C(5) |
1.11 |
C(2)-C(5)-H(13) |
114 |
|
H(13)-C(2) |
1.11 |
C(2)-C(5)-H(14) |
114 |
|
H(14)-C(2) |
1.11 |
C(1)-C(3)-H(15) |
110 |
|
H(15)-C(3) |
1.11 |
C(1)-C(7)-H(16) |
110 |
|
H(16)-C(7) |
1.12 |
C(1)-C(7)-H(17) |
110 |
|
H(17)-C(7) |
1.12 |
C(1)-C(7)-H(18) |
111 |
|
H(18)-C(7) |
1.12 |
– |
– |
Таблица 3
Общая энергия ( Е 0), электронная энергия ( Е эл), максимальный заряд на атоме водорода (qmaxH+) и универсальный показатель кислотности (pKa) молекул
|
Мономер |
- Е 0 (кДж/моль) |
- Е эл (кДж/моль) |
H+ q max |
pKa |
|
Метилциклобутан |
-28.590 |
-117.931 |
+0,09 |
34 |
|
Этилциклобутан |
-34.316 |
-155.325 |
+0,10 |
32 |
Список литературы Квантово-химический расчет молекул метилциклобутана и этилциклобутана методом AM1
- Квантово-химическое моделирование молекул n-метилстирола и n-трет-бутилстирола методом AM1/В. А. Бабкин, А. В. Игнатов, Н. А. Барановский, А. С. Петров, О. В. Стоянов, Г. Е. Заиков, А. С. Белоусов//Вестник Казанского технологического университета. -2013. -Т. 16, № 13. -С. 113-115.
- Квантово-химическое моделирование молекул циклопентадиена и 2,3-диметилциклопентадиена методом AM1/В. А. Бабкин, А. В. Игнатов, А. И. Авраменко, А. А. Козлов, Г. Е. Заиков//Вестник Казанского технологического университета. -2013. -Т. 16, № 14. -С. 33-35.
- Кеннеди, Дж. Катионная полимеризация олефинов/Дж. Кеннеди. -М.: Мир, 1978. -431 с.
- О корреляционной зависимости универсального показателя кислотности с максимальным зарядом на атоме водорода Н-кислот. Метод АМ1/В. А. Бабкин, Д. С. Андреев, В. Т. Фомичев, Г. Е. Заиков, Э. Р. Мухамедзянова//Вестник Казанского технологического университета. -2012. -Т. 15, № 10. -С. 15-19.
- Advances in Electronic Structure Theory: GAMESS a Decade Later/M. W. Sh midt,K. K. Baldrosge, J. A. Elbert, M. S. Gordon, J. H. Enseh, S. Koseki, N. Matsvnaga, K. A. Nguyen, S. J. Su [et al.]//J. Comput. Chem. -1993. -№ 14. -P. 1347-1363.
- Bode, B. M. A Graphical User Interface for GAMESS/B. M. Bode and M. S. Gordon//J. Mol. Graphics Mod. -1998. -№ 16. -P. 133-138.
- Pines, H. Isomerization of Saturated Hydrocarbons/H. Pines, W. D. Huntsman, V. N. Ipatieff//J. Am. Chem. Soc. -1953. -№ 75. -P. 2315.


