Квантово-химический расчет некоторых циклопропанов методом AM1
Автор: Бабкин Владимир Александрович, Авраменко Александр Игоревич, Фомичев Валерий Тарасович, Заиков Геннадий Ефремович
Журнал: НБИ технологии @nbi-technologies
Рубрика: Технико-технологические инновации
Статья в выпуске: 1 (8), 2013 года.
Бесплатный доступ
Впервые выполнен квантово-химический расчет некоторых циклопропанов 1,1-дих-лор-2-п-хлорфенил-2-метилциклопропана, 1,1-дихлор-2-фенилциклопропана, 1-метил-1ви-нил-2,2-дихлорциклопропана методом AM1 с оптимизацией геометрии по всем параметрам стандартным градиентным методом. Получено оптимизированное геометрическое и электронное строение этих соединений. Теоретически оценена его кислотная сила (20 J рКа J 26). Установлено, что молекула 1,1-дихлор-2-п-хлорфенил-2-метилциклопропана относится к классу очень слабых кислот (pKa > 14).
Квантово-химический расчет, метод am1, 1-дихлор-2-п-хлорфенил-2-метилциклопропана, 1-дихлор-2-фенилциклопропан, 1-метил-1винил-2, 2-дихлорциклопропан
Короткий адрес: https://sciup.org/14968273
IDR: 14968273 | УДК: 547.854.83:544.183.25
Quantum and chemical calculation of some cyclopropanes by AM1 method
For the first time it is executed quantum chemical calculation of some cyclopropanes of 1,1-dihlor-2-p-hlorphenyl-2-methylcyclopropane, 1,1-dihlor-2-phenylcyclopropane, 1-methyl-1vinil-2,2-dihlorcyclopropane by method AM 1 with optimization of geometry on all parameters. The optimized geometrical and electronic structure of this connections is received. Acid force of 1,1-dihlor-2-p-hlorphenyl-2-methylcyclopropane, 1,1-dihlor-2-phenylcyclopropane, 1-methyl-1vinil-2,2-dihlorcyclopropane is theoretically appreciated. It is established, than it to relate to a class of very weak H-acids (+20 ≤ рКа ≤ +26, where pKa-universal index of acidity).
Текст научной статьи Квантово-химический расчет некоторых циклопропанов методом AM1
Целью настоящей работы является выполненный методом AM1 с оптимизацией геометрии по всем параметрам стандартным градиентным методом, встроенным в PC GAMESS [4], квантово-химический расчет некоторых циклопропанов – 1,1-дихлор-2-п-хлорфенил-2-метилциклопропа-на, 1,1-дихлор-2-фенилциклопропана, 1-ме-тил-1винил-2,2-дихлорциклопропана [2], в приближении изолированных молекул в газовой фазе, и теоретическая оценка его кислотной силы. Для визуального представления моделей молекул использовалась известная программа MacMolPlt [3].
Результаты расчетов
Оптимизированное геометрическое и электронное строение, общая энергия и электронная энергия некоторых циклопро-
панов 1,1-дихлор-2-п-хлорфенил-2-метил-циклопропана, 1,1-дихлор-2-фенилциклопро-пана, 1-метил-1винил-2,2-дихлорциклопро-пана получены методом AM1 и показаны на рисунках 1–3 и в таблицах 1–4. Используя известную формулу рКа = 47.74 – 154.949 q maxH+ [1] (0,14 < q max H+ < 0,18-максимальный заряд на атоме водорода, рКа – универсальный показатель кислотности, см. табл. 1), находим значение кислотной силы.
Таким образом, нами впервые выполнен квантово-химический расчет некоторых циклопропанов 1,1-дихлор-2-п-хлорфенил-2-ме-тилциклопропана, 1,1-дихлор-2-фенилциклоп-ропана, 1-метил-1винил-2,2-дихлорциклопро-пана методом AM1. Получено оптимизированное геометрическое и электронное строение этих соединений. Теоретически оценена их кислотная сила +20 < рКа < +26. Установлено, что 1,1-дихлор-2-п-хлорфенил-2-метилциклопропана, 1,1-дихлор-2-фенилцик-лопропана, 1-метил-1винил-2,2-дихлорциклоп-ропана относятся к классу очень слабых Н-кислот (pKa > 14).
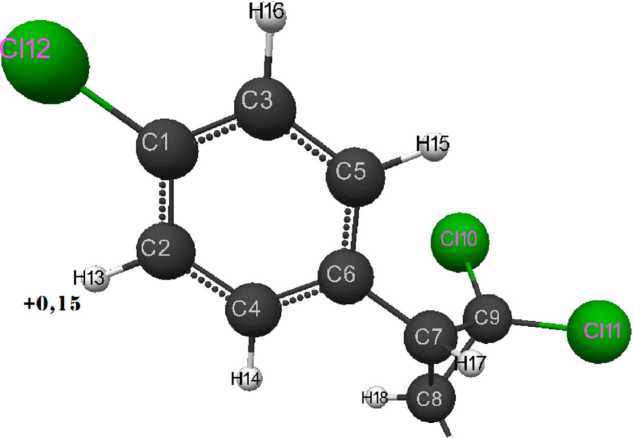
Н19
Рис. 1. Геометрическое и электронное строение молекулы 1,1-дихлор-2-п-хлорфенил-2-метилциклопропана (Е0= -228 508 кДж/моль, Еэл= -1 018 155 кДж/моль)
Таблица 1
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы
1,1-дихлор-2-п-хлорфенил-2-метилциклопропана
|
Длины связей |
R,A |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
C(2)-C(1) |
1.40 |
C(3)-C(1)-C(2) |
120 |
C(1) |
-0.04 |
|
C(3)-C(1) |
1.40 |
C(4)-C(2)-C(1) |
120 |
C(2) |
-0.11 |
|
C(4)-C(2) |
1.39 |
C(5)-C(3)-C(1) |
120 |
C(3) |
-0.13 |
|
C(5)-C(3) |
1.39 |
C(6)-C(4)-C(2) |
121 |
C(4) |
-0.11 |
|
C(6)-C(4) |
1.40 |
C(7)-C(6)-C(4) |
121 |
C(5) |
-0.11 |
|
C(6)-C(5) |
1.40 |
C(8)-C(7)-C(6) |
122 |
C(6) |
-0.06 |
|
C(7)-C(6) |
1.47 |
C(9)-C(7)-C(6) |
122 |
C(7) |
-0.11 |
|
C(8)-C(7) |
1.50 |
Cl(10)-C(9)-C(7) |
120 |
C(8) |
-0.19 |
|
C(9)-C(7) |
1.52 |
Cl(11)-C(9)-C(7) |
117 |
C(9) |
-0.07 |
|
C(9)-C(8) |
1.51 |
C(2)-C(1)-Cl(12) |
120 |
Cl(10) |
-0.01 |
|
Cl(10)-C(9) |
1.72 |
C(1)-C(2)-H(13) |
120 |
Cl(11) |
-0.03 |
|
Cl(11)-C(9) |
1.73 |
C(2)-C(4)-H(14) |
120 |
Cl(12) |
-0.04 |
|
Cl(12)-C(1) |
1.70 |
C(3)-C(5)-H(15) |
120 |
H(13) |
0.15 |
|
H(13)-C(2) |
1.10 |
C(1)-C(3)-H(16) |
120 |
H(14) |
0.14 |
|
H(14)-C(4) |
1.10 |
C(6)-C(7)-H(17) |
111 |
H(15) |
0.14 |
|
H(15)-C(5) |
1.10 |
C(7)-C(8)-H(18) |
119 |
H(16) |
0.15 |
|
H(16)-C(3) |
1.10 |
C(7)-C(8)-H(19) |
119 |
H(17) |
0.15 |
|
H(17)-C(7) |
1.11 |
– |
– |
H(18) |
0.13 |
|
H(18)-C(8) |
1.11 |
– |
– |
H(19) |
0.13 |
|
H(19)-C(8) |
1.11 |
– |
– |
– |
– |
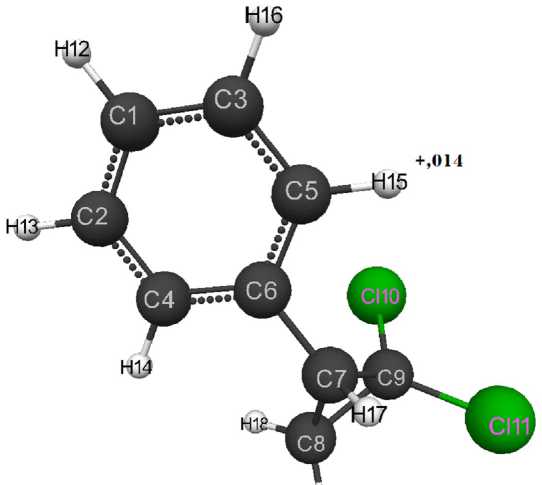

Рис. 2. Геометрическое и электронное строение молекулы 1,1-дихлор-2-фенилциклопропана (Е0= -193 770 кДж/моль, Еэл= -879 837 кДж/моль)
Таблица 2
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы
1,1-дихлор-2-фенилциклопропана
|
Длины связей |
R,A |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
C(2)-C(1) |
1.39 |
C(3)-C(1)-C(2) |
120 |
C(1) |
-0.12 |
|
C(3)-C(1) |
1.39 |
C(4)-C(2)-C(1) |
120 |
C(2) |
-0.13 |
|
C(4)-C(2) |
1.39 |
C(5)-C(3)-C(1) |
120 |
C(3) |
-0.13 |
|
C(5)-C(3) |
1.39 |
C(6)-C(4)-C(2) |
120 |
C(4) |
-0.12 |
|
C(6)-C(4) |
1.40 |
C(7)-C(6)-C(4) |
121 |
C(5) |
-0.11 |
|
C(6)-C(5) |
1.40 |
C(8)-C(7)-C(6) |
122 |
C(6) |
-0.06 |
|
C(7)-C(6) |
1.47 |
C(9)-C(7)-C(6) |
122 |
C(7) |
-0.10 |
|
C(8)-C(7) |
1.51 |
Cl(10)-C(9)-C(7) |
121 |
C(8) |
-0.19 |
|
C(9)-C(7) |
1.52 |
Cl(11)-C(9)-C(7) |
118 |
C(9) |
-0.07 |
|
C(9)-C(8) |
1.51 |
C(2)-C(1)-H(12) |
120 |
Cl(10) |
-0.02 |
|
Cl(10)-C(9) |
1.72 |
C(1)-C(2)-H(13) |
120 |
Cl(11) |
-0.03 |
|
Cl(11)-C(9) |
1.73 |
C(2)-C(4)-H(14) |
120 |
H(12) |
0.13 |
|
H(12)-C(1) |
1.10 |
C(3)-C(5)-H(15) |
120 |
H(13) |
0.13 |
|
H(13)-C(2) |
1.10 |
C(1)-C(3)-H(16) |
120 |
H(14) |
0.13 |
|
H(14)-C(4) |
1.10 |
C(6)-C(7)-H(17) |
111 |
H(15) |
0.14 |
|
H(15)-C(5) |
1.10 |
C(7)-C(8)-H(18) |
119 |
H(16) |
0.13 |
|
H(16)-C(3) |
1.10 |
C(7)-C(8)-H(19) |
119 |
H(17) |
0.14 |
|
H(17)-C(7) |
1.11 |
– |
– |
H(18) |
0.13 |
|
H(18)-C(8) |
1.11 |
– |
– |
H(19) |
0.13 |
|
H(19)-C(8) |
1.11 |
– |
– |
– |
– |
4-0,111
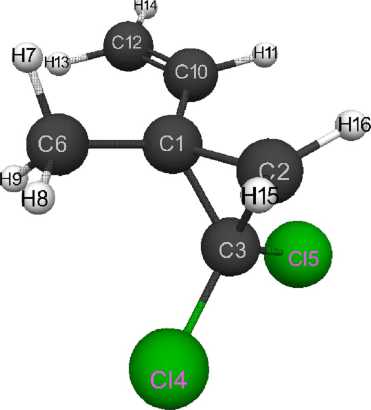
Рис. 3. Геометрическое и электронное строение молекулы 1-метил-1винил-2,2-дихлорциклопропана (Е0= -156 714 кДж/моль, Еэл= -622 705 кДж/моль)
Таблица 3
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы 1-метил-1винил-2,2-дихлорциклопропана
|
Длины связей |
R, A |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
C(2)-C(1) |
1.51 |
C(3)-C(2)-C(1) |
61 |
C(1) |
-0.05 |
|
C(3)-C(2) |
1.50 |
C(1)-C(3)-C(2) |
60 |
C(2) |
-0.19 |
|
Cl(4)-C(3) |
1.72 |
C(2)-C(1)-C(3) |
59 |
C(3) |
-0.07 |
|
Cl(5)-C(3) |
1.73 |
C(1)-C(3)-Cl(4) |
119 |
CL(4) |
-0.03 |
|
C(6)-C(1) |
1.50 |
C(1)-C(3)-Cl(5) |
119 |
CL(5) |
-0.03 |
|
H(7)-C(6) |
1.12 |
C(2)-C(1)-C(6) |
118 |
C(6) |
-0.19 |
|
H(8)-C(6) |
1.12 |
C(1)-C(6)- H (7) |
110 |
H(7) |
0.09 |
|
H(9)-C(6) |
1.12 |
C(1)-C(6)- H(8) |
111 |
H(8) |
0.09 |
|
C(10)-C(1) |
1.47 |
C(1)-C(6)- H (9) |
110 |
H(9) |
0.09 |
|
H(11)-C(10) |
1.10 |
C(2)-C(1)-C(10) |
118 |
C(10) |
-0.14 |
|
C(12)-C(10) |
1.33 |
C(1)-C(10)-H(11) |
115 |
H(11) |
0.13 |
|
H(13)-C(12) |
1.10 |
C(1)-C(10)-C(12) |
126 |
C(12) |
-0.20 |
|
H(14)-C(12) |
1.10 |
C(10)-C(12)-H(13) |
123 |
H(13) |
0.12 |
|
H(15)-C(2) |
1.11 |
C(10)-C(12)-H(14) |
122 |
H(14) |
0.18 |
|
H(16)-C(2) |
1.11 |
C(1)-C(2)-H(15) |
119 |
H(15) |
0.13 |
|
– |
– |
C(1)-C(2)-H(16) |
119 |
H(16) |
0.13 |
Таблица 4
Общая энергия (Е 0 ), суммарная энергия связей (Е эл ), максимальный заряд на атоме водорода (q max H+ ), универсальный показатель кислотности рКа алициклических олефинов
|
№ п/п |
Алициклические олефины |
-Е0 кДж/моль |
- Еэл кДж/моль |
H+ q max |
рКа |
|
1 |
1,1-дихлор-2-п-хлорфенил-2-метилциклопропана |
-228 508 |
-1 018 155 |
0,15 |
24 |
|
2 |
1,1-дихлор-2-фенилциклопропана |
-193 770 |
-879 837 |
0,14 |
26 |
|
3 |
1-метил-1винил-2,2-дихлорциклопропана |
-156 714 |
-622 705 |
0,18 |
20 |
Список литературы Квантово-химический расчет некоторых циклопропанов методом AM1
- Бабкин, В. А. О корреляционной зависимости универсального показателя кислотности с максимальным зарядом на атоме водорода Н-кислот. Метод АМ1/В. А. Бабкин [и др.]//Вестник Казанского технологического университета. -2012. -№ 10. -С. 15-19.
- Кеннеди, Дж. Катионная полимеризация олефинов/Дж. Кеннеди. -М.: Мир, 1978. -431 с.
- Bode, B. M. Mol. Graphics Mod., 16/B. M. Bode and M. S. Gordon J. -Amer. Chem. Soc., 1998. -P. 133-138.
- Shmidt, M. W. J. Comput/M. W. Shmidt [et al.]. -Chem. 14. -Chem. Rev. Lett., 1993. -P. 1347-1363.


