Квантово-химическое прогнозирование антирадикальной активности 11-дезоксимизопростола
Автор: Катаева Р.М., Аглетдинов Э.Ф., Латыпова Г.М., Катаев В.А., Халимов А.Р., Гизатуллин Т.Р.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 3 (67), 2020 года.
Бесплатный доступ
Изучена и охарактеризована прямая антирадикальная активность этилового эфира (±)-11,15-дидезокси-16-метил-16-гидроксипростагландина E1 (11-дезоксимизопростол) при проведении квантово-химических расчётов. Проведены квантово-химические расчеты структуры 11-дезоксимизопростола (11-ДМП) и его радикальных производных с неспаренным электроном у атомов углерода в 12 и 15 положениях. При сравнивании Есв частиц установлено, что более устойчивой структурой является радикал R'ДОМП12* Исходя из полученных данных, представляется вполне вероятным, что 11-дезоксимизопростол может потенциально служить антиоксидантом прямого действия, способным образовывать более устойчивые и менее реакционноспособные радикалы, чем радикалы - производные полиненасыщенных жирных кислот (ПНЖК), участвующие в цепных процессах свободнорадикального окисления в живых системах.
11-дезоксимизопростол, квантово-химическое прогнозирование, антирадикальная активность, процессы свободнорадикального окисления
Короткий адрес: https://sciup.org/142225962
IDR: 142225962 | УДК: 678.048:577.33:616-007.29
Quantum-chemical prediction of the antiradical activity of 11-deoximisoprostol
The direct antiradical activity of ethyl ether (±) -11,15-dideoxy-16-methyl-16-hydroxyprostaglandin E1 (11-deoxyimisoprostol) was studied and characterized in the course of quantum-chemical calculations. Quantum-chemical calculations of the structure of 11-deoxyimisoprostol (11-DMP) and its radical derivatives with an unpaired electron at carbon atoms in 12 and 15 positions have been performed. When comparing Eb particles, it was found that the more stable structure is the RDOMP12* radical. Based on the data obtained, it seems quite probable that 11-deoxyimisoprostol can potentially serve as a direct antioxidant capable of forming more stable and less reactive radicals than radicals-derivatives of polyunsaturated fatty acids (PUFAs) involved in free radical oxidation chain processes in the living systems.
Текст научной статьи Квантово-химическое прогнозирование антирадикальной активности 11-дезоксимизопростола
В патогенезе подавляющего большинства известных на сегодняшний день заболеваний важнейшее значение имеют неспецифические патохимические процессы, определяющие реактивность организма, его адаптивный потенциал при действии эндогенных и экзогенных факторов. Одним из наиболее значимых метаболических процессов такого рода является свободнорадикальное окисление [1]. Поэтому поиск и разработка новых эффективных антиоксидантных средств, обладающих комплексным действием, а также выявление и конкретизация свойств антиоксидантов у лекарственных веществ других фармакологических групп сохраняет актуальность [4, 5].
Исследуемое в рамках настоящей работы вещество, 11-дезоксимизопростол – этиловый эфир (±)-11,15-дидезокси-16-метил-16-гидро-ксипростагландина E1 (11-дезоксимизопростол, 11-ДМП) рассматривается как перспективное лекарственное средство с широким спектром фармакологической активности, обладающее свойствами антиоксиданта [2, 3]. Скрининг биологически активных веществ, согласно современным представлениям, является обязательным этапом при изучении антиоксидантной активности веществ. Механизм про- или антиоксидантного действия, реализуемый (или доминирующий) в конкретной ситуации, зависит от условий реакции и определяет суммарную выраженность про- и антиоксидантной активности in vivo. Поэтому для адекватного планирования эксперимента по изучению про- и антиоксидантной активности вещества in vivo и in vitro и трактовки его результатов необходимо располагать данными по квантовохимическому прогнозированию антирадикаль-ной активности [5, 8].
ЦЕЛЬ РАБОТЫ
Оценка возможности проявления антиоксидантных свойств 11-дезоксимизопростола путем квантово-химических расчетов структуры вещества и его радикальных производных.
МЕТОДИКА ИССЛЕДОВАНИЯ
Проведены квантово-химические расчеты структуры 11-ДМП и его радикальных производных с неспаренным электроном у атомов углерода в 12 и 15 положениях. В качестве структуры сравнения был выбран метиловый эфир линолевой кислоты (МЛ). Для структуры сравнения и её радикального производного с неспаренным электроном в 11-м положении углеродного скелета были проведены такие же квантово-химические расчеты с использованием программного обеспечения HyperChem Pro 6 (Hypercube Inc., США) [9]. Величины энергии связывания, значения порядков связей и зарядов на атомах рассчитывались как для изолированной частицы, находящейся в вакууме по-луэмпирическим методом AM1 (Austin Model 1) в модификации PM3. Этот же метод был использован для «оптимизации геометрии» структур по алгоритму Полака-Рибера [4].
Критерием оценки стабильности сравниваемых радикальных частиц являлась разность суммарной энергии связей частицы, образовавшейся при гомолитическом разрыве связи C-H (в рассмотренных структурах тетраэдрический углерод) и суммарной энергии связей той же радикальной частицы в режиме «оптимизации геометрии» (тригональный углерод). Дополнительным критерием оценки стабильности радикальных частиц взяты значения «порядков связей», образованных атомом углерода с неспаренным электроном и соседними атомами, орбитали которых перекрываются с p-орбиталью данного атома углерода, что служит характеристикой делокализации электронной плотности [4].
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Структура сравнения, метиловый эфир линолевой кислоты (МЛ) – соединение близкое по структуре исследуемому веществу (11-ДМП), липидные производные которой подвержены процессам свободнорадикального окисления [10] в живых системах (рис. 1).
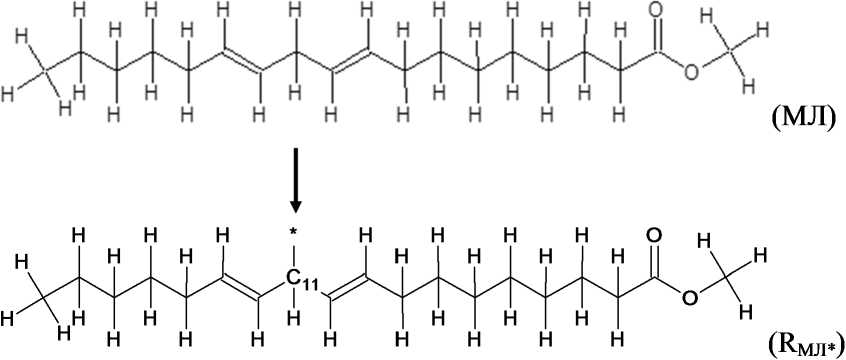
Рис. 1. Структура сравнения – метиловый эфир линолевой кислоты и его радикал
Для 11-дезоксимизопростола наиболее вероятными свободнорадикальными частицами представляются радикалы, образующиеся при гомолитическом разрыве связи C-H у 12-го или
15-го атомов углеродного скелета, соседних кратной связи атомов 13 и 14, поскольку это даёт возможность делокализации электронной плотности в π-системе трёх атомов (12, 13, 14)
или, соответственно, (13, 14, 15) и повышению устойчивости такого радикала (рис. 2).
Расчетные данные энергии связывания Е св для частиц RМЛ*, RДОМП12* и RДОМП15* составили соответственно: –21688,47 кДж/моль, –
25617,35 кДж/моль и –25601,96 кДж/моль. «Оптимизация геометрии» вышеприведённых радикальных частиц привела к изменению конфигурации атомов углерода с неспаренным электроном.
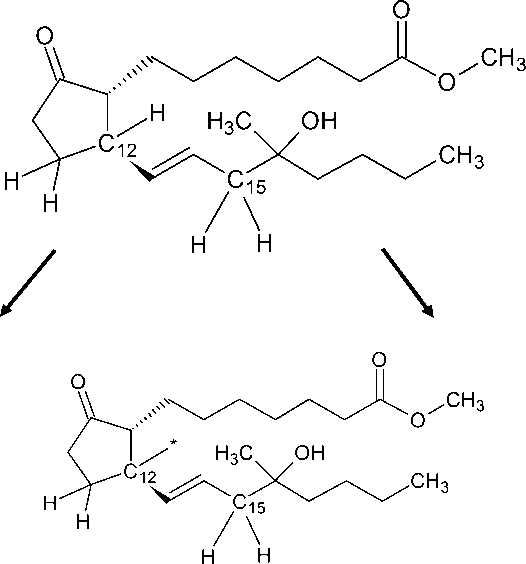
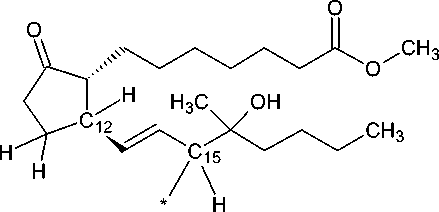
(R Д ОМП 12*) (R Д ОМП 15*)
Рис. 2. Радикалы, образующиеся при гомолитическом разрыве связи C-H у 12-го или 15-го атомов углеродного скелета 11-ДМП
Они приобрели тригональное строение и образовали планарные фрагменты:
-
- для RМЛ* (атомы С9, С10, С11, С12, С13);
-
- для RДОМП12* (атомы С12, С13, С14);
-
- для RДОМП15* (атомы С13, С14, С15).
Соответственно, Е св для этих радикальных частиц с планарными фрагментами R’МЛ*, R’ДОМП12* и R’ДОМП15* составили: – 21776,69 кДж/моль, –25711,10 кДж/моль и – 25691,46 кДж/моль. «Выигрыш» энергии вследствие делокализации электронной плотности составил соответственно: –88,22 кДж/моль, – 93,75 кДж/моль и –89,50 кДж/моль.
Порядки связи для R’ДОМП12* С12–С13 составили 1,34 и связи С13–С14 соответственно 1,41, а для R’ДОМП15* связь С13–С14 – 1,37 и С14–С15 – 1,40, что характеризует эти системы как достаточно высоко делокализованные. В радикале R’ДОМП12* частичные заряды на атомах составили: С12 δ = –0,145, С13 δ = –0,100 и C14 δ = –0,144, в радикале R’ДОМП15* частичные заряды на атомах также имеют близкие значения: С13 δ = –0,145, С14 δ = –0,112 и C15 δ = –0,139.
Сравнивая значения Е св частиц RМЛ*, RДОМП12*, RДОМП15* и R’МЛ*, R’ДОМП12*,
R’ДОМП15*, следует считать более предпочтительной, более устойчивой структурой радикал R’ДОМП12* и в сравнении с альтернативной структурой R’ДОМП15*, и в сравнении с типичными радикалами, такими как R’МЛ* – производными высших ненасыщенных жирных кислот (ВНЖК), входящих в состав липидов.
Исходя из полученных данных, представляется вполне вероятным, что 11-дезоксимизопростол может потенциально служить антиоксидантом прямого действия, способным образовывать более устойчивые и менее реакционноспособные радикалы, чем радикалы – производные ВНЖК, участвующие в цепных процессах свободнорадикального окисления в живых системах.
Кроме того, структура 11-дезоксимизопростола располагает двумя достаточно массивными углеродными цепочечными фрагментами, которые в реальных условиях могут создавать стерические препятствия для взаимодействия возможного радикала R’ДОМП12* и тем самым замедлять цепные процессы свободнорадикального окисления, а полярные группы -OH и карбонильные группы могут образовывать дополнительные водородные связи с молекулами воды и другими полярными биогенными молекулами, что может дополнительно стабилизировать данную радикальную частицу.
ЗАКЛЮЧЕНИЕ
Таким образом, квантово-механические расчёты подтверждают исходную гипотезу о возможности проявления у 11-ДМП свойств антиоксиданта прямого действия, что дает дополнительные основания для изучения и детализации антирадикальной и антиоксидантной активности 11-ДМП in vitro и in vivo .
Список литературы Квантово-химическое прогнозирование антирадикальной активности 11-дезоксимизопростола
- Дубинина, Е. Е. Продукты метаболизма кислорода в функциональной активности клеток (жизнь и смерть, созидание и разрушение). Физиологические и клинико-биохимические аспекты / Е. Е. Дубинина - Санкт-Петербург: Медицинская пресса, 2006. - 397 с. - Текст: непосредственный.
- Исследование фармакокинетических свойств 11-дезоксимизопростола при внутрижелудочном введении - Текст: непосредственный / Р. М. Катаева, Э. Ф. Аглетдинов, К. В. Булыгин [и др.]. // Сеченовский вестник. - 2019. - Т. 10, № 1. - С. 22 - 28.
- Катаева, Р. М. Влияние 11-дезоксимизопростола на перекисное окисление липидов и окислительную модификацию белков плазмы крови - Текст: непосредственный / Р. М. Катаева // Медицинский вестник Башкортостана. - 2015. - Т. 10, № 6. - С. 41 - 44.
- Мартусевич, А. К. Антиоксидантная терапия: современное состояние, возможности и перспективы. - Текст: непосредственный / А. К. Мартусевич, К. А. Карузин, А. С. Самойлов // Биорадикалы и антиоксиданты. - 2018. - Т. 5, № 1. - C. 5 - 23.
- Минкин, В. И. Теория строения молекул / В. И. Минкин, Б. Я. Симкин, Р. М. Миняев. - Ростов-на-Дону: Феникс, 1997. - 560 с. - Текст: непосредственный.
- Прайер У. Свободные радикалы. - М.: Атомиздат, 1970. - 335 с. Текст: непосредственный.
- Руководство по проведению доклинических исследований лекарственных средств / А. Н. Миронов, Н. Д. Бунятян, А. Н. Васильев [и др.]. - М.: Гриф и К, 2012. - 944 с. - Текст: непосредственный.
- Тринеева, О. В. Методы определения антиоксидантной активности объектов растительного и синтетического происхождения в фармации (Обзор) - Текст: непосредственный / О. В. Тринеева // Разработка и регистрация лекарственных средств. - 2017. - № 4. - С. 180 - 197.
- Laxmi, D. HyperChem 6.03. - Direct text / D. Laxmi, S. Priyadarshy // Biotech. Software Internet Report: The Computer Software Journal for Scientists. - 2002. - Vol. 3, № 1. - P. 5 - 9.
- Umeno, A. Involvement of free radical-mediated oxidation in the pathogenesis of pseudoexfoliation syndrome detected based on specific hydroxylinoleate isomers. - Direct text / A. Umeno // Free Radic. Biol. Med. - 2020. - Vol. 147. - P. 61 - 68.


