Лабораторная диагностика хромосомной патологии в Мурманске и Мурманской области (2006-2011 годы)
Автор: Перетрухина Инга Владимировна, Казеева Диана Олеговна
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Статья в выпуске: 4 т.16, 2013 года.
Бесплатный доступ
Определѐн оптимальный метод хромосомного анализа клеток ворсин хориона (плаценты) в диагностике хромосомных врождѐнных и наследственных болезней. Отмечается, что в комплекс обследований, способствующих повышению эффективности пренатальной диагностики, необходимо ввести обязательное медико-генетическое консультирование. На базе статистических данных выявлено максимальное значение хромосомных нарушений, составляющее 8,3 % в 2011 г., а также их общий процент (3,8 %) за последние шесть лет. Наблюдается рост полиморфизмов (1,03 %) и структурных перестроек – транслокации (0,5 %). Установлено, что хромосомных патологий выявляется на 5,1 % больше в пренатальном периоде, чем в постнатальном, что доказывает важность профилактики хромосомных заболеваний и своевременность медико-генетического консультирования.
Лимфоциты, клетки амниотической жидкости, клетки плаценты, цитогенетическая диагностика хромосомных аномалий, группа риска, кариотип, хромосомный препарат, статистика наследственных заболеваний
Короткий адрес: https://sciup.org/14294648
IDR: 14294648
Текст научной статьи Лабораторная диагностика хромосомной патологии в Мурманске и Мурманской области (2006-2011 годы)
-
1. Введение
Известно, что практически все хромосомные синдромы у детей сопровождаются теми или иными нервно-психическими нарушениями, представленными при их описании в виде признаков, называемых задержкой психомоторного, умственного и физического развития. Этими признаками характеризуются хромосомные заболевания, связанные с аномалиями аутосом, реже – гоносом или половых хромосом ( Ворсанова и др. , 1999).
За последние десятилетия существенно изменилась структура детской заболеваемости и смертности. Уменьшилось число инфекционных и алиментарных заболеваний. Однако на фоне увеличения количества вредных факторов в окружающей человека среде растёт удельный вес хромосомных заболеваний, сопровождающихся врождёнными пороками развития (ВПР) и умственной отсталостью и не имеющих методов лечения. Такие заболевания тяжёлым бременем ложатся на семью и общество ( Побединская , 2008).
Очевидна необходимость перехода от использования сложнейших и очень дорогих технологий, направленных на продолжение жизни зачастую безнадёжных больных, к другим технологиям превентивной медицины – методам пренатальной диагностики врождённых и наследственных болезней, расширению программ массового и селективного скрининга.
Целью настоящей работы явилось определение эффективности пренатальной диагностики хромосомных аномалий у плода и цитогенетических исследований, необходимых для своевременного выявления хромосомной патологии.
Для реализации данной цели были поставлены следующие задачи:
-
1. Сравнить и выявить оптимальные методы прогнозирования и диагностики хромосомных врождённых и наследственных болезней.
-
2. Определить факторы, способствующие повышению эффективности пренатальной диагностики.
-
3. Провести цитогенетическую диагностику хромосомных аномалий у беременных женщин, супружеских пар и детей.
-
4. Обработать статистические данные хромосомных патологий в городе Мурманске и Мурманской области за 2006-2011 гг., предоставленные цитогенетическим отделом Мурманского областного диагностического центра (МДЦ).
-
5. Выявить динамику хромосомных патологий за последние шесть лет в Мурманске и Мурманской области.
-
2. Материалы и методы
-
3. Результаты и обсуждение
Исследования проводились в лаборатории диагностики наследственных заболеваний медикогенетического отдела (МГО) МДЦ г. Мурманска по стандартным методикам, разработанным в лаборатории пренатальной диагностики врождённых и наследственных заболеваний человека ( ГУ НИИ АГ им. Д.О. Отта СЗО РАМН ).
Для постановки культуры лимфоцитов применяли микрометод с использованием цельной периферической крови (в отличие от макрометода, при котором применяется плазма крови) и инвазивный метод, объектом исследования которого являются клетки амниотической жидкости и клетки ворсинчатого хориона (плаценты).
В ходе работы также была проанализирована статистика хромосомных заболеваний населения г. Мурманска и Мурманской области за период с 2006 по 2011 гг., предоставленная цитогенетическим отделом МДЦ.
Определение оптимального цитогенетического метода пренатальной диагностики
Основными критериями отбора метода выбраны эффективность, продолжительность и экономичность (табл. 1) ( Баранов и др. , 2009).
Таблица 1. Особенности цитогенетического анализа клеток различного происхождения
|
Метод |
Эффективность |
Длительность культивирования |
Экономичность |
|
Клетки амниотической жидкости |
Высокая вероятность контаминации материнскими клетками (0,16 %) |
14-21 день |
Высокая стоимость питательных сред и оборудования |
|
Клетки ворсин хориона (плаценты), прямой и полупрямой методы |
Отсутствие контаминации материнскими клетками (0,4 %) |
3-4 дня (полупрямой) 2-3 дня (прямой) |
Экономичность |
|
Лимфоциты пуповинной крови |
Возможность контаминации материнскими клетками |
7-10 дней |
Экономичность |
Для хромосомного анализа клеток ворсин хориона (плаценты) используют метод (табл. 1) длительного культивирования (основным недостатком является длительность культивирования) и прямой метод, позволяющий получать препараты, удовлетворяющие всем критериям кариотипирования.
При наличии пороков развития у плода, а также в случае хромосомного мозаицизма в плаценте рекомендуется применять метод исследования лимфоцитов пуповинной крови плода (кордоцентез), который даёт наиболее адекватное представление о хромосомном статусе плода.
Таким образом, оптимальным методом пренатальной диагностики хромосомной патологии является прямой метод.
Цитогенетическая диагностика хромосомных аномалий у беременных женщин и супружеских пар
В цитогенетической лаборатории МДЦ г. Мурманска консультацию генетика получают все женщины, планирующие беременность, но особенно важно её получить парам, относящимся к так называемой "группе риска".
"Группой риска" считается пара в следующих случаях:
-
1) оба партнёра являются носителями генетических заболеваний;
-
2) у одного из партнёров обнаружен врождённый порок;
-
3) наличие инбридинга;
-
4) возраст матери больше 35 лет, а отца – старше 50 лет;
-
5) наличие в роду наследственных заболеваний;
-
6) самопроизвольное патологическое прерывание беременности;
-
7) партнёры живут в экологически неблагоприятном районе или работают на вредном производстве.
С целью определения кариотипа, соответствующего норме, исследованы хромосомные препараты (8 пробирок с различным материалом) пациентов МДЦ, отнесённых к категории "группа риска":
-
1) 5 пробирок c образцами периферической крови из вены (3 мл);
-
2) 1 пробирка c образцом ворсин хориона (инвазивная диагностика – хорионбиопсия);
-
3) 1 пробирка c образцом ткани плаценты (инвазивная диагностика – плацентоцентез);
-
4) 1 пробирка c образцом крови плода (инвазивная диагностика – кордоцентез).
Оценены качество и пригодность препаратов для анализа хромосом, осуществлён отбор метафазных пластинок для изучения индивидуальных хромосом, оценено общее количество хромосом в наборе в целом и в группах хромосом.
Анализ с помощью специальной компьютерной программы (видеотест-Карио) помог определиться в окончательной оценке состава набора по числу хромосом в каждой метафазной пластинке. Проведена оценка распределения этого числа в проанализированной выборке клеток. Осуществлена индивидуальная идентификация хромосом, в том числе и расшифровка типов численных нарушений и вариантов структурных перестроек.
После постановки клеточных культур, приготовления хромосомных препаратов, окраски и последующего анализа препаратов под микроскопом, был проведён анализ хромосом с раскладкой кариотипа по фотоотпечаткам метафазных пластинок (табл. 2).
Таблица 2. Результаты цитогенетического исследования
|
№ пациента |
Пол |
Кариотип |
Расшифровка |
Диагноз |
|
1. |
жен. |
46Xiso(X)(q10) [15]/45X[5] (15 метафаз-ных пластинок из 20) |
iso(X)(q10) – структурный дефект Х-хромосомы: изо-Х-хромосома по длинному плечу (q10) |
синдром Шерешевского – Тернера, мозаицизм по изохромосоме (изоХ) |
|
2. |
муж. |
46XY |
кариотип мужской нормальный |
|
|
3. |
муж. |
46XY |
кариотип мужской нормальный |
|
|
4. |
жен. |
46XXinv 9 |
инверсия хромосомы 9 (inv 9) |
сбалансированная хромосомная перестройка. Вариант нормы. Риск повторной неразвивающейся беременности – не менее 25 %, риск дефектов развития будущего плода – 9 %. Во время беременности рекомендуется сделать пренатальную диагностику кариотипа плода путём биопсии хориона или амниоцентеза |
|
5. |
муж. |
46XY21ps+ |
наличие увеличенных спутников коротких плеч 21 хромосомы |
кариотип мужской нормальный |
|
6. |
жен. |
45XXrob (15;21) |
Робертсоновская транслокация |
кариотип женский несбалансированный |
|
7. |
муж. |
46XY |
кариотип мужской нормальный |
|
|
8. |
жен. |
46XX |
кариотип женский нормальный |
Анализ статистических данных хромосомных патологий
Сотрудниками цитогенетической лаборатории ведётся регистрация протоколов исследований препаратов, а при обнаружении какой-либо патологии исследуемый образец остаётся в архиве хромосомных препаратов.
В результате обработки статистических данных за период 2006-2011 гг. удалось установить процент выявленных хромосомных патологий в Мурманске и Мурманской области, он составляет 3,38 % (рис. 1). Можно сделать вывод не только о значимости медико-генетического консультирования и диагностики, но и об усовершенствовании техники, подборке оптимальных методик, позволяющих максимально точно сформировать группы риска и повысить эффективность пренатальной диагностики. Немаловажную роль играет высокий профессионализм и квалификация медицинского персонала.
Стоит отметить, что общий уровень исследованных анализов на кариотип включает в себя только тех пациентов, которые добровольно наблюдались в Мурманском медико-диагностическом центре за период с 2006 по 2011 гг.
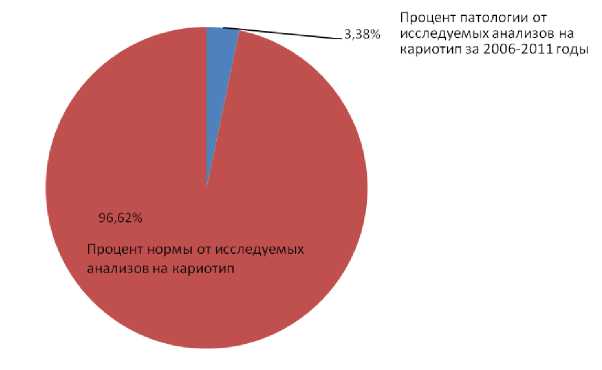
Рис. 1. Процент патологии, выявленной за 2006-2011 гг.
В 2006-2010 гг. наблюдался небольшой рост хромосомных аномалий, в среднем оставаясь стабильным. Однако в 2011 г. процент хромосомных патологий достиг максимума и составил 8,3 % (рис. 2), несмотря на резкое снижение количества направленных пациентов по сравнению с предыдущими годами. Из литературных источников известно ( Побединская, 2008), что рост патологий могут спровоцировать внешние факторы, такие как ухудшение экологической обстановки, наркомания, курение, алкоголь.
До 2010 г. процент выявленных патологий составлял около 5 % от направленных на исследование пациентов (рис. 2). В 2011 г. эта разница оказалась минимальной, что указывает на крайнюю важность предварительной диагностики. К этому периоду пациенты, направляемые на исследование, проходили комплексное обследование (включающее в себя медико-генетическое консультирование, УЗИ плода, биохимический скрининг), это позволило сформировать группы риска, тем самым обеспечив более точное диагностирование хромосомных патологий.
Процент исследованных анализов от
общего числа пациентов за 2006-2011 годы (431S человек)
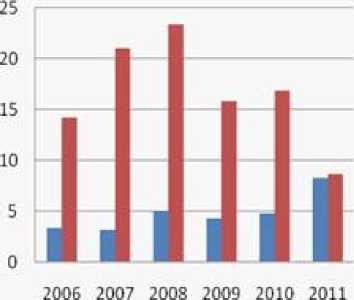
■ Процент выявленных патологий
■ Всего иссл, анализов на кариотип(%)
Рис. 2. Динамика хромосомных болезней за период с 2006 по 2011 гг.
Наиболее часто встречающиеся хромосомные болезни в Мурманске и Мурманской области за последние шесть лет: синдром Дауна, синдром Шерешевского – Тернера (рис. 3).
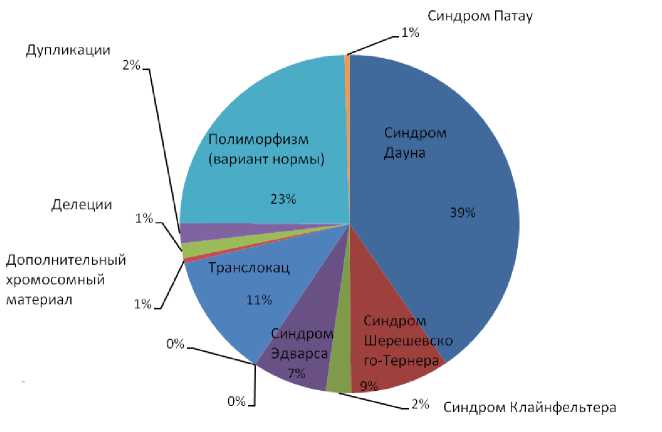
Рис. 3. Статистика наиболее часто встречаемых хромосомных болезней за 2006-2011 гг.
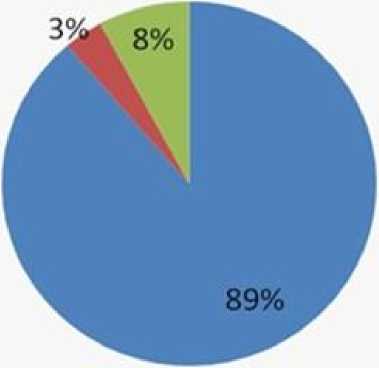
Процент хромосомных отклонений
(4.5%-выявленные патологии от общего количества пациентов)
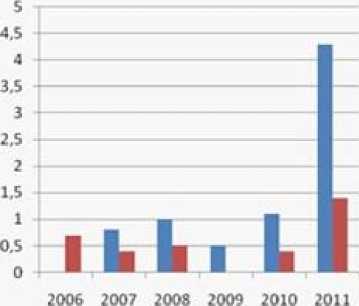
■ Полнморфюм (Мриднт нормы), %
■ tpj»C ЛОКАЦИИ, %
Рис. 4. Динамика хромосомных аномалий за 2006-2011 гг.
-
■Всего исс.
анализов на кариотип
-
■ Процент выявленной патологии у будущих родителей и тех, в чьих семьях имеются больные
-
4. Выводы
-
1. Оптимальным методом пренатальной диагностики хромосомной патологии является прямой метод.
-
2. Комплексное обследование беременных пациенток, включающее в себя УЗИ, биохимический скрининг плода, медико-генетическое консультирование, позволяет сформировать группы риска и повысить эффективность пренатальной диагностики.
-
3. Процент хромосомных патологий в Мурманске и Мурманской области за последние шесть лет составляет 3,8 %, максимальное значение зафиксировано в 2011 г. (8,3 %).
-
4. Отмечается рост полиморфизмов (1,3 %) и структурных перестроек – транслокации (0,5 %). Количество остальных хромосомных заболеваний остаётся стабильным из года в год.
-
5. Хромосомных патологий выявляется больше на 5,1 % на стадии эмбрионального развития, чем на стадии медико-генетического консультирования.
-
Процент патологии у развивающихся плодов
Рис. 5. Соотношение хромосомных патологий, выявленных на стадии пренатального и постнатального периода
Невозможно не отметить рост полиморфизмов (1,03 %) и структурных перестроек – транслокации (0,5 %). Количество остальных хромосомных заболеваний практически не увеличивается.
Хромосомные патологии выявляются больше на 5,1 % в пренатальном периоде, чем в постнатальном периоде (рис. 5). Это в очередной раз указывает на важность профилактики наследственных заболеваний и своевременного медико-генетического консультирования.
Таким образом, остро встаёт вопрос о профилактике наследственных заболеваний и своевременном медико-генетическом консультировании. Серьёзное отношение супругов к рождению ребёнка наряду с общегосударственными программами по охране окружающей среды и совершенствованию здравоохранения будут способствовать уменьшению груза наследственных и врождённых патологий.


