Лапароскопические технологии в лечении наружных панкреатических свищей после дренирования кист
Автор: Праздников Э.Н., Шевченко В.П., Баранов Г.А., Хоптяр М.С., Налетов В.В., Зинатулин Д.Р., Умяров Р.Х.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 3 (81), 2022 года.
Бесплатный доступ
Введение. Неуклонно растет количество пациентов с острым и хроническим панкреатитом. Средний возраст больных с панкреатитом в настоящее время составляет 39 лет. До 15 % возрос процент инвалидизации больных с данной патологией. Одним из вариантов осложнений у пациентов с хроничеcким панкреатитом является развитие постнекротических кист поджелудочной железы. Цель исследования. Улучшить результаты хирургического лечения больных панкреатитом, осложненного развитием постнекротических кист поджелудочной железы различной локализации, посредством применения лапароскопической миниинвазивной цистогастростомии. Материалы и методы. В статье проанализированы результаты хирургического лечения 27 больных с постнекротическими кистами поджелудочной железы различной локализации, которым было выполнено оперативное вмешательство в объеме лапароскопической миниинвазивной цистогастростомии. Результаты. Представленный метод хирургического лечения больных с постнекротическими кистами поджелудочной железы оказался эффективен у 25 больных, у одного больного был отмечен рецидив. У одного больного не представилось возможным оценить результаты лечения в связи с летальным исходом. Заключение. Лапароскопическая миниинвазивная цистогастростомия является альтернативным вариантом хирургического лечения больных с постнекротическими кистами поджелудочной железы различной локализации, для которых другие варианты миниинвазивных и резекционных операций нежелательны или невозможны по каким-либо топографо-анатомическим особенностям больного.
Панкреатит, постнекротическая киста поджелудочной железы, лапароскопическая цистогастростомия, наружное дренирование
Короткий адрес: https://sciup.org/142236577
IDR: 142236577 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2022-3-50-60
Laparoscopic technologies in the treatment of external pancreatic fistulas after cyst drainage
Introduction. The number of patients with acute and chronic pancreatitis is steadily growing. The average age of patients with pancreatitis is currently 39 years. The percentage of disability in patients with this pathology has increased to 15 %. One of the options for complications in patients with chronic pancreatitis is the development of postnecrotic pancreatic cysts. The purpose of the study. To improve the results of surgical treatment of patients with pancreatitis, complicated by the development of postnecrotic pancreatic cysts of various localization, through the use of laparoscopic minimally invasive cystogastrostomy. Materials and methods. The article analyzes the results of surgical treatment of 27 patients with postnecrotic pancreatic cysts of various localization, who underwent surgery in the scope of laparoscopic minimally invasive cystogastrostomy. Treatment results. The presented method of surgical treatment of patients with postnecrotic pancreatic cysts was effective in 25 patients, one patient had a relapse. In one patient, it was not possible to evaluate the results of treatment due to a lethal outcome. Conclusion. Laparoscopic minimally invasive cystogastrostomy is an alternative surgical treatment option for patients with postnecrotic pancreatic cysts of various localization, for whom other options for minimally invasive and resection operations are undesirable or impossible due to some topographic and anatomical features of the patient.
Текст научной статьи Лапароскопические технологии в лечении наружных панкреатических свищей после дренирования кист
Во всем мире отмечается неуклонный рост больных с острым и хроническим панкреатитом. Средний возраст пациентов с данной патологией снизился до 39 лет, а процент инвалидизации достигает 15% [1–7]. Общемировая заболеваемость острым панкреатитом достигает 4,6–100 случаев на 100 тыс. населения в год, хроническим панкреатитом – от 2 до 200 на 100 тыс. населения в год [8–12].
Течение хронического панкреатита сопровождается развитием осложнений (кровотечения из верхних отделов ЖКТ; нарушения эвакуационной функции по двенадцатиперстной кишке, обусловленные компрессией извне воспалительным инфильтратом/кистой поджелудочной железы; билиарная гипертензия с возможным развитием механической желтухи, вследствие нарушения проходимости общего желчного протока (стриктура терминального отдела холедоха); тромбоз портальной и селезеночной вен; образование ложных интрапанкреатических или перипан-креатических кист), которые зачастую могут приводить к летальным исходам [13, 14].
Развитие постнекротических кист поджелудочной железы различной локализации является одним из наиболее частых проявлений хронического панкреатита.
Основными видами хирургического лечения постнекротических кист поджелудочной железы в настоящее время являются: дренирующие и резекционные методы лечения.
Одним из методов хирургического лечения постнекротических кист поджелудочной железы является наружное дренирование кист поджелудочной железы (пункция кисты поджелудочной железы, марсупиализация, наружное чрескожное миниинва-зивное дренирование под контролем УЗИ и МСКТ, наружное дренирование лапаротомным доступом). Наружное дренирование может являться окончательным методом хирургичеcкого лечения, когда вследствие дренирования кистозных образований поджелудочной железы происходит спадение стенок кисты с полным нивелированием жалоб и клинической картины, а также отсутствием рецидива при динамическом наблюдении. Однако у большинства больных метод наружного дренирования кист поджелудочной железы является паллиативным методом лечения, целью которого является декомпрессия и диагностика генеза кисты поджелудочной железы.
Альтернативный метод хирургического лечения постнекротических кист поджелудочной железы – внутреннее дренирование кист поджелудочной железы (формирование цистогастроа-настомоза, цистодуоденоанастомоза, цистоеюноанастомоза). Формирование анастомозов возможно миниинвазивным (чрескожным и/или эндоскопическим) и лапаротомным доступом.
К резекционным методам хирургического лечения постнекротических кист поджелудочной железы относятся корпорокаудальная резекция поджелудочной железы при расположении кист в хвосте поджелудочной железы, операции Бергера и панкреатодуоденальная резекция (ПДР) или операция Whipple, при расположении кисты в головке поджелудочной железы [15]. В послеоперационном периоде частота осложнений после хирургического лечения постнекротических кист поджелудочной железы варьируется в диапазоне от 5,5 % до 40 %, летальность – от 2,5 % до 30 %.
Все вышесказанное требует разработки и введения в клиническую практику новых безопасных, эффективных и минимально инвазивных методов хирургического лечения больных с постнекротическими кистами поджелудочной железы различной локализации.
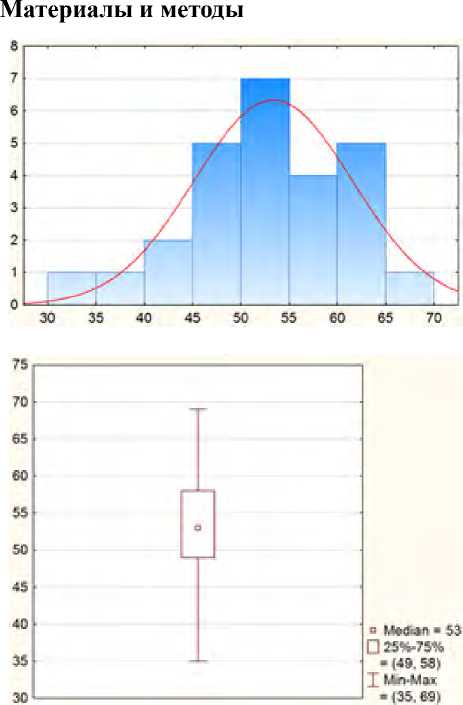
Рис. 1. Распределение больных по возрасту (возраст в годах)
Fig. 1. Distribution of patients by age (age in years)
Лапароскопическая миниинвазивная цистогастросто-мия была выполнена 27 больным с симптоматическими нефиксированными к задней стенке желудка постнекро- тическими кистами поджелудочной железы диаметром более 30 мм, а также с симптоматическими фиксированными к задней стенке желудка постнекротическими кистами поджелудочной железы диаметром более 30 мм, при невозможности безопасно выполнить пункцию кист поджелудочной железы через две стенки желудка. Ограничениями для выполнения лапароскопической мини-инвазивной цистогастростомии являлись размеры кисты менее 30 мм; наличие асцита; онкологические заболевания и резекционные вмешательства верхнего этажа брюшной полости; не поддающаяся медикаментозной коррекции гипокоагуляция.
Возраст пациентов, которым была выполнена лапароскопическая миниинвазивная цистогастростомия, варьировал от 35 до 69 лет, средний составил – 53±8,2 лет, преобладали пациенты в возрасте 49 – 58 лет (риc.1). Среди пациентов превалировали мужчины – 78%.
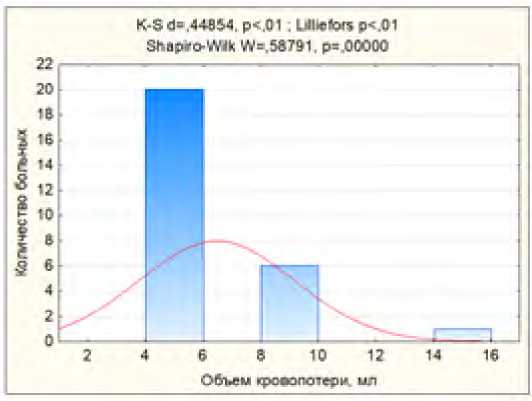
Средний размер постнекротической кисты составлял 70,5±20,5 мм, преобладали кисты с размерами от 52 до 82 мм (рис. 2).
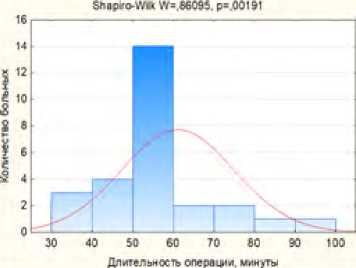
При этом средний период существования кист – 20,5±6,2 месяцев, в диапазоне от 6 до 60 месяцев (рис. 3).
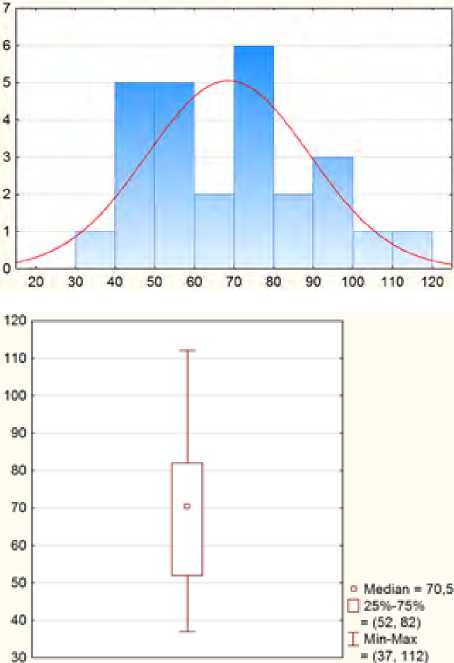
Рис. 2. Распределение больных по размеру кист (мм)
Fig. 2. Distribution of patients by cyst size (mm)
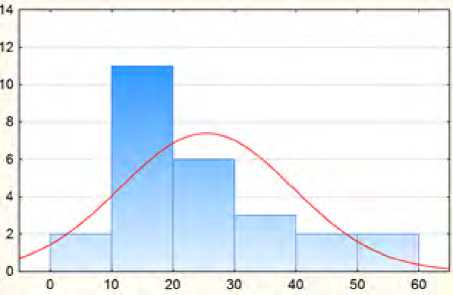
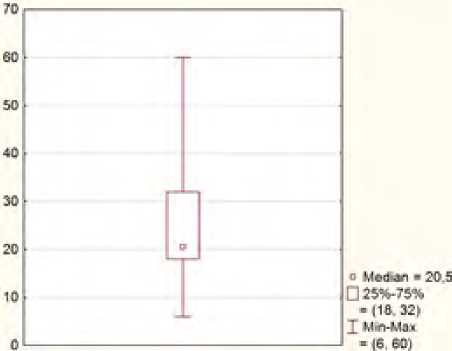
Рис. 3. Длительность существования кист (месяцы)
Fig. 3 . Duration of existence of cysts (months)
Средняя толщина стенки постнекротической кисты составила 5±1,01 мм, превалировал процент пациентов с толщиной стенки от 4 до 5 мм (рис. 4).
Методика выполнения лапароскопической миниин-вазивной цистогастростомии
Хирургическое вмешательство – лапароскопическая миниинвазивная цистогастростомия – выполнялась в 2 этапа: первым этап – чрескожное дренирование двумя дренажами через желудочно-ободочную связку под УЗИ и рентгеновским контролем; второй этап – лапароскопическая миниинвазивная цистогастростомия. Двухэтапность необходима для обеспечения максимальной безопасности пациента и предотвращения осложнений.
Дренирование постнекротической кисты выполнялось под УЗИ и рентгеновским контролем – в положении лежа на спине, в зависимости от топографо-анатомических особенностей локализации кисты, выполнялась пункция кисты поджелудочной железы иглой Chiba Biopsy Needle 18G (1,25 мм). Точка пункции для оптимальной траектории движения пункционной иглы определялась интраоперационно с соблюдений следующих условий: наименьшая длина пункционного канала; отсутствие магистральных сосудов и полых органов по ходу манипуляционного канала; угол выполнения хирургических манипуляций – 45–600. Угол менее 450 увеличивает риск прохождения иглы вдоль стенки постнекротической кисты, угол более 600 приводит к наложению рентгеновских изображений, препятствующих дальнейшим манипуляциям в данной зоне. При успешной канюляции постнекротической кисты отмечается поступление содержимого кисты по пункционной игле. Для оценки размеров и уточнения локализации, состояния стенки постнекротической кисты, проводилось контрастирование водорастворимым контрастным препаратом. Далее устанавливался проводник Лундерквиста с наконечником J-типа в просвет кисты, с последующим бужированием пункционного канала до 10 Fr и установкой по проводнику дренажа Dawson -Mueller диаметром 10,2. Дренаж фиксировался к коже отдельным узловым швом.
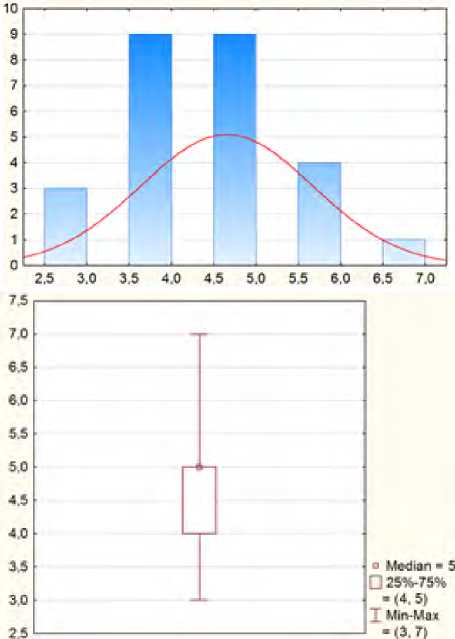
Рис. 4. Распределение больных по толщине стенки кисты (мм) Fig. 4. Distribution of patients by cyst wall thickness (mm)
Точка для установки второго дренажа определялась при двойном контрастировании полости кисты и просвета желудка. Оптимальной точкой для выполнения дренирования является место наиболее приближенное к большой кривизне в области тела желудка. Контрастирование желудка осуществлялось во- дорастворимым контрастом через назогастральный зонд. В выбранной точке через желудочно-ободочную связку по методу Сельдингера под УЗИ и рентгенологическим контролем выполнялась установка дренажа Dawson-Mueller диаметром 10,2 Fr. Дренаж фиксировался к коже отдельным узловым швом.
Второй этап хирургического лечения осуществлялся через 5–7 дней.
Установка первого троакара производилась в верхней пара-умбиликальной области, с последующим созданием карбоксипе-ритонеума. Выполнялась ревизия брюшной полости с оценкой расположения ранее установленных дренажей. Применение ультратановых дренажей позволяет предотвратить поступление содержимого кисты в свободную брюшную полость, и как следствие, предотвращает развитие воспалительных реакций в зоне расположения дренажей. Контрастирование желудка и постнекротической кисты позволяет выбрать оптимальную точку установки дренажа с последующей инвагинацией в просвет желудка (рис. 5).
А
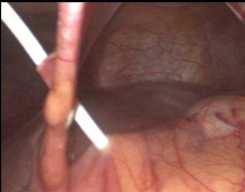
B
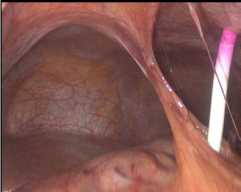
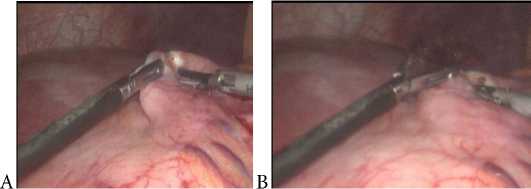
Рис. 5. Эндовидеофото дренажей, установленных через желудочно-ободочную связку в кисту поджелудочной железы: А – страховочный дренаж, В – дренаж, установленный в проекции тела желудка для инвагинации в просвет желудка Fig. 5. Endovideophoto of drains installed through the gastrocolic ligament into the pancreatic cyst: A – safety drain, B – drainage installed in the projection of the body of the stomach for invagination into the lumen of the stomach
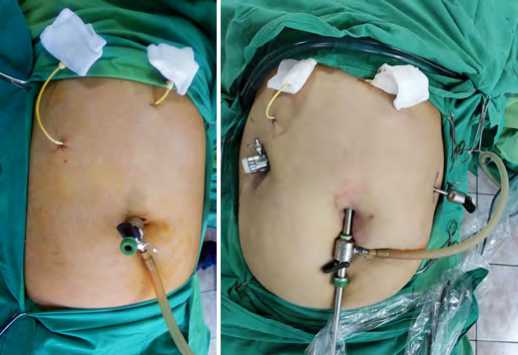
Рис. 6. Установка троакаров для лапароскопического этапа цистогастростомии. Вид передней брюшной стенки
Fig. 6. Installation of trocars for the laparoscopic stage of cystogastrostomy.
View of the anterior abdominal wall
Далее под визуальным контролем устанавливались троакары по передней подмышечной линии справа на 6–8 см ниже реберной дуги и по передней подмышечной линии слева на 6–8 см ниже реберной дуги. Данная расстановка троакаров обеспечивает оптимальный обзор зоны операции и достаточный объем движений лапароскопических манипуляторов для формирования цистогастроанастомоза (рис. 6).
Для формирования анастомоза выполнялась гастротомия, протяженностью 5 мм с применением ультразвукового скальпеля HARMONIC Johnson & Johnson, при этом мобилизация желудка не выполнялась, что сокращает время выполнения операции и объем операционной травмы ( рис . 7).
А
Рис. 7. Эндовидеофото формирования гастротомического отверстия: А – вскрытие просвета желудка ультразвуковым скальпелем Гармоник, В – сформированное гастротомическое отверстие
Fig. 7. Endovideophoto of the formation of the gastrotomy opening: A – opening the lumen of the stomach with an ultrasonic scalpel Harmonik, B – formed gastrotomy opening
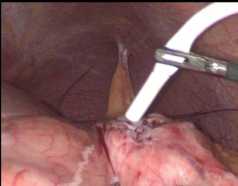
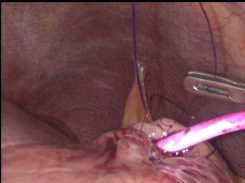
Рис. 8. Формирование миниинвазивного цистогастроанастомоза:
А – эндовидеофото погружения проксимального конца дренажа в просвет желудка, В – эндовидеофото затягивания кисетных швов Fig. 8. Formation of a minimally invasive cystogastroanastomosis: A – endovideophoto of the immersion of the proximal end of the drainage into the lumen of the stomach, B – endovideophoto of tightening purse-string sutures
Проксимальный конец ранее установленного дренажа пересекался на расстоянии 4–5 см от поверхности кожи. Данная длина дренажа является оптимальной для формирования соустья между полостью кисты и просветом желудка. Проксимальный конец дренажа погружался в брюшную полость и выполнялась инвагинации конца дренажа в просвет желудка с фиксацией 3 кисетными швами, наложенными на расстоянии до 5 мм (рис. 8). Далее выполнялась перитонизация дренажа на всем протяжении (рис. 9). Применение 3 кисетных швов с инвагинацией предыдущего шва в просвет желудка позволяет обеспечить максимальную герметичность анастомоза, а также предотвращает регургитацию желудочного содержимого в полость кисты, вследствие формирования муфты вокруг установленного дренажа.
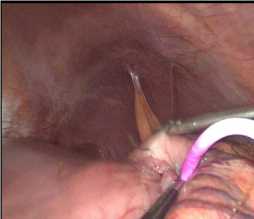
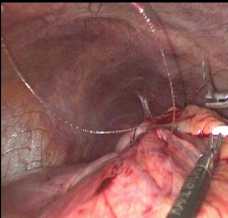
В
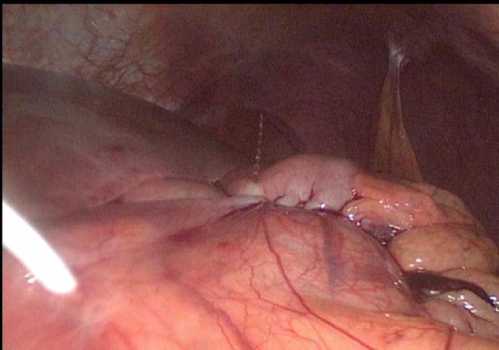
Рис. 9. Эндовидеофото перитонизации дренажной трубки
Fig. 9. Endovideophoto of drainage tube peritonization
Через 24–48 часов выполнялось контрастирование полости кисты водорастворимым контрастным препаратом для оценки функционального состояния ранее сформированного анастомоза (рис. 10).
Представленная на рисунке 10 рентгенограмма демонстрирует адекватно функционирующий сформированный анастомоз без признаков экстравазации и нарушения эвакуации содержимого постнекротической кисты в просвет желудка.
После проведения рентгенографии, при отсутствии признаков несостоятельности и при своевременной эвакуации по сформированному анастомозу, контрольный дренаж удалялся.
Контроль за функционированием сформированного анастомоза осуществлялся через 1 месяц после хирургической лечения посредством выполнения УЗ-исследования и оценки остаточной полости постнекротической кисты.
Удаление дренажа из сформированного анастомоза производилась эндоскопическим методом через 12–18 месяцев.
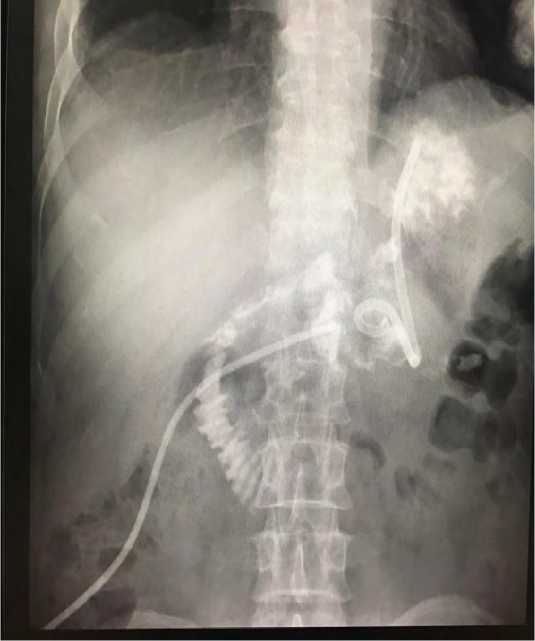
Рис. 10. Контрольная рентгенограмма через 48 часов у больного после выполнения лапароскопической миниинвазивной цистогастростомии Fig. 10. Control radiograph 48 hours later in a patient after laparoscopic minimally invasive cystogastrostomy
Результаты
При анализе хирургического лечения данной группы больных оценивались следующие критерии: длительность хирургического вмешательства, интраоперационная кровопотеря, длительность пребывания в стационаре между первым и вторым этапами хирургического лечения, длительность пребывания в отделении интенсивной терапии и реанимации, а также длительности пребывания в стационаре после второго этапа хирургического лечения.
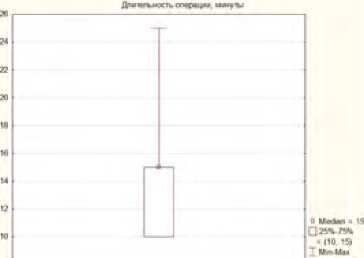
Длительность первого этапа хирургического вмешательства в среднем составляла 14,6±3,65 минут (рис. 11).
Длительность второго этапа оперативного вмешательства в среднем составляла 61,1±13,95 минут (рис. 12).
Средняя интраоперационная кровопотеря во время первого этапа хирургического лечения составляла 6,48 ± 2,7 мл (рис. 13).
Средняя интраоперационная кровопотеря во время второго этапа хирургического лечения составляла 3,2 ± 20,0 мл (рис. 14).
Средняя длительность пребывания больного в стационаре между 1 и 2 этапом хирургического лечения составляла 4,92 ± 0,95 дня (рис. 15).
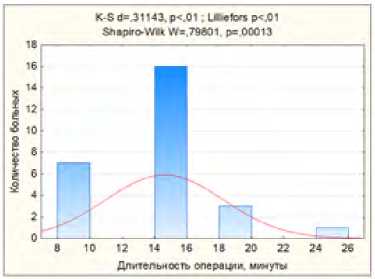
•<м И
Рис. 11. Длительность 1 этапа хирургического лечения
Fig. 11. Duration of the 1st stage of surgical treatment
К-Sd» .30950. р<01; l*elO<.01
-' МЯІЛ • 5 212SVK*
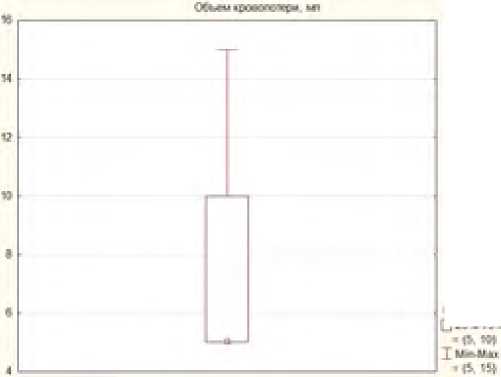
Рис. 13. Интраоперационная кровопотеря во время
1 этапа хирургического лечения
Fig. 13. Intraoperative blood loss during 1 stage surgical treatment
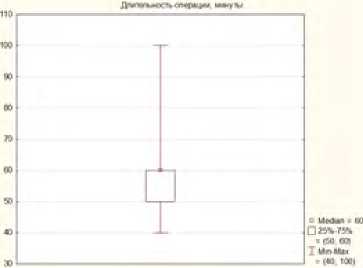
Рис. 12. Длительность 2 этапа хирургического лечения
Fig. 12. Duration of the 2nd stage of surgical treatment
Госпитализации пациентов в отделение интенсивной терапии и реанимации после первого этапа хирургического лечения не потребовалось.
Средняя длительность госпитализации больных в отделение интенсивной терапии и реанимации после второго этапа хирургического лечения составляла 1 сутки. Необходимость госпитализации в отделении интенсивной терапии и реанимации была обусловлена выраженной сопутствующей соматической патологией (рис. 16).
Средняя длительность пребывания больного в стационаре после 2 этапа хирургического лечения составляла 5,77 ± 0,89 дня (рис. 17).
Осложнения, наблюдавшиеся на различных этапах хирургического лечения представлены в табл. 1.
Рис. 14. Интраоперационная кровопотеря во время 2 этапа хирургического лечения Fig. 14. Intraoperative blood loss during stage 2 surgical treatment
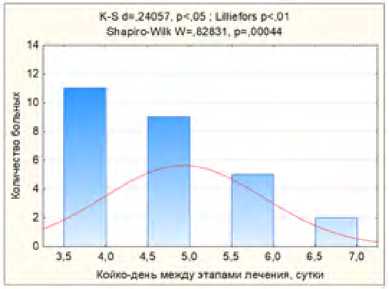

Рис. 15. Длительность пребывания больного в стационаре между 1 и 2 этапом хирургического лечения
Fig. 15. Length of stay of the patient in the hospital between the 1st and 2nd stage of surgical treatment
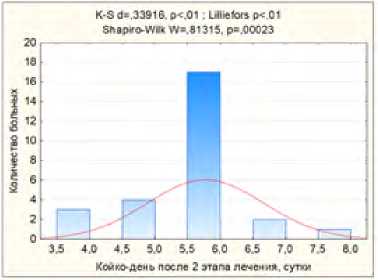

Рис. 17. Длительность пребывания больного в стационаре после 2 этапа хирургического лечения
Fig. 17. Length of stay of the patient in the hospital after stage 2 of surgical treatment
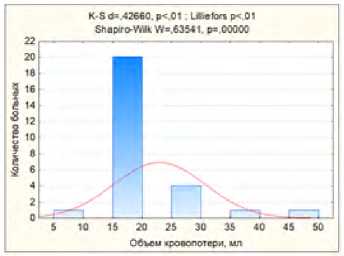
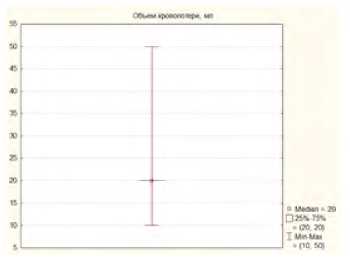
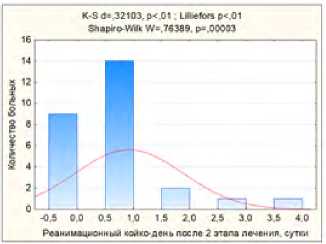
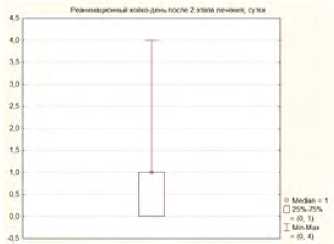
Рис. 16. Длительность госпитализации больных в отделение интенсивной терапии и реанимации после второго этапа хирургического лечения Fig. 16. Duration of hospitalization of patients in the intensive care unit and resuscitation after the second stage of surgical treatment
Таблица 1
Осложнения после хирургического лечения
Table 1
Complications after surgical treatment
|
Осложнения Complications |
Количество больных, человек Number of patients, people |
||||
|
Сlavien-Dindo I |
Сlavien-Dindo II |
Сlavien-Dindo III |
Сlavien-Dindo IV |
Сlavien-Dindo V |
|
|
1 этап хирургического лечения больных 1 stage of surgical treatment of patients |
|||||
|
Острый панкреатит Acute pancreatitis |
0 |
1 |
0 |
0 |
0 |
|
Подкожная гематома Subcutaneous hematoma |
1 |
0 |
0 |
0 |
0 |
|
Всего Total |
1 (3,7%) |
1 (3,7%) |
1 (3,7%) |
0 |
0 |
|
2 этап хирургического лечения больных 2 stage of surgical treatment of patients |
|||||
|
Дисфункция дренажа Drainage dysfunction |
0 |
0 |
1 |
0 |
0 |
|
Синдром по-лиорганной недостаточности Syndrome of multiple organ failure |
0 |
0 |
0 |
0 |
1 |
|
Всего Total |
0 |
0 |
1 (3,7%) |
0 |
1 (3,7%) |
В послеоперационном периоде наблюдался один летальный исход, обусловленный развитием полиорганной недостаточности на фоне хронической экзогенной интоксикации и механической желтухи, вследствие сдавления общего желчного протока постнекротической кистой головки поджелудочной железы.
Эффективность выполненного хирургического лечения оценивалась посредством УЗ-исследования. Исследование выполнялось через 1 и 3 месяца после оперативного вмешательства. При отсутствии гиподенсивных жидкостных образований в проекции ранее выявляемой постнекротической кисты поджелудочной железы, УЗ-картина расценивалась как полная облитерация просвета кисты и адекватно функционирующий цистогастроанастомоз. Далее УЗ-исследование выполнялось через 3 месяца Всем больным в послеоперационном периоде выполнялось ультразвуковое исследование через 1 месяц. Данная методика хирургического лечения больных с постнекротическими кистами поджелудочной железы оказалась эффективна у 25 больных. У одного больного был отмечен рецидив кисты. У одного больного оценить результаты хирургического лечения не представляется возможным ввиду летального исхода.
В случае выявления при УЗ-исследовании признаков рецидива кисты целесообразно выполнение ЭГДС с целью оценки стояния дренажа и пассажа содержимого кисты в просвет желудка. При обнаружении облитерации дренажа целесообразно его удаление. Для контроля динамики изменения размеров постнекротической кисты, пациенту показан УЗ-контроль гепатопанкреатобилиарной зоны через 1 месяц.
При выявлении увеличения размеров постнекротической кисты до 5 см, абсцедировании или компрессии билиарного тракта показано повторное хирургическое лечение. В случае отсутствия динамики или незначительного увеличения размеров больному рекомендовано УЗ-исследование через 3 месяца с последующим контролем раз в год.
Заключение
Предложенный метод является альтернативным вариантом традиционным методам хирургического лечения больных с постнекротическими кистами поджелудочной железы различной локализации. Данная методика обладает всеми преимуществами миниинвазивных вмешательств (минимальная интраоперационная кровопотеря, минимальный реанимационный и послеоперационный койко-день, низкий показатель послеоперационных осложнений, низкая летальность), что позволяет выполнять данный вид лечения как больным с неотягощенным анамнезом, так и больным с сопутствующей соматичеcкой патологией, для которых другие варианты миниинвазивных и резекционных операций нежелательны или невозможны по каким-либо топографо-анатомическим особенностям больного.
Список литературы Лапароскопические технологии в лечении наружных панкреатических свищей после дренирования кист
- Пугаев А. В. Острый панкреатит / А. В. Пугаев, Е. Е. Ачкасов. - М.: ИНФРА-М, 2019. https://doi.org/10.12737/monography_5bac927d4a2f73.37500387
- Dumnicka P., Maduzia D., Ceranowicz P., Olszanecki R., Drozdz R., Kusnierz-Cabala B. The Interplay between Inflammation, Coagulation and Endothelial Injury in the Early Phase of Acute Pancreatitis: Clinical Implications. International Journal of Molecular Sciences, 2017, 18 (2).
- Krishna S. G., Kamboj A. K., Hart P. A., Hinton A., Conwell D. L. The Changing Epidemiology of Acute Pancreatitis Hospitalizations: A Decade of Trends and the Impact of Chronic Pancreatitis. Pancreas, 2017, № 46 (4), рр. 482-488.
- Mandalia A., Wamsteker E. J., Di Magno M. J. Recent advances in understanding and managing acute pancreatitis. F1000 research, 2019, 7.
- Murthy P., Singhi A. D., Ross M. A., Loughran P., Paragomi P., Papachristou G. I., Whitcomb D. C., Zureikat A. H., Lotze M. T., Zeh H. J., Boone B. A. Enhanced Neutrophil Extracellular Trap Formation in Acute Pancreatitis Contributes to Disease Severity and Is Reduced by Chloroquine. Frontiers in immunology, 2019, № 10, рр. 28.
- Pang Y., Kartsonaki C., Turnbull I., Guo Y., Yang L., Bian Z., Chen Y., Millwood I. Y., Bragg F., Gong W., Xu Q., Kang Q., Chen J., Li L., Holmes M. V., Chen Z. Metabolic and lifestyle risk factors for acute pancreatitis in Chinese adults: A prospective cohort study of 0.5 million people. Public Library of Science Medicine, 2018, № 15, рр. 8.
- Shah A., Mourad M., Bramhall S. Acute pancreatitis: current perspectives on diagnosis and management. Journal of inflammation research, 2018, № 11, рр. 77-85.
- Faghih M., Gonzalez F. G., Makary M. A., Singh V. K. Total pancreatectomy for recurrent acute and chronic pancreatitis: a critical review of patient selection criteria. Current opinion in gastroenterology, 2017, № 33 (5), рр. 330-338.
- Rodrigues-Pinto E., Caldeira A., Soares J. B., Antunes T., Carvalho J. R., Costa-Maia J., Oliveira P., Azevedo R., Liberal R., Machado T. B., Magno-Pereira V., Moutinho-Ribeiro P. Clube Português do Pâncreas Recommendations for Chronic Pancreatitis: Etiology, Natural History, and Diagnosis. Portuguese journal of gastroenterology, 2019, № 26 (5), рр. 346-355.
- Zou W. B., Tang X. Y., Zhou D. Z., Qian Y. Y., Hu L. H., Yu F. F., Yu D., Wu H., Deng S. J., Lin J. H., Zhao A. J., Zhao Z. H., Wu H. Y., Zhu J. H., Qian W., Wang L., Xin L., Wang M. J., Wang L. J., Fang X., He L., Masson E., Cooper D. N., Férec C., Li Z. S., Chen J. M., Liao Z. SPINK1, PRSS1, CTRC, and CFTR Genotypes Influence Disease Onset and Clinical Outcomes in Chronic Pancreatitis. Clinical and Translational Gastroenterology, 2018, № 9 (11), рр. 204. https://doi.org/10.1038/s41424-018-0069-5
- Черданцев Д. В. Проблема острого панкреатита в Красноярском крае / Д. В. Черданцев [и др.] // Современные проблемы науки и образования. - 2019. - № 2.
- Zheng Z., Ding Y. X., Qu Y. X., Cao F., Li F. A narrative review of acute pancreatitis and its diagnosis, pathogenetic mechanism, and management. Annals of translational medicine, 2021, № 9 (1), рр. 69. https://doi.org/10.21037/atm-20-4802
- Козлов И. А. Хирургическое лечение осложненного хронического панкреатита / И. А. Козлов, В. А. Вишневский, А. В. Чжао // Высокотехнологическая медицина. - 2017. - № 1. - С. 43-55.
- Праздников Э. Н. Мини-инвазивная чрескожная цистогастростомия в хирургическом лечении постнекротических кист поджелудочной железы / Э. Н. Праздников [и др.] // Хирург. - 2022. - № 1-2. - С. 5-17.
- Zheng Z., Ding Y. X., Qu Y. X., Cao F., Li F. A narrative review of the mechanism of acute pancreatitis and recent advances in its clinical management. American journal of translational research, 2021, № 13 (3), рр. 833-852.


