Лазерная проточная цитометрия в лабораторном иммунологическом мониторинге эндопротезирования коленного и тазобедренного суставов
Автор: Волокитина Елена Александровна, Чепелева Марина Владимировна
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2011 года.
Бесплатный доступ
Представлен впервые разработанный алгоритм обследования больных с остеоартрозом III стадии методом лазерной проточной цитометрии (типирование лимфоцитов периферической крови) на различных этапах эндопротезирования коленного или тазобедренного суставов (до имплантации, через 5-7, 18-21 сутки, 4-7, 10-14, 22-24 месяца после опе- рации). Исследование показателей клеточного иммунитета (CD3+, CD3+CD4+, CD3+CD8+, CD3-CD19+, CD3-CD16+CD56+, CD3+CD16+CD56+, CD3+CD25+, CD3+HLA-DR) в эти сроки позволяет прогнозировать течение послеоперационного периода, а также выявлять больных из группы риска по развитию вялотекущего гнойно-воспалительного процесса в зоне имплан- тации нестабильного искусственного сустава.
Иммунофенотипирование, остеоартроз, эндопротезирование
Короткий адрес: https://sciup.org/142121447
IDR: 142121447 | УДК: 617.581/583-089.819.843-77-073
Laser flowing cytometry in the laboratory immunological monitoring of the knee and the hip endoprosthetics
The work deals with the algorithm developed for the first time and intended for examination of patients with Stage III osteoarthrosis using the method of laser flowing cytometry (typing of peripheral blood lymphocytes) at different stages of the knee or the hip endoprosthetics (before implantation, after 5-7, 18-21 days, 4-7, 10-14, 22-24 months after surgery). The investigation of cellular immunity values (CD3+, CD3+CD4+, CD3+CD8+, CD3-CD19+, CD3-CD16+CD56+, CD3+CD16+CD56+, CD3+CD25+, CD3+HLA-DR) in these periods allows to predict the course of postoperative period, as well as to reveal patients from the group of risk of developing the sluggish pyo-inflammatory process in the zone of instable artificial joint implantation.
Текст научной статьи Лазерная проточная цитометрия в лабораторном иммунологическом мониторинге эндопротезирования коленного и тазобедренного суставов
Несмотря на значительные успехи современной ортопедии, повреждения и заболевания крупных суставов до настоящего времени остаются одной из наиболее значимых проблем медицины и общества. Методом выбора при лечении поздних стадий коксартроза и го-нартроза является эндопротезирование, относящееся к числу высокоэффективных лечебно-реабилитационных технологий. Имплантацией искусственных суставов занимаются сотни клиник и исследовательских центров. В России потребность в эндопротезировании только тазобедренного сустава по предварительным расчетам составляет до 300 000 хирургических вмешательств в год. В то же время, операции по имплантации искусственного сустава по-прежнему относятся к высокой категории сложности и требуют длительной реабилитации. При остеоартрозе крупных суставов существует определенный порочный круг. С одной стороны, стойкий иммунологический дисбаланс способствует дальнейшему развитию дегенеративно-дистрофических изменений в тканях пораженного сустава и поддержанию вторичного синовита, с другой — прогрессирование патологии и нарастание в связи с этим компенсаторных реакций истощают метаболический фон и адаптационные механизмы [4]. Операционная травма способна провоци- ровать патологические иммунные реакции в организме, усугубляя уже имеющиеся нарушения, что, в свою очередь, способствует развитию послеоперационных осложнений, поэтому при подготовке больного к операции необходимо учитывать состояние системы иммунитета [1, 3]. При современном оснащении лабораторий большинства крупных больниц, в которых выполняется эндопротезирование, иммунологическое обследование пациентов вполне осуществимо, а прогностическая значимость полностью оправдывает все расходы и трудозатраты на его проведение [2, 5, 6]. Исследование показателей клеточного иммунитета на различных этапах реабилитационного периода после эндопротезирования крупных суставов позволяет прогнозировать как благоприятное течение послеоперационного периода, так и развитие послеоперационных осложнений [7, 8].
Стрессовое ремоделирование («stress shielding») — реакция костной ткани на имплантат, проявляющаяся усилением интенсивности процессов резорбции и костеобразования, рассматривается как процесс адаптации к новым условиям. Это изменение интенсивности ремоделирования с одной стороны имеет своей целью увеличение массы кости для создания тесного контакта с имплантатом, с другой — становится причиной развития нестабильности и ограничивает «срок жизни» эндопротеза. Некоторые авторы указывают на связь асептической нестабильности эндопротеза с наличием персистирующей микрофлоры в зоне имплантации. В частности, методом полимеразной цепной реакции доказано, что % протезов, удаленных при ревизии, инфицированы, тогда как традиционными методами выявляют менее 10 % инфицированных имплантатов. Определение среди больных с нестабильными эндопротезами группы риска в плане развития вялотекущего гнойно — воспалительного процесса в зоне имплантации искус- ственного сустава позволяет изменить тактику хирургического лечения: вместо одноэтапного ревизионного эндопротезирования выполнять двухэтапное ревизионное эндопротезирование с санацией зоны имплантации и установкой цементного спейсера с антибиотиком.
Цель исследования — разработка алгоритма иммунологического обследования пациентов с гонартрозом и коксартрозом до и после имплантации искусственного сустава, позволяющая сократить сроки реабилитации тяжелой группы больных путем снижения возможных ошибок в выборе тактики хирургического лечения.
МАТЕРИАЛЫ И МЕТОДЫ
Основу исследования составил анализ показателей иммунного статуса 109 больных остеоартрозом коленного и тазобедренного суставов III стадии в возрасте от 40 до 73 лет. Длительность заболевания варьировала от 5 до 35 лет. Для имплантации цементных протезов использовался костный цемент марки «Pоlacos-R».
Распределение больных по видам имплантированных цементных и бесцементных эндопротезов представлено в таблице 1.
Состояние клеточного иммунитета изучали посредством типирования лимфоцитов периферической крови методом лазерной проточной цитометрии на цитометре «BECKMAN COULTER EPICS XL» (США). Для идентификации лимфоцитов и определения их субпопуляционного состава применялся набор моноклональных антител (МКАТ) компании «Immunotech» (Франция). Т-лимфоциты (CD3+),
Т-хелперы (CD3+CD4+), цитотоксические Т-лимфоциты (CD3 + CD8 + ), В-лимфоциты (CD3 - CD19 + ), естественные киллеры (CD3 - CD16 + CD56 + ), естественные киллеры / Т-лимфоциты (CD3+CD16+CD56+), CD3+CD25+, несущие маркеры ранней активации Т-лимфоцитов, CD3+HLA-DR, несущие маркеры поздней активации Т-лимфоцитов, идентифицировали с помощью МКАТ, меченых фикоэритрином (РЕ) и флуоресцинизотиоци-анатом (FITC). Забор крови для исследования производится в количестве 6 мл из локтевой вены, натощак.
Полученные данные обрабатывались с помощью методов непараметрической статистики с использованием U-критерия Вилкоксона с применением программного обеспечения AtteStat 1.0, выполненного как надстройка к «Microsoft Exсel» программного продукта «Microsoft Office». Результаты исследования были представлены в виде медиан и интерквартильных размахов.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Первичное обследование больного проводилось до хирургического вмешательства. Полученные данные на последующих этапах исследования использовались в качестве контрольных.
Через 5-7 суток после имплантации выявлялись изменения, обусловленные массивным повреждением суставных и околосуставных тканей, внедрением инородных тел (имплантат, костный цемент). Для благоприятного течения послеоперационного периода было характерно умеренное снижение абсолютного количества лимфоцитов, повышение относительного и абсолютного числа В-лимфоцитов (CD3 - CD19 + ), уменьшение относительного количества естественных киллеров (CD3-CD56+CD16+) и естественных киллеров / Т-лимфоцитов (CD3+CD56+CD16+) (не более чем на 30 %).
При отсутствии осложнений инфекционного характера исследуемые показатели через 18-21 сутки после эндопротезирования возвращались к исходным значениям, что позволило использовать их в качестве диагностического теста для оценки течения послеоперационного периода.
Этап перехода оперированной конечности на полную нагрузку (4-7 месяцев после имплантации) характеризовался умеренным снижением относительного содержания Т-хелперов (CD3+CD4+) (не более чем на 15 %). Остальные показатели клеточного иммунитета в эти сроки не отличались от дооперационных значений.
Влияние имплантата на показатели клеточного иммунитета через 10-14 месяцев после имплантации (период начала активного функционирования эндопротеза) проявлялся снижением количества лимфоцитов (не более чем на 15 %), абсолютного числа Т-лимфоцитов (CD3 + ) (не более чем на 20%), относительного и абсолютного содержания Т-хелперов (CD3+CD4+) (не более чем на 15 %). Данные изменения были характерны для неосложненного течения послеоперационного периода.
Таблица 1
Распределение больных по виду имплантированных протезов
|
Виды бесцементных эндопротезов |
Кол-во больных |
Виды эндопротезов с цементной фиксацией |
Кол-во больных |
|
SLPS ЗАО «Altimed» (Белоруссия) |
64 |
«Smith & Nephew» (США) (тазобедренные) |
10 |
|
«Keramed» (Германия) |
2 |
«Genesis-1» (США) (коленные) |
29 |
|
«Ceraver» (Франция) |
3 |
«De Peu» (США) |
1 |
До операции (лимфоциты, моноциты, гранулоциты, CD3 , CD3*CD4 , СОЗ CDS*, СОЗ CD19 , CD3CD16+CD56+, CD3+CD16+CD56+,CD3+CD25+, CD3+HLA-DR).
5-7суток после имплантации
НЕОСЛОЖНЕННОЕ ТЕЧЕНИЕ ПОСЛ ЕОП ЕРА ПИОЧНОГО П ЕРИОДА
1 лимфоциты '
ТСОЗ СО19+ не более чем на 30 %
1CD3CD16CD56 от дооперационных 1CD3+CD16*CD56J значений
РИСК РАЗВИТИЯ
ИНФЕКЦИОННЫХ ОСЛОЖНЕНИЙ
1 лимфоциты (< 0,8х 10 /л)
Т СОЗ СО19+ (> 16 %; 0,Зх 10%)
1 CD3 CD16+CD56+ (< 6 %)
I CD3+CD16*CD56+ (< 3,3 %; 0.04х 10%)
18-21 суток после имплантации показатели возвращаются к дооперационным значениям
। лимфоциты (<0,8хЮ%)
Т СD3 CD 19+ (> 16 %; 0,3х 10%)
4-7 месяцев после имплантации
я д
1 СОЗ*СО4* (не более чем на 15% от TCD3CD19* (>16 %; 0,Зх|0%)
дооперационных значений)
Я
10-14 месяцев после имплантации
Т лимфоциты (нс более чем на 15 %)
Т СОЗ* (не более чем на 20 %)
Т CD3+CD4+ (не более чем на 15 % от дооперационных значений)
РИСК РАЗВИТИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНОГО ПРОЦЕССА В ЗОНЕ НЕСТАБИЛЬНОГО ИМПЛАНТАТА
4 о гранулоциты (>4,0x10 /л)
Т CD3CD19+(>16 %; 0,3 х 10%)
TCD3*HLA-DR (>8 %; 1,0x10%)
TCD3+CD25+(>26 %; 1,3x10%)
22-24 .месяца после имплантации
д
-
1 лимфоциты (нс более чем на 40 %)
-
1 CD3* (не более чем на 40 %)
-
1 CD3+CD4+ (не более чем на 17 %)
-
* CD3 CD16+CD56 (не более чем на 25 %)
Т CD3*CD 16 CD56* (не более чем на 13 % от дооперационных значений)
Д
Т гранулоциты (>4,0х 10%) TCD3CD19* (>16 %; О,3х 10%) TCD3 HLA-DR (>8 %; 1,0хЮ%) TCD3+CD25+(>26%; 1,3x10%)
Рис. 1. Алгоритм иммунологического обследования пациентов с остеоартрозом после эндопротезирования крупных суставов
Снижение абсолютного количества лимфоцитов (не более чем на 40 %), относительного содержания Т-лимфоцитов (CD3+) (не более чем на 15 %), абсолютного содержания Т-лимфоцитов (CD3+) (не более чем на 40 %), относительного и абсолютного содержания Т-хелперов (CD3+CD4+) (не более чем на 17 %), повышение относительного количества естественных киллеров (CD3-CD56+CD16+) (не более чем на 40 %) и естественных киллеров / Т-лимфоцитов (CD3+CD56+CD16+) (не более чем на 50 %) было характерно для благоприятного течения послеопера ционного периода. Относительное и абсолютное количество исходно повышенных клеток, экспрессирующих маркеры ранней активации Т-лимфоцитов (CD25+), в эти сроки снижалось, достигая нормальных значений. Значения показателей, превышающие 4,0×109/л для гранулоцитов, 16 % (0,35 × 109/л) для В-лимфоцитов (CD3-CD19+), 8 % (1,0 х 109/л) для CD3+HLA-DR, 26 % (0,4 х 109/л) для CD3+CD25+ свидетельствуют о вероятном развитии вялотекущего воспалительного процесса в области нестабильного имплантата (рис. 1).
ЗАКЛЮЧЕНИЕ
Данный алгоритм используется в стационаре ФГУ «РНЦ «ВТО» им. акад. Г. А. Илизарова» Минздравсоцразвития РФ во время подготовки к первичному и ревизионному эндопротезированию тазобедренных и коленных суставов и в послеоперационном периоде. Эффективность новой технологии подтверждена наблюдением на протяжении двух лет за группой из 109 больных в возрасте от 28 лет до 71 года, проле -ченных методом эндопротезирования. У 93 пациентов (85,3 %) получены хорошие функциональные результаты, признаков нестабильности эндопротеза на протяжении 2 лет наблюдения не выявлено, ближайший и отдаленный послеоперационные периоды протекали без осложнений, что было подтверждено результатами иммунологического обследования. Динамика иммунологических показателей в этой группе представлена в таблицах 2–4.
У 16 больных (14,7 %) в течение первого года после имплантации искусственного сустава были выявлены признаки нестабильности эндопротеза (тотальной или одного из компонентов). В этой группе с признаками нестабильности эндопротеза у 10 пациентов (0,09 %) с помощью иммунологических тестов был выявлен клинически не проявляющийся, вялотекущий воспалительный процесс в зоне имплантации (рис. 2), что позволило внести существенные изменения в тактику лечения: пациентам было выполнено двухэтапное реви- зионное эндопротезирование. На первом этапе удалялся нестабильный эндопротез и устанавливался цементный спейсер с антибиотиком. После регресса воспалительного процесса в зоне имплантации, подтвержденного результатами иммунологического тестирования (спустя 2-4 месяца после первого вмешательства), выполнялся второй этап лечения (удаление спейсера и реимплантация эндопротеза). Все результаты двухэтапной реимплантации хорошие. Повторного воспалительного процесса, а также признаков нестабильности реимплан-тированного протеза не выявлено, что позволяет рекомендовать данную медицинскую технологию для применения в лечебных учреждениях.
Таблица 2
Абсолютное содержание лимфоцитов, моноцитов и нейтрофилов после эндопротезирования крупных суставов при неосложненном течении послеоперационного периода (медианы значений показателей и интерквартильные размахи)
|
Лимфоциты (109/л) |
Моноциты (109/л) |
Гранулоциты (109/л) |
|
До операции |
||
|
1,56 (1,25÷2,02) |
↓ 0,16+ (0,1÷0,27) |
3,08 (2,55÷4,01) |
|
5-7 суток после эндопротезирования |
||
|
Д,29 * (0,9:1,4) |
0,2 (0,13÷0,25) |
Т 4,4 * (3,8:4,93) |
|
18-21 сутки после эндопротезирования |
||
|
1,64 (1,35÷1,95) |
0,16 (0,11÷0,24) |
3,3 (2,25÷4,28) |
|
4-7 месяцев после эндопротезирования |
||
|
1,56 (1,35÷1,83) |
0,18 (0,14÷0,26) |
3,31 (2,64÷3,87) |
|
10-14 месяцев после эндопротезирования |
||
|
| 1,24 * (1,06:1,47) |
0,16 (0,12÷0,27) |
2,91 (2,6÷3,27) |
|
22-24 месяца после эндопротезирования |
||
|
| 0,9 ** (0,71:1,43) |
0,16 (0,11÷0,29) |
3,29 (2,74÷3,58) |
|
Норма |
||
|
1,0 - 2,5 |
0,12 - 0,6 |
1,7 - 4,0 |
Примечание: * — p < 0,05, ** — p < 0,01 относительно дооперационных значений.
Таблица 3
Показатели клеточного иммунитета после эндопротезирования крупных суставов у пациентов с остеоартрозом при неосложненном течении послеоперационного периода (медианы значений показателей и интерквартильные размахи)
|
СD3+ |
CD3 - CD19 + |
CD3+CD4+ |
CD3+CD8+ |
CD3 - CD16 + CD56 + |
CD3+CD16+CD56+ |
|
|
До операции |
||||||
|
% |
73,4 (67,2÷77,5) |
9,6 (5,9÷11,8) |
45,3 (41,3÷51,8) |
26,2 (18,6÷31,2) |
13,6 (8,3÷17,9) |
6,7 (5,3÷8,8) |
|
109/л |
1,1(0,9÷1,41) |
0,16 (0,08÷0,19) |
0,72 (0,56÷0,88) |
0,37 (0,28÷0,48) |
0,21(0,11÷0,29) |
0,1 (0,08÷0,23) |
|
5 - 7 суток после эндопротезирования |
||||||
|
% |
72,8 (69,3÷78,1) |
Т 12,3 * (10,0:15,3) |
48,0 (43,4÷52,5) |
24,1(18,6÷29,0) |
1 9,3 ** (6,0:10,9) |
, 4,9 * (3,3:6,0) |
|
109/л |
1,0 (0,77÷1,27) |
Т 0,18 * (0,19:0,25) |
0,65 (0,53÷0,87) |
0,33 (0,22÷0,41) |
0,16 (0,13÷0,22) |
1 0,08 ** (0,04:0,11) |
|
18 - 21 сутки после эндопротезирования |
||||||
|
% |
75,6 (69,8÷79,7) |
8,5 (6,52÷10,2) |
47,7 (43,9÷54,4) |
24,7 (16,9÷29,1) |
12,1 (7,8÷15,8) |
6,1(4,6÷7,4) |
|
109/л |
1,16 (1,01÷1,52) |
0,13 (0,09÷0,17) |
0,76 (0,61÷0,96) |
0,39 (0,28÷0,53) |
0,19 (0,12÷0,29) |
0,08 (0,06÷0,12) |
|
4 - 7 месяцев после эндопротезирования |
||||||
|
% |
71,4 (59,6÷74,7) |
9,7 (7,2÷11,5) |
1 38,7 * (35,3:43,4) |
26,1 (18,6÷36,4) |
16,6 (13,2÷17,4) |
6,8 (4,2÷11,2) |
|
109/л |
1,04 (0,68÷1,26) |
0,14 (0,09÷0,2) |
0,6 (0,47÷0,67) |
0,38 (0,25÷0,51) |
0,21 (0,16÷0,27) |
0,11 (0,05÷0,14) |
|
10 - 14 месяцев после эндопротезирования |
||||||
|
% |
68,2 (62,7÷71,4) |
9,7 (7,2÷11,1) |
1 38,5 ** (35,5:41,8) |
30,4 (19,6÷35,8) |
17,6 (11,7÷18,8) |
7,4 (3,6÷9,5) |
|
109/л |
1 0,92 * (0,7:1,1) |
0,13 (0,1÷0,16) |
1 0,5 * (0,4:0,59) |
0,38 (0,24÷0,54) |
0,21 (0,15÷0,31) |
0,09 (0,05÷0,13) |
|
22 - 24 месяца после эндопротезирования |
||||||
|
% |
1 62,2 * (57,8:68,9) |
8,3 (5,6÷9,6) |
1 35,3 ** (34,1:38,5) |
23,1 (18,1÷26,1) |
Т 24,8 ** (21,6÷25,3) |
Т 11,9 * (8,7:13,1) |
|
109/л |
1 0,59 ** (0,47:1,01) |
1 0,08 * (0,07:0,14) |
1 0,43 ** (0,35:0,53) |
^ 0,21 * (0,16:0,39) |
0,21 (0,18÷0,29) |
0,11 (0,08÷0,14) |
|
Норма |
||||||
|
% |
60-83 |
6-16 |
37-53 |
20-34 |
8-18 |
0-6 |
|
109/л |
0,79-2,5 |
0,06-0,51 |
0,5-1,6 |
0,23-1,06 |
0,05-0,66 |
0-0,16 |
Примечание: * — p < 0,05, ** — p < 0,01 относительно дооперационных значений.
Таблица 4
|
CD3+HLA-DR (%) |
CD3+HLA-DR (10 9/л) |
CD3+CD25+ (%) |
CD3+CD25+ (109/л) |
|
До операции |
|||
|
4,11 (3,21÷6,37) |
0,06(0,04÷0,11) |
29,8 (26,0÷31,9) |
0,44(0,37÷0,52) |
|
5 – 7 суток после эндопротезирования |
|||
|
4,31 (2,42÷6,78) |
0,06 (0,03÷0,11) |
27,9 (23,1÷29,6) |
0,41(0,23÷0,45) |
|
18 – 21 сутки после эндопротезирования |
|||
|
3,9 (2,92÷6,37) |
0,07 (0,05÷0,09) |
31,8 (28,7÷33,9) |
0,63 (0,5÷0,83) |
|
4 – 7 месяцев после эндопротезирования |
|||
|
5,3 (4,2÷6,3) |
0,07 (0,06÷0,12) |
26,3 (25,7÷34,2) |
0,33 (0,29÷0,35) |
|
10 – 14 месяцев после эндопротезирования |
|||
|
5,1 (3,2÷7,6) |
0,08 (0,05÷0,1) |
↓ 20,6 * (18,2÷24,8) |
↓ 0,23 * (0,19÷0,34) |
|
22 – 24 месяца после эндопротезирования |
|||
|
5,6 (5,0÷6,4) |
0,07 (0,04÷0,12) |
↓ 18,0 ** (15,4÷22,1) |
↓ 0,18 ** (0,13÷0,23) |
|
Норма |
|||
|
0–6 |
0–0,16 |
7–18 |
0,06–0,4 |
Примечание: * — p < 0,05, ** — p < 0,01 относительно дооперационных значений.
CD3+(%)
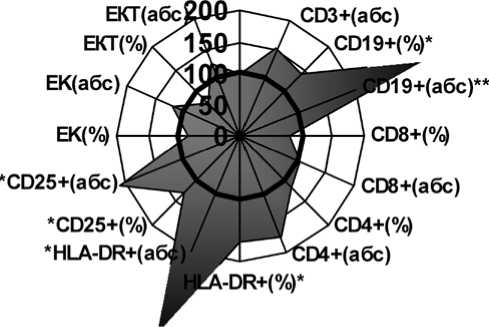
Рис. 2. Иммунологический профиль у пациентов с нестабильностью эндопротеза с выявленными во время ревизионного вмешательства признаками гнойно — воспалительного процесса в зоне имплантации; за 100 % приняты медианы показателей пациентов со стабильными имплантатами; * — p < 0,05; ** — p < 0,01 относительно значений показателя в группе со стабильными имплантатами
Динамика CD3+ HLA-DR и CD3+ CD25+ после эндопротезирования крупных суставов при неосложненном течении послеоперационного периода (медианы значений показателей и интерквартильные размахи)


