Лечение лучевых повреждений органов малого таза после лучевой терапии рака предстательной железы
Автор: Сычева Инна Владимировна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 3 т.17, 2018 года.
Бесплатный доступ
Актуальность. Лучевые повреждения органов малого таза (постлучевой ректит, цистит, уретрит) - частые осложнения после лучевой терапии рака предстательной железы. По данным различных авторов, частота поздних лучевых повреждений органов малого таза составляет до 30 %. Таким образом, часть больных, излеченных от злокачественного новообразования, приобретает новое заболевание, существенно снижающее качество жизни и требующее лечения. Материал и методы. Представлены результаты лечения 149 больных с поздним лучевым ректитом (проктитом), который развился после дистанционной лучевой терапии (n=106), брахитерапии (n=15) и сочетанной лучевой терапии (n=28) по поводу рака предстательной железы T1-3N0M0. Лучевое лечение у данных пациентов проводилось в различных учреждениях России и за рубежом. Все больные госпитализировались с лучевым проктитом II-IV степени и ремиссией рака предстательной железы. У 107 (72 %) пациентов ректиты сочетались с лучевыми повреждениями мочевыделительной системы. Нарушение потенции наблюдалось в 98 % случаев. Всем пациентам проводилось комплексное консервативное лечение. Больным с эрозивногеморрагическим и геморрагическим ректитом и циститом выполнялось химическое прижигание 1-2,5 % водным раствором формальдегида. Результаты. Удовлетворительный эффект консервативной терапии лучевого ректита был получен у 141 (95 %) больного, при формировании ректо-везикального свища ввиду неэффективности лечения 8 (5 %) больным выполнена колостомия. Химическое прижигание слизистой мочевого пузыря и прямой кишки при эрозивно-геморрагическом и геморрагическом ректите и цистите эффективно и безопасно. Отмечено, что после сочетанной лучевой терапии (СЛТ) частота и степень выраженности постлучевых осложнений больше, чем при брахитерапии (БТ) и СЛТ, но это требует дальнейшего анализа.
Рак предстательной железы, дистанционная лучевая терапия, лучевые повреждения, сочетанная лучевая терапия, лучевой цистит, лучевой ректит (проктит), лучевой уретрит, ректо-везикальный свищ
Короткий адрес: https://sciup.org/140254189
IDR: 140254189 | УДК: 616.65-006.6-08-06:615.849.1:616.718.19 | DOI: 10.21294/1814-4861-2018-17-3-64-71
Treatment of radiation-induced pelvic damage after radiation therapy for prostate cancer
Background. Radiation-induced damage to the pelvic organs (post-radiation proctitis, cystitis, urethritis) is a frequent complication after radiotherapy for prostate cancer. The reported frequency of late radiation damage to the pelvic organs is up to 30 %. Material and methods. The paper presents treatment outcomes of 149 with radiation-induced pelvic injuries caused by brachitherapy (15 patients) and combination treatment including brachitherapy and external beam radiation therapy (28 patients) for stage T1-3N0M0 prostate cancer. Radiation-induced rectitis (proctitis) was revealed in 149 patients and complications of the urinary tract after radiation treatment were noted in 107 (72 %) patients. Potency failure was observed in 98 % of cases. All patients received conservative treatment and 8 (5 %) of these patients underwent surgery after inefficient conservative treatment. Results. Favorable effect of conservative therapy of radiation-induced rectitis was obtained in 141 (95 %) patients. Eight (5 %) patients underwent colostomy due to the formation of vesicle-rectal fistula. Chemical cauterization of the mucosa of the bladder and rectum in patients with erosive hemorrhagic and hemorrhagic rectitis and cystitis was effective and safe. The frequency of post-radiation complications was found to be less after brachitherapy than after combination treatment using brachitherapy and external beam radiation.
Текст научной статьи Лечение лучевых повреждений органов малого таза после лучевой терапии рака предстательной железы
При лучевой терапии рака предстательной железы (РПЖ) в зону полей облучения могут попадать различные анатомические образования: мочевой пузырь, прямая кишка, внутритазовая клетчатка, сосудисто-нервные пучки и кости таза. Необходимо отметить, что изолированные поражения одного органа встречаются редко и в большинстве случаев они носят сочетанный характер [1–4]. Причиной развития лучевых повреждений являются ошибки при планировании и проведении лучевой терапии, когда применяются высокие разовые и суммарные дозы, превышающие толерантность здоровых тканей к ионизирующему излучению. Сложности дозиметрического планирования вызваны близким расположением органов в малом тазу. Часто не учитываются особенности распределения дозы в сопряжённых с злокачественным новообразованием органах, а также существует индивидуальная чувствительность тканей у больного к лучевой терапии [1, 2, 4, 6–18].
Факторами риска развития лучевых повреждений являются ранее перенесенные заболевания органов брюшной полости (дизентерия, брюшной тиф, хронический колит, холецистопанкреатит), мочевыводящих путей, а также хронические заболевания (сахарный диабет, тиреотоксикоз, гипертоническая болезнь) [4, 6, 9, 10, 16]. Известно, что лучевые повреждения у больных с хроническими
сопутствующими заболеваниями возникают чаще, чем у больных без патологии (70 против 18,1 %) [4, 9, 10]. Оперативное лечение до лучевой терапии и повторные облучения также являются неблагоприятными факторами.
Патофизиология лучевых повреждений заключается в том, что образуются свободные перекисные радикалы, что нарушает регенерацию поврежденных клеток. Нарушается микроциркуляция в сосудах слизистой органа, образуются тромбы в мелких сосудах, что приводит к участкам ишемии, эрозиям, язвам, а в дальнейшем возможно формирование свища. Развивается радиационно-индуцированный фиброз (РИФ), что приводит к тому, что стенки сосудов зажаты как бы в «каркасе» фиброза, становятся неэластичными, не спадаются при травматизации, клинически это проявляется в виде кровотечений, вплоть до профузных, трудно поддающихся лечению.
Большинство авторов местные лучевые повреждения подразделяют на ранние (лучевые реакции) и поздние. К ранним лучевым реакциям относятся патологические изменения, которые развиваются в процессе проведения лучевой терапии или в ближайшие 3 мес после ее завершения. Они носят функциональный характер и часто бывают обратимыми. Большинство из них купируются в течение ближайших 4 мес. Частота ранних лучевых повреждений составляет 69–84 % [3–10, 19].
Поздние лучевые повреждения формируются не ранее 3 мес после окончания лечения и, как правило, приобретают хроническое течение. В результате облучения рака предстательной железы появляются местные лучевые повреждения органов малого таза в 30 % случаев [1, 3–5]. Возникновение данной патологии в какой-то степени закономерно и связано с применением высоких суммарных доз облучения, необходимых для эрадикации опухоли. Важно, чтобы частота развития таких патологических изменений не превышала допустимого 5 % уровня, определенного рекомендациями ВОЗ. При этом не должно быть тяжелых повреждений, которые могут вызывать инвалидность и смерть больного. При этом лучевые повреждения кишки встречаются в 1–15 %, лучевые повреждения уретры, мочевого пузыря – в 15–27 % случаев. Требуется комплексное лечение для улучшения качества жизни пациентов [1, 2, 4–18].
Для оценки поздних лучевых повреждений кишечника и мочевого пузыря в большинстве центров используется классификация радиотера-певтической онкологической группы совместно с Европейской организацией по исследованию и лечению рака (RTOG/EORTC, 1995), дополненная критериями кооперативной группы исследователей для более точной характеристики преимущественно ранних токсических эффектов. Мы также используем эндоскопическую классификацию циститов и ректитов по М.С. Бардычеву, так как местное лечение в дальнейшем мы подбираем в зависимости от эндоскопической картины.
Клиническая картина характеризуется наличием патологических примесей в кале и моче: слизи, крови; дизурическими явлениями, нерегулярным стулом (возможны и запоры, и поносы), болевым синдромом (периодическим или постоянным) разной интенсивности и локализации (внизу живота, в области промежности), усиливающимся при акте дефекации и мочеиспускании [3, 4, 4, 11].
Существующие методы лечения лучевых повреждений органов малого таза остаются недостаточно эффективными, часто регистрируются рецидивы патологического процесса. Компенсаторные механизмы, как правило, лишь частично сглаживают клиническую картину повреждений. Ремиссия достигается у 35–65 %, рецидивы наблюдаются у 30–80 % пациентов [1, 3, 4]. Хирургическое лечение требуется 10–15 % больных, но при этом отмечают высокий уровень сложности операций, частота осложнений достигает 15–80 %, послеоперационная летальность – 3–25 % [1, 3–5, 11–13, 17, 20], возможно, это связано с плохой регенерацией облученных тканей. Показаниями к оперативному лечению являются стенозы кишки, стриктуры уретры, свищи, рецидивирующие профузные кровотечения из кишки и мочевого пузыря. Тяжелые осложнения после операций: сепсис, кишечная непроходимость, формирование повторного свища. В некоторых случаях ограничиваются колостомией и эпицистостомией. Многие авторы рекомендуют начинать с консервативной терапии и при ее неэффективности использовать малоинвазивную хирургию (эндоскопическое лечение). Только при использовании всех перечисленных методов рекомендуется прибегать к объемным хирургическим операциям с пластикой [1, 3–5, 11, 12, 18–24]. Таким образом, поиск и внедрение в практику эффективных методов лечения местных лучевых повреждений кишечника являются актуальными.
Цель исследования – оценить результаты лечения лучевых повреждений кишечника после лучевой терапии рака предстательной железы, эффективность химического прижигания слизистой 1–2,5 % водным раствором формальдегида при эрозивно-геморрагическом и геморрагическом ректите и цистите, проанализировать частоту развития лучевых осложнений.
Материал и методы
В период с 2009 по 2016 г. в отделении хирургического и консервативного лечения лучевых повреждений с группой реконструктивно-пластической хирургии наблюдалось 149 больных в возрасте от 57 до 84 лет с местными лучевыми повреждениями кишечника, которые развились после дистанционной лучевой терапии (ДЛТ), брахитерапии и сочетанной лучевой терапии. Все больные проходили курс лучевой терапии в различных учреждениях России и за рубежом на разном оборудовании. Всем больным перед лучевой терапией (ЛТ) проводилась гормональная терапия (ГТ) в режиме максимальной андрогенной блокады (МАБ) с целью уменьшения объема предстательной железы. Дистанционная лучевая терапия выполнена 106 больным (71 % от общего количества пациентов), СОД 60–80 Гр, БТ – 15 (10 %), СОД 140–145 Гр, СЛТ – 28 (19 %), СОД: ДЛТ 44–46 Гр и БТ – 110 Гр.
Все больные, включенные в исследование, были с ремиссией рака предстательной железы. Для диагностики поздних лучевых повреждений органов малого таза и исключения прогрессирования основного заболевания использовался следующий алгоритм: сбор жалоб и анамнеза, осмотр, включая пальцевое исследование прямой кишки, клиниколабораторные анализы, посев мочи, копрограмма, кал на дисбактериоз. Инструментальные обследования включали УЗИ почек, мочевого пузыря, при необходимости цистоскопию и уретроскопию, экскреторную урографию, ректоскопию или колоноскопию, ректографию, фистулографию, МРТ или СКТ.
Все больные были с постлучевым проктитом (ректитом) II–IV степени. Частота сочетания постлучевых ректитов с другими местными лучевыми повреждениями представлена в табл. 1. Последние четыре патологии наблюдались только при ДЛТ. Результаты эндоскопического исследования на момент поступления в отделение представлены в табл. 2. Наиболее часто в зону облучения при лучевом лечении РПЖ попадали прямая кишка – 142 (95,3 %) случая, ректосигмоидный отдел кишки – 4 (6 %) наблюдения, тонкая кишка – в 1 % случаев, что связано с ее анатомической удаленностью от органа-мишени – предстательной железы.
Всем пациентам с ректитом проводилось комплексное консервативное лечение. Общая и местная терапия лучевых повреждений кишечника и мочевого пузыря ранее подробно описана в наших статьях [3–4]. Общая терапия включала в себя диету № 5, обильное питье, нормализацию стула, гемостатическую, заместительную, противовоспалительную, вазоактивную, при необходимости обезболивающую, антибактериальную терапию. Местное лечение циститов и ректитов заключалось в инстилляциях в мочевой пузырь бескатетерным способом (чтобы снизить травматизацию уретры) и ректальных микроклизм. Использовались 10 %
Таблица 1
Частота сочетания постлучевого ректита с другими местными лучевыми повреждениями
|
Вид лучевых повреждений |
Число больных |
|
Лучевой ректит |
149 (100 %) |
|
Нарушение потенции |
146 (98 %) |
|
Лучевой цистит |
75 (50,3 %) |
|
Лучевой уретрит и некроз уретры |
21 (14,1 %) |
|
Стриктура уретры |
11 (7,4 %) |
|
Синдром тазовой боли |
19 (12,8 %) |
|
Отеки нижних конечностей |
3 (2,0 %) |
|
Фиброз кожи и подкожной жировой |
3 (2,0 %) |
|
клетчатки |
|
|
Вутритазовый лучевой фиброз |
9 (6 %) |
|
Остеорадионекроз |
1 (0,7 %) |
Таблица 2
Результаты эндоскопического обследования больных с постлучевыми ректитами
При неэффективности консервативных мероприятий при эрозивно-геморрагическом и геморрагическом цистите и ректите проводилось химическое прижигание 1 % водным раствором в мочевом пузыре с использованием уретрального катетера и 2,5 % водным раствором формальдегида в прямой кишке с использованием ректоскопа. Эта процедура хорошо переносится больными, не требует анестезии, может выполняться в амбулаторных условиях. Время экспозиции раствора 2 мин. Достигается хороший терапевтический эффект. Осложнений не наблюдалось, за исключением гиперемии лица у 1 пациента, при этом артериальное давление было в норме и дополни-
Таблица 3
Результаты лечения постлучевых ректитов
Эндоскопическая форма ректита
Улучшение эндоскопической картины (% от больных с данной эндоскопической картиной)
Частота формирования свища, количество больных
Геморрагический, n=93 (62 %)
Эрозивно-геморрагический, n=25 (17 %)
Язвенно-некротический, n=31 (21 %)
93 (100 %)
25 (100 %)
Язвы зарубцевались 23 (74 %)
8 (26 %)
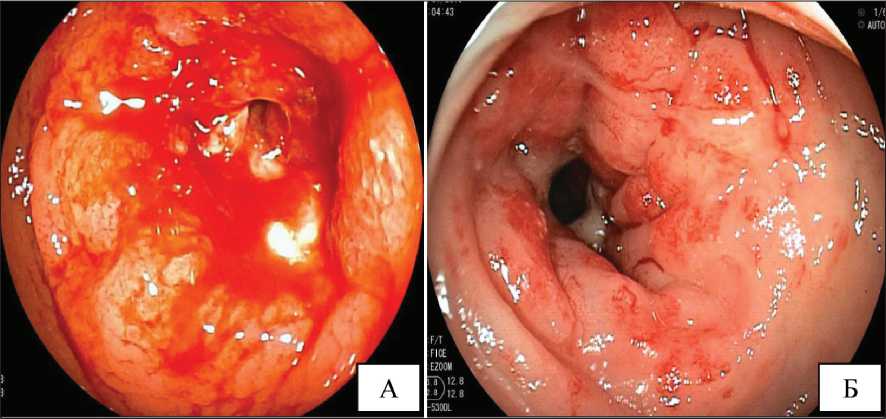
Рис. 1. Пациент с диагнозом РПЖ T2сN0M0. Комбинированное лечение в 2009 г.: ГТ + СЛТ. СОД: ДЛТ 46 Гр и БТ 110 Гр. Поздний лучевой эрозивно-геморрагический ректит, по классификации RTOG/EORTC III ст.:
А – эндоскопические изменения до лечения, Б – эндоскопическая картина сразу после химического прижигания слизистой 2,5 % водным раствором формальдегида
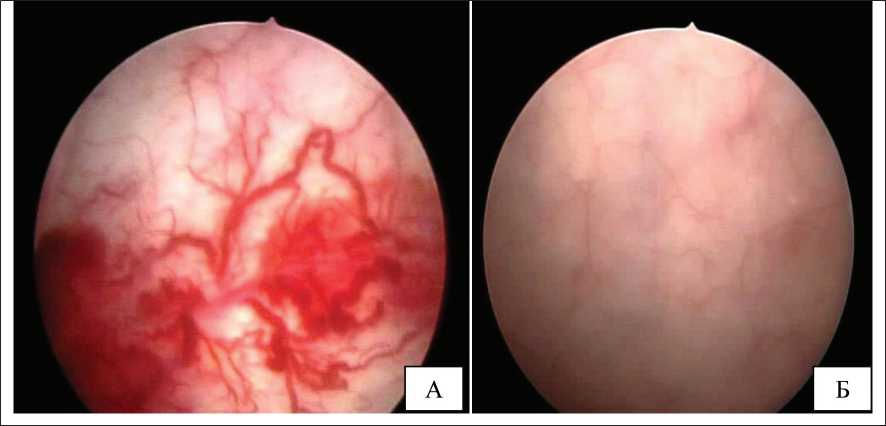
Рис. 2. Пациент с диагнозом РПЖ T2вN0M0. Комбинированное лечение в 2008 г.: ГТ + БТ. СОД 145 Гр.
Поздний лучевой геморрагический цистит, по классификации RTOG/EORTC II ст.:
А – эндоскопические изменения до лечения, Б – эндоскопическая картина через 3 мес после лечения (консервативная терапия 1 курс + химическое прижигание)
тельных назначений не потребовалось. Возможно неоднократное прижигание через 3–6 мес (до 2–3 раз). Противопоказанием к химическому прижиганию являются язвенные дефекты и стеноз кишки и уретры, так как при этом высока вероятность формирования свища. В зарубежной литературе описано использование 4–10 % спиртового раствора формалина под спинальной анестезией. Эффективность метода составила 70–100 %, но описаны такие осложнения, как язвы, свищи, трещины, стеноз анального канала, недержание кала в 18–27 % [10, 17, 25].
Больные с язвенно-некротическим ректитом получали также сульфасалазин, омепрозол, вазоактивные и ферментные препараты (трипсин или химотрипсин, местно).
Результаты и обсуждение
После проведенного лечения (1-го или нескольких курсов консервативного лечения и химического прижигания) отмечена положительная динамика у 141 (94,6%) больного (табл. 3). У всех пациентов наблюдалась нормализация общего анализа крови, снижение частоты и объема кровотечений, улуч-
|
Хирургическое лечение |
Таблица 4 |
|
Вид хирургического лечения |
Количество |
|
пациентов |
Колостомия
Уретротомия, трансуретральная резекция, предстательной железы, трансуретральная резекция, коагуляция или трансуретральная резекция, лазерная коагуляция Литотрипсия камня мочевого пузыря Эпицистостомия
10 (6,7%)
17 (11,4%)
1 (0,7 %) 7 (4,7%)
шение общего состояния. Больные, у которых язвы зарубцевались (n=23), поступили в отделение на ранних этапах формирования дефекта, когда он носил поверхностный характер. Сроки заживления язв составили от 3 мес до 1,5 лет.
Эффективность химического прижигания при эрозивно-геморрагическом и геморрагическом ректите была отмечена в 83 % (рис. 1), при циститах – в 79 % (рис. 2) случаев. У 6 человек (4,0 % из всех мужчин с ректитами и 19,4 % из всех больных с язвенно-некротическими ректитами), которые поступили с глубокой язвой, в срок от 1 года до 6 лет сформировался везико-ректальный свищ (рис. 3). У 2 пациентов (1,3 % из всех больных и
-
6,5 % из больных с язвенно-некротическим ректи-том) сформировался свищ в мягкие ткани.
Колостомия была выполнена 10 (6,7 %) пациентам: в 8 случаях по поводу язвенно-некротического ректита с формированием свища, в 2 наблюдениях по поводу постлучевого геморрагического ректита с рецидивирующимися профузными кровотечениями из кишки (в дальнейшем у этих больных колостома была закрыта). Эпицистостомия выполнена у 7 человек, из них у 6 больных в связи с формированием ректо-везикального свища, у 1 пациента по поводу стриктуры уретры и возникновения острой задержки мочи в дальнейшем выполнена уретротомия и удалена эпицистостома. Остальные операции были выполнены по поводу постлучевой стриктуры уретры, доброкачественной гиперплазии предстательной железы и кровотечения из мочевого пузыря в нашем учреждении либо по месту жительства (табл. 4). В дальнейшем 6 больным с колостомой и эпицистостомой были рекомендованы реконструктивно-пластические операции с различными вариантами деривации мочи.
При анализе частоты язвенно-некротического ректита в сравниваемых группах использовался критерий Фишера. При этом установлено, что после проведения СЛТ этот вид пост-лучевых осложнений
Таблица 5
Частота развития постлучевых осложнений со стороны прямой кишки
Вид лучевых повреждений Брахитерапия (n=15) ДЛТ (n=106) СЛТ (n=28)
Язвенно-некротический ректит 2 (13 %) 17 (16 %) 12 (43 %)
Эрозивно-геморрагический ректит 2 (1,9 %) 5 (17,9 %)
Свищ 2 (13,3 %) 2 (1,9 %) 4 (14,3 %)
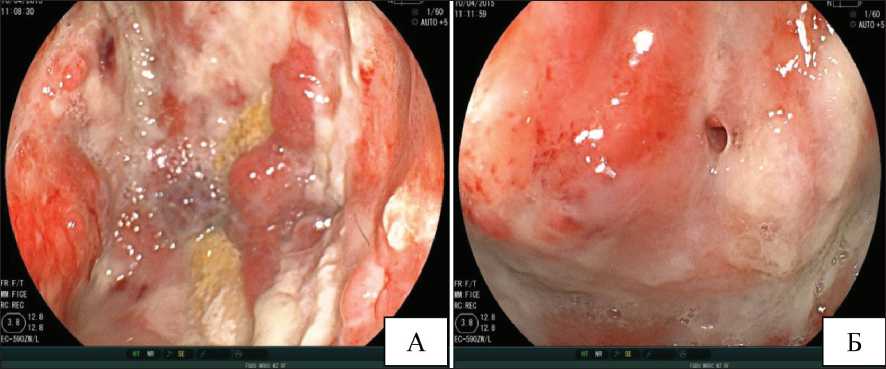
Рис. 3. Больной Р. Комбинированное лечение рака предстательной железы T2N0M0 в 2010 г.: ГТ в режиме МАБ + БТ. СОД 140 Гр.
Местный рецидив в 2013 г., лечение: ГТ + ДЛТ СОД 36 Гр:
А – ректоскопия (больной лежит на левом боку): все стенки прямой кишки изъязвлены и покрыты массивным некрозом, местами определяются бугристые разрастания грануляционной ткани, чуть выше визуализируется устье ректо-везикального свища, при гистологическом исследовании биопсийного материала – фрагменты грануляционной и соединительной ткани;
Б – прицельный снимок ректо-везикального свища. Больному выполнено оперативное лечение в объеме сигмостомии, эпицистостомии
наблюдался значимо чаще – в 12 (43 %) случаях, – чем при применении после БТ, ДЛТ – в 2 (13 %) и 17 (16 %), р=0,048 и р=0,002 соответственно (табл. 5). При сравнении данного показателя между группами БТ и ДЛТ значимых различий не выявлено (р=0,57). Кроме того, осложнения при СЛТ носили более выраженный характер, чаще наблюдались свищи (табл. 5).
Заключение
Консервативная терапия лучевых повреждений органов малого таза позволяет улучшить качество жизни пациентов. Химическое прижигание слизистой мочевого пузыря и кишки является безопасным и эффективным методом лечения лучевых эрозивно- геморрагических и геморрагических ректитов, циститов, что позволяет сократить сроки лечения и частоту госпитализаций. После СЛТ осложнения встречаются чаще, чем после БТ и ДЛТ, что требует дальнейшего анализа. Вероятно, это связано с отработкой методики выполения СЛТ, так как наиболее тяжелые постлучевые осложнения возникли в 2008– 11 г. Эффективность лечебных мероприятий при поздних лучевых повреждениях непосредственно зависит от сроков поступления в специализированное учреждение, степени тяжести патологического процесса, возраста пациента и сопутствующих хронических заболеваний. Лечение должно быть комплексным и сочетать местное воздействие с коррекцией нарушенных функций организма.
Список литературы Лечение лучевых повреждений органов малого таза после лучевой терапии рака предстательной железы
- Пасов В.В., Курпешева А.К. Осложнения и повреждения органов и тканей при лучевой терапии. Основы лучевой диагностики и терапии: национальное руководство. М.: ГЭОТАР-Медиа, 2012. 962-990.
- Столярова И.В., Винокурова В.Л. Проблемы больных после лечения рака шейки матки. Профилактика и лечение постлучевых осложнений. Практическая онкология. 2002; 3: 220-227.
- Сычева И.В., Пасов В.В., Курпешева А.К. Консервативные методы лечения местных лучевых повреждений, формировавшихся в результате сочетанной лучевой терапии и брахитерапии рака предстательной железы. Сибирский онкологический журнал. 2012; 5: 57-60.
- Сычева И.В., Пасов В.В. Лучевые повреждения органов малого таза после лечения ранних стадий рака предстательной железы (обзор литературы). Радиация и риск. 2014; 23 (4): 99-115.
- Бардычев М.С., Цыб А.Ф. Местные лучевые повреждения. М.: Медицина, 1985. 230.


