Лечение нейропатической плантарной язвы при синдроме диабетической стопы (клиническое наблюдение)
Автор: Швец Л.И., Лвина Ю.М.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические случаи
Статья в выпуске: 1 (75), 2021 года.
Бесплатный доступ
Введение. Сахарный диабет - тяжелое заболевание, твердо занимающее первое место по инвалидизации и третье место по смертности в мире. Одним из самых грозных осложнений сахарного диабета является синдром диабетической стопы, так как именно это осложнение является основным «виновником» ампутации и инвалидизации пациентов. Осложняет лечение плантарных язв отсутствие болевой чувствительности у пациентов с нейропатией. Широко и с успехом применяемые современные методы лечения не приведут к заживлению язвенного дефекта без разгрузки стопы. Для профилактики образования и рецидивов плантарных нейропатических язв оптимальным является изготовление индивидуальной ортопедической обуви.Клинический случай. Больной Р., 58 лет обратился с жалобами на повышение температуры до 38,40 С, на покраснение и отек левой стопы и голени, на наличие мозоли с изъязвлением на 1 пальце левой стопы, покраснение, отек и язвенный дефект 2 пальца левой стопы. Не получив медицинской помощи в поликлинике и в центре диабетической стопы, пациент обратился к нам. При первом осмотре была удалена ногтевая фаланга с изъеденной суставной поверхностью 2 пальца левой стопы. Дальнейшее лечение в течение трех недель привело к заживлению язвенных дефектов. Однако после прекращения ношения ортеза и длительной нагрузки на стопу у больного произошло кровоизлияние в мозоль 1 пальца с последующим инфицированием. Отказ от ношения ортеза затянул процесс лечения на три месяца. Только после того, как больной стал применять разгрузочную обувь, язва зарубцевалась.Заключение. Данное клиническое наблюдение демонстрирует проблемы в лечении диабетической язвы стопы. Неправильная тактика врачей амбулаторного звена едва не привела к утере части конечности у пациента. Неадекватное отношение пациента к своему заболеванию усложнило и удлинило лечение язвенного дефекта. Только общие усилия позволят снизить инвалидизацию и смертность при таком осложнении, как диабетическая стопа.
Диабетическая стопа, нейропатия, трофическая язва, ортез
Короткий адрес: https://sciup.org/142230021
IDR: 142230021 | УДК: 616.379-008.64 | DOI: 10.17238/issn2072-3180.2021.1.94-100
Treatment of neuropathic plantar ulcer in diabetic foot syndrome (clinical observation)
Introduction. Diabetes mellitus is a serious disease, firmly occupying the first place in disability and the third place in mortality in the world. One of the most dangerous complications of diabetes mellitus is diabetic foot syndrome, since this complication is the main "culprit" of amputation and disability of patients. The absence of pain sensitivity in patients with neuropathy complicates the treatment of plantar ulcers. Widely and successfully applied modern methods of treatment will not lead to the healing of the ulcer defect without unloading the foot. To prevent the formation and recurrence of plantar neuropathic ulcers, it is optimal to make individual orthopedic shoes.Clinical case. Patient R., 58 years old, complained of an increase in temperature to 38.40 C, redness and swelling of the left foot and lower leg, the presence of calluses with ulceration on 1 finger of the left foot, redness, swelling and ulcerative defect of 2 fingers of the left foot. Without receiving medical care in the polyclinic and in the diabetic foot center, the patient turned to us. At the first examination, the nail phalanx was removed with a pitted articular surface of 2 fingers of the left foot. Further treatment for three weeks led to the healing of ulcerative defects. However, after stopping wearing the orthosis and prolonged load on the foot, the patient suffered a hemorrhage in the callus of the 1st finger with subsequent infection. The refusal to wear the orthosis delayed the treatment process for three months. Only after the patient began to use unloading shoes, the ulcer was healed. Conclusion. This clinical observation demonstrates problems in the treatment of diabetic foot ulcers. The wrong tactics of the outpatient doctors almost led to the loss of a part of the patient's limb. The inadequate attitude of the patient to his disease has complicated and prolonged the treatment of the ulcer defect. Only joint efforts will reduce disability and mortality in such a complication as diabetic foot.
Текст научной статьи Лечение нейропатической плантарной язвы при синдроме диабетической стопы (клиническое наблюдение)
Сахарный диабет — тяжелое заболевание, твердо занимающее первое место по инвалидизации и третье место по смертности в мире [1]. В XXI веке сахарный диабет (СД) стал ведущим неинфекционным заболеванием. Каждый год численность заболевших сахарным диабетом в мире в среднем увеличивается на 7 млн. Последние десятилетия рост сахарного диабета приобрел такой темп, что в мировом медицинском сообществе стали говорить об этом заболевании как об «эпидемии диабета». По прогнозам 2000 года на 2030 год количество больных сахарным диабетом возрастет до 366 миллионов [1]. Однако уже на сегодняшний день в мире насчитывается 463 миллиона больных сахарным диабетом. В России диабетом болен каждый 13. При этом в общей структуре заболеваемости сахарным диабетом диабету 2 типа принадлежит около 85%, и отмечается активное «омоложение» данной патологии. Если несколько десятилетий назад диабет 2 типа считался заболеванием преимущественно пожилых людей, то сейчас получены данные о выявлении этого типа заболевания у детей с двух лет. И это особенно тревожно в плане развития такого серьезного осложнения как диабетическая стопа, так как именно это осложнение является основным «виновником» ампутации и инвалидизации пациентов. По данным Foster and Lauver, в мире выполняется больше миллиона ампутаций по поводу диабетической стопы, что составляет 70% всех ампутаций нетравматического характера [2]. По данным государственного регистра РФ, среднее количество ампутаций составляет 6,4 случая на 1000 пациентов. Как правило, причиной ампутации конечности являются гнойно-трофические осложнения при синдроме диабетической стопы. Предшествует развитию флегмоны стопы и влажной гангрены наличие длительно существующей хронической диабетической язвы стопы, склонной к прогрессированию и устойчивостью к лечению из-за снижения регенерационных процессов в ране. Необходимо отметить, что такое резистентное к терапии течение чаще имеют трофические язвы, возникшие на фоне диабетической нейропатии. Осложняет лечение отсутствие болевой чувствительности у пациентов с нейропатией. Это часто приводит к непониманию больным тяжести и опасности ситуации и, как следствие, игнорированию назначений врача. Среди клинических форм синдрома диабетической стопы на долю нейропатической формы приходится около 70% [3]. Федеральный регистр сахарного диабета РФ зарегистрировал диабетическую нейропатию у 33,6% пациентов с СД 1 типа и 18,6% пациентов с СД 2 типа [4]. По данным проспективного рандомизированного исследования Пизанского университета, у пациентов с сахарным диабетом высокого риска частота образования язв составила 61% через 3 года и 72% через 5 лет [5]. Еще в 1999 году Международная рабочая группа по диабетической стопе разработала рекомендации по профилактике и лечению диабетической стопы [6]. ВОЗ разработала программу по диабету. В России с 2020 года началась разработка Федерального проекта «Борьба с сахарным диабетом», который планируется включить в состав национального проекта «Развитие здравоохранения». Повсеместно создаются Центры диабетической стопы и школы диабета, основной задачей которых является профилактика возникновения синдрома диабетической стопы и оказания квалифицированной помощи при наличии данного осложнения. Однако все принимаемые меры на настоящий момент не приводят к уменьшению больных с синдромом диабетической стопы. Когортное исследование эффективности амбулаторного лечения синдрома диабетической стопы показало сохранение язвенного дефекта стопы в течение 12 месяцев у 35% больных и недостаточное применение разгрузочных методов лечения [7].
В добавление к основным стандартным методам лечения диабетических язв в последние десятилетия активно применяется реваскуляризация стопы в основном путем эндоваскулярных вмешательств. Это значительно повысило и ускорило заживление язвенных дефектов при ишемической форме диабетической стопы, но не решила проблему нейропатических язв, которые и составляют основную массу в данном осложнении.
По-прежнему при лечении данной патологии применяется общая и местная антибактериальная терапия, мазевые повязки на основе полиэтиленгликоля. Широко и с успехом применяются современные щадящие самофиксирующиеся повязки типа супрасорба и гидроколла на всех стадиях язвенного дефекта (очищение от некротических тканей, адсорбирующие повязки, повязки, стимулирующие грануляционную ткань и эпителизацию). Но, несмотря на самые современные способы лечения, заживление плантарных язв невозможно без разгрузки стопы. Эффективная разгрузка считается важной частью успешного клинического лечения язв диабетической стопы [8, 11]. На настоящий момент применяются разнообразные разгрузочные методики от рутинных (строгий постельный режим, костыли, коляска) до самых современных. Повсеместно проводятся исследования по сравнению эффективности современных методов [9, 10]. На первый план все больше и больше выдвигается ношение ортопедической разгрузочной обуви и стелек (Рис. 1, 2) [11, 12].
Разработаны новые модели разгрузочной обуви с использованием вакуумных подушек и с пневмофиксацией для голено- стопного сустава VACOdiaped улучшающий регенрационные процессы благодаря снижению и распределению давления через вакуумную подушку (Рис. 3, 4).
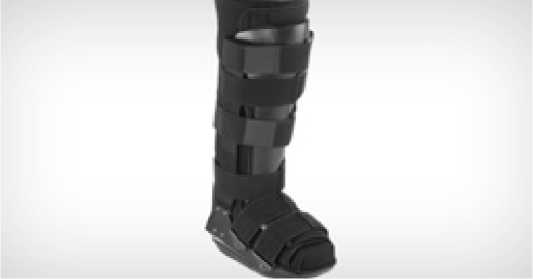
Рис. 1. Диабетический сапожок Чарткорт Конформер

Рис. 4. VACOdiaped

Рис. 2. Диабетические стельки для обуви

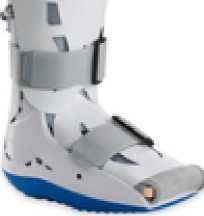
Рис. 3. Тутор диабетический («сапог») с пневмофиксацией для голеностопного сустава XP DIABETIC WALKER
Для профилактики образования и рецидивов плантарных нейропатических язв оптимальным является изготовление индивидуальной ортопедической обуви [13, 14].
В дополнение ко всему вышесказанному необходимо отметить, что при лечении диабетических язв стопы необходимо абсолютное понимание тяжести заболевания самим пациентом. Отсутствие болевой чувствительности при нейропатии снижает критическое отношение больного к своему состоянию, приводя к дезаггравации и игнорированию назначений врача. В соответствии с этим врач, проводящий лечение пациентов с трофическими язвами, должен постоянно кропотливо объяснять пациенту необходимость выполнения всех условий для успешного лечения.
Несмотря на появление большого количества центров диабетической стопы, качество амбулаторной помощи пациентам с трофическими нарушениями не всегда соответствует современным требованиям. Все средства для лечения нейропа-тичесой язвы стопы и все усилия медперсонала не приведут к положительному результату до тех пор, пока пациент не уяснит себе всю тяжесть заболевания и необходимость выполнения требования врачей. В качестве иллюстрации вышесказанного мы позволили себе продемонстрировать клинический случай.
Клинический случай
Больной Р., 58 лет, педагог, 18.11.2019 г. обратился с жалобами: на повышение температуры до 38,4 0С, покраснение и отек левой стопы и голени, на наличие мозоли с изъязвлением на 1 пальце левой стопы, на повышение АД до 180/100 мм рт. ст., на снижение зрения на оба глаза (эффект «падающего снега»).
Из анамнеза известно, что около 20 лет страдает сахарным диабетом 2 типа. Раньше лечился нерегулярно, диету не соблюдал. Последние годы принимает сахароснижающие препараты, инсулин. Год назад отметил повышение артериального давления, ухудшение зрения. В июле 2019 г. на первом пальце левой стопы появилась мозоль, которая постоянно увеличивалась в размерах. Два месяца назад после многодневной длительной ходьбы отметил появление язвы в центре мозоли. К врачам не обращался. Неделю назад отметил покраснение и отек 2 пальца левой стопы. На следующий день появились отек и гиперемия левой голени в нижней и средней третях, язва на 2 пальце левой стопы. Больной обратился в районную поликлинику, был осмотрен терапевтом и хирургом поликлиники, ему была выполнена рентгенография левой стопы, после чего больному было рекомендовано обратиться в центр диабетической стопы. Подолог после осмотра рекомендовал пациенту промывать язвы хлоргексидином. Назначенная терапия эффекта не дала, у больного появилась гипертермия выше 38,0 0С.
Получает биосулин Н 40 МЕ в сутки.
При осмотре: общее состояние относительно удовлетворительное. Повышенного питания. Кожные покровы и видимые слизистые обычной окраски, периферических отеков нет. В легких дыхание везикулярное, хрипов нет. ЧДД 18 в минуту. Тоны сердца приглушенные, ритмичные, акцент 2 тона над аортой. ЧСС 86 в мин, АД 160/100 мм рт. ст., живот правильной формы, равномерно участвует в акте дыхания, не вздут, при пальпации мягкий, безболезненный во всех отделах. Печень по краю реберной дуги, безболезненная при пальпации. Симптом Пастернацкого отрицательный с обеих сторон. Пульсация артерий нижних конечностей отчетливая на всех уровнях с обеих сторон. Патологических шумов над ними не выслушивается.
Status localis: диабетическая деформация обеих стоп, крючкообразные пальцы (Рис. 5). Левая стопа и голень до уровня средней трети пастозны, гиперемированы. Болевая чувствительность на обеих стопах отсутствует, тактильная чувствительность резко снижена. На медиальной поверхности 1 пальца левой стопы в области межфалангового сустава мозоль размером до 20 мм в диаметре. В центре мозоли располагается язвенный дефект 7 мм в диаметре и глубиной 5 мм без отделяемого, с вялыми грануляциями. При ревизии язвы пуговчатым зондом свищевых ходов не определяется. 2 палец левой стопы синюшно-багровой окраски, отечный, на медиальной поверхности щелевидный дефект 5 мм с незначительным гнойным отделяемым. При ревизии раны зондом в дне определяется кость. При проведении кюретажа раны ложкой Фолькмана удалена ногтевая фаланга с изъеденной суставной поверхностью. После промывания раны удалены несколько костных фрагментов размером до 1 мм. В рану введена марлевая турунда с раствором повидон-иод. Язва на 1 пальце очищена ложкой Фолькмана от старых грануляций и некротических тканей, промыта хлоргексидином, наложена повязка с повидоном. Необходимо отметить, что ткани обоих пальцев хорошо кровоточили. На рентгенограмме стопы отмечается остеомиелит ногтевой фаланги 2 пальца стопы, фаланги 1 пальца интактны. Поскольку больной категорически отказался от госпитализации, решено было осуществлять лечение на дому.
Диагноз: Сахарный диабет 2 типа, субкомпенсированный. Синдром диабетической стопы, нейропатическая форма. Нейропатическая язва 1 пальца левой стопы. Остеомиелит ногтевой фаланги 2 пальца левой стопы. Диабетическая нефропатия. Диабетическая ретинопатия.
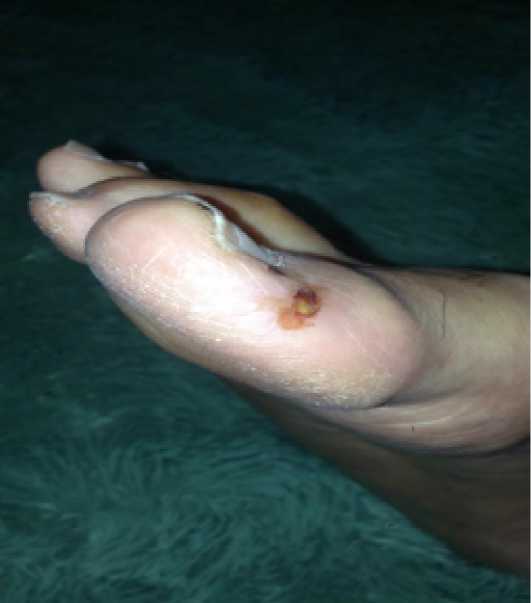
Рис. 5. Диабетическая стопа справа
Назначено: постельный режим, антибактериальная терапия аугментином 850+150 2 раза в сутки, метформин 1000 мг 2 раза в сутки, перевязки с повидоном 2 раза в сутки, обязательное ношение разгрузочного «башмака».
Гликемический профиль:
-
9 .00. — 9,4 ммоль/л
-
13 .00. — 10,6 ммоль/л
-
17 .00. — 9,8 ммоль/л
-
21 .00. — 9,2 ммоль/л
-
6 .00. — 8,7 ммол/л
Через двое суток гиперемия стопы и голени отсутствует, температура нормализовалась, отечности 2 пальца стопы не отмечалось, раны на обоих пальцах чистые, без гнойного отделяемого. Через 2 недели после начала лечения рана на 2 пальце зажила вторичным натяжением, ногтевая пластина сохранна.
Больному выполнено УЗДГ-исследование, по данным которого кровотоки в артериях нижних конечностей с обеих сторон в пределах нормы. Гемодинамически значимых изменений артерий не выявлено.
Через 3 недели язва на 1пальце левой стопы зажила с образованием гиперкератоза. Пациент вышел на работу в школу, продолжая носить ортез (Рис. 6) в течение месяца. В дальнейшем 6 месяцев жалоб не предъявлял.
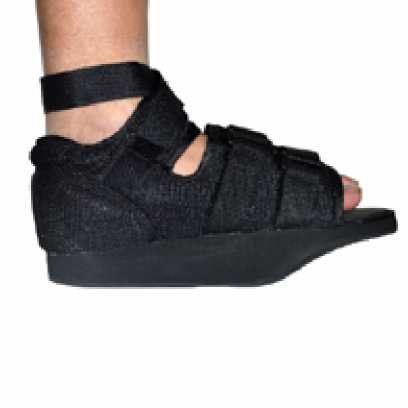
Рис.6. Ортез
В августе 2020 после двухнедельной экскурсии, сопровождавшейся длительной ходьбой, отметил почернение мозоли и появление геморрагического отделяемого.
При осмотре местно: мозоль на медиальной поверхности 1 пальца левой стопы в области межфалангового сустава с участком кровоизлияния, с гнойно-геморрагическим отделяемым со зловонным запахом (Рис. 7). Мозоль иссечена, проведена ревизия раны зондом. Затеков нет. Кость и суставная капсула не определяются. Грануляций нет. Рана промыта хлоргексидином, наложена повязка с повидоном.
Перевязки в течение двух недель с повидоном не принесли желаемого результата. Хотя гнойное отделяемое исчезло, но грануляции не появлялись несмотря на то, что при кюретаже раны ложкой Фолькмана отмечалась хорошая кровоточивость тканей. Допуская, что это связано с действием иодопирона на грануляции, было решено перейти на современные повязки «Гидроколл». Однако расположение язвенного дефекта в сочетании с постоянным хождением пациента нарушали положение самофиксирующей повязки и приводили к ее дислокации с места язвенного дефекта. В связи с этим было решено перейти на бинтовые повязки с 5% диоксидиновой мазью. Спустя неделю применения мази появились сочные грануляции, язвенный дефект стал уменьшаться в размере. Но категорический отказ от ортеза и продолжение работы, связанной с постоянной нагрузкой на стопу, привели к появлению радиальных трещин на оставшихся участках мозоли (Рис. 8).
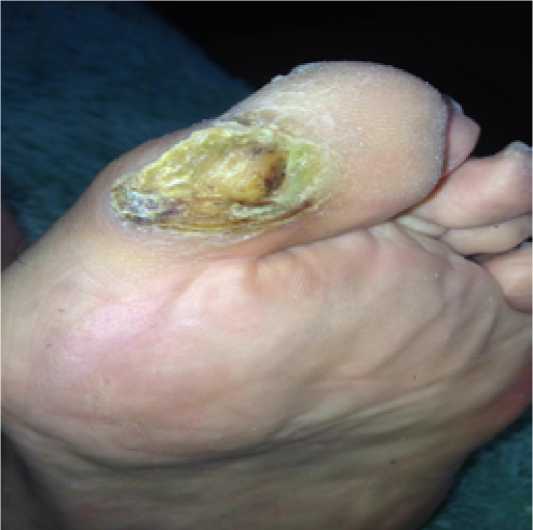
Рис. 7. Кровоизлияние в мозоль
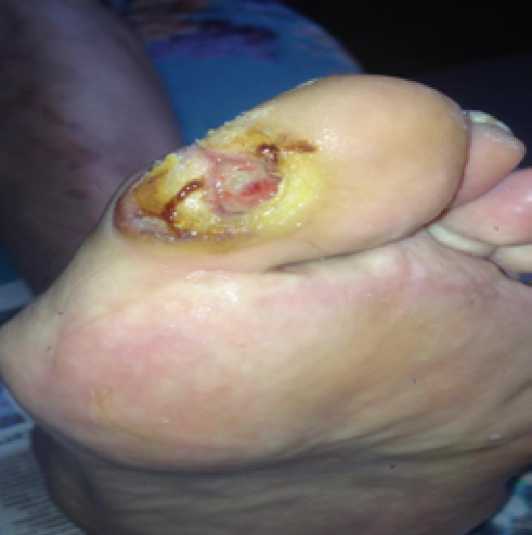
Рис. 8. Радиальные трещины на фоне гранулирующей раны
Только после того, как больной начал снова носить ортез, язва начала прогрессивно уменьшаться в размерах (Рис. 9). И спустя три месяца от начала лечения полностью зарубцевалась. К сожалению, окончательно справиться с гиперкератозом нам не удалось. Пациенту были даны разъяснения, о том, что в случае прекращения ношения ортеза до полного исчезновения гиперкератоза, язвенный дефект образуется вновь.
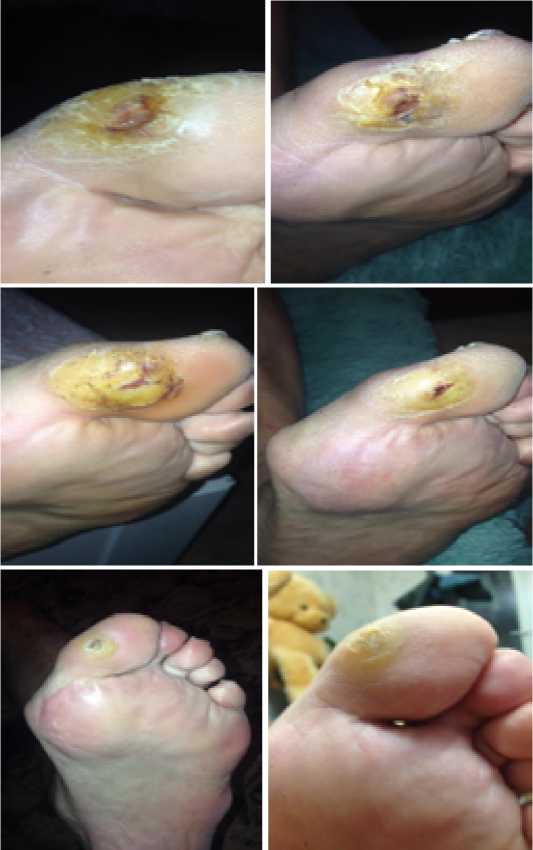
Рис. 9. Поэтапное заживление язвенного дефекта
Заключение
Данное клиническое наблюдение демонстрирует ошибки и сложности в лечении диабетической язвы стопы. Неправильная тактика врачей амбулаторного звена едва не привела к утере части конечности у пациента. Неадекватное отношение пациента к своему заболеванию усложнило и удлинило лечение язвенного дефекта. Успешное лечение трофических язв при нейропатической форме синдрома диабетической стопы зависит от согласованности всех участников процесса. Большая ответственность в этом вопросе ложится на медицинских работников амбулаторного звена. Только общие усилия позволят снизить инвалидизацию и смертность при таком серьезном осложнении сахарного диабета как диабетическая стопа.
Список литературы Лечение нейропатической плантарной язвы при синдроме диабетической стопы (клиническое наблюдение)
- Wild S., Roglic G., Green A., Sicree R., King H. Global prevalence of diabetes: estimates for the year 2000 and projections for 2030. Diabetes Care, 2004, Vol. 27, No. 5, рр. 1047–1053. https://doi.org/10.2337/diacare.27.5.1047
- Pokorna J. Importance of education in the prevention of diabetic foot syndrome. Neuro Endocrinol. Lett., 2017, Vol. 38, No. 4, рр. 255–256.
- Анциферов М.Б., Комелягина Е.Ю. Синдром диабетической стопы. М.: МИА, 2013. 304 с.
- Дедов И.И, Шестакова М.В., Викулова О.К. Эпидемиология сахарного диабета в Российской Федерации: клинико-статистический анализ по данным Федерального регистра сахарного диабета. Сахарный диабет, 2017. № 29 (1). С. 13–41.
- Rizzo L., Tedeschi A., Fallani E., Coppelli A., Vallini V., Iacopi E. et al. Custom-made orthesis and shoes in a structured follow-up program reduces the incidence of neuropathic ulcers in high-risk diabetic foot patients. Int. J. Low. Extrem. Wounds, 2012, Vol. 11, No. 1, рр. 59–64.
- Bus S.A., Lavery L.A., Monteiro-Soares M., Rasmussen A., Raspovic A., Sacco I.C.N. et al. On behalf of the International Working Group on the Diabetic Foot (IWGDF). IWGDF Guidelines on the Prevention and Management of Diabetic Foot Disease, 2019. URL: iwgdfguidelines.org
- Берсенева Е.А., Удовиченко О. Эффективность амбулаторного лечения синдрома диабетической стопы в повседневной практике кабинета «Диабетическая стопа»: когортное исследование. Сахарный диабет, 2014. № 3. С. 107–112.
- Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению. РМЖ, 2015. № 12. С. 768–770.
- Н.Д. Бабанов, Д.В. Фролов, Е.В. Крюков, Е.Н. Панова, О.В. Кубряк. Исследование регуляции двигательной нагрузки тренинга с визуальной обратной связью у пациентов с диабетической полинейропатией. Сахарный диабет, 2021.Т. 24. № 1. С. 55–61.
- Lavery L.A., LaFontaine J., Higgins K.R., Lanctot D.R., Constantinides G. Shear-reducing insoles to prevent foot ulceration in high-risk diabetic patients. Adv. Skin Wound Care, 2012, Vol. 25, No. 11, рр. 519–524.
- Morona J.K., Franks C.I., Betts R.P. et al. Comparison of the clinical effectiveness of different off-loading devices for the treatment of neuropathic foot ulcers in patients with diabetes: a systematic review and metaanalysis. Diabetes Metab. Res. Rev., 2013, Vol. 29, No. 3, рр. 183–193. https://doi.org/10.1002/dmrr.2386
- de Oliveira A.L., Moore Z. Treatment of the diabetic foot by offloading: a systematic review. J. Wound Care, 2015, Vol. 24, No. 12, рр. 560–562. https://doi.org/10.12968/jowc.2015.24.12.560
- Van De Weg F.B., Van De Windt D.A., Vahl A.C. Wound healing: total contact cast vs. custom-made temporary footwear for patients with diabetic foot ulceration. Prosthet. Orthot. Int., 2008, Vol. 32, No. 1, рр. 3–11. https://doi.org/10.1080/03093640701318672
- Götz J., Lange M., Dullien S., Grifka J., Hertel G., Baier C. et al. Off-loading strategies in diabetic foot syndrome-evaluation of different devices. Int. Orthopaed., 2016, No. 41, рр. 239–246. https://doi.org/10.1007/s00264-016-3358-1


