Лечение пациента с диссеминированной герминогенной опухолью яичка на фоне терминальной хронической болезни почек, требующей проведения гемодиализа
Автор: Абляметова А.С., Зоринова А.В., Летучих А.Н., Исраелян Э.Р., Царева А.С., Румянцев А.А.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Клинические случаи
Статья в выпуске: 3 т.14, 2024 года.
Бесплатный доступ
Среди онкологических пациентов существует когорта больных с терминальной хронической болезнью почек (ХБП), развившейся вследствие различных причин и требующей назначения гемодиализа. Проведение противоопухолевого лекарственного лечения при данном сопутствующем заболевании возможно, однако требует выбора наиболее оптимальных модифицированных режимов химиотерапии (ХТ) с целью достижения максимальной эффективности и минимизации токсичности лечения. В данном клиническом случае мы описываем наш лечебный подход для пациента, находящегося на гемодиализе, с метастатической несеминомной герминогенной опухолью (ГО) яичка неблагоприятного прогноза по классификации International Germ Cell Cancer Collaborative Group (IGCCCG). Нами был проведен анализ литературных данных, отражающих применение различных лекарственных препаратов и режимов ХТ, используемых для лечения ГО у пациентов с ХБП.
Герминогенная опухоль, химиотерапия, хроническая болезнь почек, гемодиализ
Короткий адрес: https://sciup.org/140310096
IDR: 140310096 | DOI: 10.18027/2224-5057-2024-019
Treatment of a patient with disseminated testicular germ cell tumor associated with terminal chronic kidney disease requiring hemodialysis
There is a cohort of cancer patients with terminal chronic kidney disease (CKD) due to various causes and requiring hemodialysis. Antitumor drug therapy in this concomitant disease is possible, but requires selection of the most optimal modified chemotherapy (CT) regimens to maximize efficacy and minimize treatment toxicity. In this case report we describe our therapeutic approach for a patient on hemodialysis with a metastatic non-seminomatous germ cell tumor (GCT) of the testis of poor prognosis according to the International Germ Cell Cancer Collaborative Group (IGCCCG) classification. We analyzed the literature datareflecting the use of different drugs and CT regimens used for the treatment of GCT in patients with CKD.
Текст научной статьи Лечение пациента с диссеминированной герминогенной опухолью яичка на фоне терминальной хронической болезни почек, требующей проведения гемодиализа
ГО являются сравнительно редкой патологией, составляя около 1 % всех злокачественных новообразований, однако это наиболее частые опухоли у мужчин в возрасте 20–35 лет. Цисплатин-содержащая ХТ для пациентов с данным заболеванием позволяет достичь высокой частоты объективных ответов, что ассоциировано с улучшением отдаленных результатов лечения. Таким образом, ХТ является неотъемлемым компонентом в лечении ГО, одним из важных аспектов эффективности которой является соблюдение адекватной дозоинтенсивности несмотря на токсичность проводимой терапии [4,5]. Для других видов злокачественных новообразований стратегии по минимизации нежелательных явлений (НЯ) ХТ могут включать как отсрочки в лечении, так и снижение доз препаратов, однако эти варианты не приемлемы для пациентов с агрессивно протекающими ГО, так как могут вызвать резистентность к проводимой терапии [6].
Стандартным подходом для пациентов неблагоприятного прогноза по классификации IGCCCG является проведение 4 курсов ХТ в режиме ВЕР (блеомицин, этопозид, цисплатин), позволяющих обеспечить 5-летнюю общую выживаемость равную 67% [7]. При противопоказаниях к назначению блеомицина возможно проведение 4 курсов ХТ в режимах PEI (цисплатин, этопозид, ифосфамид) или TIP (паклитаксел, ифосфамид, цисплатин). При схожей эффективности обе комбинации являются более миело-токсичными [7,8].
Таким образом, стандартный подход к лекарственному лечению метастатических ГО хорошо известен. Однако существует когорта пациентов с ХБП, развившейся вследствие различных причин (сопутствующая патология, нефриты, лекарственное повреждение почек, нарушение физиологического пассажа мочи из-за обструкции мочевых путей), которым требуется проведение ХТ по поводу ГО. Проведение заместительной почечной терапии в виде гемодиализа позволяет преодолеть у данных пациентов ограничения к назначению цисплатина, связанные со сниженной скоростью клубочковой фильтрации, однако у них повышается риск развития гематологических НЯ. Ограниченные и противоречивые данные о концентрациях химиотерапевтических препаратов и их клиренсе в таких ситуациях затрудняют принятие решения в выборе оптимального режима ХТ, изменении дозы того или иного препарата. В исследовании CANDY, изучавшем проведение ХТу пациентов с почечной недостаточностью, получающих гемодиализ, продемонстрировано, что у 44% пациентов развилась токсичность вследствие недостаточной коррекции дозы химиопрепаратов ввиду отсутствия единых рекомендаций для данной группы пациентов [9].
КЛИНИЧЕСКИЙ СЛУЧАЙ
Пациенту Н., 46 лет, в марте 2018 года был установлен диагноз «Гранулематоз Вегенера с поражением почек (гломерулонефрит) и легких (пульмонит)», других проявлений заболевания отмечено не было. Получал специфическую терапию системными глюкокортикостероидами (ГКС) и ритуксимабом. С мая 2019 года находился на программном гемодиализе по поводу быстропрогрессирующего гломерулонефрита, ХБП 5-й стадии. При обследовании в рамках подготовки к трансплантации почки была выявлена опухоль правого яичка, метастазы в забрюшинных лимфатических узлах, легких. Пациент обследован:
-
• Ультразвуковое исследование (УЗИ) мошонки от 30.06.2020: в правом яичке образование до 41 мм;
-
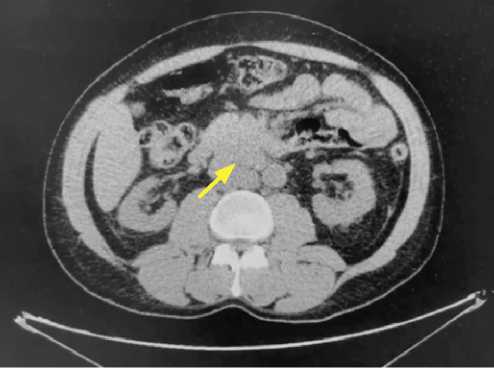
• Компьютерная томография (КТ) органов грудной клетки, органов брюшной полости, органов малого таза от 14.07.2020: в легких множественные метастазы до 10 мм; увеличенные забрюшинные лимфатические узлы (парааортальные, паракавальные) до 40 мм, подвздошный лимфатический узел справа до 14 мм (рис. 1);
-
• Концентрация опухолевых маркеров от 15.07.2020: альфа-фетопротеин (АФП) — 1062,38 нг/мл, бета-субъединица хорионического гонадотропина человека (бета-ХГЧ) — 30075 мМе / мл.
По месту жительства на первом этапе была выполнена орхофуникулэктомия (ОФЭ) справа 22.07.2020. По данным гистологического исследования образование представлено ГО смешанного строения, состоящей из эмбриональной карциномы (75 %), опухоли желточного мешка (10%), постпубертатной зрелой тератомы (10%), элементов трофобласта (5%), с лимфоваскулярной инвазией, с распространением в семенной канатик. При этом при контроле концентрации опухолевых маркеров от 14.08.2020 был выявлен рост концентрации АФП до 1853 нг/мл, бета-ХГЧ до 126165 мМе/мл, активности лактатдегидрогеназы (ЛДГ) до 1560 Ед /л (верхняя граница нормы 450 Ед/ л). Таким образом, пациенту был установлен диагноз — несемином-ная ГО правого яичка рТ3N2M1aS3 (IIIC стадия), неблагоприятный прогноз по IGCCCG.
Для дальнейшего лечения пациент обратился в НМИЦ онкологии имени Н.Н. Блохина. На момент обращения состояние пациента оценено как удовлетворительное, жалобы на боли в поясничной области и в паховой об-
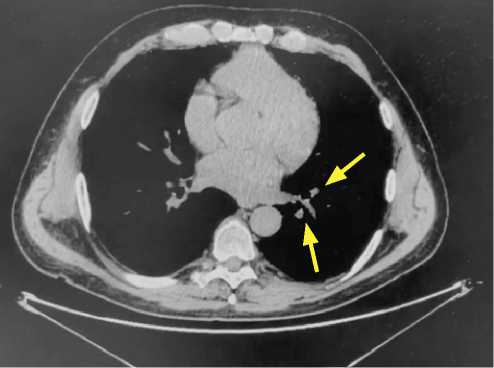
Рисунок 1. КТ перед началом лечения
Figure 1: CT scan before the start of treatment
ласти справа. По данным лабораторных исследований от августа 2020 года: анемия 2-й степени (гемоглобин 81 г/л), ХБП 5-й стадии (креатинин — 785 мкмоль/л, СКФ (по формуле СKD-EPI) — 6 мл/мин / 1,73 м 2 ).
По данным магнитно-резонансной томографии головного мозга от 15.08.2020: без патологии.
Учитывая неблагоприятный прогноз по IGCCCG, высокий уровень бета-ХГЧ, сопутствующую патологию (ХБП 5-й стадии), требующую проведения гемодиализа, было принято решение провести 1-й курс ХТ в стабилизационном режиме ЕР: этопозид 100 мг/м 2 в/в капельно + цисплатин 20 мг/м 2 в/в капельно в дни 1–3 на фоне проведения гемодиализа через час после окончания ХТ.
С 20.08.2020 по 24.08.2020 проведен 1 курс в режиме ЕР с последующими сеансами гемодиализа и с поддержкой гранулоцитарным колониестимулирующим фактором (Г-КСФ). Гемодиализ проводился на аппарате 4008S на диализаторе Fх100 с использованием бикарбонатного картриджа Bi-Bag (бикарбонатный сухой гранулированный 8,4 % концентрат). В качестве сосудистого доступа использовали артерио-венозную фистулу нижней трети левого предплечья, обеспечивающую скорость кровотока 240 мл/мин, общая антикоагуляция — 3500 Ед гепарина.
В межкурсовом интервале после 1 курса отмечено развитие гематологической токсичности (анемия 3 степени, нейтропения 3 степени), потребовавшей гемотрансфузии 2 доз эритроцитной взвеси, клинически отмечена положительная динамика в виде уменьшения болевого синдрома в поясничной области.
Пациент обсужден на онкологическом консилиуме, учитывая невозможность использования блеомицина ввиду высокого риска развития пульмональной токсичности в данной клинической ситуации (блеомицин не подвергается гемодиализу, возраст пациента старше 40 лет, метастатическое поражение легких, риск развития пульмонита на фоне гранулематоза Вегенера), принято решение о продолжении лечения в режиме TIP: пакли- таксел 120 мг/м2 в/в капельно в день 1 и 2 + ифосфамид 1500 мг/м2 в / в капельно (+ месна 100 % дозы ифосф-амида в/в) во 2–5 дни + цисплатин 25 мг/м2 в/в капельно во 2–5 дни, с 6 по 10 день — первичная профилактика фебрильной нейтропении (ФН) Г-КСФ.
С 04.09.2020 по 10.09.2020 проведен 1 курс в режиме TIP (суммарно 2 курс). Гемодиализ проводился в дни введения цисплатина через 1 час после окончания ХТ. Межкурсовой интервал осложнился развитием тромбоцитопении 4 степени с геморрагическим синдромом в виде носовых кровотечений, ФН 4 степени, сепсиса, что потребовало массивной сопроводительной терапии в условиях отделения реанимации и интенсивной терапии.
Учитывая дозолимитирующую токсичность проводимого лечения, было принято решение о редукции дозы паклитаксела до 175 мг/м 2 в день 1 и отмене 5 дня ХТ со 2 курса, что соответствует 25% редукции дозы цисплатина и ифосфамида. С 01.10.2020 по 05.10.2020 проведен 2 курс ХТ в режиме TIP с редукцией доз (суммарно 3 курс). После 2 курса ХТ было отмечено развитие анемии 2 степени.
С 20.10.2020 по 25.10.2020 проведен 3 курс ХТ в модифицированном режиме TIP (суммарно 4 курс). Межкурсовой интервал осложнился развитием артралгии 2 степени, полинейропатии 1 степени, анемии 2 степени, тромбоцитопении 3 степени, что привело к задержке очередного курса ХТ на 6 суток. Принимая во внимание гематологическую токсичность проводимого лечения, приведшую к задержке лечения, было решено провести 4 курс в режиме TIP с редукцией дозы ифосфамида до 1200 мг/м 2 в дни 2–4. С 17.11.2020 по 20.11.2020 проведен 4 курс ХТ 1 линии, без осложнений. Запланированное противоопухолевое лекарственное лечение было завершено в полном объеме.
Динамика опухолевых маркеров на фоне проведения ХТ 1-й линии представлена на графике 1.
По данным КТ через 3 недели после окончания ХТ отмечено значительное уменьшение количества и размеров
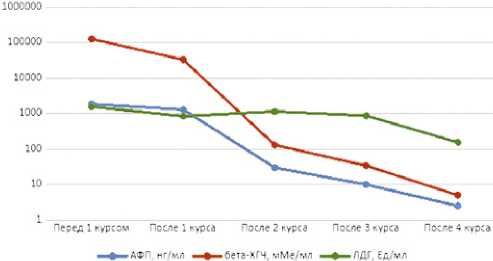
График 1. Динамика онкомаркеров на фоне ХТ
Diagram 1. Dynamics of oncomarkers during chemotherapy рассеянных мелких очагов в обоих легких, крупный участок инфильтрации в верхней доле слева практически перестал определяться; увеличенных забрюшинных лимфатических узлов не выявлено (рис. 2).
Уровень онкомаркеров от 12.12.2020 — в пределах нормы.
На момент последнего контакта с пациентом (май 2024 года) данных за прогрессирование заболевания, проявления поздней токсичности проводимой терапии не было. Пациент продолжает получать специфическую иммуносупрессивную терапию системными ГКС ежедневно и заместительную почечную терапию в виде гемодиализа 3 раза в неделю по поводу гранулематоза Вегенера.
Принимая во внимание отсутствие данных за прогрессирование ГО яичка в течение более 3 лет, наличие гранулематоза Вегенера в стадии ремиссии и терминальной ХБП, требующей проведения еженедельного гемодиализа, рекомендована трансплантация почки. На данный момент пациент включен в лист ожидания трансплантации донорской почки.
ОБСУЖДЕНИЕ
Данный клинический случай демонстрирует возможный вариант лечения пациента с ГО и ХБП, получающего гемодиализ. Несмотря на редукцию доз и развитие НЯ, у пациента был достигнут полные маркерный и радиологический ответы. ГО являются курабельным заболеванием даже при диссеминированных формах в связи с высокой чувствительностью к цисплатин-содержащей ХТ. Исключение данного препарата из схемы лечения значимо ухудшает отдаленные результаты [10]. Для пациентов с терминальной ХБП, получающих программный гемодиализ, нефротоксичность, связанная с цисплатином, уже не является лимитирующим фактором. Но данная когорта пациентов более подвержена другим дозозависимым НЯ, таким как миелосупрессия и нейропатия [11]. Ввиду быстрого и прочного связывания цисплатина с белками плазмы крови его элиминация посредством гемодиализа наиболее эффективна при сокращении интервала между введением препарата и началом гемодиализа, ведь именно связанная фракция оказывает большее влияние на развитие НЯ. Поэтому у больных с терминальной ХБП целесообразно снижение дозы препарата не менее, чем на 50% и немедленное проведение гемодиализа после ХТ (в течении 3 часов после окончания лечения). Однако такое снижение дозы цисплатина несет риск развития лекарственной резистентности [12,13]. Таблица 1 отражает сравнительную характеристику препаратов, используемых при лечении ГО, и их рекомендуемые дозы при лечении пациентов, находящихся на гемодиализе [14–16].
Ввиду отсутствия консенсуса по тактике ведения данной когорты пациентов ранее опубликованные клинические случаи отражают различные подходы к лечению. В одном из описанных наблюдений пациенту с внегонад-ной ГО средостения и терминальной ХБП на первом этапе было выполнено хирургическое лечение в объеме удале-
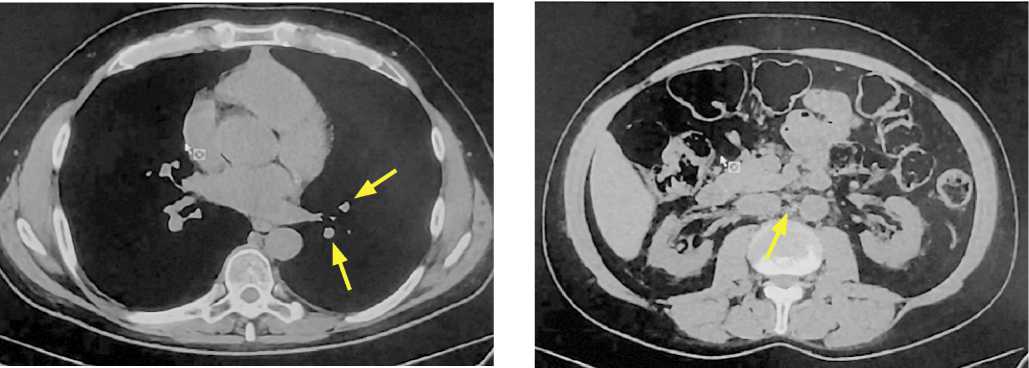
Рисунок 2. КТ после окончания лечения
Figure 2: CT scan after the treatment completion
ния опухоли средостения с последующим проведением ХТ в режиме ЕР с редукцией доз препаратов (цисплатина на 50 % и этопозида на 40%) в дни 1–5 и с Г-КСФ профилактикой. При попытке эскалации доз до 75 % от стандартных отмечена панцитопения 3–4 степени. При сроке наблюдения за пациентом 12 месяцев не отмечено прогрессирования заболевания [17].
Kieran J. Moore с соавторами представили несколько иной подход. Пациенту с несеминомной ГО яичка неблагоприятного прогноза по IGCCCG и ХБП 5 стадии после ОФЭ проводилась ХТ в режиме ЕР со стандартной дозой цисплатина (20 мг/м 2 ) и редукцией дозы этопозида на 40% (60 мг / м 2 ) в дни 1–5 на фоне Г-КСФ профилактики. Гемодиализ проводился в дни ХТ через 1 час после ее завершения. Лечение осложнилось ФН 3 степени и сенсорной нейропатией нижних конечностей 3 степени, приведшей к ограничению двигательной активности. В течение 10-летнего периода наблюдения отмечена некоторая регрессия нейропатии, тем не менее пациент нуждается в посторонней помощи, признаков прогрессирования ГО не отмечено [11].
Michael Froehner и соавторы описывают клинический случай пациента с ГО яичка и терминальной ХБП, которому проводилась ХТ в режиме ЕР с редукцией дозы цисплатина на 50% (10 мг/м 2 ) и дозы этопозида на 40 % (60 мг / м 2 ) в дни 1–5 с последующей эскалацией до режима PEI с 3 курса на фоне Г-КСФ профилактики. Гемодиализ проводился через 1 час после завершения ХТ. Межкурсовой интервал (после 3 курса в режиме PEI) осложнился развитием облитерирующего бронхиолита с организующейся пневмонией, приведшие к задержке 4 курса ХТ на 2 месяца. В течение следующего курса (с редукцией дозы ифосфамида на 25%) отмечен эпизод эпилепсии. По завершении ХТ 1 линии был достигнут полный маркерный ответ, через 15 месяцев после завершения лечения данных за прогрессирование не получено [18].
Принимая во внимание высокие риски развития кровотечения, синдрома распада опухоли, инфекционных осложнений, наличие у пациента ХБП, требующей проведения гемодиализа, первый курс ХТ в представленном нами клиническом случае был проведен в режиме EP с редукцией доз препаратов на 40 %.
В собственном ретроспективном исследовании, проведенном на базе онкоцентра имени Н. Н. Блохина, включавшем пациентов с ГО и тяжелым соматическим статусом и/или сверхвысокой концентрацией опухолевых маркеров, было продемонстрировано, что проведение первого цикла ХТ в режиме ЕР с редукцией доз (так называемый «стабилизационный» курс) позволило снизить число жизнеугрожающих осложнений с 76 % до 44% без ухудшения общей выживаемости (отношение рисков 0,99, 95 % доверительный интервал 0,44–2,26) в сравнении с историческим контролем (ХТ в полных дозах). После проведения 1 курса в стабилизационном режиме и улучшения общего состояния пациента лечение продолжалось согласно прогнозу по IGCCCG [19].
Безусловно, стандартом 1 линии ГО неблагоприятного прогноза является 4 курса ХТ в режиме BEP [20]. Однако в данном случае применение блеомицина было ограничено тем фактом, что препарат не подвергается гемодиализу, обуславливая крайне высокий риск развития фатального пульмонита [21]. Альтернативой ХТ в режиме BEP является ифосфамид-содержащие схемы [22,23]. Прямое сравнение режимов BEP и TIP в 1 линии ХТу пациентов с промежуточным и неблагоприятным прогнозами по IGCCCG показало их равную эффективность (одногодичная выживаемость без прогрессирования в обеих группах 72%) при большей гематологической токсичности последнего [23].
После 2 лет наблюдения кривая выживаемости пациентов с ГО выходит на плато и риск дальнейшего прогрессирования крайне низок. В нашем случае на качество жизни и прогноз значительное влияние оказывает терминальная ХБП, в связи с чем было рекомендовано рассмотрение возможности выполнения трансплантации почки.
Данное клиническое наблюдение демонстрирует важность терапии больных с ГО и тяжелой сопутствующей патологией в специализированных центрах, имеющих достаточный опыт в лечении данной когорты пациентов [24,25].
ВЫВОДЫ
Наш клинический случай описывает возможный вариант лечения пациента с распространенной ГО яичка и терминальной ХБП, требующей проведение гемодиализа, с достижением полного ответа. Однако токсичность проводимого лечения показывает необходимость более подробного изучения измененной фармакокинетики химиопрепаратов, разработки оптимальных модифицированных режимов ХТ для пациентов со злокачественными заболеваниями, находящихся на гемодиализе, с целью достижения наилучших отдаленных результатов лечения при минимизации токсичности терапии.


