Лечение предсердных тахиаритмий у грудного ребенка
Автор: Баталов Роман Ефимович, Арчаков Евгений Александрович, Якимова Евгения Валентиновна, Свинцова Лилия Ивановна, Усенков Станислав Юрьевич, Бочаров Сергей Николаевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Случай из практики
Статья в выпуске: 1 т.30, 2015 года.
Бесплатный доступ
Представлен клинический случай лечения предсердных тахиаритмий у грудного ребенка. В течение госпитализации выполнялось катетерное лечение внутрипредсердной тахикардии и трепетания предсердий, подбор антиаритмической терапии.
Радиочастотная аблация, внутрипредсердная тахикардия, трепетание предсердий
Короткий адрес: https://sciup.org/14919994
IDR: 14919994 | УДК: 616.125.3
Treatment of atrial tachyarrhythmia in an infant
The article presents a clinical case of treatment of atrial tachyarrhythmias in an infant. During the hospitalization, catheter ablation of atrial tachycardia and atrial flutter was performed and antiarrhythmic therapy was selected.
Текст научной статьи Лечение предсердных тахиаритмий у грудного ребенка
Данные о распространенности аритмий в детском возрасте свидетельствуют, что нарушения функции синусового узла встречаются у 9% новорожденных, суправентрикулярная экстрасистолия отмечается у 40–77% детей, желудочковая экстрасистолия – у 14–57%, атриовентрикулярная блокада I–III степени имеет место у 11– 37% детей, брадиаритмии – у 0–2%, пароксизмальная тахикардия встречается с частотой 1:3000, а различные варианты желудочковых тахикардий – у 3% детей в возрасте до 16 лет [3].
Наиболее частыми и клинически значимыми нарушениями ритма у детей младшего возраста являются суправентрикулярные тахикардии (СВТ). Примерно у 50% детей СВТ диагностируются в неонатальном периоде. В структуре СВТ преобладают внутрипредсердные тахикардии, которые являются наиболее частыми хроническими и непрерывно рецидивирующими нарушениями сердечного ритма в возрасте до 3 лет, составляя вместе с синдромом Вольфа–Паркинсона–Уайта (WPW) 90–92% всех СВТ у детей раннего возраста.[1]. Согласно исследованиям J.C. Salerno и соавт. [10], признаки аритмогенной кардиомиопатии (АКМП) и недостаточность кровообращения в конечном итоге регистрировались у 50–80% пациентов с непрерывно рецидивирующей предсердной тахикардией. Проспективные наблюдения за детьми 2–10 лет с предсердными тахикардиями показали, что даже при частоте сердечных сокращений (ЧСС) 150 уд./мин АКМП развивается в течение 5 мес. у 62% детей, независимо от возраста и пола ребенка.
Нарушения ритма сердца у детей первого года жизни весьма разнообразны. Многие из них нестойкие и исчезают в течение первых месяцев жизни, что объясняется незавершенностью формирования проводящей системы сердца к моменту рождения ребенка.
Резюмируя разноречивые данные о структуре СВТ у детей раннего возраста, можно заключить, что внутри-предсердные тахикардии являются наиболее частыми хроническими и непрерывно рецидивирующими нарушениями сердечного ритма у детей до года.
Ведущим этиопатогенетическим фактором развития аритмии у детей раннего возраста является наличие арит-могенного субстрата. Одна из самых распространенных в настоящее время гипотез рассматривает нарушения онтогенеза структур сердца как причину возникновения предсердных эктопий [7]. Нарушение процессов формирования проводящего миокарда приводит к сохранению отдельных клеток, способных при соответствующих условиях приводить к возврату их эктопической активности [6, 8].
Среди органических заболеваний сердца, предрасполагающих к реализации аномальных электрофизиологических механизмов возбуждения миокарда, следует отметить врожденные пороки сердца, врожденный кардит, кардиомиопатии. Провоцирующими аритмогенную активность миокарда факторами могут служить сепсис, гипогликемия, транзиторные гипо- и гипертиреоз, дист-
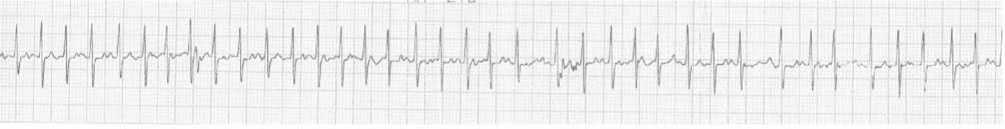
Рис 1. Фрагмент ЭКГ пациентки при поступлении (отведение V3, 25 мм/с). Внутрипредсердная тахикардия с ЧСС 216 уд./мин
ресс-синдром, заболевания легких и т.д. Результаты морфологических исследований аритмогенного миокарда показывают, что в ряде случаев он является следствием диффузного перерождения большой зоны, в частности стенок предсердий.
Особенностью клинического течения аритмии у детей является быстрое развитие явлений недостаточности кровообращения. Лечение тахиаритмии у детей первых лет жизни является чрезвычайно трудной задачей.
Приводим собственное клиническое наблюдение.
Пациентка Т. в возрасте 60 дней была доставлена в отделение детской кардиологии реанимационной бригадой. Из анамнестических данных известно, что ребенок от первой беременности, протекавшей на фоне туберкулеза у матери, диагностированного в первом триместре. Терапию противотуберкулезными препаратами мать получала в течение 7 мес. внутриутробного развития ребенка. Тахикардия у плода была выявлена внутриутробно, в связи с чем родоразрешение было выполнено путем большого кесарева сечения в 37 недель. Масса тела при рождении 2580 г, что соответствует нормальному соотношению гестационного срока и веса при рождении. В раннем постнатальном периоде ребенок был госпитализирован в стационар по месту жительства с диагнозом: Многофокусная предсердная пароксизмальная тахикардия. Учитывая факт антенатальной манифестации тахикардии, возникло предположение об инфекционном генезе развития нарушения ритма сердца. В связи с этим ребенок был обследован на наличие внутриутробных инфекций. Был проведен иммуноферментный анализ крови, результатами которого явилось обнаружение иммуноглобулинов класса G к цитомегаловирусу и вирусу простого герпеса, IgM не обнаружены, что свидетельствовало об инфекции у матери. В последующем через 3 мес. ребенок был обследован на наличие иммуноглобулинов класса М к цитомегаловирусу и вирусу простого герпеса. Результат был отрицательным. Следует отметить, что на протяжении всего периода пребывания пациентки в стационаре биохимических маркеров и данных в общем анализе крови за острое воспаление не было. Имела место умеренная анемия, по поводу чего был назначен мальтофер 3 мл per os в сутки. На момент поступления зарегистрирована внутрипредсердная тахикардия (рис. 1).
Состояние ребенка оценивалось как тяжелое в связи с наличием тахикардии, сопровождающейся клиническими признаками недостаточности кровообращения, функциональный класс IIA. Кожные покровы мраморные, сухие, чистые. При аускультации легких дыхание пуэриль-ное. Частота дыхательных движений (ЧДД) в покое 60 уд./мин. Тоны громкие, аритмичные. ЧСС 216 уд./мин. SpO2 98%. Артериальное давление (АД) 65/40 мм рт. ст.
Пульс на лучевых и бедренных артериях симметричный удовлетворительного наполнения. Живот мягкий, отмечается увеличение печени до 4 см из-под реберной дуги. Вес 3,9 кг. Проведено холтеровское мониторирование (рис. 2). Зарегистрирована постоянная предсердная тахикардия с проведением 2:1 с эпизодами аберрантного проведения на желудочки с ЧСС 280 уд./мин, редко синусовый ритм. Среднесуточная ЧСС 168 уд./мин – значительно выше возрастной нормы. Кроме стандартных размеров и объемов камер для динамической оценки показателей ЭхоКГ мы использовали отклонение объемов камер сердца от индивидуально прогнозированных антропометрических норм, выраженное в процентах. Такой подход принят для динамической оценки показателей ЭхоКГ в связи с увеличением размеров сердца при изменении возраста и антропометрических данных [2]. В связи с признаками нарушения кровообращения в виде снижения АД и одышки в покое, а также рефрактерностью к проводимой антиаритмической терапии, в том числе кор-дароном в дозе до 10 мг/кг/сутки, проводимой с момента установки диагноза, было решено провести электро-импульсную терапию. В условиях внутривенной седации пропофолом выполнено 3 попытки синхронизированной кардиоверсии, однако во всех случаях отмечался кратковременный эффект с повторным перезапуском тахикардии.
В отделении проводился подбор антиаритмической терапии: пропанорм 10 мг/кг/сутки в течение 3 дней, дигоксин 0,025 мг/кг/сутки, анаприлин 2 мг/кг/сутки, амиодарон 5–10 мг/кг/сутки. Монотерапия антиаритми-ческими препаратами была неэффективна, в связи с чем использовалась комбинированная терапия: дигоксин и анаприлин в стандартных дозах, которая также не дала нужного эффекта. При первоначальном назначении каждого нового антиаритмического препарата или комбинаций препаратов отмечался кратковременный контролирующий эффект, заключающийся в уменьшении среднесуточной ЧСС, преимущественно за счет замедления проведения по атриовентрикулярному (АВ) соединению до 2:1, с последующим восстановлением до 1:1. Учитывая рефрактерность тахикардии к медикаментозной терапии, сопровождающейся клиническими симптомами недостаточности кровообращения, признаками аритмогенной кардиомиопатии по данным ЭхоКГ, заключающимся в увеличении объемов предсердных камер, умеренной депрессии сократительной функции левого желудочка (ЛЖ), в возрасте 2 мес. было решено провести радиочастотную аблацию (РЧА).
При операции использовалась комбинированная анестезия. Под местной инфильтрационной анестезией раствором новокаина 0,5% – 10 мл по методике Сельдинге-
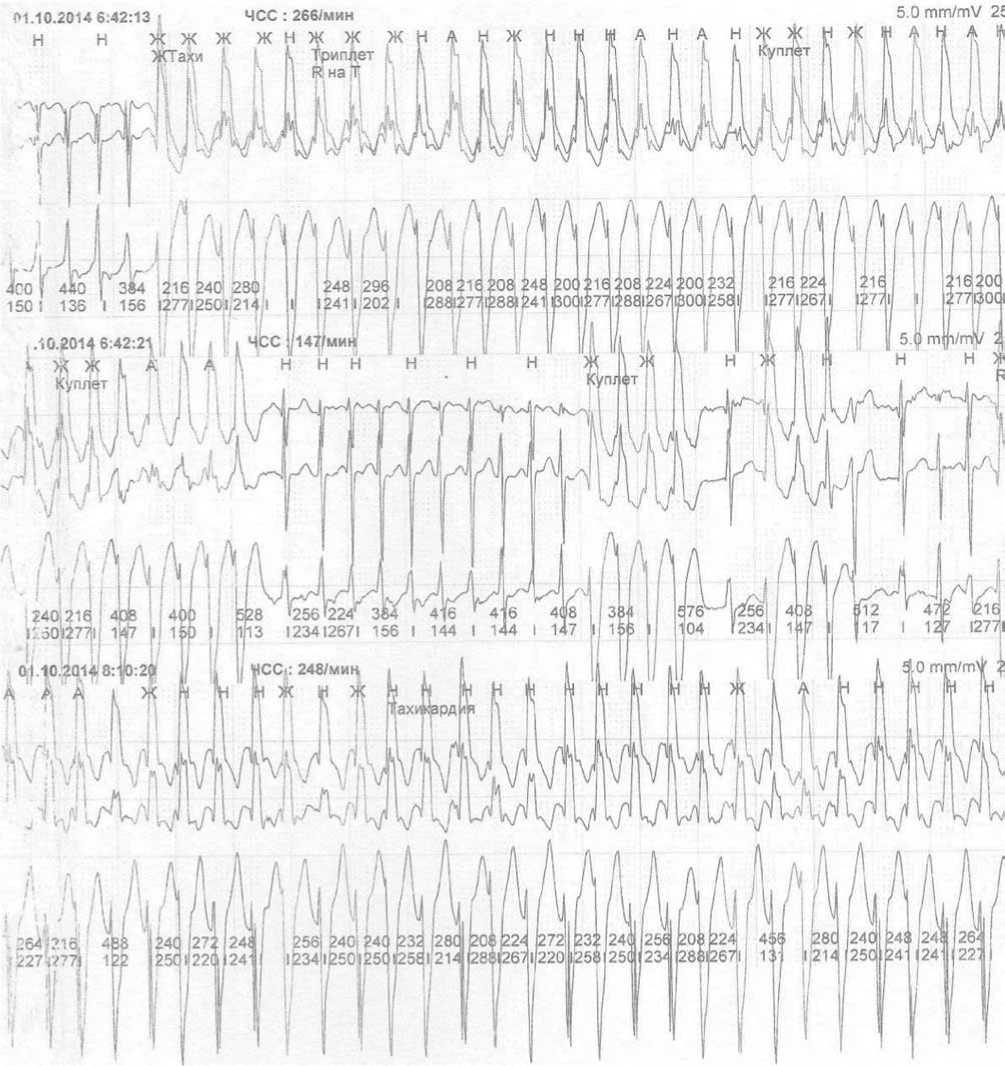
Рис. 2. Фрагмент суточного мониторирования ЭКГ
ра выполнена пункция бедренных вен слева и справа, установлены интродьюсеры, через которые в полость сердца проведено 2 электрода – один диагностический 5 Fr QUAD JOS (Bard, USA) и управляемый 5 Fr Marinr MC (Medtronic, USA). Диагностический электрод установлен на свободную стенку правого предсердия. Документирована непрерывно-рецидивирующая правопредсердная тахикардия с циклом 120 мс, в том числе и с аберрантным проведением на желудочки, которая трансформировалась в типичное трепетание предсердий сначала по часовой, затем против часовой стрелки с циклами 150 и 185 мс соответственно (рис. 3–5).
На кава-трикуспидальный истмус нанесена серия РЧ- аппликаций, параметры аблации: мощность 15 Вт, температура 50 оС. Сформирована линия от клапана до нижней полой вены. Трепетание предсердий трансформировалось в правопредсердную тахикардию.
Выполнено картирование правого предсердия. В месте наиболее раннего возбуждения – нижняя треть задне-боковой стенки правого предсердия – нанесено РЧ-воздействие. Тахикардия купирована (рис. 6). Сохранялись эпизоды частой предсердной экстрасистолии, в том числе и залповой.
При повторном картировании правого предсердия выявлена область наиболее раннего возбуждения в области ушка правого предсердия, куда и нанесена серия ап-
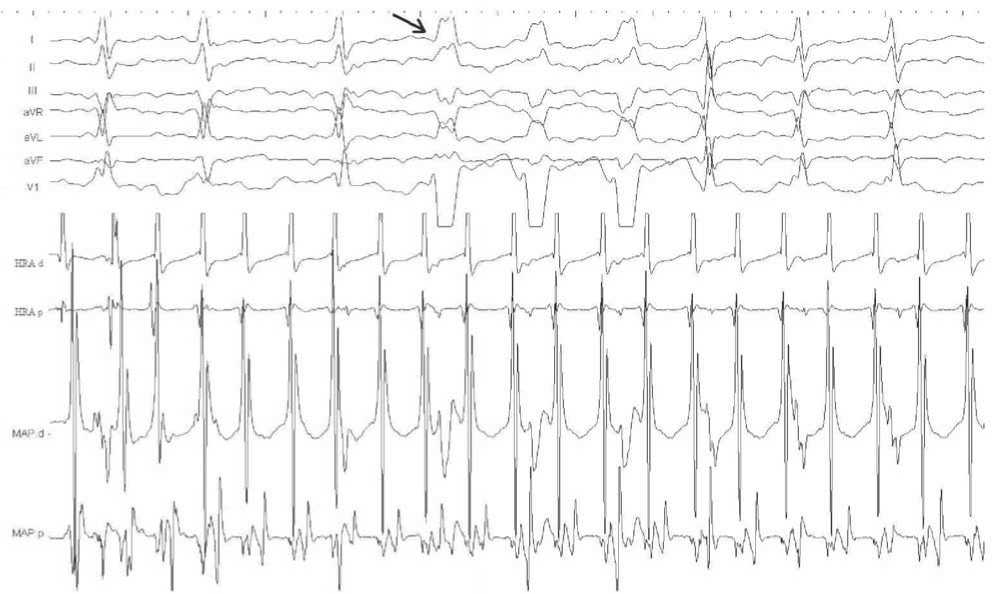
Рис. 3. Фрагмент внутрисердечного электрофизиологического исследования (ВСЭФИ), 100 мм/с. Правопредсердная тахикардия с циклом 120 мс, эпизод с аберрантным проведением на желудочки – указан стрелкой. I, II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, V1 – первое грудное отведение, HRA d, HRA p – дистальный и проксимальный полюсы электрода, расположенного в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
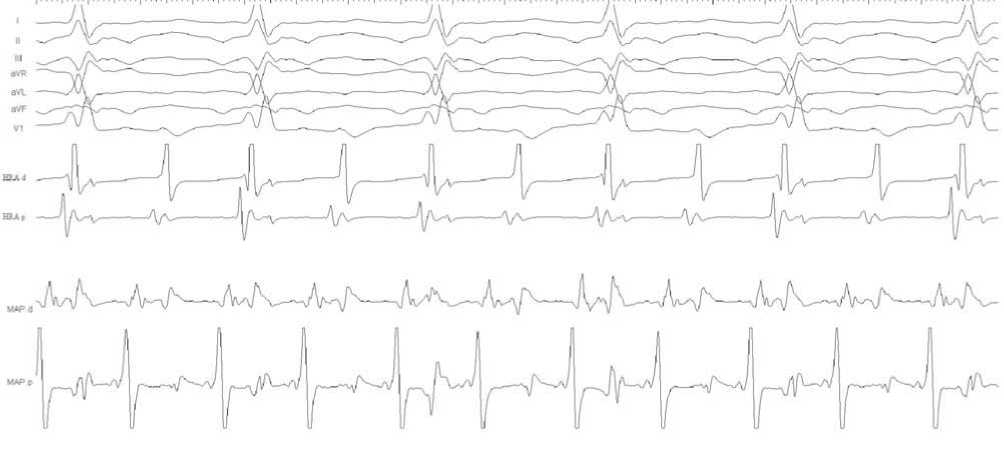
Рис. 4. Фрагмент внутрисердечного электрофизиологического исследования (ВСЭФИ), 100 мм/с. Типичное трепетание предсердий с циклом 185 мс. I, II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, V1 – первое грудное отведение, HRA d, HRA p – дистальный и проксимальный полюсы электрода, в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
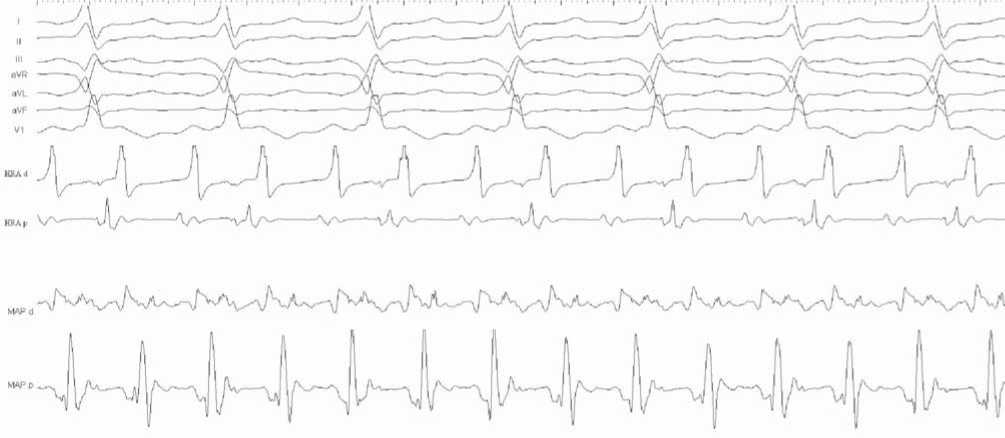
Рис. 5. Фрагмент внутрисердечного электрофизиологического исследования (ВСЭФИ), 100 мм/с. Трепетание предсердий с циклом 150 мс. I, II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, V1 – первое грудное отведение, HRA d, HRA p – дистальный и проксимальный полюсы электрода, расположенного в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
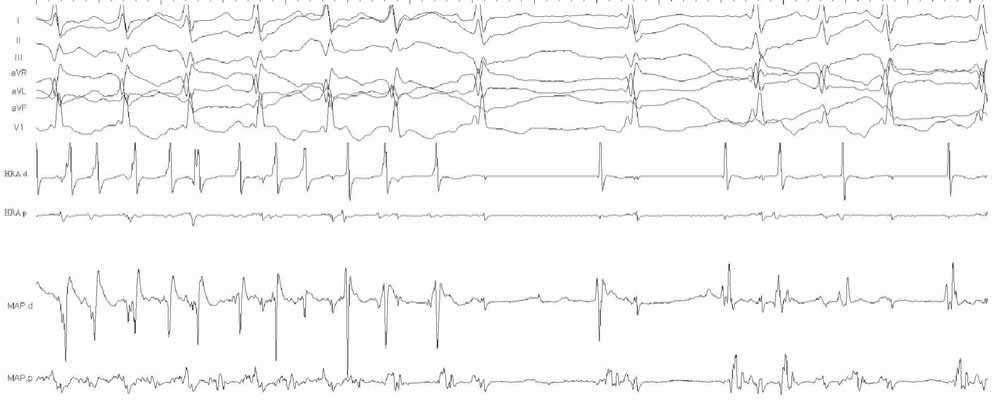
Рис. 6. Фрагмент внутрисердечного электрофизиологического исследования (ВСЭФИ), 50 мм/с. Восстановление синусового ритма при воздействии на кава-трискуспидальный истмус. I, II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, V1 – первое грудное отведение, HRA d, HRA p – дистальный и проксимальный полюсы электрода, расположенного в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
пликаций, что привело к значительному урежению экстрасистолии, но полностью устранить ее не удалось.
Через 4 ч после операции трепетание предсердий рецидивировало с ЧСС до 300 уд./мин. С целью поддержания нормосистолии проводилась инфузия кордарона в течение 2 суток. Одномоментно проводилось насыщение кордароном в таблетированной форме. Так как эффекта в виде урежения ЧСС от проводимой терапии не наблюдалось, через 7 дней решено было выполнить повторную РЧА.
При второй операции после установки электродов – 5 Fr QUAD JOS (Bard, USA) в высоких отделах свободной стенки правого предсердия и картирующего 5 Fr Marinr MC (Medtronic, USA) зарегистрировано типичное трепетание предсердий с циклом 218 мс (рис. 7).
На область кава-трикуспидального истмуса нанесена серия РЧ-аппликаций. Трепетание купировано на воздействии (рис. 8). Синусовый ритм с частой предсердной экстрасистолией.
Выполнялось картирование правого предсердия. Наносились аппликации на область наиболее раннего возбуждения – на ушко правого предсердия. Экстрасистолия полностью не устранена. На момент окончания операции наблюдался стойкий синусовый ритм с редкой
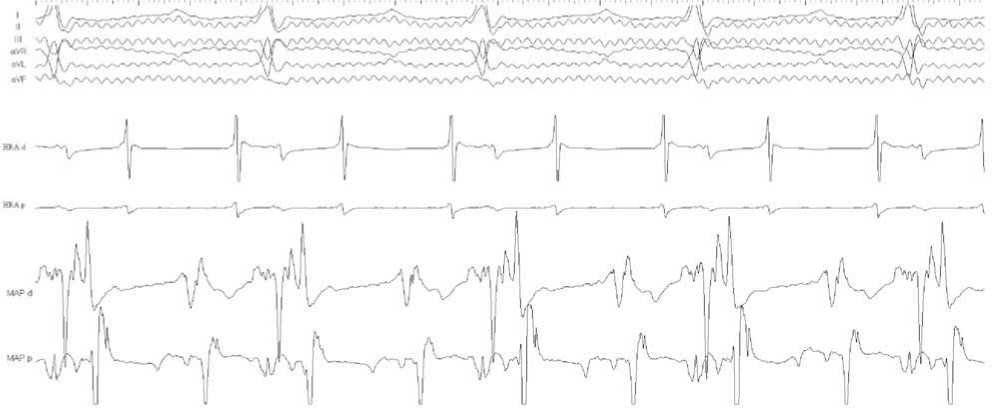
Рис. 7. Фрагмент ВСЭФИ, 100 мм/с. Типичное трепетание предсердий с циклом 218 мс. I, II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, HRA d, HRA p – дистальный и проксимальный полюсы электрода, расположенного в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
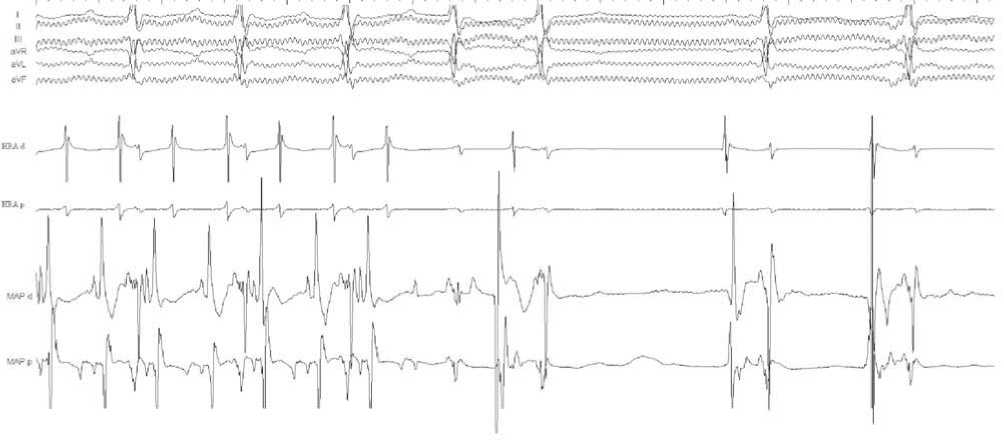
Рис. 8. Фрагмент ВСЭФИ, 100 мм/с. Восстановление синусового ритма при воздействии на кава-трикуспидальном перешейке. I, II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, HRA d, HRA p – дистальный и проксимальный полюсы электрода, расположенного в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
единичной предсердной экстрасистолией.
Картина послеоперационного течения у пациентки была идентична первой: в пределах первых суток после РЧА вновь рецидив трепетания предсердий, в связи с чем использовалась комбинированная терапия: кордарон и анаприлин в стандартных дозировках. Так как эффекта от антиаритмической терапии не наблюдалось, несмотря на высокий риск осложнений, пациентка вновь была взята в операционную, где ей повторно была выполнена РЧА трепетания предсердий.
На момент начала операции регистрировалось типич- ное трепетание предсердий. При третьем вмешательстве также наносились аппликации на кава-трикуспидальном перешейке. Тахикардия купирована на воздействии. В отличие от первых двух процедур удалось установить в коронарный синус еще один электрод Marinr, что позволило провести стимуляцию с электрода, расположенного в коронарном синусе. Получены локальные критерии блока истмуса (рис. 10). В дальнейшем при учащающей и программируемой стимуляции индуцировать какую-либо тахикардию не удалось.
В послеоперационном периоде по данным СМЭКГ
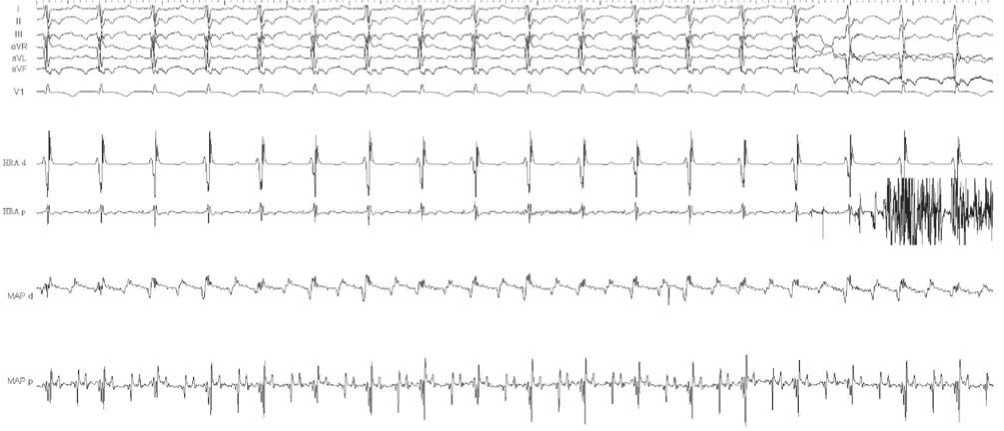
Рис. 9. Фрагмент ВСЭФИ, 50 мм/с. Типичное трепетание предсердий. I,II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, V1 – первое грудное отведение, HRA d, HRA p – дистальный и проксимальный полюсы электрода, расположенного в высоких отделах свободной стенки правого предсердия. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода Рис. 10. Фрагмент ВСЭФИ, 200 мм/с. Стимуляция с электрода, расположенного в коронарном синусе. На картирующем электроде интервал между А-А’ 100 мс. I,II, III, AVR, AVL, AVF – стандартные и усиленные отведения ЭКГ, V1 – первое грудное отведение, CS d, CS p – дистальный и проксимальный полюсы электрода, расположенного в коронарном синусе. MAP d, MAP p – дистальный и проксимальный полюсы картирующего электрода
регистрировалась залповая предсердная экстрасистолия, среднесуточная ЧСС 120 уд./мин. В связи с возможным проаритмогенным действием кордарон был отменен, назначена монотерапия попранололом в дозе 6 мг в сутки, на фоне чего по данным суточного мониторирования электрокардиографии при выписке среднесуточная ЧСС составляла 88 уд./мин, что ниже возрастной нормы, также зарегистрирована суправентрикулярная экстрасистолия до 10 тысяч в сутки, в том числе залповые суправентрикулярные экстрасистолы до 6 комплексов. Состояние при выписке удовлетворительное. Аппетит, сон не нарушены. В весе прибавляет. Дыхание пуэрильное, проводится над всеми отделами. Тоны сердца громкие. ЧСС 94 уд./мин. Одиночная экстрасистолия до 8 уд./мин. SpO2 98%. АД 86/44 мм рт. ст. Вес 5,84 кг. Пациентка выписана.
Обсуждение
Несмотря на накопленный опыт до настоящего времени дискутируются вопросы об оптимальном возрасте выполнения вмешательства, о возможности и необходимости использования РЧА при лечении аритмий у детей, о тактике ведения пациентов в случае неэффективности РЧА тахикардий и аритмий (повторное хирургическое вмешательство или постоянная антиаритмическая терапия). В рутинной клинической практике врачу приходится сталкиваться с необходимостью принятия решений относительно метода, сроков, а самое главное, выбора способа для конкретного ребенка. К сожалению, однозначного ответа на все эти вопросы нет. Часто приходится учитывать возраст пациента, состояние гемодинамики, переносимость аритмии, возможности проведения вмешательства. Не стоит забывать, что, несмотря на прилагаемые усилия, эндокардиальные вмешательства это не всегда являются панацеей. И в случае их неэффективности приходится прибегать к медикаментозной антиарит-мической терапии, что также имеет свои трудности. Одними из самых сложных для устранения аритмий являются предсердные тахикардии, а сочетание трех видов тахиаритмий (залповая предсердная экстрасистолия, предсердная тахикардия, трепетание предсердий), как у представленной пациентки, способно поставить в тупик. Усугубляется все также тем, что чем меньше пациент и размеры его сердца, тем больше ограничены возможности для манипуляций катетером. Часто нет возможности воспользоваться нефлюороскопическим навигационным оборудованием ввиду отсутствия катетеров соответствующих размеров. Но все трудности отступают, когда необходимо решить судьбу пациента – сохранение аритмии с гемодинамическими нарушениями или попытка, пусть даже и неоднократная, устранить аритмию. Именно с такими трудностями и выбором нам пришлось столкнуться у представленной пациентки. Гемодинамически осложненная тахикардия с отсутствием контролируемой ЧСС при использовании медикаментозных препаратов вынудила трижды проводить внутрисердечное исследование для устранения аритмии. При первой попытке удалось безвозвратно устранить только предсердную тахикардию. Трепетание было устранено с третьей попытки, и только после того, как была использована стимуляция из коронарного синуса. Попытки устранения предсердной экстрасистолии из ушка правого предсердия не увенчались успехом, поэтому была использована медикаментозная терапия. Представленным клиническим случаем мы хотим показать, что разумная настойчивость при проведении вмешательств в сочетании с адекватно подобранной медикаментозной терапией позволяет устранить аритмии, и, самое главное, редуцировать их гемодина- мические последствия.
Список литературы Лечение предсердных тахиаритмий у грудного ребенка
- Бокерия Е.Л. Эктопическая предсердная тахикардия у детей: клиника, диагностика и лечение//Анналы аритмологии. -2006. -№ 3. -С. 16-19.
- Марцинкевич Г.И., Соколов А.А. Особенности эхокардиографии у детей, антропометрические и возрастные нормы//Российский педиатрический журнал. -2012. -№ 2. -С. 17-21.
- Свинцова Л.И., Ковалев И.А., Мурзина О.Ю. и др. Опыт лечения тахиаритмий у детей младшего возраста//Вестник аритмологии. -2007. -№ 46. -С. 12-16.
- Школьникова М.А., Березницкая В.В. Нарушения сердечного ритма у детей первого года жизни//Физиология и патология сердечно-сосудистой системы у детей первого года жизни/под ред. М.А. Школьниковой, Л.А. Кравцовой. -М.: Медпрактика, 2002 -86 с.
- Jaeggi E., Fouren J.C., Drblik S.P. Fetal atrial flutter: diagnosis, clinical features, treatment and outcome//J. Pediatr. -1998. -Vol. 132(2). -P. 335-339.
- Jongbloed M.R.M., Schalij M.J., Poelmann R.E. et al. Embryionic conduction tissue: a spatial correlation with adult arrythmogenic areas. Transgenic CCS-lacZ expression in the cardiac conduction system of murine embryos//J. Cardiovasc. Electrophysiol. -2004. -Vol. 15. -P. 349-355.
- Kaltan J., Shah M. Evaluation of the child with arrhythmia//Pediatr. Clin. N. Am. -2004. -Vol. 51. -P. 1537-1551.
- Myung K. Park. Fetal and perinatal circulation//Pediatric Cardiology for Practitioners. -2009. -P. 121.
- Practical management of pediatric cardiac arrhythmias/ed. by V.L. Zeigler, P.G. Gillette. -Armonk, NY: Futura Publishing, 2001. -422 p.
- Salerno J.C., Kertesz N.J., Friedman R.A. Clinical course of atrial ectopic tachycardiais age-dependant: Results and treatmet in children №3 or ≥3 year of age//J. Amer. Coll. Cardiol. -2004. -Vol. 43(3). -P. 438-444.


