Лекция по остеологии. Многоуровневый характер структуры минерального матрикса и механизмы его формирования
Автор: Аврунин А.С., Тихилов Р.М., Аболин А.Б., Щербак И.Г.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Лекция
Статья в выпуске: 2, 2005 года.
Бесплатный доступ
Авторы представляют данные анализа литературы по структуре минерального матрикса костной ткани в лекционной форме. По их мнению, он представляет собой четырехуровневую структуру. Первый уровень внутренняя структура минерала, второй морфология минерала, третий копланарное объединение минералов, четвертый макроструктурное объединение минералов в единый комплекс внутри каждого костного органа. Показаны наиболее вероятные механизмы, определяющие стабильность воспроизведения параметров минерального матрикса на каждом уровне. В результате их функционирования формируются те варианты структуры минерального матрикса, которые являются запрограммированным отражением специфики данного участка органических структур.
Минеральный матрикс
Короткий адрес: https://sciup.org/142120811
IDR: 142120811
Lecture on osteology. The multilevel character of mineral matrix structure and the mechanisms of its formation
The authors present the analysis of the literature data on bone tissue mineral matrix structure as a lecture. In their opinion, it represents a four-level structure. The first level is the internal structure of a mineral, the second mineral morphology, the third coplanar integration of minerals, and the fourth macrostructural integration of minerals in a single complex within each bone organ. The most probable mechanisms determining the stability of reproduction of mineral matrix parameters at each level are shown. As a result of their functioning those variants of mineral matrix structure are formed which are the programmed reflection of the specificity of the site of organic structures given.
Текст обзорной статьи Лекция по остеологии. Многоуровневый характер структуры минерального матрикса и механизмы его формирования
При использовании современных научноисследовательских технологий мы зачастую сталкиваемся с физиологическими процессами, которые не удается связать с какой-либо известной анатомо-морфологической структурой. И наоборот: электронный микроскоп позволяет увидеть множество структурных деталей, функциональное значение которых неясно или вовсе неизвестно. Настоящее сообщение является попыткой связать морфологические характеристики минерального матрикса и физиологические механизмы его формирования. Необходимость подобной систематизации вызвана тем, что, несмотря на большой массив публикаций посвященных исследованию костной ткани [5, 7-11, 13, 14, 16, 27, 29, 35, 36], последняя остается одной из наименее изученных структур организма. В значительной мере это обусловлено трудностями определения истинных параметров минерального матрикса, так как костная ткань на этапе подготовки к исследованию подвергается различным механическим, химическим, температурным и другим воздействиям. В результате, как отмечает Kim с соавторами [26], возможны трансформация минеральной фазы, повреждение минералов, изменение их размеров и так далее. Тем не менее, к настоящему времени накоплен значительный объем фактических данных, характеризующих минеральный матрикс костной ткани, в том числе его состав, структуру, обмен и регулирование [5, 7-11, 13, 14, 16, 27, 29, 35, 36].
Понятие «минеральный матрикс» возникло как следствие деления межклеточного вещества костной ткани на органическую и минеральную составляющие. Анализ современных данных позволяет выделить четыре уровня организации минерального матрикса:
-
1) первичный (внутренняя структура минерала);
-
2) вторичный (морфология минерала, т. е. его форма и размеры);
-
3) третичный (копланарное1 объединение минералов);
-
4) четвертичный (объединение минералов в единый комплекс внутри каждого костного органа).
Первичная структура. В костной ткани обнаружены дикальцийфосфатдигидрат, октакальцийфосфат, аморфный фосфат кальция, трикальцийфосфат и гидроксиапатит. Структурное сходство перечисленных соединений фосфатов кальция позволяет образовывать смеси по типу «сэндвич» или «вещество на поверхности». Иными словами, в одном минерале возможно объединение нескольких форм кристаллических решеток с одновременным включением структуры аморфного компонента [9].
В минеральном матриксе нормальной костной ткани содержание аморфного фосфата кальция не превышает 5 %. Минералы представлены преимущественно гидроксиапатитом, содержащим по 5-10 % СО 3 2- " и НРО 4 2- групп [26, 31]. Доля ионов НРО 4 2- уменьшается с возрастом, что обусловлено их замещением ионами СО 3 2- [9, 30]. В основе этих сдвигов лежит гете-роионный обмен2, в результате которого в кристаллическую решетку гидроксиапатита включаются также Mg2+, Sr2+, Ra2+, Na+, CO32-, F- и др. [13]. В итоге состав кристаллов (в основном, его поверхностные слои) отражает состав интерстициальной жидкости окружающей минерал.
Каковы же механизмы, обеспечивающие преимущественное формирование именно гидроксиапатита? Ведь в обычных условиях построение его наименьшей структурной единицы Са 10 (РО 4 ) 6 (ОН) 2 требовало бы одновременного столкновения 18 ионов, обладающих необходимой энергией активации, что совершенно невозможно из статистических соображений. В то время как аморфная фаза формируется достаточно легко при достижении в растворе минимально необходимой концентрация ионов Са2+ и НРО 4 2- [13].
В настоящее время можно выделить три таких механизма:
-
1. Инициация формирования гидроксиапатита путем эпитаксии3 на органической матрице [22].
-
2. Формирование гидроксиапатита путем эпитаксии на ранее образовавшихся кристаллах (их гидратном слое) [13].
-
3. Перестройка различных фаз минералов в гидроксиапатит под влиянием ионного насоса клеток остеоцитарного ряда [1,4, 11].
Инициация формирования гидроксиапатита путем эпитаксии на органической матрице. Основным нуклеатором4 процесса кристаллизации является костный сиалопротеин. На него приходится 8-12 % от общего количества неколлагеновых белков. Это обильно фосфорилированный протеин, имеющий высокое сродство не только к ионам кальция (связывает до 83 Са2+), но и к кристаллам гидроксиапатита. Поэтому костный сиалопротеид может не только способствовать зарождению кристалла, но и эффективно ограничивать его рост в зависимости от своего физического состояния (иммобилизованный или растворенный) [22].
Роль фосфопротеинов в инициации кристаллообразования подтверждается тем, что увеличение их концентрации в декальцинированной костной ткани значительно уменьшает требуемое для нуклеации время (лаг-период). Причем замена костного фосфопротеина на фосвитин (из желтка яйца), имеющий ряд аналогичных химических и структурных характеристик, не изменяют характера минералообразования. Этот процесс не возникает после удаления 90 % и более фосфата из любого фосфопротеина [32].
Другим условием минерализации коллагеновых структур является наличие ковалентной связи между фосфопротеинами и фибриллами коллагена [32]. Подобная жесткая фиксация фосфопротеинов обеспечивает необходимую пространственную ориентацию гидроксиапатита по осям (длина, ширина, толщина) при его формировании путем эпитаксии на органической матрице. Это обеспечивает также и пространственную ориентацию минеральных структур на третичном и четвертичном уровнях организации минерального матрикса относительно ориентации органического. А в связи с тем, что ультраструктура органического матрикса формируется соответственно силовым линиям, то, следовательно, и ультраструктура минерального также формируется соответственно преобладающим векторам механических нагрузок. В результате все элементы костной ткани располагаются соответственно силовым линиям в костном органе.
Формирование гидроксиапатита путем эпитаксии на ранее образовавшихся кристаллах. В настоящее время есть все основания предполагать, что большинство кристаллов гидроксиапатита формируется путем эпитаксии на гидратной оболочке «первичного» кристалла, т.е. сформи- рованного на органической матрице. Образование гидратного слоя обусловлено электрическим полем, возникающим вокруг минерала в связи с асимметрией ионных групп входящих в его состав. Внутри кристалла каждый катион окружен удерживающим его полем, создаваемым анионами, и, наоборот, каждый анион окружен полем, созданным катионами. Однако на поверхности кристалла возникают остаточные электрические заряды каждого находящегося в нем иона. Это приводит к тому, что вокруг кристалла в виде мозаики возникают слои адсорбированных ионов с противоположным по знаку зарядом. Последовательные слои ионов фосфата и гидратированных ионов кальция, имеют стереометрические параметры, аналогичные параметрам решетки гидроксиапатита [13]. Тем самым создаются условия для формирования новых кристаллов гидроксиапатита путем эпитаксии на ионах гидратной оболочки минерала.
Перестройка различных фаз минералов в гидроксиаппатит под влиянием ионного насоса клеток остеоцитарного ряда . В процессе минерализации органического матрикса по разным причинам могут возникать отклонения в структуре минерала и для преобразования их в гидроксиапатит требуется механизм, обеспечивающий ускоренную перестройку. Этот процесс определяется действием остеоцитарного насоса, вызывающего попеременное уменьшение и увеличение в интерстициальной жидкости концентрации минералообразующих ионов (эффект «качелей»)5. В результате минерал то формируется, то частично рассасывается. Поэтому преобразование аморфной структуры в кристаллическую происходит благодаря постоянному химическому взаимодействию минерала с омывающей его межклеточной жидкостью [1, 4, 11].
Проследим теперь, как этот процесс приводит к "созреванию" минерала, то есть, к получению наиболее устойчивой (наименее растворимой) его формы. В основе этого лежит тот факт, что энергия отрыва иона от аморфной фазы ниже, чем от кристаллической. Поэтому, когда ионный насос обеспечивает экскрецию ионов из костной ткани и происходит растворение минерального вещества, в первую очередь удаляются ионы, входящие в состав аморфной фазы. Вероятность отрыва элемента, входящего в состав кристаллической фазы, заметно ниже. Когда же ионный насос нагнетает минералообразующие ионы в интерстициальную жидкость, их концентрация увеличивается, начинается отложение минерального вещества, и часть ионов оказывается в более устойчивом состоянии, формируя кристаллическую решетку. Следовательно, в дальнейшем вероятность их отрыва при растворении минера- ла намного ниже. Таким образом, под действием ионного насоса происходит ускоренное преобразование аморфной фазы в кристаллическую [1].
Описанные выше физиологические механизмы обеспечивают преимущественное формирование гидроксиапатита и обладают взаимодополняющими свойствами. Однако необходимо подчеркнуть, что основополагающим элементом этого процесса все же являются стереохимические параметры органического матрикса. Остановимся на некоторых аспектах его формирования.
Взаимосвязь органического и минерального матрикса . Формирование органического матрикса начинается после внутриклеточного синтеза его компонентов и продолжается после их секреции во внеклеточную среду, где процесс организации органических структур идет путем самосборки. Одним из его элементов является объединение молекул коллагена в протофибриллы и микрофибриллы, затем в фибриллы, а фибриллы в волокна. Завершает этот процесс формирование волокнистого каркаса матрикса с характерной для костной ткани структурой. В эту структуру встраиваются разнообразные неколлагеновые белки [2, 3, 12, 15].
Спектр органических компонентов, синтезированных клетками остеоцитарного ряда, зависит от особенностей регуляторно-метаболического статуса организма в конкретный момент времени. Например, гормон роста и паратгормон вызывают увеличение синтеза белка, связывающего инсулинподобный фактор роста III. Концентрация инсулинподобного фактора роста I возрастает под влиянием паратгормона. Под действием 17β-эстрадиола увеличивается содержание инсу-линподобных факторов роста I и II и фактора трансформации 1β [33, 34].
Таким образом, можно говорить о существовании определенной программы самосборки органического матрикса, структура которого определяется следующими условиями: совокупностью синтезируемых клетками компонентов, ионным составом среды, рН внеклеточной среды и т. д. А в связи с тем, что все эти условия определяются регуляторно-метаболическим статусом организма в момент формирования органического матрикса, то в итоге формируется наиболее вероятный в конкретных условиях вариант объединения молекул в единое целое.
Выявление же незначительных отклонений затруднительно, так как морфологическое распределение неколлагеновых белков в костной ткани известно плохо, их трудно распознать под электронным микроскопом, а количественные характеристики их состава зависят от типа кости [15]. Тем не менее, установлено, что у пациентов, страдающих болезнью Педжета, распределение остеопонтина зависит от типа и тяжести болезни. Существенные различия найдены и в распределении остеонектина, остеокальцина и декорина между нормальной костной тканью и синтезированной de novo при болезни Педжета [25]. Выявленные сдвиги отражают отклонение в их синтезе и/или инкорпорации в процессе ремоделирования кости и могут явиться следствием нарушения трансляции костного матрикса, а затем и его минерализации.
После формирования органического матрикса лаг-период до начала отложения минералов занимает около 8 суток. После инициации этого процесса образование минеральных структур протекает лавинообразно [21]. В указанный временной интервал происходит ферментное преобразование органического матрикса, включая разрушение ингибиторов минералообразования [18, 23].
По-видимому, в результате ферментного воздействия создаются определенные физикохимические условия, включая формирование структуры «каналов» для движения ионных потоков (кальция и фосфатов) в направлении центров инициации. Движение потока ионов в направлении последних определяется тем, что при формировании минерала переход ионов из растворимого в нерастворимое состояние в участке инициации вызывает локальное снижение их концентрации в растворе. В результате образуется градиент концентраций, который и определяет направление движения ионных потоков. Остеоцитарный насос обеспечивает при этом постоянное восполнение концентрации минералообразующих ионов в интерстициальной жидкости зоны зарождения кристаллов.
В связи с тем, что преобразование растворимой фазы в нерастворимую всегда происходит при участии центров инициации, последние можно разделить на две группы: обеспечивающие формирование кристаллической структуры путем эпитаксии (по-видимому, это основной вариант) и инициирующие формирование аморфной структуры. Именно количественное соотношение этих центров определяет преимущественно кристаллическую структуру большинства «первичных» минералов, а характер распределения этих центров в органическом матриксе и их пространственная ориентация обеспечивает специфику третичного и четвертичного уровней пространственной организации минеральной фазы.
Вторичная структура. Морфология кристаллов определяется их формой и размерами. В настоящее время выделено два варианта их формы: пластинчатые и стрежнеобразные (игольчатые) [9]. Проведенные в последние годы электронномикроскопические исследования изолированных кристаллов из костной ткани рыбы, цыпленка, мыши и быка выявили только кристаллы, имеющие форму очень тонких пластин [26]. Стержне- и иглообразных кристаллов не установлено ни в одном из образцов костей. Объём- ные стереоснимки, полученные при электронной микроскопии молодых изолированных кристаллов, показали, что кристаллические пластинки апатита могут быть изогнуты, согнуты, а также свернуты на себя и на близлежащие кристаллы. В результате возникает иллюзия, что это иглоподобные (стержнеподобные) кристаллы [30]. Их ширина 3-5 нм, длина колеблется от 5-7 нм до 100-120 нм. Кристаллы же пластинчатой формы имеют средние размеры 1,5-3,5 нм х 5-10 нм х 40-50 нм (табл. 1). То есть, можно предположить, что увеличение длины иглоподобных кристаллов связано с объединением нескольких изогнутых микрокристаллов в единый комплекс.
Таблица 1
Размеры кристаллов
|
Исследованный образец кости |
Ширина (нм) |
Длина (нм) |
Толщина (нм) |
|
Бык [26] |
15,8 ± 7,2 (2,9-42,2) |
27,3±7,2 (6,9-61,7) |
<1,5-2 |
|
Мышь [26] |
12,0±4,3 (3,9-26,5) |
21,2±7,6 (6,9-50,0) |
<1,5-2 |
|
Цыпленок [26] |
12,2±4,8 (2,9-26,5) |
23,3±8,4 (8,8-53,9) |
<1,5-2 |
|
Сельдь [26] |
15,4±10,0 (2,3-58,5) |
37,3±19,0 (2,6-98,3) |
<1,5-2 |
|
Человек [8] |
7-8 |
13-14 |
2-4 |
|
По данным литературы [13] |
- 7,5 |
«20 |
3-4 |
Другим морфологическом параметром являются размеры кристаллов. В этой связи обращает на себя факт близости их средних значений не только у разных организмов, но и при формировании in vitro. Следовательно, должен существовать единый механизм, определяющий эти параметры. В последние годы дискутируется роль органических молекул в этом процессе. Это связано с тем, что стереохимические параметры белков кости создают возможность их связывания с образовавшимися кристаллами, что может обеспечивать торможение кристаллического роста в определенных направлениях.
Однако если бы этот механизм действительно определял размеры кристаллов, белки находились бы между кристаллами, образующими копланарные объединения. Подобное внедрение сомнительно по двум причинам. Во-первых, оно сделало бы невозможным синтез кристаллов путем эпитаксии на гидратной оболочке первичных кристаллов. Во-вторых (и это главное), применение современных технологий не выявило межкристаллического (внутрикопланарного) расположения белковых молекул.
Вернее всего, ограничение размеров кристаллов вызвано тем, что гидроксиапатит, содержащийся в костной ткани, обладает очень малой растворимостью. Как известно, при смешивании растворов соли (точка А на рис. 1) происходит некоторая агрегация ионов. Эти твердые частицы стабильны лишь в том случае, если они очень малы. При возрастании концентрации ионов в растворе (при переходе от точки Б к точке В) состояние раствора можно считать метастабильным, так как действительная величина растворимости превышает нормальную растворимость, или растворимость «макрокристаллов». При таких концентрациях часть вещества может находиться в твердой фазе, но радиус частиц может варьировать только от R1 до R2. Эти частицы не будут спонтанно расти, так как более крупные кристаллы растворяются лучше, чем мелкие [13]. По нашему мнению, именно этот механизм ограничивает размеры кристаллов в костной ткани, в то время как белковые ингибиторы кристаллообразования, скорее всего, влияют на параметры третичного уровня организации минерального матрикса.
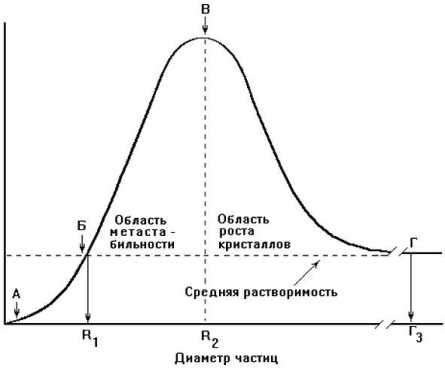
Рис. 1. Теоретическая зависимость между размером частиц и растворимостью какой-либо соли, предсказанная уравнением Кнаппа [13]
Третичная структура. При образовании новых кристаллов на гидратной оболочке ранее сформированных возникают их копланарные объединения, в которых минералы объединены конец в конец или бок в бок. При этом полного слияния кристаллических решеток микрокристаллов не происходит. Размеры копланарных объединений находятся в следующих пределах: длина 29,9-37,3 нм, ширина 18,8-21,9 нм [8]. Каков же механизм, обеспечивающий формирование подобной структуры? По-видимому, это результат рассмотренного выше процесса эпитаксии кристаллов на гидратной оболочке «первичного» кристалла, сформированного на органической матрице. Обращает на себя внимание малый разброс размеров копланарных объединений, что свидетельствуют о наличии ограничительного механизма, определяющего эти размеры. С одной стороны, на это может влиять характер распределения и размеры гидрофильных и гидрофобных участков в молекулах белков в зоне роста копла-нарных объединений минералов. С другой стороны распределение белковых ингибиторов роста кристаллов (о которых было сказано вы- ше). Эти два механизма не взаимоисключают, а дополняют друг друга.
Определенную роль играет и то обстоятельство, что в органическом матриксе центры кристаллизации имеют строгую пространственную повторяемость распределения основного центра кристаллизации костного сиалопротена [22] и соответствующее чередование гидрофильных и гидрофобных участков в коллагеновых структурах. В этих условиях рост копланарных объединений может ограничиваться расстоянием от центра инициации первичного кристалла до ближайшего гидрофобного участка. Подобный механизм базируется на ультраструктурной пространственной повторяемости элементов, формирующих органический матрикс, и поэтому определяет малый разброс размеров копла-нарных объединений.
Четвертичная структура. Минералы располагаются внутри коллагеновых фибрилл и внефибриллярно. В межфибриллярных пространствах копланарные объединения кристаллов, прилегающие к коллагеновым фибриллам, окружают их, формируя манжетки, и контактируют с внутрифибриллярными минеральными образованиями. На отдалении от коллагеновых фибрилл кристаллические объединения входят в состав плотных групп, в которых они размещаются в одном направлении. По отношению друг к другу такие группы расположены под разными углами. Внутрифибриллярные объединения кристаллов образуют ряд параллельных, спирально закрученных пластов [8].
Образование подобной упорядоченной структуры возможно в том случае, если основным механизмом формирования минералов является эпитаксия. В этом случае пространственное расположение центров инициации первичных кристаллов определяет направление их осей соответственно особенностям структуры органического матрикса в данном участке. Последующие кристаллы растут, формируя копланарное объединение, также путем эпитаксии на данном кристалле, протекающей в соответствии с расположением его осей. Оси очередного копланарного объединения определяются уже пространственным расположением следующего центра инициации. Следовательно, происходит некоторый сдвиг направления осей по отношению к предыдущему копланарному объединению. В результате формируется определяемый структурой органического матрикса пространственный вариант структуры минерального. По сути, последняя является запрограммированным отражением не только особенностей распределения органических молекул в костной ткани, но и особенностей их вторичного, третичного и четвертичного уровней организации, отражающих основные направления силовых линий механических нагрузок в каждом костном органе. Нарушение функционирования любого из рассмотренных выше механизмов приведет к нарушению структуры минерального матрикса, что вызовет изменение механических свойств костной ткани в целом. Это в свою очередь вызовет нарушение процесса механотрансдукции и нарушит равновесие между резорбцией костной ткани и ее синтезом, что мы и наблюдаем в процессе старения организма.


