Мацитентан: эволюция класса антагонистов рецепторов эндотелина для повышения эффективности и безопасности лечения легочной артериальной гипертензии
Автор: Мартынюк Тамила Витальевна, Наконечников Сергей Николаевич, Чазова Ирина Евгеньевна
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2013 года.
Бесплатный доступ
Легочная артериальная гипертензия (ЛАГ) - тяжелое прогрессирующее заболевание, которое характеризуется выраженным ремоделированием мелких легочных артерий и артериол, приводит к декомпенсации правого желудочка и гибели больных. В результате открытия патогенетических мишеней ЛАГ были созданы и внедрены в клиническую практику лекарственные препараты, восполняющие дефицит эндогенного простациклина и оксида азота, блокирующие эффекты эндотелина-1 (ЭТ-1). Роль последнего в патогенезе ЛАГ обусловлена мощным вазоконстриктивным потенциалом, комплексом эффектов, ответственных за развитие ремоделирования легочных сосудов. История клинического применения антагонистов рецепторов эндотелина (АРЭ) началась в 2001г. с бозентана. Его эффективность была показана в серии рандомизированных клинических исследований. Мацитентан - новый мощный пероральный АРЭ двойного действия, специально созданный для улучшения эффективности и повышения безопасности терапии за счет тканевой специфичности препарата. Новая молекула блокирует рецепторы ЭТ типа А и В, имеет улучшенные физико-химические свойства, направленные на повышение пенетрации препарата в ткани. В экспериментальных работах мацитентан предотвращал повышение давления в легочной артерии и гипертрофию правого желудочка, улучшал выживаемость животных. В исследовании SERAPHIN влияние мацитентана на заболеваемость и смертность изучалось у 742 больных с ЛАГ, получавших препарат в дозах 3 мг и 10 мг, по сравнению с плацебо. Применение мацитентана в дозах 3 мг и 10 мг способствовало снижению риска заболеваемости и смертности при ЛАГ на 30% и 45%, соответственно. К 6 месяцу наблюдения в группах лечения мацитентаном 3 мг и 10 мг прирост дистанции в тесте 6-минутной ходьбы по сравнению с плацебо составил плюс 16,8-22,0 м. Функциональный класс улучшился по сравнению с исходным к 6 месяцу лечения у 13% больных в группе плацебо, 20% - в группе мацитентана 3 мг (р=0,04) и 22% - в группе 10 мг (р=0,006). По сравнению с группой плацебо терапия мацитентаном вызывала достоверное снижение легочного сосудистого сопротивления и повышение сердечного индекса. Терапия характеризовалась благоприятным профилем переносимости. В октябре 2013 г. мацитентан (OPSUMIT) 10 мг однократно в сутки одобрен Администрацией по контролю качества пищевых продуктов и лекарственных препаратов (США) для лечения больных ЛАГ для предотвращения прогрессирования болезни.
Легочная артериальная гипертензия, эндотелин-1, антагонисты рецепторов эндотелина, бозентан, мацитентан
Короткий адрес: https://sciup.org/14342737
IDR: 14342737
Macitentan: the evolution of the class endothelin receptor antagonists to improve efficacy and safety of PAH treatment
Pulmonary arterial hypertension (PAH) is a severe progressive disease, characterized by advanced remodeling of small pulmonary arteries and arterioles, which ultimately leads to right heart failure and death. Due to discovery of PAH pathophysiological targets, new medications have been developed and implemented into clinical practice. These medications compensate the deficiencies of endogenous prostacyclin and nitric oxide and also block the effects of endothelin-1 (ET-1). The role of the latter in PAH pathophysiology is related to its strong vasoconstrictory properties, as well as to a number of effects responsible for arterial wall remodeling. Clinical use of endothelin receptor antagonists (ERA) started in 2001, with the first agent of the class, bosentan, whose efficacy was demonstrated in a number randomized controlled trials. Macitentan is a novel potent double action oral ERA, developed with the purpose to improve efficacy and safety of PAH treatment through its tissue specificity. The new molecule blocks endothelin receptors type A and B and possesses improved physicochemical properties allowing for improved tissue penetration. Macitentan prevents an increase in pulmonary arterial pressure, right ventricle hypertrophy and improves survival in animal models. The SERAPHIN Study evaluated the effects of macitentan on morbidity/mortality in 742 PAH patients, randomized to macitentan 3 mg or 10 mg daily or placebo. Macitentan 3 mg and 10 mg daily was shown to reduce morbidity and mortality by 30% and 45%, respectively. By 6 month of the follow-up, there was an improvement in 6-minute walking test by + 16.8 m for macitentan 3 mg and +22.0 m for macitentan 10 mg daily. An improvement of the functional class, compared to baseline, was observed by 6 mo in 13% of placebo patients, 20% of macitentan 3 mg daily patients (p=0.04) and in 22% of 10 mg daily patients (0.006). Compared to placebo, macitentan significantly reduced pulmonary vascular resistance and improved cardiac index. It demonstrated a favorable safety profile. US Food and Drug Administration (FDA) approved macitentan (OPSUMIT) 10 mg once daily for the treatment of pulmonary arterial hypertension to delay disease progression.
Текст научной статьи Мацитентан: эволюция класса антагонистов рецепторов эндотелина для повышения эффективности и безопасности лечения легочной артериальной гипертензии
|
Мартынюк Тамила Витальевна |
Руководитель лаборатории легочной гипертензии отдела системных гипертензий НИИ Кардиологии им. А.Л. Мясникова, к.м.н. |
|
Наконечников Сергей Николаевич |
Ученый секретарь ФГБУ РКНПК МЗ РФ, д.м.н., профессор |
|
Чазова Ирина Евгеньевна |
Директор НИИ Кардиологии им. А.Л. Мясникова, член-корр. РАМН, д.м.н., профессор |
Легочная артериальная гипертензия (ЛАГ) – тяжелое прогрессирующее заболевание, при котором выраженное ремоделирование мелких легочных артерий и артериол приводит к перегрузке правого желудочка, развитию правожелудочковой сердечной недостаточности и фатальному исходу [1]. В патогенезе заболевания играют роль взаимодействия комплекса генетических, молекулярных и гормональных нарушений. Дисфункция эндотелия легочных сосудов рассматривается в качестве интегрального фактора в патофизиологии ЛАГ. Независимо от вида инициирующего стимула возникают вазоконстрикция, ремоделирование и нарушение эластичности стенки легочных сосудов, тромбоз in situ. Основными терапевтическими мишенями при ЛАГ являются дефицит оксида азота и простациклина, а также повышенная продукция эндотелина-1 (ЭТ-1) [2]. Применение лекарственных препаратов из классов простаноидов, донаторов оксида азота и антагонистов рецепторов эндотелина (АРЭ) приводит к существенному повышению физической активности пациентов, уменьшению выраженности клинических симптомов, замедлению темпов прогрессирования заболевания и улучшению выживаемости пациентов с различными формами ЛАГ [1,3].
ЭТ-1 играет важнейшую роль в патогенезе ЛАГ. Это обусловлено не только его мощным вазоконстриктивным действием, но и комплексом эффектов, ответственных за развитие ремоделирования легочных сосудов, а именно способностью стимулировать клеточную пролиферацию и дифференцировку клеток, продукцию факторов роста, провоспалительных цитокинов, биологически активных веществ. У больных с ЛАГ (идиопатическая легочная гипертензия (ИЛГ) и ассоциированные формы) определяются значительно повышенные уровни ЭТ-1 в плазме крови, его усиленная экспрессия обнаруживается в легочной ткани [1,4,5,6]. При сравнительном анализе содержания ЭТ-1 в крови, взятой из желудочков сердца у больных с ИЛГ, был выявлен существенный градиент его концентрации по сравнению с контролем, что указывает на нарушенный клиренс и/или повышенную легочную продукцию [4].
Основные эффекты АРЭ связаны с предотвращением патологических эффектов ЭТ-1. ЭТ-1 является одним из наиболее мощных и длительно действующих эндогенных вазоконстрикторов, в 100 раз превышающий эффект норадреналина и в 10 раз – ангиотензина II. Эффекты ЭТ-1 реализуются за счет связывания с двумя типами рецепторов типа А (ЭТA) – гладкомышечных клеток и типа В (ЭТВ) – эндотелиальных и гладкомышечных клеток [6]. Активация ЭТA-рецепторов гладкомышечных клеток приводила к вазоконстрикции легочных сосудов. Стимуляция рецепторов ЭТВ в изолированном легком с помощью селективного агониста вызывала вазоконстрикцию легочных сосудов только в условиях блокады продукции оксида азота, однако, эти эффекты селективных АРЭ изучались только на экспериментальных моделях ЛАГ. Блокада ЭТA-рецепторов приводила к уменьшению легочного сосудистого сопротивления (ЛСС) на 25%. Блокада ЭТВ-рецепторов не оказывала влияния на величину ЛСС. На основании результатов экспериментальных исследований можно сделать вывод о преобладающей роли ЭТA-рецепторов по сравнению с ЭТВ в отношении вазоконстрикторного и пролиферативного действия ЭТ-1 [4]. ЭТВ-рецепторы присутствуют в эндотелиальных клетках, преимущественно в дистальных отделах микроциркуляторного русла легких. Их активация приводит к освобождению оксида азота и простациклина, а также клиренсу ЭТ-1 в легких. В физиологических условиях первоначально осуществляется клиренс примерно 47% циркулирующего ЭТ-1. У многих пациентов с ЛАГ клиренс ЭТ-1 остается сохранным, несмотря на выраженное ремоделирование легочных сосудов. Таким образом, лечение селективными АРЭ может быть потенциально более эффективным благодаря сохранению вазодилатирующего эффекта и осуществлению клиренса ЭТ-1 с помощью активации эндотелиальных ЭТВ-рецепторов, хотя эта гипотеза требует подтверждения в клинической практике.
ЭТ-1 обладает провоспалительными эффектами и вызывает увеличение сосудистой проницаемости, активирует нейтрофилы и тучные клетки, стимулирует продукцию цитокинов и индуцирует экспрессию интегринов, облегчая миграцию клеток и способствуя адгезии [4].
Оба класса рецепторов – ЭТA и ЭТB – экспрессируются на фибробластах с преобладанием рецепторов типа В. Роль ЭТB рецепторов продемонстрирована на различных моделях: их хроническая стимуляция приводила к развитию фиброза. ЭТ-1 индуцирует пролиферацию фибробластов, хемотаксис и продукцию компонентов экстрацеллюлярного матрикса [7].
Для АРЭ характерно направленное действие, всесторонняя блокада эффектов ЭТ-1, опосредуемых ЭТA и ЭТB рецепторами или исключительно рецепторов типа ЭТA,, отсутствие взаимодействия с рецепторами других типов. В экспериментальных работах на биологических моделях ЛАГ, при постоянном применении АРЭ наблюдалось уменьшение легочного сосудистого сопротивления, регресс гипертрофии сосудистой стенки и правого желудочка, уменьшение содержания коллагена в легочной ткани и выраженности воспалительных реакций [1,4,6].
Бозентан (Траклир, «Actelion») – первая молекула из класса АРЭ, воздействующая на систему ЭТ-1. АРЭ непептидной природы – дериват пиримидина, блокирующий оба типа рецепторов (ЭТA и ЭТВ), был внедрен в клиническую практику за рубежом с 2001 г. В 2006 г. бозентан первым из препаратов специфической ЛАГ-терапии был одобрен в нашей стране для лечения больных с ИЛГ, ЛАГ на фоне склеродермии без выраженного фиброза легких и синдромом Эйзенменгера с целью улучшения толерантности к физическим нагрузкам и замедления темпов прогрессирования заболевания [2].
За последние годы эффективность бозентана была доказана в целом ряде рандомизированных, плацебо контролируемых исследований у больных с ИЛГ, ЛАГ на фоне системных заболеваний соединительной ткани (СЗСТ), синдроме Эйзенменгера (рисунок 1) [1,7,8,9].
В пилотном многоцентровом рандомизированном, двойном слепом, плацебо контролируемом исследовании «351» бозентан или плацебо в соотношении 2:1 назначались 32 больным ИЛГ или ЛАГ вследствие системной склеродермии с функциональным классом (ФК) III (ВОЗ) [7]. Пациенты получали стартовую дозу бозентана по 62,5 мг два раза в день в течение первых 4 недель с последующим увеличением дозы до 125 мг дважды в день. К 12 неделе были обнаружены статистически достоверные различия в динамике дистанции в тесте 6-минутной ходьбы (Т6МХ) на фоне тера- пии бозентаном +76 м (р=0,021). Бозентан оказывал позитивные эффекты на ФК, индекс одышки по Боргу, гемодинамические показатели (сердечный индекс (р<0,0001); ЛСС (р=0,0002); среднее давление в легочной артерии (ДЛАср.) (р=0,02); среднее давление в правом предсердии (ДППср.) (р=0,02)), а также увеличивал время до развития клинического ухудшения.
В исследование BREATHE-1 (Bosentan Randomized trial of Endothelin Antagonist Therapy) включались больные с ИЛГ (70%) и ЛАГ вследствие СЗСТ с ФК III (91,4%) и IV (8,4%) (ВОЗ) [26]. Пациенты рандомизировались в соотношении 1:1:1 для получения 62,5 мг бозентана или плацебо дважды в день в течение 4 недель с последующим увеличением дозы до 125 мг или 250 мг два раза в день в течение 12 недель. К 16 неделе в объединенной группе пациентов, принимавших бозентан, разница дистанции в Т6МХ составила 44 м (р<0,001). Меньший прирост дистанции в Т6МХ по сравнению с исследованием «351» вероятно был обусловлен наличием больных с исходным ФК IV. Применение бозентана в обеих группах приводило к существенному улучшению гемодинамических параметров и клинических исходов [1]. Назначение бозентана приводило к улучшению ФК, уменьшению индекса одышки по Боргу и достоверному увеличению времени до клинического ухудшения (р=0,002). Не было выявлено достоверных различий в конечных точках в зависимости от дозы бозентана. Наибольший прирост дистанции в Т6МХ (+46м) наблюдался в группе, получавшей бозентан 250 мг дважды в день, однако, при этом отмечалась более высокая частота побочных эффектов в виде повышения
Бозентан
Исследования в субпопуляциях больных с ЛАГ
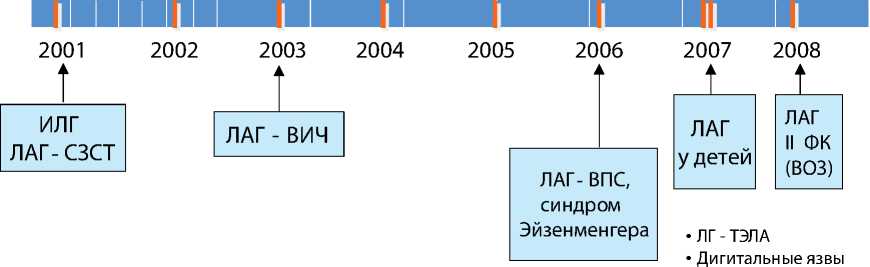
• Идиопатический фиброз легких
печеночных трансаминаз (14% против 5%, соответственно). Повышение толерантности к нагрузкам сохранялось у больных при лечении на протяжении более одного года и ассоциировалось с улучшением гемодинамических параметров и ФК. В рамках исследования BREATHE-1 были получены данные о позитивном влиянии бозента-на на систолическую и диастолическую функцию желудочков сердца по данным эхокардиографии (ЭхоКГ) и Допплер-ЭхоКГ в виде увеличения к 16 неделе лечения СИ (р=0,007), скорости раннего диастолического наполнения левого желудочка (р=0,003), конечно-диастолической площади левого желудочка (р=0,003); уменьшения конечно-диастолической площади правого желудочка (р=0,057), процента больных, имевших перикардиальный выпот (р=0,05) [1].
В открытом неконтролируемом исследовании BREATHE-3 эффективность и безопасность терапии бозентаном изучалась у детей в возрасте 4-17 лет [1]. Доза препарата у детей титруется в зависимости от веса. В результате лечения бозентаном в виде монотерапии или в комбинации с эпопро-стенолом к 12 неделе наблюдалось улучшение гемодинамических параметров.
У больных с ЛАГ на фоне ВИЧ в неконтролируемом исследовании BREATHЕ-4 бозентан вызывал положительную динамику Т6МХ (+91м, р<0,001), гемодинамических параметров (СИ, р<0,001; ЛСС, р<0,001; ДЛАср., р=0,002) и Допплер-ЭхоКГ-показателей, а также улучшение качества жизни. Лечение бозентаном не оказывало влияния на эффективность антиретровирусной терапии. Существенных лекарственных взаимодействий между этими препаратами не отмечалось [1].
В рандомизированном плацебо контролируемом исследовании BREATHЕ-5 у 54 пациентов с синдромом Эйзенменгера к 16 неделе лечения бозентан достигалось достоверное снижение ЛСС (р=0,038), ДЛАср. (р=0,036) и повышение толерантности к физическим нагрузкам с приростом дистанции в Т6МХ (+53,1 м, р=0,0079). При этом терапия бозентаном не ухудшала насыщение крови кислородом и характеризовалась хорошей переносимостью [1].
В проспективном, рандомизированном, плацебо контролируемом исследовании EARLY (Endothelin Antagonist tRial in miLdlY symptomatic PAH patients) было показано, что у пациентов на ранних стадиях ЛАГ (ФК II по ВОЗ) 24-х недельная терапия бозентаном в сравнении с плацебо сопровождалась снижением ЛСС (р<0,0001), риска развития клинического ухудшения (3,2% против 14% в группе плацебо), ухудшения ФК без достоверного влияния на толерантность к физиче- ской нагрузке (суммарная разница в Т6МХ 19,1м, р=0,076) [8].
Накоплены данные о долгосрочной терапии бозентаном. Положительная динамика сохраняется у больных с ЛАГ на фоне 12-месячного приема бозентана [1,2]. При монотерапии бозентаном выживаемость пациентов (кривые Каплан-Майера) к 12 и 24 месяцам составила 85% и 70% против предсказанной 69% и 57%, соответственно [7].
Эффективность и безопасность комбинированной специфической ЛАГ-терапии, включавшей бозентан и постоянную инфузию эпопростенола, изучалась в двойном слепом, рандомизированном, плацебо контролируемом исследовании BREATHЕ-2 у 33 больных ЛАГ с ФК III (76%) и IV (24%) (ВОЗ). Через два дня после начала терапии эпопростенолом пациенты рандомизировались для приема бозентана (62,5 мг дважды в день с увеличением дозы через 4 недели до 125 мг два раза) и плацебо в соотношении 2:1. К 16 неделе в обеих группах отмечалось снижение ЛСС, ДЛАср., ДППср., увеличение СИ, дистанции в Т6МХ и улучшение ФК. В группе комбинированной терапии отмечалась тенденция к лучшим результатам [9].
В исследовании STEP комбинация бозента-на с ингаляционным илопростом по сравнению с плацебо показала достоверное улучшение ФК (р=0,002), гемодинамических показателей (ДЛАср., р<0,001; ЛСС, р<0,001), увеличение времени до клинического ухудшения (р=0,022). Дистанция в Т6МХ суммарно увеличилась на 26 метров (р=0,051) [10].
Начальная доза бозентана составляет 62,5 мг 2 раза в сутки. Спустя 4 недели дозу после оценки переносимости лечения следует увеличить до 125 мг 2 раза в сутки. Дозозависимое повышение уровня трансаминаз отмечается примерно у 10% больных и является обратимым после снижения дозы или отмены препарата [2]. Наиболее вероятным механизмом действия бозентана на уровни печеночных трансаминаз является дозозависимая конкуренция с желчными солями, их задержка оказывает гепатотоксический эффект. Рекомендуется регулярный ежемесячный контроль уровня трансаминаз на фоне терапии бозента-ном. Возможно снижение уровня гемоглобина вследствие гемодилюции. Бозентан противопоказан при беременности, поскольку обладает тератогенным эффектом. При одновременном приеме с бозентаном снижается концентрация гормональных контрацептивов [1].
Создание АРЭ, обладающих селективным действием в отношении рецепторов типа ЭTВ, представлялось обоснованным с точки зрения повышения эффективности. Как показали экспе- риментальные исследования, сохранение активации ЭTB рецепторов приводит к увеличению клиренса ЭТ-1 в легких, повышению продукции NO и простациклина, способствует натрийурезу [4].
Амбризентан – несульфонамидный селективный АРЭ в 2007 г. был одобрен Администрацией по контролю качества продуктов питания и лекарственных средств (США) для лечения больных ЛГ (ФК II-III, ВОЗ) в дозе 5 и 10 мг для улучшения толерантности к физическим нагрузкам и предотвращения прогрессирования заболевания. Препарат исследовался в пилотном и двух рандомизированных исследованиях ARIES-1 (Ambrisentan in PAH- a phase III, Randomized, Double-blind, placebo-controlled, multicenter, Efficacy Study of Ambrisentan on Subjects with pulmonary arterial hypertension) и ARIES-2. У больных с ИЛГ, ЛАГ на фоне СЗСТ и ВИЧ-инфекции была доказана клиническая эффективность терапии в виде улучшения клинической симптоматики, гемодинамических параметров, повышения толерантности к нагрузкам, увеличении времени до развития клинического ухудшения [1]. Лечение амбризентаном сопровождалось существенным увеличением дистанции в Т6МХ. На фоне терапии стабилизировалось состояние больных ЛАГ, уменьшалась потребность в трансплантации, предсердной септостомии, госпитализациях по поводу прогрессирования заболевания. При длительном наблюдении в рамках открытого исследования за 383 больными, получавшими амбризентан, 95% больных остались в живых в течение 1 года и 94% продолжали принимать препарат.
В нашей стране в 2012 г. для лечения больных с ЛАГ ФК II-III амбризентан (Волибрис, «ГлаксоСмитКляйн Трейдинг») рекомендован в дозе 5 мг 1 раз в сутки с возможным увеличением до 10 мг. На фоне терапии амбризентаном чаще по сравнению с бозентаном возникают периферические отеки. Частота нарушений функции печени составляет 0,8 до 3%, что требует ежемесячного контроля. Вместе с тем, как при применении в отношении рецепторов типа А селективных, так и двойных АРЭ, имеется риск повышения уровня трансаминаз. В конце 2010 г. селективный антагонист рецепторов эндотелина типа А ситакзентан был запрещен к применению вследствие выявления необратимого гепатотоксического действия. Это произошло после его внедрения в клиническую практику в целом ряде стран после получения результатов двух рандомизированных исследований STRIDE- 1 (Sitaxsentan To Relieve Impaired Exercise) и STRIDE- 2. У больных с ИЛГ, ЛАГ на фоне СЗСТ и ВПС при ФК II-III ситакзентан в дозе 100 и 300 мг один раз в сутки к 12 неделе лечения приводил к достоверному улучшению толерантности к физическим нагрузкам, гемодинамических параметров, клинических исходов по сравнению с группой плацебо [1]. Дальнейшее наблюдение за больными в течение года показывало сохранение эффективности лечения.
В экспериментальных работах была установлена субпопуляция ЭTB-рецепторов, локализованных на гладкомышечных клетках, которые в случае активации способствуют вазоконстрикции. На животных моделях ЛАГ показано изменение плотности рецепторов с повышенной экспрессией ЭTA и сниженной экспрессией ЭTB-рецепторов. Таким образом, применение двойных АРЭ может иметь преимущества за счет ослабления негативных эффектов ЭТ-1 в отношении гладкомышечных клеток [11].
Iglarz M. и соавт. открыли новый двойной антагонист ЭТ-1 мацитентан с целью оптимизации тканевых эффектов препарата за счет повышения липофильности [12]. Создание новой молекулы под названием ACT-064992 было результатом скрининга нескольких молекул АРЭ для выявления той, которая обладает наиболее высоким коэффициентом распределения.
Идея оптимизации блокады системы ЭТ-1 основана на том, что он обладает паракринным эффектом, действуя локально. Почти 80% ЭТ-1, продуцируемого эндотелиальными клетками, се-
Таблица 1 . Физико-химические параметры мацитентана, бозентана и амбризентана
|
Коэффициент распределения |
Неионизированные формы (%) (рН 7,4) |
|
|
Мацитентан |
800:1 |
6 |
|
Бозентан |
20:1 |
1 |
|
Амбризентан |
1:2,5 |
0,01 |
кретируется в направлении базальной мембраны, поэтому в кровотоке обнаруживается в меньших концентрациях, чем в тканях [13]. Современные АРЭ показали весьма ограниченную тканевую пенетрацию из-за наличия высокой пропорции ионизированных форм (99% у бозентана и 99,9% у амбризентана [14]. Это означает, что только незначительная доля препарата может проникнуть через липофильные клеточные мембраны и достигнуть тканевых ЭТ-рецепторов. Увеличение тканевой пенетрации для улучшения взаимодействия с ЭТ-рецепторами может повысить не только вазодилатирующий эффект АРЭ, но и их влияние на сосудистое ремоделирование.
Мацитентан (ACT-064992 [N-[5-(4-бромофенил)-6-(2-(5-бромопиримидин-2-илокси)этокси)-пиримидин-4-ил]- N ’-пропиламиносульфонамид] – новый двойной АРЭ, созданный с целью улучшения эффективности и повышения безопасности терапии за счет тканевой специфичности препарата. Новая молекула блокирует рецепторы ЭТ типа А и В, имеет улучшенные физико-химические свойства за счет увеличения доли неионизиро-ванных форм молекулы, что позволяет препарату проникать через липофильные клеточные мембраны и повысить пенетрацию препарата в ткани (таблица 1) [12].
Повышенная пенетрация в ткани за счет липофильных свойств способствует терапевтическим преимуществам, в частности, удлинению периоду полужизни in vivo, а также более мощному воздействию на аутикринно-паракринные эффекты эндотелина.
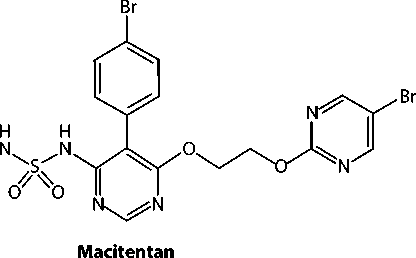
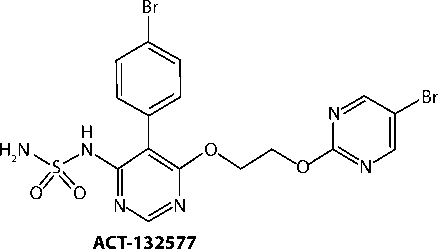
Мацитентан и его фармакологически активный метаболит ACT-132577 связываются с мембранными рецепторами эндотелина типа А и В, экспрессия которых на поверхности эндотелиальных и гладкомышечных клеток значительно повышена. Химическая структура мацитентана и его метаболита показана на рисунке 2.
Мацитентан и его метаболит ACT-132577 обладают высокой аффинностью к рецепторам типов А и В и приводят к мощному ингибированию вызываемого ЭТ-1 повышению содержания внутриклеточного кальция. Установлено, что in vivo препарат снижает артериальное давление у гипертензивных крыс, улучшает выживаемость крыс с мононокроталин-индуцированной ЛАГ и уменьшает выраженность протеинурии, что показано на экспериментальных моделях с сахарным диабетом, индуцированным стрептозотоци-ном [15,16].
Блокада ЭТ-рецепторов in vivo способствует повышению плазменных концентраций ЭТ-1. На существенно большую эффективность ма-цитентана in vivo указывает то, что сравнимое с бозентаном повышение содержания ЭТ-1 он вызывает в 10 раз в меньшей дозе. Это согласуется с результатами экспериментальной работы на гипертензивных крысах, в которой сопоставимое с бозентаном снижение артериального давления достигалось при применении в 10 раз меньшей дозы мацитентана. Это может быть связано как с большей липофильностью последнего, так и его
Рисунок 2. Химическая структура мацитентана и его активного метаболита
ТЕРАПИЯ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИСЕГОДНЯ И ЗАВТРА
Более 60 000 пациенто-лет опыта применения по всему миру

КРАТКАЯ ИНФОРМАЦИЯ О ПРЕПАРАТЕ РЕВАЦИО®
Торговое название: РЕВАЦИО®
Международное непатентованное название: силденафил
Более подробную информацию см. в Инструкции (Инструкция по медицинскому применению препарата РЕВАЦИО® одобрена Минздравсоцразвития РФ от 09.02.2011 г. с изменениями от 07.11.2012 г. и 22.04.2013 г.)

Представительство Корпорации «Пфайзер Эйч. Си. Пи. Корпорэйшн» (США):
Россия, 123317, Москва, Пресненская наб., д. 10, БЦ «Башня на Набережной» (блок С).
Тел.: +7 (495) 287 50 ОО. Факс: +7 (495) 287 53 ОО
* Data on file. Pfizer Inc. New York, NY. Предоставляется no первому требованию.
улучшенной способностью связываться с рецепторами или лучшей биодоступностью при пероральном приеме.
В экспериментальной работе мацитентан и ACT-132577 предотвращали индуцированное ЭТ-1 сокращение изолированной аорты крыс (ЭTA-рецепторы) и индуцированное сарафоток-сином S6c сокращение изолированной трахеи крыс (ЭTB-рецепторы). В монокроталиновой модели ЛАГ мацитентан вызывал снижение давления в легочной артерии и предотвращал развитие гипертрофии правого желудочка более эффективно, чем бозентан при применении в 10 раз меньшей дозе [16]. Кроме того, назначение маци-тентана способствовало значительному улучшению выживаемости животных. У крыс с сахарным диабетом при длительном назначении он способствовал снижению артериального давления и предотвращал поражение органов-мишеней, в частности структурные изменения почечных клубочков [15].
Следовательно, мацитентан оказался эффективен при применении в различных экспериментальных моделях при заболеваниях с хронической активацией системы эндотелина, в том числе при ЛАГ.
Клинические исследования фазы I и II продемонстрировали, что мацитентан имеет дозозависимую фармакокинетику, отличается хорошей переносимостью у здоровых добровольцев и больных с артериальной гипертонией [19].
Недавно завершилось исследование SERAPHIN (Study of ACT-064992 on Morbidity and Mortality in Patients With Symptomatic Pulmonary Arterial
Hypertension) (фаза III). SERAPHIN – длительное исследование с оценкой клинических событий явилось наиболее крупным из проведенных за последние годы рандомизированных исследований у больных с ЛАГ (таблица 2).
Обращает на себя внимание то, что большинство исследований отличались краткосрочным периодом наблюдения и включали небольшое число пациентов (таблица 2).
На протяжении многих лет целью клинических исследований было изучение лекарственной терапии на переносимость физических нагрузок [18]. В качестве первичной конечной точки рассматривалась динамика дистанции в Т6МХ (таблица 2). Целью рандомизированного многоцентрового, двойного слепого, плацебо контролируемого клинического исследования SERAPHIN явилась оценка влияния мацитентана на заболеваемость и смертность больных с ЛАГ [19]. Первичной конечной точкой было время до развития первого эпизода заболеваемости и смертности. Клинические события были выбраны в качестве конечных точек в соответствии с рекомендациями IV Мирового симпозиума по ЛГ (рисунок 3).
Критериями включения явились возраст больных старше 12 лет, наличие ИЛГ, наследуемой ЛАГ, ЛАГ вследствие СЗСТ, оперированных врожденных пороков сердца – системно-легочных шунтов, ВИЧ, ЛАГ, индуцированной приемом лекарственных препаратов. Для включения в исследование была необходима верификация диагноза с помощью катетеризации правых отделов сердца. При оценке функционального статуса больные должны были проходить в Т6МХ>50м и иметь ФК
Таблица 2. Клинические исследования у больных ЛАГ
|
ЛС |
Исследование |
Количество пациентов |
Длительность |
Первичные конечные точки |
|
Бозентан |
Исследование 351 BREATH-1 BREATH-5 EARLY |
32 213 54 185 |
12 недель 16 недель 16 недель 24 недели |
6 МТХ 6 МТХ ЛССиндекс, SpO2 ЛСС, 6 МТХ |
|
Амбризентан |
ARIES-1 ARIES-2 |
202 192 |
12 недель 12 недель |
6 МТХ 6 МТХ |
|
Силденафил |
SUPER-1 PACES |
277 267 |
12 недель 16 недель |
6 МТХ 6 МТХ |
|
Тадалафил |
PHIRST |
405 |
16 недель |
6 МТХ |
|
Мацитентан |
SERAPHIN |
742 |
ОЦЕНКА клинических событий Минимальный период наблюдения 1 год |
Время до развития клинического ухудшения |
II, III, IV (ВОЗ). Сопутствующая терапия включала ингибиторы фосфодиэстеразы типа 5 или простаноиды (ингаляционные и пероральные формы), антагонисты кальция, а также L-аргинин при приеме указанных препаратов в стабильных дозах на протяжении не менее 3 месяцев до включения больных в исследование. В течение 28 дней после скрининга 742 пациента были рандомизированы в соотношении 1:1:1 для получения мацитентана 3 мг (n=250) и 10 мг (n=242) или плацебо (n=250) один раз в сутки. При оценке клинического статуса больных проводился Т6МХ, устанавливался ФК, анализировались лабораторные данные на визитах скрининга, рандомизации, через 3 и 6 месяцев от начала лечения и далее каждые 6 месяцев до завершения исследования. Уровни печеночных трансаминаз и гемоглобина анализировались ежемесячно и в течение 28 дней после завершения исследования. В рамках подисследования у ряда больных через 6 месяцев от начала лечения проводилась повторная катетеризация правых отделов сердца. Динамическое наблюдение за больными на фоне терапии мацитентаном/ плацебо осуществлялось до развития первичной конечной точки. Больные с нефатальным клиническим ухудшением завершали участие в двойном слепом исследовании и включались в открытое наблюдение с приемом мацитентана 10 мг. Больные без признаков клинического ухудшения продолжали наблюдение в рамках двойного слепого исследования.
Комбинированной конечной точкой в исследовании SERAPHIN явился период времени до развития первого события, связанного с ухудше- нием течения ЛАГ (прогрессирование ЛАГ, инициация терапии парентеральными простаноидами, трансплантация легких, предсердная септостомия) [19]. Прогрессирование ЛАГ устанавливалось при достижении совокупности трех критериев – снижение дистанции в Т6МХ на 15 и более % по сравнению с исходной (результат подтверждался в двух тестах, проведенных в различные дни в течение 2-недельного периода), ухудшение клинической симптоматики ЛАГ (ухудшение ФК, появление признаков декомпенсации правого желудочка без существенной динамики при применении пероральных диуретиков), потребность в дополнительной терапии. Все случаи ухудшения ЛАГ рассматривались специальным комитетом для верификации первичной конечной точки и решения вопроса о переводе больных в открытое наблюдение.
Вторичные конечные точки включали динамику дистанции в Т6МХ, % больных с улучшением ФК к 6 месяцу наблюдения, смерть по причине ЛАГ или госпитализации вследствие клинического ухудшения ЛАГ, смерть от любых причин. Для оценки безопасности лечения изучались нежелательные явления и отклонения в лабораторных тестах.
Включение больных осуществлялось в 151 центре из 39 стран за период с мая 2008 г. до декабря 2009 г. Период наблюдения должен был составить не менее 1 года для последнего включенного в исследование больного и до 4,5 лет для первого рандомизированного больного. Включение больных в исследование SERAPHIN завершилось в декабре 2009 г. Средний период наблю-
Рисунок 3. Клиническое ухудшение в исследовании SERAPHIN
Время до развития первого события-заболеваемость и смертность
1:1:1
Мацитентан 3мг и 10 мг Плацебо
1 прием в сутки
Study with
Endothelin Receptor Antagonist in Pulmonary
Аrterial Hypertension to Improve cliNical outcome


Потребность в простаноидах в / в или п/к
ФАТАЛЬНЫЙ ИСХОД
или
Предсердная септостомия
или
Трансплантация легких
или
или
Клиническое ухудшение

Ухудшение клинической симптоматики в виде увеличения ФК или появления / прогрессирования ПЖ декомпенсации
+
дистанции в Т 6 МХ > 15% в 2- х последоватальных тестах
+
Потребность в присоединении :
-
• Простаноидов per os или инг .
-
• ИФДЭ 5
-
• Др . АРЭ
-
• в ./ в диуретиков
Таблица 3. Снижение риска заболеваемости и смертности при ЛАГ
|
Первичная конечная точка в исследовании SERAPHIN Мацитентан снижает риск заболеваемости и смертности у больных с ЛАГ |
||
|
Доза Мацитентана (мг) |
Снижение относительного риска (%) |
p |
|
3 |
30 |
0,0108 |
|
10 |
45 |
<0,0001 |
|
Вторичные конечные точки Достоверная динамика отмечалась при применении Мацитентана |
||
|
||
|
N Engl J Med 2013; vol 369, N9:809-819 |
||
дения в исследовании составил 85,3 недель, 99,5 недель и 103,9 недель, соответственно, в группах лечения плацебо, мацитентаном в дозах 3 и 10мг.
За период наблюдения клинические события, свидетельствующие о прогрессировании заболевания, возникли у 287 больных. Первичная конечная точка была достигнута у 46,4%, 38,0% и 31,4% больных в группах плацебо, мацитентана 3 и 10 мг, соответственно. Применение мацитентана в дозах 3 и 10 мг способствовало снижению риска заболеваемости и смертности при ЛАГ на 30% и 45%, соответственно (таблица 3).
Наиболее часто первичной конечной точкой было развитие клинического ухудшения. Терапия мацитентаном оказалась эффективной как у больных с ЛАГ, получавших стабильную специфическую ЛАГ-терапию, так и у ранее нелеченных больных.
К 6 месяцу наблюдения в группе плацебо дистанция в Т6МХ уменьшилась на 9,4 м, в группах лечения мацитентаном прирост дистанции составил 7,4 м при назначении дозы 3 мг (эффект терапии +16,8 м по сравнению с плацебо) и 12,5 м при назначении 10 мг (эффект терапии +22,0 м по сравнению с плацебо). ФК улучшился по сравнению с исходным к 6 месяцу лечения у 13% больных в группе плацебо, 20% – в группе мацитента-на 3 мг (р=0,04) и 22% – в группе 10 мг (р=0,006). По сравнению с группой плацебо терапия маци-тентаном вызывала достоверное снижение ЛСС и повышение СИ.
Терапия характеризовалась благоприятным профилем переносимости. Участие в исследовании по причине развития нежелательных явлений отмечалось у 31 больного (12,4%) в группе плацебо, 34 (13,6%) и 26 (10,7%) в группах маци-тентана 3 мг и 10 мг, соответственно. В таблице 4 показана частота наиболее частых побочных явлений.
Частота более чем 3-х кратного повышения трансаминаз была незначительной: 3,6% и 3,8% при применении мацитентана в дозах 3 и 10 мг, 4,5% – в группе плацебо.
Совсем недавно в октябре 2013 г. препарат
Таблица 4. Нежелательные явления в исследовании SERAPHIN
|
Число больных с нежелательными явлениями (%) |
Плацебо |
Мацитентан 3 мг |
Мацитентан 10 мг |
|
Прогрессирование легочной гипертензии |
87 (34,9%) |
75 (30,0%) |
53 (21,9%) |
|
Развитие декомпенсации правого желудочка |
56 (22,5%) |
37 (14,8%) |
32 (13,2%) |
|
Побочные эффекты |
|||
|
Назофарингит |
29 (10,4%) |
37 (14,8%) |
34 (14,0%) |
|
Головная боль |
22 (8,8%) |
33 (13,2%) |
33 (13,6%) |
|
Анемия |
8 (3,2%) |
22 (8,8%) |
32 (13,2%) |
|
Повышение АСЛ/АЛТ>3ВГН |
4,5% |
3,6% |
3,4% |
N Engl J Med 2013; vol 369, N9:809-819
мацитентан (OPSUMIT) был одобрен Администрацией по контролю качества пищевых продуктов и лекарственных препаратов (США) для лечения больных с ЛАГ (группа 1) для предотвращения прогрессирования болезни (смерть, потребность в назначении парентеральных простаноидов, клиническое ухудшение ЛАГ (уменьшение дистанции в Т6МХ, ухудшение клинической симптоматики, потребность в дополнительной ЛАГ-терапии). Рекомендованная доза составляет 10мг 1 прием в день.
Полученные данные по изучению эффективности мацитентана у больных с ЛАГ, его влиянию на заболеваемость/ смертность и безопасности при длительном лечении убедительно свидетельствуют о том, что задача оптимизации терапии АРЭ в настоящее время решена. В клиническую практику внедряется новый перспективный препарат из этого класса, и его появление в нашей стране в ближайшее время позволит значительно улучшить возможности лекарственной терапии у больных, страдающих этим тяжелым недугом.
-
1. Galie N, Hoeper M.M., Humbert M., et al. Guidelines for the diagnosis and treatment of pulmonary hypertension: the Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology and the European Respiratory Society, endorsed by the International Society of Heart and Lung Transplantation. Eur Heart J 2009; 30 (20):2 493-537.
-
2. Национальные рекомендации ВНОК по диагностике и лечению легочной гипертензии, 2007.
-
3. Humbert M, Sitbon O, Chaouat A, et al. Survival in patients with idiopathic, familial, and anorexigen-associated pulmonary arterial hypertension in the modern management era.Circulation 2010;122:156–163.
-
4. Stewart DJ, Levy RD, Cernacek P. Increased plasma endothelin-1 in primary pulmonary hypertension: marker or mediator of disease? Ann Intern Med 1991;114:464-469.
-
5. Мартынюк Т.В., Чазова И.Е., Масенко В.П. и со-авт. Эндотелиальная дисфункция у больных с легочной гипертензией. // Кардиология. 1997. №10. С.25-29.
-
6. Dupuis J, Hoeper M.M. Endothelin receptor antagonists in pulmonary arterial hypertension. Eur Respir J 2008; 31: 407-415.
-
7. Rubin LJ, Badesch DB, Barst RJ et al. Bosentan therapy for pulmonary arterial hypertension. N Engl J Med 2002;346:896-903.
-
8. Galie N, Rubin LJ, Jansa P etal. Treatment of
patients with mildly symptomatic pulmonary arterial hypertension with bosentan (EARLY study): a double-blind, randomized, controlled trial. Lancet 2008; 371: 2093-2100.
-
9. Humbert M, Barst RJ, Robbins IM et al. Combination of bosentan with epoprostenol in pulmonary arterial hypertension: BREATHE-2. Eur Respir J 2004;24:353-359.
-
10. McLaughlinVV, Oudiz RJ, Frost A. et al. Randomized study of adding inhaled iloprost to existing bosentan in pulmonary arterial hypertension Am J Respir Crit Care Med 2006; 174:1257-1263.
-
11. Clozel M.,Gray G.A. Are there different ETB receptors mediating constriction and relaxation? J Cardiovasc Pharmacol 1995;26 (Suppl 3): S262-S264.
-
12. Iglarz M, Binkert C, Morrison K, et al. Pharmacology of macitentan, an orally active tissue-targeting dual endothelin receptor antagonist. J Pharmacol Exp Ther 2008; 327: 736–745.
-
13. Wagner OF, Christ G, Wojta J, et al. Polar secretion of endothelin-1 by cultured endothelial cells. J Biol Chem 1992; 267: 16066–16068.
-
14. Raja SG. Macitentan: a tissue-targeting endothelin receptor antagonist for the potential oral treatment of pulmonary arterial hypertension and idiopathic pulmonary fibrosis. Curr Opin Investig Drugs 2010; 11: 1066–1073.
-
15. Ding SS, Qiu C, Hess P, Xi JF, et al. Chronic endothelin receptor blockade prevents both early hyperfiltration and late overt diabetic nephropathy in the rat. J Cardiovasc Pharmacol 2003; 42: 48-54.
-
16. Jasmin JF, Lucas M, Cernacek P, and Dupuis J (2001) Effectiveness of a nonselective ET(A/B) and a selective ET(A) antagonist in rats with monocrotaline-induced pulmonary hypertension. Circulation 103: 314-318.
-
17. McLaughlin VV, Badesch DB, Delcroix M, et al. End points and clinical trial design in pulmonary arterial hypertension. J Am CollCardiol 2009; 54: Suppl. 1, S97–S107.
-
18. Souza R. SERAPHIN: results from a landmark study. Abstracts from ERS Congress 2012. www. clinicaltrials.gov.NCT00660179.
-
19. Pulido T, Adzerikho I, Channick R.N., et al. Macitentan and morbidity and mortality in pulmonary arterial hypertension. N Engl J Med 2013;369 (9):865–866.
Список литературы Мацитентан: эволюция класса антагонистов рецепторов эндотелина для повышения эффективности и безопасности лечения легочной артериальной гипертензии
- Galie N, Hoeper M.M., Humbert M., et al. Guidelines for the diagnosis and treatment of pulmonary hypertension: the Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology and the European Respiratory Society, endorsed by the International Society of Heart and Lung Transplantation. Eur Heart J 2009; 30 (20):2 493-537.
- Национальные рекомендации ВНОК по диагностике и лечению легочной гипертензии, 2007.
- Humbert M, Sitbon O, Chaouat A, et al. Survival in patients with idiopathic, familial, and anorexigen-associated pulmonary arterial hypertension in the modern management era.Circulation 2010;122:156-163.
- Stewart DJ, Levy RD, Cernacek P. Increased plasma endothelin-1 in primary pulmonary hypertension: marker or mediator of disease? Ann Intern Med 1991;114:464-469.
- Мартынюк Т.В., Чазова И.Е., Масенко В.П. и соавт. Эндотелиальная дисфункция у больных с легочной гипертензией.//Кардиология. 1997. №10. С.25-29.
- Dupuis J, Hoeper M.M. Endothelin receptor antagonists in pulmonary arterial hypertension. Eur Respir J 2008; 31: 407-415.
- Rubin LJ, Badesch DB, Barst RJ et al. Bosentan therapy for pulmonary arterial hypertension. N Engl J Med 2002;346:896-903.
- Galie N, Rubin LJ, Jansa P etal. Treatment of patients with mildly symptomatic pulmonary arterial hypertension with bosentan (EARLY study): a double-blind, randomized, controlled trial. Lancet 2008; 371: 2093-2100.
- Humbert M, Barst RJ, Robbins IM et al. Combination of bosentan with epoprostenol in pulmonary arterial hypertension: BREATHE-2. Eur Respir J 2004;24:353-359.
- McLaughlin VV, Oudiz RJ, Frost A. et al. Randomized study of adding inhaled iloprost to existing bosentan in pulmonary arterial hypertension Am J Respir Crit Care Med 2006; 174:1257-1263.
- Clozel M.,Gray G.A. Are there different ETB receptors mediating constriction and relaxation? J Cardiovasc Pharmacol 1995;26 (Suppl 3): S262-S264.
- Iglarz M, Binkert C, Morrison K, et al. Pharmacology of macitentan, an orally active tissue-targeting dual endothelin receptor antagonist. J Pharmacol Exp Ther 2008; 327: 736-745.
- Wagner OF, Christ G, Wojta J, et al. Polar secretion of endothelin-1 by cultured endothelial cells. J Biol Chem 1992; 267: 16066-16068.
- Raja SG. Macitentan: a tissue-targeting endothelin receptor antagonist for the potential oral treatment of pulmonary arterial hypertension and idiopathic pulmonary fibrosis. Curr Opin Investig Drugs 2010; 11: 1066-1073.
- Ding SS, Qiu C, Hess P, Xi JF, et al. Chronic endothelin receptor blockade prevents both early hyperfiltration and late overt diabetic nephropathy in the rat. J Cardiovasc Pharmacol 2003; 42: 48-54.
- Jasmin JF, Lucas M, Cernacek P, and Dupuis J (2001) Effectiveness of a nonselective ET(A/B) and a selective ET(A) antagonist in rats with monocrotaline-induced pulmonary hypertension. Circulation 103: 314-318.
- McLaughlin VV, Badesch DB, Delcroix M, et al. End points and clinical trial design in pulmonary arterial hypertension. J Am CollCardiol 2009; 54: Suppl. 1, S97-S107.
- Souza R. SERAPHIN: results from a landmark study. Abstracts from ERS Congress 2012. www. clinicaltrials.gov.NCT00660179.
- Pulido T, Adzerikho I, Channick R.N., et al. Macitentan and morbidity and mortality in pulmonary arterial hypertension. N Engl J Med 2013;369 (9):865-866.


