Масс-спектрометрическое изучение водно-ацетонитрильных растворов унитиола
Автор: Кулешов Денис Олегович, Кулешова Т.Э., Бобков Д.Е., Дьяченко А.А., Галль Н.Р., Галль Л.Н.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Приборостроение физико-химической биологии
Статья в выпуске: 3 т.28, 2018 года.
Бесплатный доступ
Унитиоловый тест с измерением времени полуокисления унитиола электрохимическими и фотометрическими методами нашел широкое применение в изучении биологического влияния геомагнитных и космофизических факторов на живые организмы. Изучение продуктов окисления унитиола и скоростей их образования было проведено методом масс-спектрометриии с электрораспылением. Показано, что в масс-спектрах водно-ацетонитрильных растворов унитиола наряду с катионированным натрием ионом мономера унитиола (C3H7O3S3Na)Na+ присутствуют в значительном количестве ионы катионированных натрием ассоциатов унитиола общего вида (C3H7O3S3Na) n Na+, где величина n достигала 8. Интенсивности пиков ассоциатов уменьшались с увеличением числа молекул в ассоциате, однако общая интенсивность ассоциатов превышала интенсивность мономера. С повышением концентрации относительная суммарная интенсивность ассоциатов возрастала, что позволяет предположить их образование непосредственно в водном растворе. Изучение процессов окисления может дать дополнительную информацию о влиянии внешних условий на окислительно-восстановительные процессы живого организма.
Влияние физических факторов, унитиоловый тест, масс-спектрометрия с электрораспылением, ассоциаты
Короткий адрес: https://sciup.org/142214875
IDR: 142214875 | УДК: 542.9 | DOI: 10.18358/np-28-3-i7283
Mass-spectrometric study of unithiol water-acetonitril solutions
Unithiol test is widely used for study of biological effect on living organisms of geomagnetic and space physical factors; the test is based on semi oxidation time measurements done electrochemically or photo metrically. To measure the products of unithiol oxidation reaction and rates of their production, ESI mass-spectrometric study has been made. Unithiol associates cathionated with Na+ have been found in mass-spectra of its water-acetonitrile solutions with general formula (C3H7O3S3Na) n Na+ with n up to 8; they present in essential amount together with Na+ cathionated monomer ion. Associate peak intensities were decreased with the molecular number, but their total intensity was higher than that of monomer. The associate total intensity grows with increase in concentration, this is an evidence for their production directly in the solution. Unithiol oxidation process study can give additional information about the outer factor effect on oxidation and reduction processes in a living body.
Текст научной статьи Масс-спектрометрическое изучение водно-ацетонитрильных растворов унитиола
В настоящее время все более пристальное внимание в науках о жизни уделяется изучению роли слабых физических факторов, особенно электромагнитных полей, в процессах, протекающих в молекулярных системах живых организмов. В связи со сверхнизкими интенсивностями этих факторов, проявляющихся, однако, в выраженных макроскопических реакциях живых систем, для их регистрации используются, как правило, биологические тесты, а потому весьма актуальной является задача изучения молекулярных систем и биохимических процессов, которые могут быть задействованными в таких реакциях в качестве тестовых.
Как известно, огромную роль в биохимических процессах, протекающих в живых системах, играют окислительно-восстановительные реакции (ОВР). К их числу относятся ОВР тиолов, окисление которых в мягких физиологических условиях приводит к образованию дисульфидов, причем эта реакция является обратимой. Биотиолы в мягких физиологических условиях легко вступают в разнообразные химические реакции, причем на их скорость оказывают влияние любые внешние воздействия, вызывающие изменения пространствен- ной конфигурации тиолсодержащей молекулы или окружающей ее среды [1]. Важнейшим признаком тиоловых соединений, определяющим их специфическую биологическую активность, является высокая реакционная способность сульфгидрильных групп, обусловленная уникальными особенностями атома серы: легкой поляризуемостью электронов и подвижностью незанятых d-орбиталей [2]. Это позволило в рамках концепции прямой зависимости биохимических реакций и физиологических процессов от окислительно-восстановительного состояния биологической системы [3] и окружающей ее среды [4] выделить окислительно-восстановительные превращения тиоловых соединений в качестве единой тиол-дисульфидной системы организма (ТДС), представляющей собой совокупность реакционноспособных тиоловых соединений, находящихся в организме в данный момент в восстановленном и окисленном состояниях и сохраняющих способность к их изменению — окислению или восстановлению.
В.В. Соколовским было показано [5], что состояние ТДС организма может быть количественно охарактеризовано отношением концентраций сульфгидрильных и дисульфидных групп, т. е. величиной тиол-дисульфидного отношения (ТДО), являющегося интегральным показателем реакции организма на действие окружающей среды. Возможность количественно определить ТДО в свою очередь позволила перейти от теоретических концепций биологических редокс-систем к их практическому использованию при изучении механизмов развития и поиске путей лечения заболеваний, а также при использовании ТДО в качестве показателя физиологического состояния организма, его неспецифической резистентности. Используя ТДО в качестве инструмента для оценки редокс-состояния живого организма, В.В. Соколовский впервые доказательно связал между собой процессы жизнедеятельности и их изменение под действием солнечной активности, раскрыв, тем самым, биологический механизм влияния внешних физико-химических и космогеофизических факторов на физиологическое состояние живого организма. Исследования в этом направлении, интерес к которым сильно вырос в связи с развитием космонавтики и появлением гелиобиологии как самостоятельного направления исследований, базировались на регистрации ТДО крови in vivo и регистрации его изменения в корреляции с изменением внешних факторов, воздействующих на организм человека, выступающий в данном случае в качестве биологического теста. Однако признанные успехи химического теста Дж. Пиккарди (реакция гидролиза хлорида висмута) в установлении влияния космических процессов на свойства этого коллоидного раствора вдохновили В.В. Соколовского [6] предложить модельную химическую систему для изучения реакции ТДС организма на влияние внешних химических, физических и биологических факторов. В качестве перспективной модели ТДС им было предложено использовать реакцию окисления унитиола (2,3-димеркаптопропан- сульфоната-1 натрия) нитритом натрия, причем за количественный критерий было принято время полуокисления тиоловых групп унитиола (ВПОУ). Им предполагалось, что пространственная близость двух SH-групп облегчает образование внутримолекулярной дисульфидной связи при окислении в "мягких" условиях и, таким образом, позволяет имитировать функциональный центр белков, ответственный за их редокс-превращения. Полная корреляция между величинами ТДО in vivo и ВПОУ, неизменно подтверждаемая в многолетних экспериментах группы В.В. Соколовского, позволяет считать этот тест полноценным химическим сенсором in vitro для изучения редокс-изменения состояния тиоловых соединений живого организма. Унитиоловый тест с измерением ВПОУ нашел широкое применение в изучении биологического влияния геомагнитных и космофизических факторов на живые организмы [7].
В работах В.В. Соколовского унитиоловый тест реализовывался с использованием электрохимических и спектрофотометрических методов, крайне трудоемких, связанных с ручным титрованием растворов и требующих значительной затраты времени. При этом единственным результатом каждого измерения являлось определение ВПОУ, в то время как возможность определения продуктов окисления и изучения скоростей их образования может дать дополнительную информацию о влиянии факторов различной природы на биологические объекты. Такая информация может быть получена при использовании масс-спектрометрического детектирования процесса окисления унитиола, и первым этапом такого исследования является масс-спектрометрическое изучение растворов унитиола.
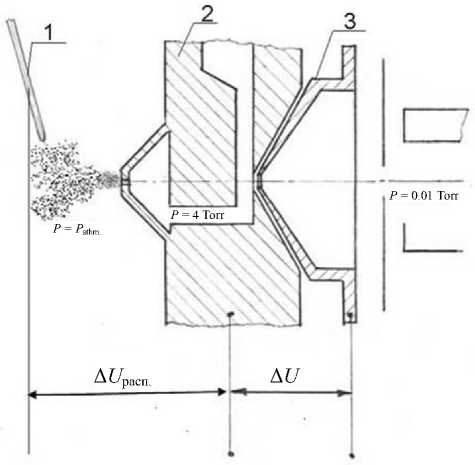
Рис. 1. Схематичное изображение газодинамического интерфейса времяпролетного масс-спектрометра МХ-5310.
1 — распыляющий капилляр, 2 — газодинамическое сопло, 3 — скиммер
ОБОРУДОВАНИЕ И РЕАКТИВЫ
Исследования проводились на хроматомасс-спектрометре высокого разрешения МХ-5310 (ИАП РАН, Россия) с ионизацией электрораспылением. Интерфейс масс-спектрометра, характерные размеры и напряжения на элементах системы распыления раствора представлены на рис. 1. В качестве образца для исследования использовались фармацевтический препарат в ампулах, содержащий 5 % раствор унитиола, и порошковый моногидрат унитиола. Для поддержания необходимого pH использовалась уксусная кислота. Для приготовления растворов использовалась дистиллированная вода и ацетонитрил класса 0.
РЕЗУЛЬТАТЫ
Типичный масс-спектр унитиола представлен на рис. 2. Масс-спектр получен путем прямого ввода пробы в масс-спектрометр с помощью шприцевого насоса. Исследуемая проба готови- лась из фармацевтического препарата унитиола разведением 1 % уксусной кислотой в 100 раз, а затем ацетонитрилом — в 10 раз. Масс-спектр записывался в течение 5 мин. Скорость подачи пробы на ввод в узел распыления масс-спектрометра составляла 1 мкл/мин. Давления в интерфейсе, газонаполненной квадрупольной ячейке и масс-анализаторе были постоянными в ходе всех экспериментов и составляли 4 Торр (интерфейс), 10–2 Торр (газонаполненная квадрупольная ячейка), 1.6·10–7 Торр (масс-анализатор). Калибровка шкалы масс осуществлялась по резерпину. Точность определения m/z составляла 10 ppm во всех измерениях.
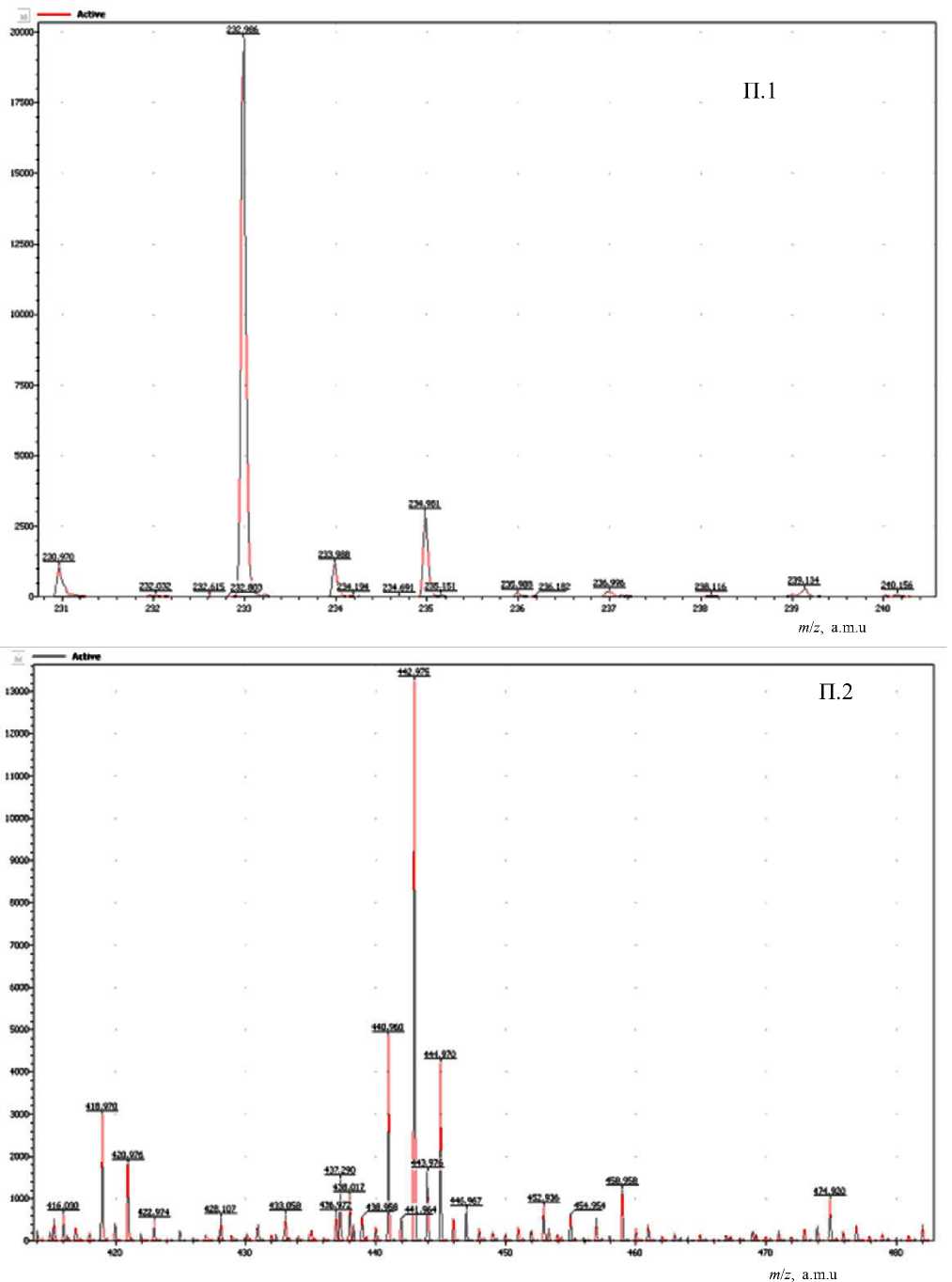
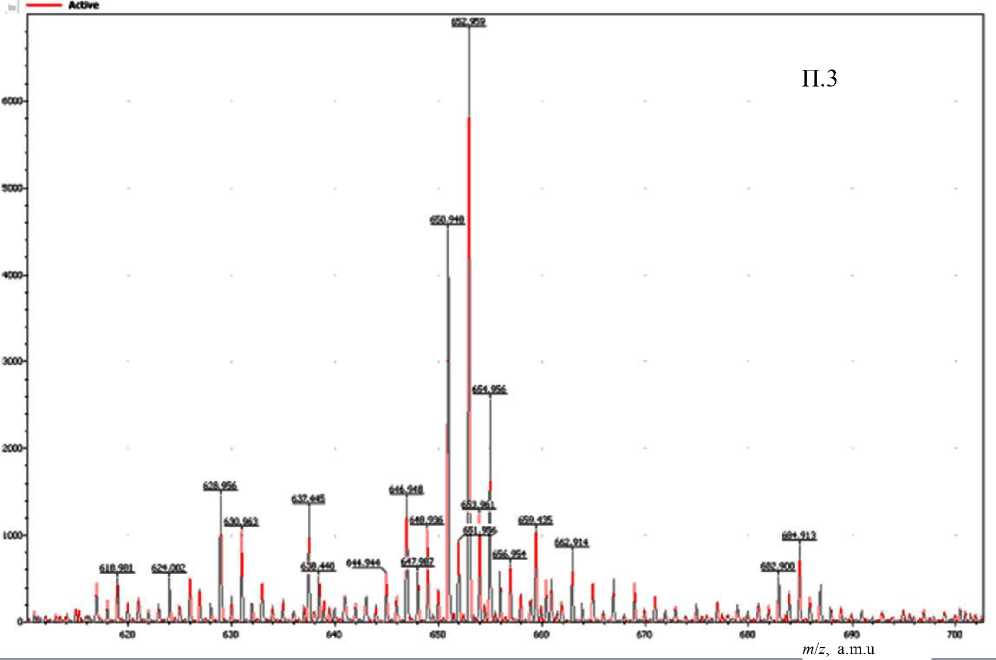
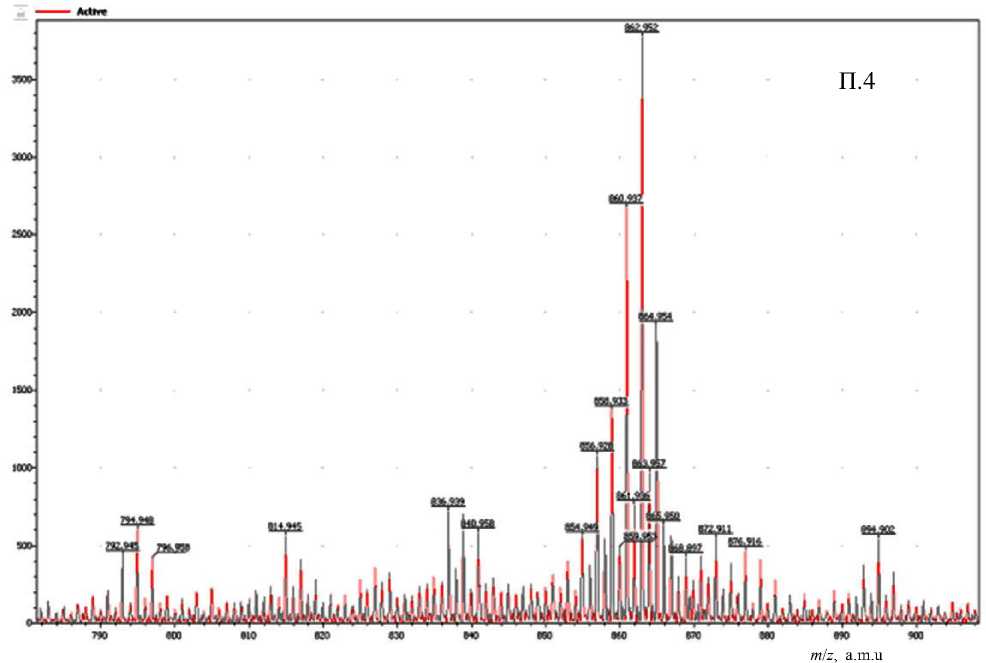
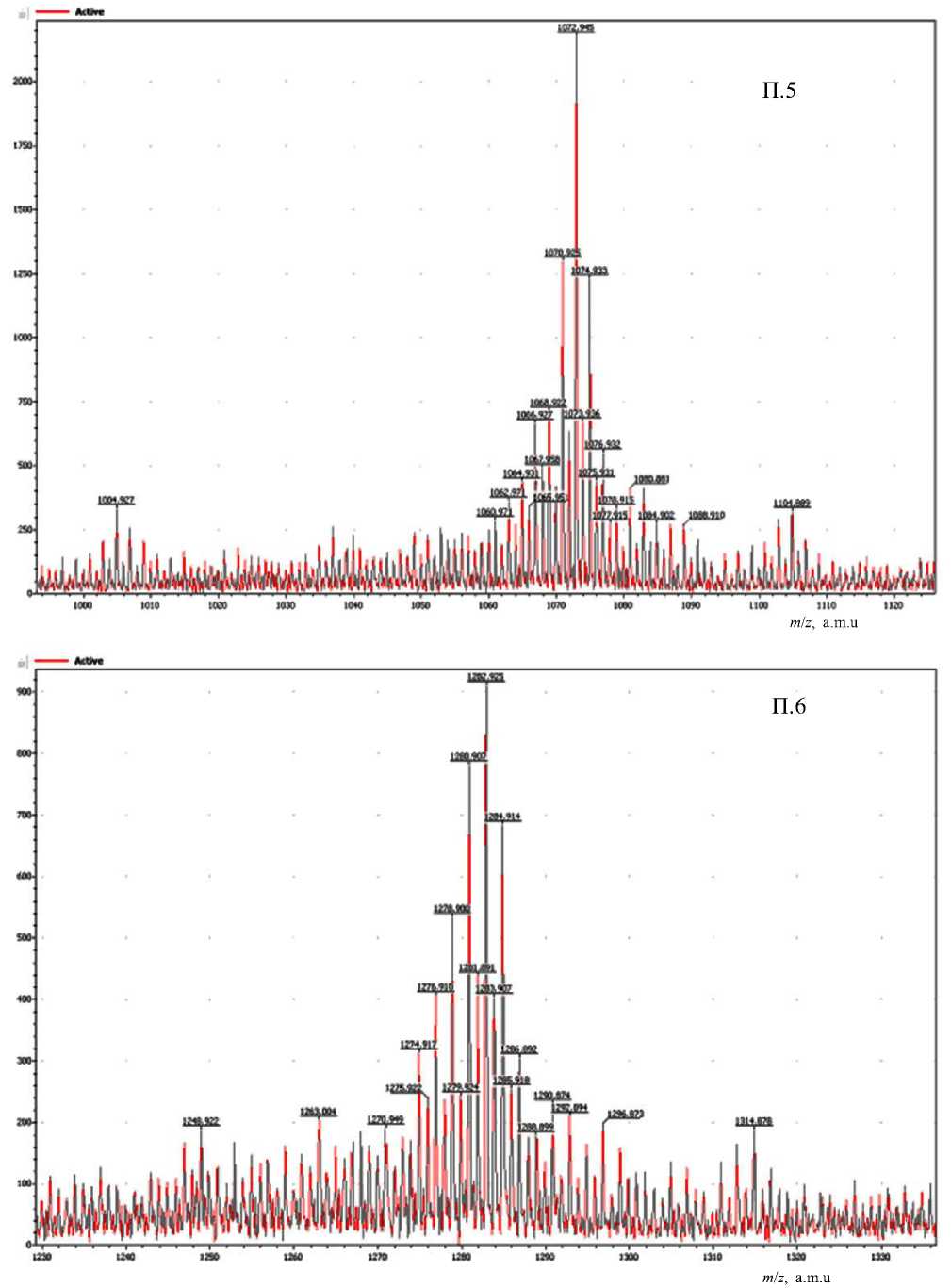
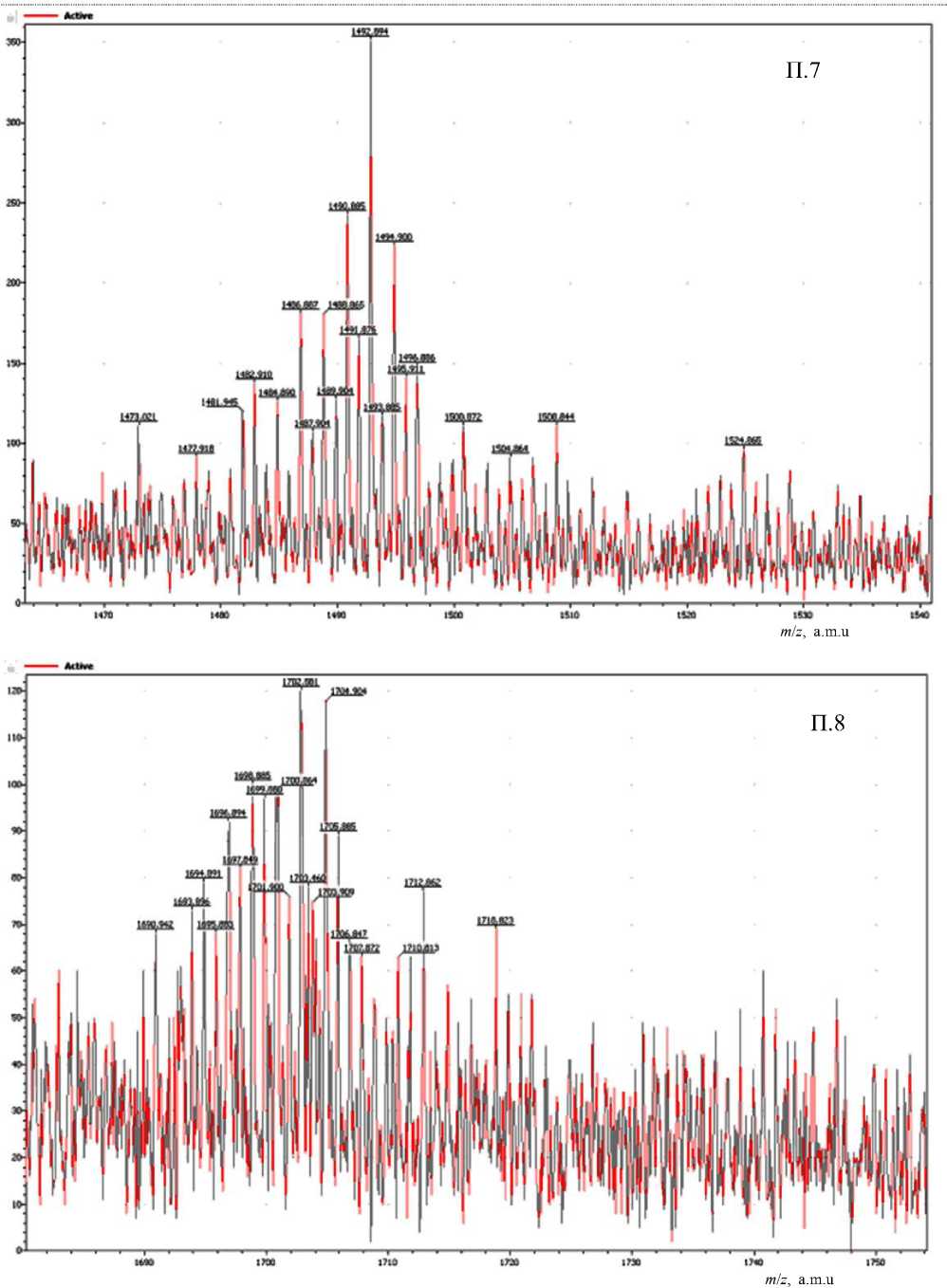
Как видно из рис. 2, в масс-спектре унитиола зарегистрированы восемь групп пиков с наиболее интенсивными ионами m / z = 232.98, 442.97, 652.95, 862.95, 1072.9, 1282.9, 1492.8, 1702.9. Для проведения идентификации ионов эти группы более детально представлены в Приложении, П.1–П.8.
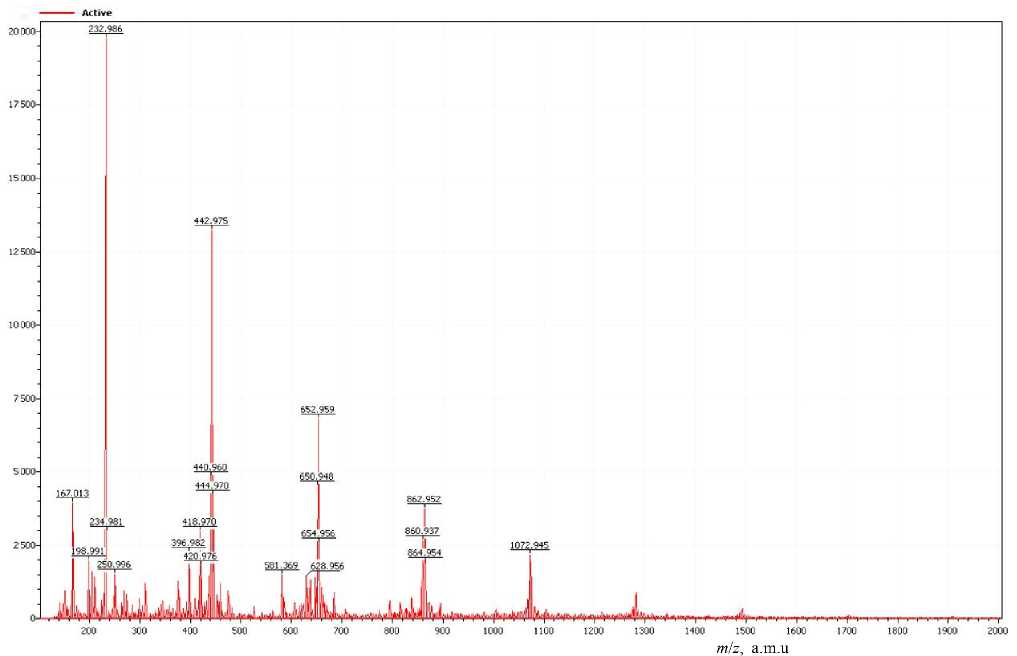
Рис. 2. Масс-спектр раствора унитиола ( C = 2.38·10 –4 моль/л) в диапазоне m / z 100–2000.
Напряжение распыления — 3200 В, разность потенциалов между соплом и скиммером — Δ U =120 В
Ранее уже было установлено [8], что молекулы унитиола, наблюдаемые в масс-спектре, образуют ионы, катионированные натрием. Это позволяет считать, что пик m / z = 232.98 в первой группе ионов (Приложение, рис. П.1) есть катионированный натрием ион унитиола, что подтверждается его изотопными (по сере) пиками с m / z = 233.98 и 234.98. Аналогично можно считать, что основной пик второй группы ионов m / z = 442.975 есть катионированый натрием ион ассоциата двух мо-ноизотопных молекул унитиола, причем ионы с m / z = 443.97 и 444.97 являются его изотопными (по сере). В этой же группе пик с m / z = 440.96 является моноизотопным ионом катионированной натрием молекулы ациклического димера унитио-ла, а пики m / z = 441.96 и 442.97 — его изотопными. В остальных группах ионов (Приложение, рис. П.3–П.8) основные пики соответствуют ассоциатам, образованным тремя, четырьмя и далее до восьми молекулами унитиола, что позволяет описать все катионированые ассоциаты, представленные на рис 2 (Приложение, П.1–П.8), общей формулой (C 3 H 7 O 3 S 3 Na) n Na+, где n = 1,…, 8. Кроме уже перечисленных, в спектрах всех групп также присутствуют ионы, соответствующие продуктам окисления унитиола в свободной и ассоциированной формах, катионированных ионом натрия.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Присутствие в спектре водного раствора уни-тиола интенсивных групп ионов ассоциатов с n = 2
и более, вместо ожидаемых только ионов мономеров ( n = 1), позволяет сделать два предположения:
-
1) ассоциаты возникают в результате комплекса физических процессов при электрораспылитель-ной ионизации либо
-
2) ассоциаты образуются непосредственно в водном растворе при растворении унитиола.
Для проверки первого предположения было исследовано влияние условий распыления раствора и транспортировки ионов в интерфейсе на состав ионов унитиола в различных группах масс-спектра. В качестве изменяющихся условий были взяты напряжение распыления U расп. , определяющее структуру аэрозоля, и разница потенциалов между соплом и скиммером Δ U , характеризующая не только столкновительные процессы в интерфейсе, но и пропускание ионов в отверстие скиммера (рис. 1). Напряжение распыления U расп. изменялось от 2400 В до 4000 В с шагом 400 В; разность потенциалов Δ U между соплом и скиммером изменялась дискретно от 40 В до 240 В при фиксированных напряжениях распыления U расп. и U ским. . Скорость подачи пробы в масс-спектрометр во всех измерениях составляла 1 мкл/мин.
На рис. 3 представлено изменение количества ионов ассоциатов в зависимости от параметров распыления и фокусировки ионов в интерфейсе. Из рисунка видно, что в широком диапазоне изменения напряжения распыления относительное количество ассоциатов изменяется незначительно, не более чем на 20%, но весьма существенно зависит от напряжения между соплом и скиммером.
Σ I + n %
250 г
200 •
50 •
О
250 AZ7 [В] 300
Рис. 3. Влияние потенциала распыления U расп. и разности потенциалов между соплом и скиммером Δ U на величину относительного количества ионов ассоциатов унитиола с различным числом n молекул в ассоциате.
1 — n = 2; 2—– n = 3; 3 — n = 4; 4 — n = 5; 5 — n = 6
Состав исследуемых проб
|
C (унитиол), моль/л |
V (р-р унитиола ( C = 10 –3 моль/л)), мкл |
V (1% р-р CH 3 COOH), мкл |
V (ацетонитрил), мкл |
|
10–5 |
10 |
490 |
|
|
2∙10–5 |
20 |
480 |
|
|
3∙10–5 |
30 |
470 |
|
|
4∙10–5 |
40 |
460 |
|
|
5∙10–5 |
50 |
450 |
|
|
6∙10–5 |
60 |
440 |
500 |
|
7∙10–5 |
70 |
430 |
|
|
8∙10–5 |
80 |
420 |
|
|
9∙10–5 |
90 |
410 |
|
|
10 –4 |
100 |
400 |
|
|
2.5∙10–4 |
250 |
250 |
При этом наряду с ионами мономера ионы ассоциатов присутствуют всегда, составляя от 60 % до 200 % от их интенсивности. Перераспределение кластеров разных масс в масс-спектре в зависимости от Δ U , видимо, связано с более сложными электрогазодинамическими процессами, не учитываемыми в данном случае.
Второе объяснение присутствия в масс-спектре ассоциатов больших масс связано с предположением, что они были образованы непосредственно в растворе при растворении унитиола. Для его проверки была проведена регистрация масс- спектров в диапазоне концентраций 10–5– 2.5∙10–4 М. Для этого раствор порошкового моногидрата унитиола первоначально готовился в 1 % уксусной кислоте с концентрацией C = = 10–3 моль/л. Далее из этого раствора путем его разбавления 1 % уксусной кислотой CH3COOH и ацетонитрилом CH3CN готовились пробы, состав которых приведен в таблице. Полученные пробы вводились в область распыления интерфейса масс-спектрометра через распылительный капилляр с помощью шприцевого насоса. Скорость
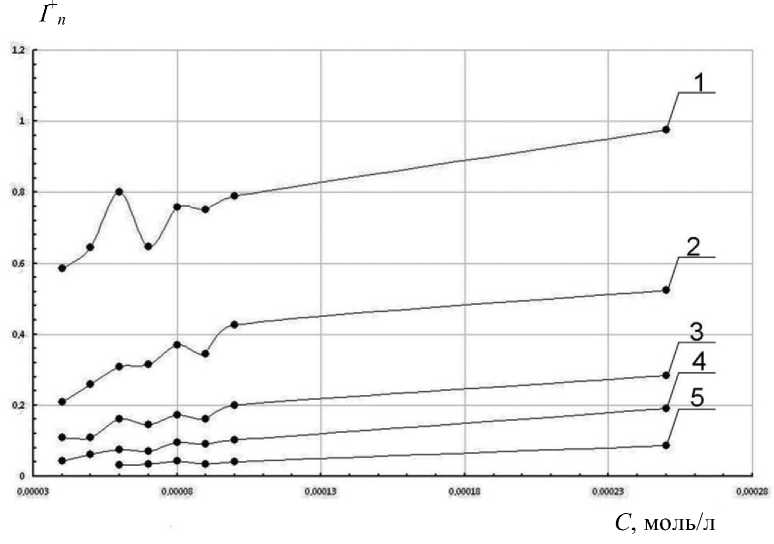
Рис. 4. Изменение относительного количества ионов ассоциатов унитиола с различным числом n молекул в ассоциате при изменении концентрации раствора С моль/л.
1 — n = 2, 2 — n = 3, 3 — n = 4, 4 — n = 5, 5 — n = 6. Интенсивности пиков ассоциатов нормированы на интенсивность аналитического сигнала мономера унитиола
подачи составляла 1 мкл/мин (рис. 1). В ходе работы записывалось по 5 спектров на каждую точку, значения интенсивностей пиков в которых усреднялись. Погрешности определения интенсивностей в области низких концентраций (до 3·10–5 М) составляли величины до 20 %, в связи с чем в дальнейшем обсуждении эти концентрации не рассматривались. При увеличении концентрации унитиола интенсивности пиков воспроизводились значительно лучше, и при концентрациях выше 4∙10–5 М погрешность определения интенсивностей даже наиболее слабых пиков не превышала 6 %. Каждый спектр записывался в течение 50 с. В качестве электрических параметров для изучения зависимости вида масс-спектра унитиола от его концентрации были использованы следующие их величины: U расп. = 3200 В и U сопл. = 180 В. Результаты измерений представлены на рис. 4.
Из рис. 4 видно, что в диапазоне концентраций от 4∙10–5 до 2.5·10–4 моль/л с увеличением концентрации унитиола в растворах, приготовленных из кристаллического моногидрата унитиола, относительное содержание ионов-ассоциатов в масс-спектре растет с увеличением концентрации, что подтверждает предположение о том, что ассоциаты возникают непосредственно в растворе уни-тиола. Значительные колебания относительных интенсивностей пиков связаны, предположительно, со взаимопревращениями ассоциатов унитиола в растворе. Такой же характер имеет зависимость содержания в масс-спектре ионов-ассоциатов от концентрации для растворов унитиола, приготовленных путем разведения 1 % уксусной кислотой исходного фармацевтического препарата "унитиол".
ЗАКЛЮЧЕНИЕ
Как следует из проведенных измерений, в масс-спектрах водно-ацетонитрильных растворов уни-тиола наряду с катионированным натрием ионом мономера унитиола (C 3 H 7 O 3 S 3 Na)Na+, присутствуют в значительном количестве ионы катиониро-ванных натрием ассоциатов унитиола общего вида (C 3 H 7 O 3 S 3 Na) n Na+, где наблюдаемая величина n достигала 8. Интенсивности пиков ассоциатов уменьшались с увеличением числа молекул в ассоциате, однако общая интенсивность суммы ассоциатов превышала интенсивность мономера. С повышением концентрации относительная суммарная интенсивность ассоциатов возрастала, что подтверждает второе предположение, а именно, что ассоциаты возникают непосредственно в водном растворе унитиола и далее в таком виде находятся в растворе. Это означает, что процесс окисления является значительно более сложным, чем это предполагалось создателями унитиолового теста. Изучение этих процессов может дать дополнительную информацию о влиянии внешних условий на окислительно-восстановительные процессы живого организма.
ПРИЛОЖЕНИЕ
Фрагменты полного масс-спектра унитиола: группы пиков ассоциатов n = 1–8
Работа выполнена при поддержке госзадания
№ 43-12, а также при финансовой поддержке Российского научного фонда (проект 14-50-00068)
Список литературы Масс-спектрометрическое изучение водно-ацетонитрильных растворов унитиола
- Соколовский В.В. Тиолдисульфидная система в реакции организма на факторы окружающей среды. СПб.: Наука, 2008. 112 с.
- Jocelyn P. Biochemistry of the SH-group. The occurrence, chemical properties, metabolism and biological function of thiol and disulphides. London, N.Y.: Acad. Press, 1972. 404 p.
- Essex D. Redox control of platelet function//Antioxidants and redox signaling. 2009. Vol. 11, no. 5. P. 1191-1225.
- Daynes R., Enioutina E., Jones D. Role of redox imbalance in the molecular mechanisms responsible for immunosenescence//Antioxidants and redox signaling. 2003. Vol. 5, no. 5. P. 537-548.
- Соколовский В.В. Тиоловые антиоксиданты в молекулярных механизмах неспецифической реакции организма на экстремальное воздействие//Вопросы медицинской химии. 1988. Т. 34, № 6. C. 200-210.
- Соколовский В.В., Соколовская Т.М., Шубина Л.Н. О биохимическом механизме токсического действия двуокиси азота//Фармакология и токсикология. 1974. Т. 37, № 4. С. 469-471.
- Горшков Э.С., Иванов В.В., Соколовский В.В. Редокс реакции в космобиологии. СПб.: Изд. Политехн. университета, 2014. 194 с.
- Kuleshov D.O., Berezkina T.E., Russkikh Y.V., et al. Application of high-performance liquid chromatography/high-resolution mass spectrometry to the investigation of sodium 2, 3-disulfanyl-1-propanesulfonate (unithiol) and products of its oxidation with hydrogen peroxide//Journal of Analytical Chemistry. 2016. Vol. 71, no. 14. P. 1381-1388.


