Математическая модель образования и движения анионных вакансий при восстановлении металлов в комплексных оксидах
Автор: Гамов Павел Александрович, Дрозин Александр Дмитриевич, Чернобровин Виктор Павлович, Дукмасов Владимир Георгиевич, Чаплыгин Борис Александрович, Пластинин Борис Глебович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 4 т.18, 2018 года.
Бесплатный доступ
Предложено математическое описание процесса образования и движения анионных вакансий при восстановлении металлов в комплексных оксидах с позиции диффузионных и тепловых процессов, протекающих в фазах восстановителя и оксида, а также химических реакций на поверхности раздела фаз. Рассмотрена система, состоящая из сферической частицы руды, находящейся в атмосфере газообразного восстановителя. Частица руды представляет собой гомогенный газонепроницаемый комплексный оксид следующего компонентного состава: O, Fe, Si, Mg. Газовая фаза состоит из двух компонентов - СО и СО2. Поверхность рудной частицы является непроницаемой для компонентов обеих фаз. Восстановитель не может проникать внутрь куска, и все обменные процессы протекают на границе раздела. Для фазы рудной частицы составлены уравнения теплопроводности, а также уравнения диффузии компонентов фазы. Для газовой фазы, окружающей частицу, также составлены уравнения теплопроводности и диффузии реагентов с учетом изменения размеров частицы. Для поверхности раздела получено уравнение теплопередачи, связывающее тепловые потоки из обеих фаз к поверхности раздела с тепловым эффектом химических реакций. Кроме того, получены уравнения массопереноса компонентов рудной фазы, связывающие удаление атомарного кислорода с поверхности раздела с подводом его к поверхности раздела из глубины рудной частицы. Составлены уравнения массопереноса компонентов газовой фазы, связывающие подвод реагентов к поверхности раздела фаз с расходом их на поверхности. Учтено влияние основных физико-химических параметров на скорость образования и движения восстановительных вакансий. Составлена математическая модель.
Восстановление металлов, комплексные руды, моделирование
Короткий адрес: https://sciup.org/147232512
IDR: 147232512 | УДК: 669-1 | DOI: 10.14529/met180402
Mathematical model of anionic vacancy formation and motion during reduction of metals from complex oxides
The paper proposes a mathematical description of anion vacancies being formed and moving when metals are reduced from complex oxides; the process is described in terms of the diffusion and thermal processes occurring in the reductant and oxide phases, as well as in terms of chemical reactions occurring at the interface. It dwells upon a system consisting of a spherical ore particle contained in the atmosphere of a gaseous reductant. Ore particle is a homogeneous gas-tight complex oxide of the following composition: O, Fe, Si, Mg. The gas phase consists of two components, СО and СО2. The ore-particle surface is impervious to the components of both phases. The reductant is unable to get inside the particle, meaning that all the exchange processes occur at the interface. For the ore-particle phase, the researchers have constructed a thermal-conductivity equation as well as phase-component diffusion equation. For the gaseous phase around the particle, the researchers have constructed the equations of thermal-conductivity and diffusion of reagents, which take into account alterations of the particle size. A heat-transfer equation has been derived for the interface, which links both phase-to-interface heat fluxes to the thermal effects of chemical reactions. Furthermore, ore-phase component mass transfer equations have been derived to link the removal of atomic oxygen from the interface to such oxygen being channeled from the ore-particle depth to the interface. Gas-phase component mass transfer equations have been derived to link the supply or reagents to the interface and the superficial flow of such reagents. The research takes into account how basic physicochemical parameters affect the reducing-vacancy formation rate and motion speed. A mathematical model is compiled.
Текст научной статьи Математическая модель образования и движения анионных вакансий при восстановлении металлов в комплексных оксидах
Интерес к бескоксовым способам извлечения железа постоянно растет, повышается необходимость вовлечения в производство бедных и комплексных руд. Следствием этого явилось большое количество работ, посвященных изучению процесса восстановления железа из различных рудных и нерудных материалов с использованием углеродсодержащих восстановителей разного качества. Однако в результате сложности состава рудного материала картина выделения в нем металла в процессе восстановления сильно отличается от результатов восстановления железа в богатых рудах [1–3]. Для бедных и комплексных руд это, как правило, равномерное выделение частиц металла по всему объему оксидной вмещающей фазы. И хотя такие руды обычно являются плотными материалами с низкой газопроницаемостью, восстановление идет с большой скоростью при относительно невысокой температуре [4–6]. Всё это вызывает серьёзные трудности в объяснении механизма восстановления металлов с использований классических положений.
Один из наиболее активно развивающихся подходов к объяснению процесса восстановления металлов из комплексных оксидных материалов основан на рассмотрении твердофазных процессов, протекающих в несовершенных (дефектных) кристаллах [7, 8]. При нагреве в восстановительных условиях кристаллическая решётка оксида насыщена анионными вакансиями (примесными, обусловленными присутствием примесных катионов пониженного заряда, термическими – парными дефектами Шоттки, и восстановительными). Часть вакансий содержит «лишние» (дефектные) электроны. Генератором таких вакансий является восстановитель, который на поверхности реагирования извлекает из решётки оксида кислород, отдавая ему свои валентные электроны, а ранее локализованные у аниона электроны остаются в решётке оксида, удерживаясь электрическим полем. Таким образом, восстановитель взаимодействует не с молекулой оксида металла, а с анионом кислорода кристаллической решетки, например, по реакциям:
( MgFeSiO 4 ) = ( Mg 2 + ) + ( Fe 2 + ) + ( Si 4 + ) + 4 ( O 2 - ) (1) { CO } + ( O 2 - ) = { CO2 } + ( V a2 - ) (2) ( Fe 2 + ) + ( V a2 - ) = Fe (3) ( Mg 2 + ) + ( Si 4 + ) + 3 ( O 2 - ) = ( MgSiO g ) (4)
( MgFeSiO4 ) + { CO } = Fe + ( MgSiO3 ) + { CO2 } , (5) где Va 2 - - восстановительная вакансия, содержащая два электрона. В круглых скобках указаны компоненты оксидной фазы, в фигурных – газовой, без скобок – металлической фазы.
Если в ближайшем окружении все катионы обладают равным сродством, то при перемещении вакансии электроны легко переходят от одного катиона к другому, сопровождая вакансию от места появления до места её стока. В местах стока таких вакансий и формируются зародыши металлической фазы.
Данный подход позволяет объяснить высокую скорость процесса восстановления, а также появление металлической фазы внутри объёма оксидной, куда доступ восстановителя отсутствует. Однако он в значительной мере является качественным и не позволяет оценить степень влияния различных физикохимических параметров на скорость процесса восстановления.
В данной работе предпринята попытка перейти к количественному описанию, построить математическую модель, способную учитывать не только химические реакции, протекающие на поверхности раздела руда – восстановитель, но и учесть диффузионные потоки в системе.
Обоснование методики
В качестве основы для разработки модели взяты результаты предшествующих работ [9–12].
Рассмотрим систему, состоящую из частицы руды (фаза Ф), находящейся в атмосфере газообразного восстановителя (фаза V ). Поверхность рудной частицы F является непроницаемой для компонентов обеих фаз, следовательно, восстановитель не может проникать внутрь куска, и все обменные процессы протекают на границе раздела.
Считаем частицу сферической. Введём сферическую систему координат с началом в центре частицы (см. рисунок). Всю систему также считаем сферической. Полагая, что начальное распределение параметров состояния системы (концентраций компонентов, скоростей, температуры и других величин) обладает сферической симметрией. Можно
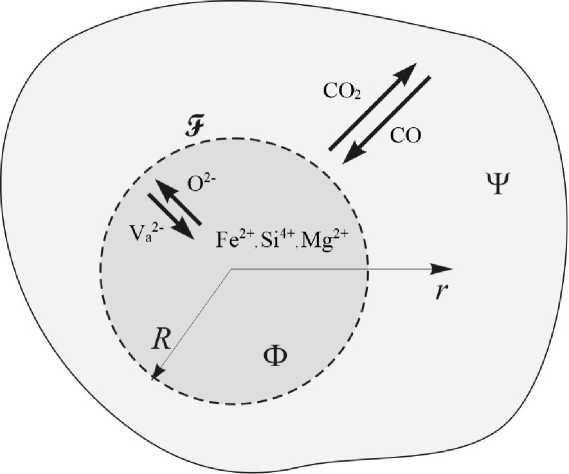
Графическая модель процесса восстановления, протекающего в системе «рудная частица Ф – восстановительная газовая фаза Ψ »
считать, что и в дальнейшем в любой момент времени распределение всех характеризующих систему величин обладает сферической симметрией.
В общем виде химические реакции на поверхности радела фаз можно представить в следующем виде:
« 11 R 1 + - + П 1 m R m = P 1 ,
....................................., (6)
1. В фазе рудной частицы Ф протекают процессы теплопроводности и диффузии:
1) уравнение теплопроводности:
д т = х Ф ХАГ 2 д Т ) д t р Ф c p r 2 д r V д r J ,
n n 1 R 1 + — + n nm R m = P n ,
где R 1 , — , R m - набор компонентов фазы V ;
где T – температура в данной точке; t – время; λ – коэффициент теплопроводности; ρ – плотность; c P - теплоемкость фазы; r ° - расстояние от центра частицы,
2) уравнения диффузии компонентов фа-
P 1 , — , P n - набор компонентов фазы Ф;
n ij ( i = 1, — n ; j = 1, — m ) - стехиометрические коэффициенты реакций. Причем компоненты одной фазы неограниченно растворимы друг в друге и нерастворимы в компонентах другой фазы.
Для примера допустим, что частица руды (фаза Ф) представляет собой гомогенный газонепроницаемый комплексный оксид следующего компонентного состава: O, Fe, Si, Mg. Газовая фаза V состоит из двух компонентов -СО и СО2. При достижении температуры на-
зы Ф :
д c Ф 2
О2
д t
= D Ф 2
О2
1 д r 2 д r
r
V
чала восстановления активизируются реакции
(1)–(5). Ключевой реакцией, отвечающей за массообмен между фазами, является реакция
(2). Для записи этой реакции в виде (6) преобразуем её с учетом ( O 2 - ) = ( O ) + ( V a2 - ) . Тогда
получим [1] { CO } + [1] ( O ) = [1] { CO2 } (в квадратных скобках указаны стехиометрические коэффициенты реакции), или
[ - 1] { CO } + [1] { CO 2 } = [1] ( о ) . (7)
Получена запись вида (6), в которой символом R 1 обозначен CO, R 2 – CO 2 . Продукт реакций (O) обозначен соответственно P 1 . Стехиометрические коэффициенты реакций n ij в случае (7) равны n 11 = - 1, n 12 = 1. И хотя в такой записи отсутствуют прямой учет восстановительных вакансий, их количество обратно пропорционально числу удаленных атомов кислорода из решетки оксида ( O ) . Процессы, описываемые реакциями (1), (3), (4), не связаны с массопереносом между фазами Ф и V и потому не включены в рассмотрение. Тем не менее, фаза Ф помимо аниона О2– содержит катионы Fe2+, Si4+, Mg2+, которые могут участвовать в диффузионных процессах, поэтому их также надо учитывать при составлении математической модели.
Ф д c n . 2 О2 -
дr
,
д c Ф 2+
Fe2+ д t
д c Ф 4+
Si4+ д t
= D Ф
Fe
= D Ф
Si
1 д
-2+ r 2 д r
r 2
V
Г
'4+ r 2 д r
r
V
V
Ф
' F
д r V
Ф д c и I
. 2 Si4 +
д r
V
,
,
где ci – массовая концентрация i -го
компо-
нента; Di o – коэффициент диффузии i -го компонента.
-
2. В фазе Ψ, окружающей частицу, также протекают процессы теплопроводности и диффузии реагентов. Однако вследствие изменения размеров частицы соответствующие уравнения будут несколько сложнее:
-
1) уравнение теплопроводности:
д T XV 1 д Г 2 д Т )
-
= r 2 +
-
д t pV c V r 2 д r V д r J
+
Г пФ ^
TV- 1
V PF J
R 2 dR д Т r 2 dt д r ’
где ρF – плотность на границе частицы; R – радиус частицы.
2) уравнения диффузии компонентов фазы V :
V д c CO
+
д t
(„Ф
V pF
= D v ± А
CO r 2 д r
V r2 ecC»
V д r J
+
—
^
V
R 2 dR д c C i O r 2 dt д r
3. Поверхность раздела фаз:
1) уравнение теплопередачи, связывающее тепловые потоки из фаз Ф и V к поверхности раздела фаз с тепловым эффектом химической реакции (7):
' J [ t, R (t)-0]-x"^- [ t, R (t)- 0]- n
+£ IO AHO = 0, i=1
где I O – мольная скорость удаления кислорода с единицы площади поверхности раздела фаз; A H о - мольная энтальпия реакции (7);
-
2) уравнение массопереноса компонентов фазы Ф , связывающее удаление атомарного кислорода О с поверхности раздела фаз (в соответствие с химическими реакциями (7)) с подводом его к поверхности раздела из глубины рудной частицы:
Р Ф DО’-^с Ф ’ - [ * • R ( t ) - 0 ] +
+[ с0,-( t, R (t))-1] Vo’—1о = 0,(15)
Р Ф D Fe ’ - AF 1 1 ’ R ( t ) — 0 ] +
+ c 0e2+( t, R (t)) Vo’-1 о = 0,(16)
Р Ф D AAS4 t - R ( t ) - 0 ]+
+ с^Д t, R (t)) VO2-1 о = 0,(17)
где νi – молярная масса продукта i , умноженная на его стехиометрический коэффициент, в химической реакции образования продукта i ;
-
3) уравнение массопереноса компонентов фазы " , связывающие подвод реагентов к поверхности раздела фаз с расходом их в соответствие с химической реакцией (7):
р" D'Co |сTo [t,R(t) + 0] + о r L J
V co ) I о = 0, (18)
n
+ ! ( с 'о ( t , R ( t ) ) V o ’
I - —
k = 1
-
4) уравнение химического равновесия химической реакции (7):
-O — a Ф K ( T ) = 0, a CO
-
4. Уравнение изменения размера частицы:
dR dt
= р Ф Vo2 - I о.
5. Граничные условия:
ST
1) ( t ,0) = 0;
d r
(21)
дс Ф
2) -c^- ( t ,0) = 0, i = 1,..., n - 1; d r
(22)
3) - ( t , » ) = - 0 ;
(23)
4) c" ( t , w ) = c 0 " , i = 1,..., m - 1.
(24)
где ai – химическая активность компонента i ; K – константа равновесия химической реак- ции.
Обсуждение результатов
Полученная модель позволяет проводить расчет процесса образования и движения анионных вакансий в объёме комплексного оксида, рассматривая процесс восстановления как взаимодействие восстановителя не с молекулой оксида металла, а с анионом кислорода кристаллической решетки. При этом кислород переходит из решетки оксида (фазы Ф) в газовую фазу Ψ, оставляя после себя восстановительную вакансию, а продукт реакции CO2 удаляется из зоны реакции. Развитие этого процесса приводит к образованию потока восстановительных вакансий, который направлен от поверхности рудной частицы в её объем. В противоположном направлении происходит движение анионов кислорода. В предложенной модели химическая реакция на поверхности раздела фаз описывается уравнением (7). А движение восстановительных вакансий рассматривается как процесс уменьшение концентрации анионов кислорода O2– в объеме фазы Ф. Таким образом, зная изменение концентрации кислорода в любой точке рудной частицы в произвольный момент времени, можно судить о количестве восстановительных вакансий в данной части объема и во всей частице в целом. Процесс восстановления завершится, когда количество анионов кислорода фазы Ф уменьшится на значение, пропорциональное содержанию восстанавливаемого металла, в данном случае Fe.
Необходимо отметить, что данная модель не рассматривает аннигиляцию восстановительных вакансий с образованием металлической фазы, тем не менее из результатов экспериментов [13–15] можно сделать вывод о том, что выделение металлической фазы идет с минимальными энергетическими затратами и в тех частях объема рудных частиц, где происходит скопление восстановительных вакансий.
Заключение
Разработана математическая модель процесса образования и движения анионных вакансий в объёме комплексного оксида, позволяющая учитывать влияние основных физикохимических параметров на скорость появления и перемещения восстановительных вакансий, и, как следствие, на скорость процесса восстановления.
Список литературы Математическая модель образования и движения анионных вакансий при восстановлении металлов в комплексных оксидах
- Effect of Alumina on the Gaseous Reduction of Magnetite in CO/CO2 Gas Mixtures/Y.E. Kapelyushin, X. Xing, J. Zhang et al.//Metallurgical and Materials Transactions B. -2015. -Vol. 46, no. 3. -P. 1175-1185. DOI: 10.1007/s11663-015-0316-z
- In-Situ Study of Gaseous Reduction of Magnetite Doped with Alumina Using High-Temperature XRD Analysis/Y.E. Kapelyushin, Y. Sasaki, J. Zhang et al.//Metallurgical and Materials Transactions B. -2015. -Vol. 46, no. 6. -P. 2564-2572. DOI: 10.1007/s11663-015-0437-4
- Effects of Temperature and Gas Composition on Reduction and Swelling of Magnetite Concentrates/Y.E. Kapelyushin, Y. Sasaki, J. Zhang et al.//Metallurgical and Materials Transactions B. -2016. -Vol. 47, no. 4. -P. 2263-2278. DOI: 10.1007/s11663-016-0719-5
- Рощин, В.Е. Твердофазное предвосстановление железа -основа безотходных технологий переработки комплексных руд и техногенных отходов/В.Е. Рощин, С.П. Салихов, А.Д. Поволоцкий//Вестник ЮУрГУ. Серия «Металлургия». -2016. -Т. 16, № 4. -С. 78-86. DOI: 10.14529/met160408
- Role of a silicate phase in the reduction of iron and chromium and their oxidation with carbide formation during the manufacture of carbon ferrochrome/V.E. Roshchin, A.V. Roshchin, K.T. Akhmetov, S.P. Salikhov//Russian Metallurgy (Metally). -2016. -Vol. 2016, no. 11. -P. 1092-1099. DOI: 10.1134/S0036029516090123
- Formation of a Network Structure in the Gaseous Reduction of Magnetite Doped with Alumina/Y.E. Kapelyushin, Y. Sasaki, J. Zhang et al.//Metallurgical and Materials Transactions B. -2017. -Vol. 48, no. 2. -P. 889-899.
- DOI: 10.1007/s11663-016-0897-1
- Salikhov, S.P. Theoretical Aspects of Pyrometallurgical Processing of Sideroplesite Ore/S.P. Salikhov, A.V. Roshchin, V.E. Roshchin//Chernye Metally. -2018. -No. 8. -P. 13-18.
- Рощин, В.Е. Физика процессов окисления и восстановления металлов в твердой фазе/В.Е. Рощин, А.В. Рощин//Металлы. -2015. -№ 3. -С. 19-25.
- Дрозин, А.Д. Рост микрочастиц продуктов химических реакций в жидком растворе/А.Д. Дрозин. -Челябинск: Изд-во ЮУрГУ, 2007. -57 с.
- Model for nanocrystal growth in an amorphous alloy/P.A. Gamov, A.D. Drozin, M.V. Dudorov, V.E. Roshchin//Russian Metallurgy (Metally). -2012. -Vol. 2012, no. 11. -P. 1002-1005.
- DOI: 10.1134/S0036029512110055
- Yaparova, N.M. Method for internal heat source identification in a rod based on indirect temperature measurements/N.M. Yaparova, A.D. Drozin//Ural Conference on Measurements (UralCon), 2017 2nd International. -IEEE, 2017. -P. 93-98.
- DOI: 10.1109/URALCON.2017.8120693
- Drozin, A.D. Calculating of the True Sizes and the Numbers of Spherical Inclusions in Metal/A.D. Drozin//Metallography, Microstructure, and Analysis. -2017. -Vol. 6, no. 3. -P. 240-246.
- DOI: 10.1007/s13632-017-0354-9
- Рощин, В.Е. Физическая интерпретация теории восстановления/окисления металлов/В.Е. Рощин, А.В. Рощин//Вестник ЮУрГУ. Серия «Металлургия». -2016. -Т. 16, № 4. -С. 29-39.
- DOI: 10.14529/met160404
- Рощин, А.В. Трансформация ионной химической связи в металлическую при восстановлении металлов/А.В. Рощин, В.Е. Рощин, С.П. Салихов//ХХ Менделеевский съезд по общей и прикладной химии. -2016. -С. 109-109.
- Bilgenov, A.S. Statistical Analysis of Metal Particles Forming during Reduction of Oxides with Low Iron Content/A.S. Bilgenov, Y. Kapelyushin, P.A. Gamov//Solid State Phenomena. -2018. -Vol. 284. -P. 673-678.
- DOI: 10.4028/www.scientific.net/SSP.284.673


