Математическая модель процесса нейтрального выщелачивания и сгущения в производстве цинка
Автор: Дюнова Диана Николаевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 1 т.13, 2013 года.
Бесплатный доступ
Рассматривается математическая модель процесса нейтрального выщелачивания и сгущения, основу которой составляют уравнения материального баланса. Разработана топологическая модель исследуемого объекта. Полученная модель, позволяющая определять расходы выходных материальных потоков процесса и их состав, реализована в вычислительной среде Simulink.
Математическая модель, процесс выщелачивания, материальный баланс
Короткий адрес: https://sciup.org/147156805
IDR: 147156805 | УДК: 66.01.001.57
Mathematical model of neutral leaching and condensation process in zinc production
The paper considers a mathematical model of neutral leaching and condensation process based on material balance equations. The topological model of the studied object is developed. The model obtained permits to define expenditures of output material flows of the process and their composition. It is implemented in Simulink software environment.
Текст научной статьи Математическая модель процесса нейтрального выщелачивания и сгущения в производстве цинка
Выщелачивание продуктов обжига – основной технологический передел производства цинка гидрометаллургическим способом, который в значительной мере определяет технико-экономические показатели производства в целом, в первую очередь извлечение металла, расход электроэнергии, себестоимость цинка [1].
Цель процесса выщелачивания – более полное извлечение цинка и других полезных компонентов сырья в раствор при минимальном его загрязнении примесями.
Исходным сырьем является огарок, получаемый в результате окислительного обжига цинкового сульфидного материала. Выщелачивание представляет собой процесс растворения цинкового огарка в жидком растворителе. На практике процесс осуществляют отработанным электролитом, получаемым в процессе электролиза раствора сульфата цинка. При выщелачивании в раствор переходят цинк, кадмий, медь, железо и другие компоненты. Нерастворимые в слабых растворах серной кислоты соединения остаются в твердом остатке от выщелачивания – кеке.
При непрерывном способе производства цинка выщелачивание включает две ступени. Задача первой стадии выщелачивания – получение раствора, пригодного для очистки растворов от примесей железа, алюминия, мышьяка, сурьмы, крем-некислоты методом гидролиза, что можно провести лишь в нейтральной среде (рН = 5,2–5,4).
Цинк содержится в огарке в виде соединений: ZnO, ZnSO4, ZnS, ZnO·Fe2O3, 2ZnO·SiO2. Оксид цинка растворяется в растворе серной кислоты. Сульфат цинка хорошо растворяется в воде, поэтому цинк, содержащийся в сульфатной форме, полностью переходит в раствор на нейтральной стадии выщелачивания. Феррит и сульфид цинка в разбавленных растворах серной кислоты практически нерастворимы и переходят в твердый остаток. Наиболее легко растворяется оксид меди с образованием сульфата меди. Ферриты и сульфиды меди переходят в кек. Кадмий присутствует в обожженном концентрате в виде СdО, CdSO4, CdS, СdO·Fe2O3. Хорошо растворяется оксид кадмия с образованием сульфата. Ферриты и сульфиды кадмия переходят в твердый остаток. Свинец при сернокислотном выщелачивании практически весь переходит в кек в виде труднорастворимого сульфата PbSO4. Присутствующий в огарке оксид железа FeO легко взаимодействует со слабой серной кислотой; трехвалентное соединение Fe2O3 практически не растворимо. При выщелачивании обожженного концентрата получается нейтральная пульпа (смесь сульфатного раствора и нерастворимого остатка) с содержанием твердого 20–70 г/л. Для проведения последующих технологических операций ее подвергают разделению на твердую и жидкую фазы путем сгущения и отстаивания. Здесь протекают довольно сложные физикохимические процессы, которые внешне проявляются в осаждении твердых частиц в жидкой среде. После отстаивания получается верхний слив с содержанием твердого 1– 4 г/л и сгущенная пульпа с определенным отношением масс жидкой и твердой фаз (ж :т) = (2–3) : 1.
Рассматривая процессы нейтрального выщелачивания и сгущения как единый объект, выделим основные группы его параметров. Входными параметрами являются расход потока огарка, верхнего слива кислых сгустителей (ВСКС) и поток отработанного электролита (ОЭ). Продукты передела – верхний слив нейтральных сгустителей (ВСНС), нижний слив нейтральных сгустителей (НСНС), содержащий твердую фазу НСНС т и жидкую фазу НСНСж.
С целью исследования процесса нейтрального выщелачивания цинковых огарков и изучения его характеристик интерес представляет получение математической модели, позволяющей определять количество получаемых продуктов рассматриваемого производственного передела на основе информации о количестве поступающих на переработку материальных потоков и их химических составах.
Математическую модель выщелачивания и сгущения представим в виде совокупности балансовых соотношений по твердой и жидкой фазам, а также по компонентам, переходящим в раствор и образующим «цинковый» кек.
Баланс по твердой фазе определяется соотношением:
F НСНСт = F 1 ( C ZnO (1 - a 1 ) + C 2ZnOSiO2(1 -a 1 ) +
+ C ZnS + C ZnO . Fe 2 O 3 + C CuS + C CuS . Fe2O3 + C PbO +
+ C PbSO4 + C CdS + C CdO . Fe2O3 + C SiO2 +
+ C ^3 + C Пр ), (1)
где FНСНС – расход твердой фазы нижнего слива нейтральных сгустителей, кг/ч; F1 – расход огарка, кг/ч; C1ZnO – содержание в огарке оксида цинка, %; C2ZnO.siO2 — содержание силиката цинка в огарке, %; C1ZnS – содержание в огарке сульфида цинка, %; CZnO.Fe2O3 — содержание в огарке феррита цинка, %; CC1 uS – содержание в огарке сульфида меди, %; СcuO.Fe2O3 — содержание феррита меди в огарке, %; C1PbO – содержание оксида свинца в огарке, %; CP1bSO – содержание сульфата свинца в огарке, %; C1Fe O – содержание в огарке оксида железа (III), %; Cп1р – содержание прочих компонентов в огарке, %; α1 – доля оксида цинка, пере- шедшего в раствор.
Баланс по жидкой фазе:
Q ВСНС р ВСНС = Q ВСКС р ВСКС + F 1 + Q O3 р O3 -
FНСНСт бнСНСж рНСНСж,
6нСНС„ рНСНС„ = FНСНСT а2, жжт где QВСНС — расход ВСНС, м3/ч; рВСНС - плотность ВСНС, кг/м3; QВСКС – расход ВСКС, м3/ч; рВСКС — плотность ВСКС, кг/м3; F1 - расход цинкового огарка, кг/ч; QО3 - расход ОЭ, м3/ч; рО3 -плотность ОЭ, кг/м3; Q – расход жидкой ж фазы НСНС, м3/ч; рнснс - плотность жидкой ж фазы НСНС, кг/м3; а2 - величина ж: т в НСНС.
Балансовое соотношения по цинку в растворах:
ВСНС ВСКС
( Q ВСНС + Q НСНС™ ) С Zn = Q ВСКС С Zn +
ж
+ Q O3 С Zn3 + [а 1 F 1 ( C ZnO z1 + C 2ZnO . SiO2 z 2 ) +
+ F 1 C ZnSO4 z 3 ] , (4)
где С Z В n СНС – концентрация цинка в ВСНС, г/л;
ВСКС ОЭ
С Zn – концентрация цинка в ВСКС, г/л; С Zn – концентрация цинка в ОЭ, г/л; z 1 , z 2 , z 3 – стехиометрические коэффициенты пересчета; C 1 ZnSO – концентрация сульфата цинка в огарке, %.
Балансовое соотношение по меди в растворе:
ВСНС ВСКС
( Q ВСНС + Q НСНС„ ) С Си = Q ВСКС С Cu +
ж
+ F 1 ( C CuO z 4 + C CuSO4 z 5 ) ] , (5)
где С C В u СНС – концентрация меди в ВСНС, г/л; С C В u СКС – концентрация меди в ВСКС, г/л; z 4 , z 5 – стехиометрические коэффициенты пересчета; C 1 CuSO – концентрация сульфата меди в огарке, %;
C 1 CuO – концентрация оксида меди в огарке, %.
Балансовое соотношение по кадмию в растворе:
( QВ СНС + Q НСНС Ж ) ССВСНС
ВСКС
= Q ВСКС С Cd
+
+ F 1 C CdO z 6 + C CdSO4 z 7 , (6) где С C В d СНС – концентрация кадмия в ВСНС, г/л; С C В d СКС – концентрация кадмия в ВСКС, г/л;
z 6 , z 7 – стехиометрические коэффициенты пересчета; C C 1 dSO – концентрация сульфата кадмия в огарке, %; C 1 CdO – содержание оксида кадмия в огарке, %.
Баланс по компонентам, образующим твердую фазу НСНС:
|
F НСНСт |
НСНСт С ZnO = |
(1 — « 1 ) F 1 C ZnO , |
(7) |
|
F НСНСт |
НСНСт С 2ZnO . SiO 2 |
= (1 - а 1 ) F1 C 2ZnO . SiO 2 , |
(8) |
|
F НСНСт |
НСНСт С ZnS = |
F 1 C Z 1 nS , |
(9) |
|
F НСНСт |
С НСНСт ZnO . Fe 2 O 3 |
= F 1 C ZnO . Fe2O3 , |
(10) |
|
F НСНСт |
НСНСт С CuS = |
F 1 C C1uS , |
(11) |
|
F НСНСт |
НСНСт С CuO . Fe 2 O 3 |
= F1 C CuO . Fe2O3 , |
(12) |
|
F НСНСт |
НСНСт С PbSO 4 = |
F 1 ( C PbSO4 + C PbO z 8 ) , |
(13) |
|
F НСНСт |
НСНСт С CdS = |
F 1 C C1dS , |
(14) |
|
F НСНСт |
НСНСт С CdO . Fe 2 O 3 |
= F1 C CdOTe2O3 , |
(15) |
|
F НСНСт |
НСНСт С SiO 2 = |
F 1 C S 1 iO2 , |
(16) |
|
F НСНСт |
НСНСт С Fe 2 O 3 = |
F 1 C F1e2O3 , |
(17) |
|
F НСНСт |
НСНСт С пр = |
F 1 C п1р , |
(18) |
НСНС где СZnO т – содержание оксида цинка в твердой фазе НСНС, %; СНСНСт – содержание силиката 2ZnO.SiO2
цинка в твердой фазе НСНС, %; С Z Н n С S НСт – содержание сульфида цинка в твердой фазе НСНС, %;
НСНС
СZпO.FeT2Oз - содержание феррита цинка в твердой фазе НСНС, %; СPНbСSНOСт – содержание сульфата свинца в твердой фазе НСНС, %; СCНdСSНСт – содержание сульфида кадмия в твердой фазе НСНС, %; СCНdСOНFСeт O – содержание феррита кадмия в твер- дой фазе НСНС, %; СSНiOСНСт – содержание кремнезема в твердой фазе НСНС, %; СFНeСOНСт – содержание оксида железа (III) в твердой фазе НСНС, %; НСНС
С пр т – содержание прочих компонентов в твер-
С CuO z 4 + С CuSO4 z 5 ,
Q BCHC + Q HCHC ж
b 15 =
ВСКС С Cd
Q BCHC + Q HCHC„
ж
дой фазе НСНС, %; z 8 – стехиометрический коэффициент пересчета.
Система соотношений (1) – (18) представляет математическую модель нейтрального выщелачивания и сгущения нейтральных пульп. Особенности модели позволяют перейти к ее топологическому аналогу. На рис. 1 представлен сигнальный граф объекта, отражающий причинно-следственные связи между переменными (сигналами). Вершины сигнального графа соответствуют переменным модели, а ветви – коэффициентам или передаточным функциям, характеризующим связь между переменными.
Коэффициентам передач графа соответствуют соотношения:
b1 = C ZnO a 1 + C 2ZnOSiO 2 a 1 + C ZnS + С ZnO - Fe2O3 +
С CdO z 6 + С CdSO4 z 7 b 16 =-------------4— ;
Q BCHC + Q HCHC. ж
+ C CuS + C CuS - Fe2O3 + C PbO + C PbSO4 + C CdS +
+ C CdO - Fe2O3 + C SiO2 + C Fe2O3 + C 1р ;
b 2 a 2 ; b 3 = Р ВСКС ; b 4 = ——
Piiciic, Р вснс Р вснс
ж
b 5 = _Р оЭ_ ; b 6 =--—; b 7 = - Р нСНС ж ;
Р вснс Р вснс Р вснс
ВСКС ОЭ b 8 =----С”-------; b 9 =-----CZn------
QВСНС + QНСНС QВСНС + QHCHC„ жж
b 10 =
a 1 C ZnO z1
b 12 =
Q BCHC + Q HCHC„ ж
C 1ZnSO4 z 3
a 1 C 2ZnOSiO2 z 2 b 11 =---------------- 2-----;
Q BCHC + Q HCHC.,. ж
b 13 =
ВСКС С Cu
b 17 = (1- a 1 ) С ZnO . b 18 = (1 a 1 ) С 2ZnOSiO 2 .
F НСНСт F НСНСт
-
b 19 = ( ZnS ; b 20 = ZnO ' Fe2O 3 ;
F НСНСт F НСНСт
11 b 21 = -C Cu^ ; b 22 = h CuOIeA ;
F НСНСт F НСНСт
С PbO + С PbSO4 z 8
-
b 23 =-----------4— ;
F НСНСт
F НСНСт F НСНСт
11 1
-
b 26 = SiO 2 ; b 27 = Fe 2 O3 ; b 28 =--- пр— .
F НСНСт F НСНСт F НСНСт
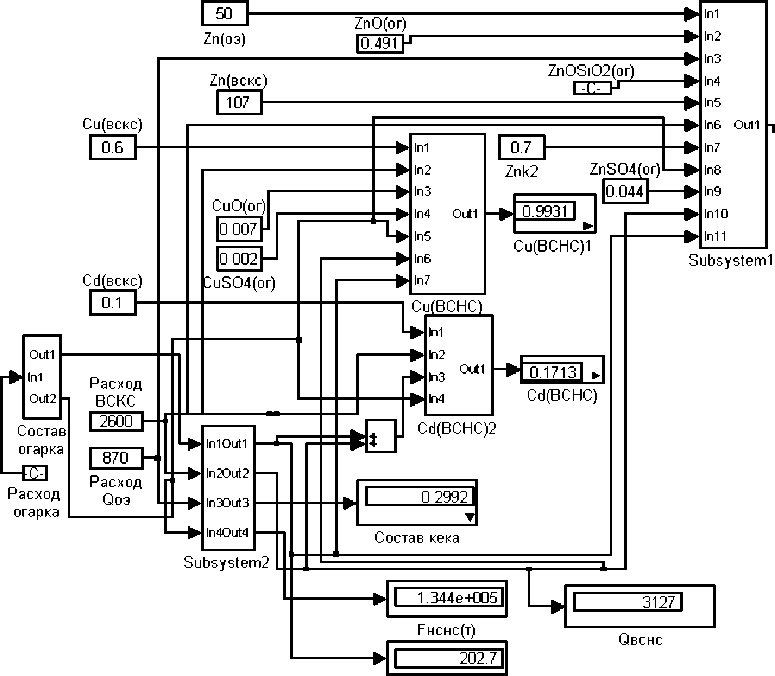
Решение сигнального графа может быть найдено с помощью операций эквивалентного последовательного преобразования [2]. Топологическая модель объекта была реализована в приложении Simulink вычислительной среды MATLAB (рис. 2).
При проведении вычислительного эксперимента полагалось, что в выщелачивательный цех подается обожженный цинковый концентрат в количестве 3,79 т/ч следующего состава, %: ZnO – 49,079; ZnSO 4 – 13,29; 2ZnO·SiO 2 – 4,42; ZnS – 0,76; ZnO·Fe 2 O 3 – 19,56; CuO – 0,69; CuSO 4 – 0,20; CuS – 0,119; CuO·Fe 2 O 3 – 0,30; CdO – 0,125; CdSO 4 – 0,034; CdS – 0,035; CdO·Fe 2 O 3 – 0,07;
Q BCHC + Q HCHC,,
ж
Q BCHC + Q HCHC ж
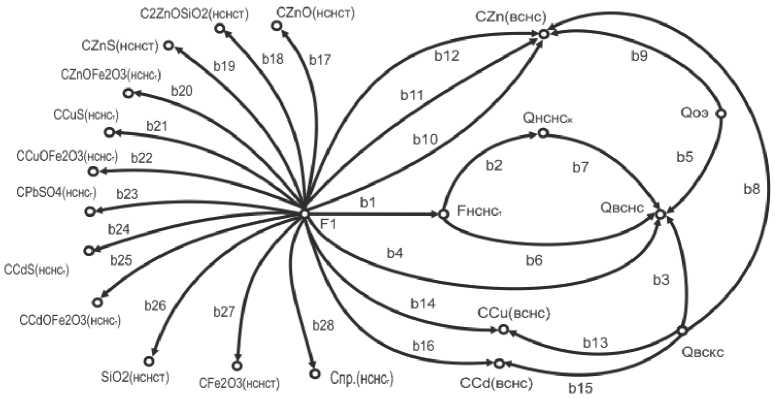
Рис. 1. Сигнальный граф процесса нейтрального выщелачивания и сгущения
Онснс(ж)
Рис. 2. Simulink-модель процесса нейтрального выщелачивания и сгущения

Zn(BCHC)
PbSO 4 – 1,14; PbO – 0,85; FeO – 0,87; Fe 2 O 3 – 0,568; SiO 2 – 1,97; прочие – 5,99.
Для взаимодействия с огарком поступает ВСКС в количестве 118 м3/ч, содержащий: Zn – 107 г/л; Cu – 0,6 г/л; Cd – 0,1 г/л; H 2 SO 4 – 1,5 г/л и отработанный электролит в количестве 36 м3/ч, содержащий: Zn – 50 г/л; H 2 SO 4 – 0,1 г/л. Значения α 1 , α 2 и плотности соответствующих веществ являются исходными данными для расчета, полученными по данным практики работы цинкового производства.
В результате расчета получено: расход ВСНС – 141,6 м3/ч; расход НСНСж – 2,74 м3/ч; расход
НСНСт – 1822 кг/ч. ВСНС содержит: Zn – 108 г/л; Cu – 0,7 г/л; Cd –0,1 г/л. Состав НСНС т , %: ZnO – 29,92; 2ZnO·SiO 2 – 2,82; ZnS – 1,4; ZnO·Fe 2 O 3 – 39,61; CuS – 0,603; CuO·Fe 2 O 3 – 0,203; CdS – 1,016; CdO·Fe 2 O 3 – 2,031; PbSO 4 – 1,62; Fe 2 O 3 – 1,625; SiO 2 – 1,016, прочие – 14,22.
Полученная математическая модель позволяет получить статические характеристики объекта моделирования в виде зависимостей Q ВСНС( Q ВСКС), C Zn(ВСНС) ( Q ВСКС ), Q ВСНС ( Q ОЭ ), C Zn(ВСНС) ( Q ОЭ ) (рис. 3–6).
Таким образом, разработанное математическое описание процесса нейтрального выщелачи-
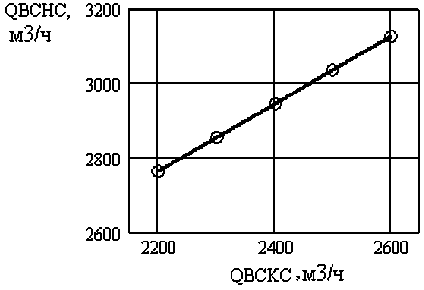
Рис. 3. Статическая характеристика Q ВСНС ( Q ВСКС )
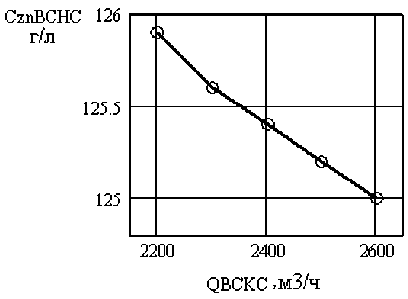
Рис. 4. Статическая характеристика C Zn(ВСНС) ( Q ВСКС )
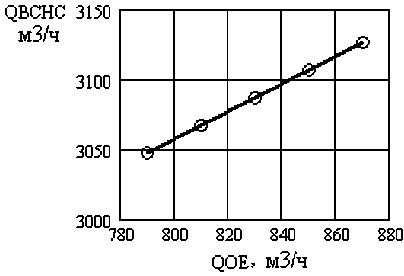
Рис. 5. Статическая характеристика Q ВСНС ( Q ВСКС )
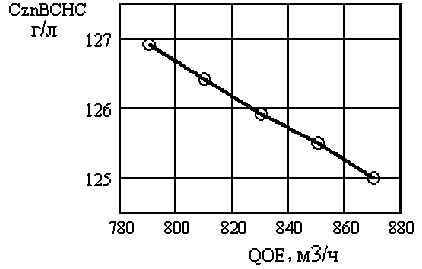
Рис. 6. Статическая характеристика C Zn(ВСНС) ( Q ВСКС )
вания и сгущения позволяет прогнозировать количественные значения массовых расходов выходных материальных потоков ВСНС, НСНСт, НСНСж, а также их компонентов на основе измерительной информации о массовых расходах входных потоков. Математическая модель может быть использована при проектировании новых и анализе функционирования действующих гидрометаллургических систем, а также для решения вопросов по установлению расходных норм по сырью, технологическим показателям и определе- нию неучтенных потерь компонентов сырья в условиях промышленной эксплуатации.
Список литературы Математическая модель процесса нейтрального выщелачивания и сгущения в производстве цинка
- Снурников, А.П. Гидрометаллургия цинка: учеб. пособие/А. П. Снурников. -М.: Металлургия, 1981 -382 с.
- Кафаров, В.В. Принципы математического моделирования химико-технологических систем: учеб. пособие/В.В. Кафаров, В.Л. Перов, В.П. Мешалкин. -М.: Химия, 1974 -343 с.


