Механизм ионной проводимости твердого электролита LiPON
Автор: Рудый А.С., Новожилова А.В.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Физико-математические науки
Статья в выпуске: 5-5 (92), 2024 года.
Бесплатный доступ
На основании результатов анализа структурной модели твердого электролита LiPON, предложенной в работах Дж. Бейтса и др., показано, что полученное значение проводимости не может быть дрейфовой проводимостью. Выполнен расчет тока смещения через дебаевский диэлектрик, определены диэлектрические потери и рассчитана соответствующая им проводимость. Близость полученных результатов к результатам Дж. Бейтса и др. позволяет отнести полученные ранее значения проводимости к току смещения. Таким образом, данные импеданс-спектроскопии в области средних частот не могут использоваться для оценки дрейфовой проводимости твердого электролита LiPON.
Твердый электролит, импеданс-спектроскопия, элемент постоянной фазы, дрейфовая проводимость, ток смещения
Короткий адрес: https://sciup.org/170205292
IDR: 170205292 | DOI: 10.24412/2500-1000-2024-5-5-137-141
Ionic conductivity mechanism of solid electrolyte LiPON
Based on the results of the analysis of the structural model proposed by J. Bates et al. for the impedance of the solid electrolyte LiPON, it is shown that the conductivity value cannot be attributed to the drift current. In the present work the displacement current through the Debye dielectric is calculated, the dielectric losses determined, and the corresponding conductivity is obtained. The proximity of the results obtained to the results of J. Bates et al. allows us to attribute the previously obtained conductivity values to the displacement current. Thus, mid-frequency impedance spectroscopy data cannot be used to estimate the drift conductivity of the LiPON solid electrolyte.
Текст научной статьи Механизм ионной проводимости твердого электролита LiPON
Твердотельные тонкопленочные литий-ионные аккумуляторы относятся к сравнительно новыми перспективным химическим источникам энергии. В подавляющем большинстве таких аккумуляторов в качестве твердого электролита используется фосфор-оксинитрид лития (LiPON). Важнейшие характеристики LiPON были изучены еще в середине 90-х его разработчиками Дж. Бейтсом и др. [1-7]. Эти работы стали классическими и более поздние исследования опираются на их результаты. В частности, в работе [5] было получено значение проводимости σ = 2.3 ⋅ 10-4 S ⋅ m-1, которое стало практически критерием достоверности результатов других авторов. В то же время параметры структурной модели LiPON, приведенные в [5], позволяют усомнится в правильной интерпретации именно этого параметра.
На рисунке 1 приведена структурная модель LiPON, которая использовалась в работе [5] для аппроксимации диаграмм Боде.
Рис. 1. Эквивалентная схема тестовой структуры Pt|LiPON|Pt, где R el и R r – активное сопротивление электролита и реактивного слоя соответственно, Z el и Z r – элементы постоян-
ной фазы. Z i – импеданс интерфейса Pt|LiPON|Pt, C g – «геометрическая емкость» тестовой структуры [5]
Здесь R el и R r – активное сопротивление электролита и реакционного слоя. Элементы Z el , Z r и Z i , моделируют импеданс электролита, реакционного слоя и интерфейсов
Pt|LiPON|Pt соответственно. Символом Z в работе [5] используется для обозначения элементов постоянной фазы (CPE)
Z = A(j ω ) -α ,
где A – постоянная, ω – циклическая частота, а α – фактор неидеальности. Элементы R r и Z r , описывающее реакционный слой, имеют смысл только при напряжении смещения более 5 V, поэтому далее не рассматриваются. Чтобы оценить степень адекватности структурной модели реальной системе необходимо определить физический смысл основных структурных элементов и оценить их параметры.
Элемент Z i при α = 0.96 ÷ 0.98 имеет смысл неидеальной емкости с небольшим протеканием. Для значений Ai = 1.3 ⋅ 106 и α о 1 емкость элемента Z i составляет достаточно большую величину Ci = 0.77 µ F . Такая емкость характерна для плотного двойного электрического слоя (ДЭС). При площади контакта S = 4 ⋅ 10 - 6 m 2 толщина слоя в рамках модели Гельмгольца составляет 0.46 ⋅ 10 - 10 m . Обычно ДЭС с протеканием описывается схемой Рэндлса, изображающей емкость с параллельным ей сопротивлением утечки. Это сопротивление моделирует редокс процессы, которые определяют величину тока утечки. В [5] схема Рэндлса заменяется введением неидеальной емкости Z i для которой α< 1 . Но в этом случае утечка имеет диффузионную природу, в то время как протекание ДЭС не может происходить иначе, как через редокс процесс. Другими словами, это не тот механизм утечки, который моделирует схема Рэндлса.
Элементы Z el и R el моделируют диффузионный и дрейфовый перенос ионов лития. В работе [5] при нулевом смещении эти параметры имеют значения
R el = 3.7 ⋅ 103 Ω , A = 3.1 ⋅ 10 7 Ω⋅ s -α и α= 0.66 . Последний параметр указывает на то, что элемент Z достаточно близок к диффузионному элементу Варбурга. Импеданс Варбурга Z = AW (1 - j) / ω , где A W = A/ 2 – коэффициент (амплитуда) Варбурга, получается из элемента постоянной фазы Z = A(j ω ) -α при α= 1 / 2 . То обстоятельство, что α> 1 / 2 означает, что элемент Zel не является чисто диффузионным, а имеет некоторую емкость.
На частоте ω 103 , которой соответствует локальный минимум мнимой части импеданса Pt|LiPON|Pt [5], величина Re Zel = Aelω-α cos(απ / 2) составляет 1.6 ⋅ 105 Ом , что на два порядка больше R . Из чего можно заключить, что в LiPON преобладает дрейфовый механизм переноса заряда. Однако это противоречит сразу двум фактам. Во-первых, при полученной выше толщине ДЭС поле внутри электролита ослаблено на четыре порядка и перенос заряда не может быть преимущественно дрейфовым. Во-вторых, полученное Дж. Бейтсом и др. значение проводимости σ = 2.3 ⋅ 10-4 S ⋅ m-1 дает очень высокое значение концентрации подвижных ионов лития. В рамках теории Друде концентрацию ионов можно рассчитать, как c=σkBT/Dq2, где D – коэффициент диффузии ионов лития. Для значения D 10-15 м2 ⋅ с-1 [8] и проводимости σ = 2.3 ⋅ 10-4 S ⋅ m-1 концентрация ионов составляет c =2,5 ⋅1028 m-3 , т.е. сопоставима с концентрацией атомов в металлическом литии c =4, 6 ⋅1028 m-3 . Если же учесть ослабление поля внутри LiPON на четыре порядка, то проводимость, а соответственно и концентрация должны быть еще выше. Очевидно, что реальная концентрация ионов лития должна быть несколько ниже полученной величины.
Кроме указанных противоречий, значение σ = 2.3 ⋅ 10 - 4 S ⋅ m - 1 не соответствует данным таблицы II, приведенной в работе [5]. Для сэндвич-структуры Pt|LiPON|Pt с площадью контакта S = 0.04 cm 2 , пленки LiPON толщиной 1 мкм и сопротивлением R = 3.7 ⋅ 103 Ω элементарный расчет дает удельное сопротивление ρ = 1, 48 ⋅ 104 Ω ⋅ m . Соответствующая проводимость составляет σ = 6,8 ⋅ 10 - 5 S ⋅ m - 1, что меньше приведенного в работе значения. Этому значению проводимости соответствует уже меньшая концентрация ионов лития c = 7,3 ⋅ 1027m - 3 .
Результаты работы [8], в которой использовалась схема Рэндлса (рис. 2), дают значения проводимости 8.7 ⋅ 10 - 5 S ⋅ m - 1, которое близко к 6,8 ⋅ 10 - 5 S ⋅ m - 1 [5]. Близость полученных значений □ создает впечатление, что этот результат соответствует истинному значению омического сопротивления. Однако это не так. Дело в том, что поле внутри электролита согласно [5] ослаблено на четыре порядка, что эквивалентно увеличению сопротивления на ту же величину. Единственное разумное объяснение сравнительно небольшой величины R el состоит в том, что это сопротивление току смещения. При колебаниях потенциала на электродах имеет место только изменение концентрации Li+ в плотной части ДЭС (слой Штерна) и в его диффузной части. Перемещения ионов в этом случае невелики и ограничены плотными и диффузными слоями ДЭС. При этом сопротивление току смещения не является чисто реактивным, так как при перемещении заряда в пределах ДЭС происходит диссипация энергии. По всей видимости, омическое сопротивление R el характеризует скорость диссипации энергии, связанную именно с этими процессами.
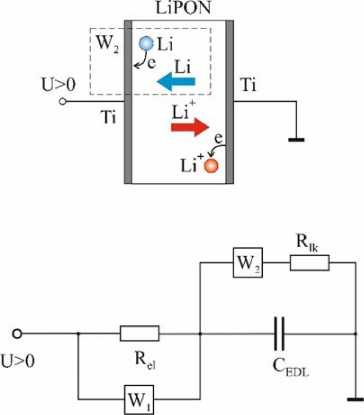
Рис. 2. Структурная модель LiPON. Стрелками показано направление движения зарядов при положительном потенциале на электроде [8]
Для оценки величины сопротивления току смещения достаточно найти отношение напряжения U0ej ω t к току смещения I = j ω S ε ε ( ω )E e j ω t
Zdp = δ / jωSε0ε(ω), (2)
где E0 = U0/ d , d – толщина LiPON, □ – циклическая частота. Для дебаевской зависимости диэлектрической проницаемости от частоты ε ( ω ) соотношение (2) принимает вид
ˆ d ωτ(1 - ρ) - j(1 + ω2τ2ρ)
dp Sε0ωε(0) 1+ (ωτρ)2 ,
где τ – постоянная времени релаксации поляризации, ρ = ε∞ / ε (0) . Вещественная часть (3) имеет вид
Re Zdp ≈ S ε 0 ε (0)1 +ω 2 τ 2 ρ 2 .
Нетрудно убедиться, что при параметрах S = 6.4 ⋅ 10 - 5 m2 , ω= 103s - 1 и τ 0.017s , ε (0) О 104 , ε ∞ п 1 , d = 10 - 6 m , характерных для Pt|LiPON|Pt, ReZ имеет порядок 103 Ω (табл. 1). Таким образом, Re Z ≈ R и предположение, что Rel – сопротивление тока смещения вполне логично. Далее полученные значения проводимости для тока смещения обозначаются как σ , а именно σ = 6,8 ⋅ 10 - 5 S ⋅ m - 1 (работа [5]), σ = 8.7 ⋅ 10 - 5 S ⋅ m - 1 (работа [8]) и σ = 1.3 ⋅ 10 - 5 S ⋅ m - 1 (настоящая работа).
Таблица 1. Сопоставление параметров структурных моделей LiPON. Все параметры из работы [5] пересчитаны для площади контакта 0,64 см2, как в работе [8]
|
R el , Ом |
A Wel , □ /s 1/2 |
С DEL, □ F |
Толщина ДЭС по Гельмгольцу, m |
□ , S/cm расчет по R el |
□ , S/cm по Друде |
c, m-3 |
|
|
Бейтс и др. [5] |
231,3 |
~1,9∙106 |
12 |
0.47∙10-10 |
6,8∙10-7 |
- |
7,3∙1027 |
|
Работы [8,9] |
180,0 |
1∙104 |
0,21 |
2.7∙10-9 |
8,7∙10-7 |
- |
1,7∙1027 |
|
Оценки наст. работы |
103 |
- |
- |
10-10 – 10-9 |
1,6∙10-7 |
- |
Приведенные значения σ dp полезно сравнить с дрейфовой проводимостью LiPON, которая с учетом соотношения Эйнштейна имеет вид σ dr = Dq2c / kT . Для коэффициента диффузии D = 1.5 ⋅ 10 - 15 m2 ⋅ s - 1 [8] и концентрации c = 1.7 ⋅ 1027 m - 3 , полученной в [9], дрейфовая проводимость составляет σ dr = 1.6 ⋅ 10 - 5 S ⋅ m - 1 (табл. 1). Эта величина оказывается достаточно близкой к значению проводимости
σ = 6,8 ⋅ 10 - 5 S ⋅ m - 1 [5]. Причина, по которой эти параметры близки, состоит в том, что механизмы диссипации импульса ионов в обоих случаях одинаковы. Соответственно значения времени релаксации поляризации импульса также близки.
Результаты анализа работы [5] и ее сопоставления с данными работы [8] позволяют сделать вывод, что экспериментальное значение проводимости обусловлено током смещения. Причина состоит в ослаблении поля, а следовательно, и дрейфового тока внутри электролита. Полученное в [5] значение проводимости ха- рактеризует в основном диэлектрические потери, но никак не способность электролита LiPON переносить электрический заряд, т.е. выполнять основную функцию в составе ТТЛИА. Основными механизмами переноса заряда через электролит является дрейф и диффузия ионов лития.
Список литературы Механизм ионной проводимости твердого электролита LiPON
- Bates J.B., Dudney N.J., Gruzalski G.R., Zuhr R.A., Choudhury A., Luck C.F., Robertson J.D., SolidStateIonics 53-56, 647 (1992).
- Bates J., Dudney N., Gruzalski G., Zuhr R., Choudhury A., Luck C., Robertson J., J. Power Sources 43, 103(1993).
- Bates J.B., Gruzalski G.R., Dudney N.J., Luck C.F., Xiaohua Yu, Solid State Ionics,70-71, 619(1994).
- Bates J.B., Dudney N.J., Lubben D.C., Gruzalski G.R., Kwak B.S., Xiaohua Yu, Zuhr R.A., ibid. 54, 58(1995).
- Yu X., Bates J.B., Jellison-Jr. G.E., Hart F.X., J. Electrochem. Soc. 144, 524-532(1997). DOI: 10.1149/1.1837443
- Xiaohua Yu, Bates J.B., Jellison G.E. Proceedings of the Symposium on Thin Film Solid Ionic Devices and Materials, 95 (22), 23 (1995).
- Bates J.B., Dudney N.J., Luck C.F., Sales B.C., Zuhr R.A., J. Am. Ceram. SOC. 76, 929 (1993).
- Rudy A., Mironenko A., Naumov V., Novozhilova A., Skundin A., Fedorov I., Batteries 7(2), 21 (2021). DOI: 10.3390/batteries7020021 EDN: YBKEHG
- Рудый А.С., Лебедев М.В., Новожилова А.В. Физика твердого тела, 65 (9), 1527 (2023). DOI: 10.21883/FTT.2023.09.56248.47 EDN: TFZFNW


