Меланизация полиаминофенолов в процессе биотрансформации парацетамола клетками Rhodococcus ruber ИЭГМ 77
Автор: Коротаев М.Ю., Вихарева Е.В., Ившина И.Б.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2016 года.
Бесплатный доступ
Методами C ЯМР -спектроскопии и хромато-масс-спектрометрии установлено, что в составе нерастворимых в воде продуктов, образующихся в процессе биотрансформации парацетамола клетками Rhodococcus ruber ИЭГМ 77, присутствуют производные индола и бензофурана. Предложен механизм образования сопряженных индольных и бензофурановых циклических систем в результате последовательной ферментативной окислительной поликонденсации аминофенольных соединений. Образующиеся полиаминофенолы преобразуются в меланиноподобные соединения. По нашим данным, молекулы по-лиаминофенолов, а также индольные и бензофурановые фрагменты в химической структуре меланино-подобных соединений содержат симметричные ("Sym") и асимметрические ("Asym") участки, включающие ароматические и хиноидные кольца с эквивалентными заместителями в пара- и мета-положении соответственно. Впервые обоснованная возможность ферментативной меланизации поли-аминофенолов клетками R. ruber ИЭГМ 77 рассматривается с позиции гипотезы гумификации.
Парацетамол, биотрансформация, актинобактерии рода rhodococcus, хромато-масс-спектрометрия, 13c ямр-спектроскопия
Короткий адрес: https://sciup.org/147204765
IDR: 147204765 | УДК: 579.695
Polyaminophenol melanization in the process of paracetamol biotransformation by Rhodococcus ruber ИЭГМ 77
Precipitate formed in the process of paracetamol biotransformation by Rhodococcus ruber IEGM 77 was found to include indole and benzofuran ring fragments using 13C NMR spectroscopy and chromatography-mass-spectrometry methods. Mechanisms of the formation of conjugated indole and benzofuran cyclic systems resulting from the fermentative condensation of polyaminophenols contained in the precipitate chemical structure have been proposed. According to our data, polyaminophenol molecules and indole and benzofuran fragments in chemical structure of melanin-like compounds contain symmetric ("Sym") and asymmetric ("Asym") sites comprising aromatic and quinoid rings with equivalent substituents in para- and ortho- positions, respectively. Originally substantiated possibility of enzyme melanization of polyaminophenols by R. ruber IEGM 77 cells is viewed from the perspective of humification hypothesis.
Текст научной статьи Меланизация полиаминофенолов в процессе биотрансформации парацетамола клетками Rhodococcus ruber ИЭГМ 77
Биологическая деструкция лежит в основе биотехнологических способов утилизации органических, в том числе фармацевтических, отходов [Wu, Zhang, Chen, 2012]. В качестве биодеструкторов широко ис пользуются почвенные микроорганизмы, выделяемые из природных сред [De Gusseme et al., 2011; Zhang et al., 2013]. Наряду с этим биодеструкция органических соединений является естественным процессом, протекающим в природе при трансформации растительных остатков в гуминовые вещества. Последние представляют собой смесь высокомолекулярных азотсодер-
жащих соединений ароматической и алифатической природы.
Согласно данным, представленным в работе F.J. Stevenson [1994], одним из механизмов образования гуминовых веществ является ферментативная окислительная поликонденсация хиноидных соединений с аминокислотами. Наличие азо-метиновых связей в химической структуре гумусовых кислот подтверждает данный механизм [Орлов, 1990]. Однако процессы гумусообразования не исчерпываются одними только химическими взаимодействиями карбонильных и аминогрупп реагирующих соединений, иначе в качестве продуктов реакции идентифицировались бы только производные полиаминофенолов и полифеноксазинов, последние из которых присутствуют в молекулах гуминовых кислот [Орлов, 1990; Thorn, Mikita, 1992]. Отличительной особенностью гумификации является образование как азот-углеродных, так и углерод-углеродных полимеробразую-щих связей [Орлов, 1990]. Следовательно, биохимическое взаимодействие хинонов с соединениями, содержащими аминогруппу, гипотетически может привести к синтезу индольного кольца, представленного в молекулах гуминовых кислот и родственных им меланинов [Орлов, 1990; Thorn, Mikita, 1992; Bosetto et al. 1997; Subianto, 2006]. Последние являются продуктами полимеризации индол-5,6-хинона и 5,6-дигидроксииндол-2-карбо-новой кислоты, образующихся при окислении тирозина и триптофана.
В ранее проведенных нами исследованиях показано, что биодеструкция парацетамола клетками Rhodococcus ruber ИЭГМ 77 сопровождается образованием черного аморфного осадка полимерной природы [Коротаев и др., 2015]. В соответствии с данными элементного анализа, спектрофотометрии, ИК- и 'Н ЯМР-спектроскопии продукты, содержащиеся в полученном осадке, представляют собой полиаминофенолы, структурные единицы которых включают остатки 2,5-диаминобензол-1,4-диола, 4,6-диаминобензо л-1,3-диола, 2,5-дигидрокси- 1,4-бензохинондиимина, 2-амино-5 -гидрокси-1,4-бензохинонимина [Коротаев и др., 2016]. Однако данные методы не позволили получить информацию о характере углерод-углеродных связей в образующихся нерастворимых продуктах (НП) биотрансформации парацетамола. Для установления в структуре НП полимеробразующих углерод-углеродных химических связей и более детального выяснения механизмов биотрансформации парацетамола родококками с позиций общей теории гумификации целесообразно исследование данного осадка методами 13С ЯМР спектроскопии и хромато-масс-спектрометрии. Целью настоящей работы является оценка возможности биосинтеза меланин-родственных соединений (меланизации образующихся полиаминофенолов) при биотрансформации парацетамола клетками R. ruber ИЭГМ 77.
Материалы и методы исследований
Для биодеструкции парацетамола (Аныцо Лу-ань Фармасьютикал Ко., Лтд., Китай) использовали штамм R. ruber ИЭГМ 77 из Региональной профилированной коллекции алканотрофных микроорганизмов (официальный акроним коллекции ИЭГМ, номер во Всемирной федерации коллекций культур WDCM 768, . Выделение осадка из постферментационной среды осуществляли в соответствии с условиями, описанными в работе [Ivshina et al., 2006].
Спектроскопия ЯМР 13С
Спектры 13С ЯМР НП записывали в ДМСО-б6 на спектрометре ЯМР Broker DRX-500 (Broker BioSpin GmbH, Германия) с рабочей частотой 125.8 МГц. Химические сдвиги представляли относительно Me4Si.
Хромато-масс-спектрометрия
Для анализа использовали пробы, представляющие собой (1:12,78)=1/(1+12.78) = 7.3% (масс.) растворы НП в этилацетате. Хроматограммы и масс-спектры НП снимали на газовом хроматографе Agilent 7890А с масс-спектрометрическим детектором Agilent 5975С на капиллярной неполярной колонке HP-5ms (Agilent Technologies, США). Условия анализа: ионизация методом электронного удара (70 eV); объём вводимой пробы - 1 мкл; скорость потока газа-носителя (гелий) - 1 мл/мин.; без деления потока; температура испарителя - 280°С; температура колонки программируемая (в течение первых 5 мин 70°С, затем повышение до 310°С со скоростью 18°С в 1 мин. и выдерживание на данном уровне 10 мин.); диапазон анализируемых масс - 40-400 m/z; задержка работы детектора на выход растворителя -3.5 мин.
Результаты исследования и их обсуждение
Полученные спектры 13С ЯМР НП подтверждают наличие в НП полиаминофенольных и феноксазиновых фрагментов и свидетельствуют о присутствии индольных и бензофураноидных циклических систем (рис. 1, 2): 92.98 (Сь СЦ; 93.92 (Сп, С2); 94.53 (Сш, С3); 115.61 (Сп,2), 115.64 (Сг.гж.з); 124.63, 125.02, 125.41 (C-N); 150.75, 154.63, 154.86, 155.39 (С-О); 148.37, 161.47 (C=N); 177.34 (С=О).
Результаты хромато-масс-спектрометрического исследования растворов НП в этилацетате пред- ставлены на рис. 3 и 4.
На хроматограмме (рис. 3) отмечается выраженный пик со временем удерживания 22.60 мин с масс-спектром (рис. 4). включающим следующие характеристические ионы, т г (%): 41.00 (23.03); 55. 00 (9.56); 57.20 (100.00); 91.00 (10.31); 117.00 (5.10); 131.20 (5.93); 147.20 (10.69); 191.20 (12.37); 316.40 (33.94). Идентифицировать по библиотеке масс-спектров данное соединение не удалось. Тем не менее, гипотетические структурные фрагменты, установленные методом 13С ЯМР-спектроскопии (см. рис. 2), объясняют механизм фрагментации компонента НП со временем удерживания 22.60 мин. (рис. 5).
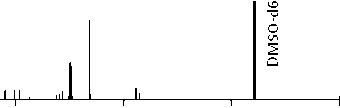
150 100 50 0
Химический сдвиг, м.д.
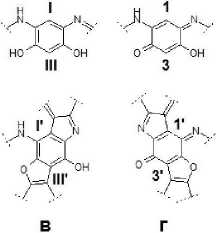
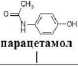
Как видно из рис. 5, характеристические ионы в масс-спектре компонента НП со временем удерживания 22.60 мин. являются продуктами фрагментации конденсированной системы, состоящей из индольных колец. В соответствии с данными, представленными в работах [Коротаев и др., 2016; Ivshina et al., 2006], биотрансформация парацетамола родококками осуществляется по пути I и II, при реализации которых образуются асимметричные (‘Msym”) и симметричные (“Sym”) участки молекул полиаминофенолов 1г и Пг соответственно (рис. 6).
Abundance
200000 0
57,2
41,0 э1 с д
191,2
„^1.0 147,2
5Ъл 1Э12
117,0
m/z—> 30,00 130,00 230,00 330,00 430,00
Рис. 4. Масс-спектр компонента НП со временем удерживания 22.60 мин.
Рис. 1. Спектр 13С ЯМР НП (ДМСО-а6, 125.8 МГц):
39.64,39.80, 92.98, 93.92, 94.53, 115.35, 115.40, 115.61, 115.64, 122.78, 124.12, 124.63, 124.87, 125.02, 125.41, 125.76, 128.64, 129.81, 131.12, 143.80, 148.37, 150.75, 154.63, 154.86, 155.39, 161.47, 177.34, 178.89
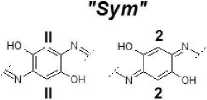
"Asym"
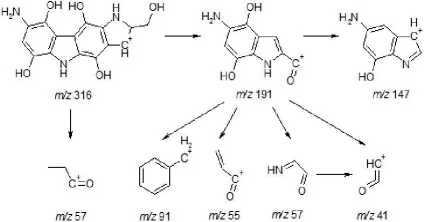
Рис. 5. Фрагментация и характеристические ионы компонента НП со временем удерживания 22.60 мин.
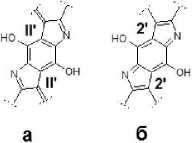
Рис. 2. Структурные фрагменты молекул НП, представленные остатками:
а - 2,5-диаминобензол-1,4-диола; б - 2,5-дигидрокси-1,4-безохинондиимина; в - 4,6-диаминобензол-1,3-диола; г - 2-амино-5-гидрокси-1,4-бензохинонимина

Abundance
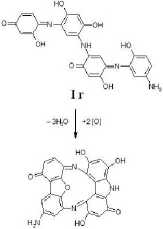
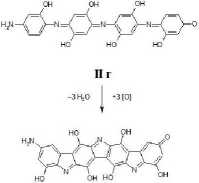
Рис. 6. Предполагаемая схема меланизации полиаминофенолов (путь I и II)
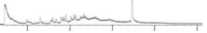
3,50 7.00 10,5014,0017,5021.00 24,502.6,00
Рис. 3. Хроматограмма раствора НП в
этилацетате
Вероятно, в процессе дальнейшей биотрансформации родококками уАкупГ и “Sym" участки молекул полиаминофенолов подвергаются меланизации с образованием полииндолобензофурановых
и полииндольных циклических конденсированных систем соответственно.
Впервые обоснованную нами возможность ферментативной меланизации полиаминофенолов клетками R. ruber ИЭГМ 77, по-видимому, можно рассматривать с позиции образования гуминопо-добных веществ (гумификации).
Заключение
Молекулы продуктов, получаемых при биологической трансформации парацетамола клетками Rhodococcus ruber ИЭГМ 77, включают аминофе-нольные и феноксазиновые, а также индольные и бензофурановые фрагменты. Таким образом, данные продукты имеют гуминоподобную природу и образуются в результате ферментативной меланизации полиаминофенолов.
Работа выполнена при частичной поддержке Комплексной программы Уральского отделения РАН (проект 15-12-4-10) и гранта Российского научного фонда (14-14-00643).
Список литературы Меланизация полиаминофенолов в процессе биотрансформации парацетамола клетками Rhodococcus ruber ИЭГМ 77
- Коротаев М.Ю. и др. Химическая структура осадка, образующегося в процессе биотрансформации парацетамола клетками Rhodococcus ruber ИЭГМ 77//Биофармацевтический журнал. 2016. Т. 8, № 1. С. 13-19
- Коротаев М.Ю. и др. Определение средней молекулярной массы нерастворимых продуктов биодеструкции парацетамола клетками Rhodococcus ruber ИЭГМ 77//Фундаментальные исследования. 2015. № 2, Ч. 26. С. 58505854
- Орлов Д. С. Гумусовые кислоты почв и общая теория гумификации. М.: Изд-во МГУ, 1990. 325 с
- Bosetto M. et al. Study of the humic-like compounds formed from L-tyrosine on homoionic clays//Clays Minerals. 1997. Vol. 32. P. 341-349
- De Gusseme B. et al. Degradation of acetaminophen by Delftia tsuruhatensis and Pseudomonas aeruginosa in a membrane bioreactor//Water Research. 2011. Vol. 45. P. 1829-1837
- Ivshina I.B. et al. Catalysis of the biodegradation of unusable medicines by alkanotrophic rhodococci//Applied Biochemistry and Microbiology. 2006. Vol. 42, № 4. P. 392-395
- Stevenson F.J. Humus Chemistry: Genesis, Composition, Reactions. New York: John Wiley & Sons, 1994. 512 p
- Subianto S. Electrochemical Synthesis of Melanin-Like Polyindolequinone. Thesis of dissertation. -Brisbane St Lucia: The University of Queensland, 2006. 197 p
- Thorn K.A., Mikita M.A. Ammonia fixation by humic substances: a nitrogen-15 and carbon-13 NMR study//The Science of the Total Environment. 1992. Vol. 113. P. 67-87
- Wu S., Zhang L., Chen J. Paracetamol in the environment and its degradation by microorganisms Applied Microbiology Biotechnology. 2012. Vol. 96. P. 875-884
- Zhang L. et al. Degradation of paracetamol by pure bacterial cultures and their microbial consortium//Applied Microbiology and Biotechnology. 2013. Vol. 97, № 8. P. 3687-3698


