Менеджмент пациента с множественными травматическими внутричерепными гематомами в нейрохирургической клинике: обзор литературы и клинический случай
Автор: Яриков А.В., Ермолаев А.Ю., Фраерман А.П., Смирнов П.В., Логутов А.О., Цыбусов С.Н.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 10 т.9, 2023 года.
Бесплатный доступ
Множественные травматические внутричерепные гематомы являются одним из видов тяжелой ЧМТ, которые выделяются высокой летальностью и приводят к инвалидизации. В статье подробно описан патогенез ЧМТ, особенности клинической картины, изложены основные принципы лечения и приведены клинические примеры комплексного лечения множественных внутричерепных гематом. Своевременное лечение вторичных механизмов повреждения при ЧМТ приведет к значительному снижению летальности и тяжелых инвалидизирующих последствий. Медикаментозная терапия представлена рядом групп лекарственных средств: блокаторы кальциевых каналов, антиоксиданты и антигипоксанты, антагонисты NMDA-рецепторов, блокаторы воспалительного и иммунного ответа, стабилизаторы мембран клеток, улучшающие синаптическую передачу, блокаторы апоптоза, препараты с нейронспецифическим нейротрофическим действием, иммуносупрессоры, ингибиторы ренин-ангиотензин-альдостероновой системы.
Тяжелая чмт, патогенез чмт, множественные внутричерепные гематомы, реабилитация чмт, нейропротективная терапия
Короткий адрес: https://sciup.org/14128639
IDR: 14128639 | УДК: 616.8-089 | DOI: 10.33619/2414-2948/95/12
Management of a patient with multiple traumatic intracranial hematomas in a neurosurgical clinic: literature review and clinical case
Multiple traumatic intracranial hematomas are one of the types of severe TBI, which are distinguished by high mortality and lead to disability. The article describes in detail the pathogenesis of TBI, the features of the clinical picture, outlines the basic principles of treatment and provides clinical examples of complex treatment of multiple intracranial hematomas. Timely treatment of secondary damage mechanisms in TBI will lead to a significant reduction in mortality and severe disabling consequences. Drug therapy is represented by a number of groups of drugs: calcium channel blockers, antioxidants and antihypoxants, NMDA receptor antagonists, inflammatory and immune response blockers, cell membrane stabilizers that improve synaptic transmission, apoptosis blockers, drugs with neuron-specific neurotrophic action, immunosuppressors, inhibitors of the renin-angiotensin-aldosterone system.
Текст обзорной статьи Менеджмент пациента с множественными травматическими внутричерепными гематомами в нейрохирургической клинике: обзор литературы и клинический случай
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 616.8-089
В РФ каждый год более 700 тыс. лиц получают черепно-мозговую травму (ЧМТ), которая является одной из главных причин смертности и инвалидизации среди людей молодого и среднего возраста [1, 2]. По этой причине вопросы лечения и реабилитация лиц с ЧМТ являются весьма актуальными [3, 4]. Количество людей с ЧМТ растет ежегодно и среди них доминируют лица трудоспособного возраста (20–50 лет) [5, 6].
Частота ЧМТ в РФ составляет около 400–450 случаев на 100 тыс. населения в год, из них 50 тыс погибают, а еще 50 тыс. становятся официальными инвалидами [7, 8].
В США ежегодно фиксируется около 1,4–1,6 млн ЧМТ, в Европе — более 750 тыс (235 случаев на 100 тыс населения) [9, 10]. В структуре летальности всех типов травм 30– 50% приходится на ЧМТ [4].
Общая летальность при ЧМТ, в том числе ЧМТ легкой и средней степени тяжести, насчитывает 5–10%. При тяжелых видах ЧМТ с присутствие внутричерепных гематом, очагов ушиба головного мозга (ГМ) летальность набирает 41–85% [4, 11]. Число инвалидов после ЧМТ в США достигает 3 млн человек, в РФ более 2 млн [5, 12]. В структуре ЧМТ лица с сотрясением ГМ составляют 50%, с компрессией ГМ, внутричерепными гематомами — около 12–20%, с ушибом ГМ — около 30% [13].
На множественные гематомы приходится 0,74% всей ЧМТ. Анализ причин ЧМТ в РФ свидетельствует, что в 40,0–78,0% случаев они являются следствием бытовых травм, в 9,7– 30,0% ситуаций возникают из-за дорожно-транспортных происшествий, в 4,0–15,0% случаев связаны с производством и 1,5–2,0% — со спортивным травматизмом [14]. Поэтому ЧМТ занимает лидирующее место по приносимому суммарному медико-социальному и экономическому ущербу от всех типов травм [15].
Наиболее сложной группой являются лица со снижением сознания до уровня комы (8 баллов и менее по шкале комы Глазго (ШКГ)), что свидетельствует о тяжелой ЧМТ [1, 16].
Mноговариантность подходов к тактике лечения множественных внутричерепных гематом таит в себе много противоречий и потенциальных ошибок.
Цель – изучить распространенность, особенности клинической картины и тактики лечения множественных травматических интракраниальных гематом.
Патогенез ЧМТ
Современные видения о патогенезе ЧМТ базируются на выделении первичных и вторичных факторов поражения ГМ [7, 12, 17]. Первичные повреждения появляются в момент травмы [18]. Проявление первичных определяется от точки приложения повреждающего агента, интенсивности и продолжительности воздействия [19, 20].
В участке первичного повреждения ГМ возникает некроз мозгового вещества, повреждение нейронов и глиальных клеток, организуются синаптические разрывы, тромбоз сосудов, нарушается целостность сосудистой стенки. К первичным относят интракраниальные гематомы, очаги ушибов ГМ, первичные ушибы ствола ГМ, нарушения ликвороциркуляции, диффузные аксональное повреждения ГМ [5, 12, 21].
Факторы, способствующие формированию вторичного повреждения ГМ, делятся на интракраниальные и экстракраниальные [7, 22].
К интракраниальным факторам относят внутричерепную гипертензию, ишемию и нарушения гемодинамики ГМ, окклюзионную гидроцефалию, отек ГМ и дислокационный синдром [23]. Экстракраниальные факторы вторичного повреждения ГМ представляются артериальная гипотензия, гипоксемия, гиповолемия, гипертермия, анемия, гипер- и гипокапния, расстройства водно-электролитного и энергетического обменов [12, 13, 24].
Одномоментно с процессами вторичных повреждений в ответ на ЧМТ в клетке запускаются процессы нейропротекции и нейрорегенерации, главную роль в которых играют эндогенные нейротрофические факторы — специфические внутриклеточные нейрорегуляторные белки. Главными нейропротекторными свойствами нейрорегуляторных белков являются: ограничение эксайтотоксичности, подавление процессов апоптоза, снижение скорости агрегации патологических белковых молекул, угнетение воспалительного ответа и предотвращение образования свободных радикалов [25].
Однако на фоне повреждения при массивных очагах ушибов, некроза и ишемии ГМ фиксируется недостаток нейрорегуляторных белков или их действие сильно ограничено, что ведет к расстройству трофических и регенераторных функций клетки и превалированию процессов вторичного повреждения над процессами нейрорепарации [12, 26].
Нейропротективная терапия.
Нейропротекция — это комплекс мероприятий, состоящий из использования фармакологических препаратов и определенных методов лечения, направленных на снижение или прекращение действия этиологических и патогенетических механизмов повреждения ГМ [27]. Следовательно, ведущими задачами нейропротекции у лиц с ЧМТ представляются предотвращение процессов вторичного повреждения, блокада биохимических каскадов, ведущих к гибели клетки, а также стимулирование и поддержка нейрорегенерации и нейрогенеза [28].
В настоящее время имеется несколько групп нейропротекторных препаратов, воздействующих на разные звенья биохимического каскада вторичного повреждения ГМ [2, 10, 12, 15, 27, 28]:
-
1) Блокаторы кальциевых каналов (нимодипин, бреинал, дилцерен, нимопин, нимотоп) уменьшают поступление в клетку ионов кальция, снижают эксайтотоксическое действие и предупреждают апоптоз.
-
2) Антиоксиданты и антигипоксанты (армадин, актовегин, солкосерил, нейрокс, мексидол, полиэтиленгликольсупероксиддесмутаза, цитофлавин, нейрокард, астрокс, мексифин, токоферол, метостабил, аскорбиновая кислота, асковит, ноотропил, пирацетам, нооцетам, мелатонин, кавинтон, винпоцетин, коэнзим Q10) являются антагонистами синтазы азота, предотвращают образование свободных радикалов, восстанавливают активность ферментов антиоксидантной защиты, ускоряют гликолиз, повышают устойчивость к гипоксии, улучшают кровоток ГМ.
-
3) Антагонисты NMDA-рецепторов (мемантин, меманталь, меморель, нооджерон, акатинол, мемикар, мирведол, меманейрин) способствуют торможению эксайтотоксического действия глутамата.
-
4) Блокаторы воспалительного и иммунного ответа (циклоферон, ингибиторы ЦОГ-2, антитела CD11 и CD18) блокируют активность фосфолипаз и увеличивают концентрацию противовоспалительных цитокинов.
-
5) Стабилизаторы мембран клеток (промежуточные продукты синтеза фoсфaтидилхoлина: рекогнан, цитиколин, цераксон, пронейро, квинель, нейропол, нейрохолин, нооцил, цересил канон, препараты магния: магния сульфат, аспангин, паматон, калия: аспаркам, панаспар, панангин)
-
6) Улучшающие синаптическую передачу (предшественники синтеза ацетилхолина — церетон, церепро, глеацер, холитилин, делецит, глиатилин).
-
7) Блокаторы апоптоза (ингибиторы каспазы-3, ингибиторы кальпаинов).
-
8) Препараты с нейронспецифическим нейротрофическим действием (кортексин, церебролизат, церебролизин).
-
9) Иммуносупрессоры (циклоспорин А) подавляют иммунный ответ.
-
10) Ингибиторы ренин-ангиотензин-альдостероновой системы (эналаприл, лизиноприл, трандолаприл) проявляет выраженный антигипоксический и противосудорожный эффект.
Множественные внутричерепные гематомы (МВЧГ).
ВМЧГ — сочетание двух и более гематом одного или различных видов: эпи-, субдуральных, внутримозговых [12, 29]. Частота МВЧГ составляет 15–20 % [29, 30].
По топографическому расположению различают [7, 12, 31]:
-
1. «Поэтажные», когда локализованы в области одного полушария, непосредственно одна над другой.
-
2. «По соседству», когда обе гематомы локализуются в одном и том же полушарии на расстоянии одна от другой.
-
3. Двусторонние, когда МВЧГ локализуются над разными полушариями.
В большинстве наблюдений для МВЧГ характерно отсутствие светлого промежутка. Чаще наблюдается сочетание двух гематом, реже трех. В 70–75% случаев МВЧГ локализуются в одной гемисфере, в 25–30% — в обеих гемисферах, а также могут локализоваться субтенториально [7, 32].
Среди травматических МВЧГ составляют у детей 9%, у людей молодого и среднего возраста — 23%, у пожилых и стариков — 45% [33]. Развитие МВЧГ в основном возникает при тяжелой ЧМТ с формированием множественных очагов ушиба ГМ, различных источников кровотечения [34].
Тактика хирургического лечения определяется локализацией, объемом повреждений, степенью их воздействия на ГМ [23, 35].
При хирургическом лечении больных с МВЧГ чаще производят костнопластическую трепанацию и санацию очагов повреждения. При «поэтажном» расположении МВЧГ очаги удаляют, как правило, из одного доступа. При расположении очагов повреждения в разных участках ГМ удаление проводят из разных доступов [2, 16, 35].
При множественных повреждениях у лиц со снижением уровня сознания менее 9 баллов по ШКГ, значение второго вентрикуло-краниального коэффициента (ВКК-2) менее 10% целесообразно выполнение обширной декомпрессивной краниотомии с целью профилактики развития послеоперационного отека ГМ и повышения внутричерепного давления [36].
Смертность при острых МВЧГ, вызывающих сдавление ГМ, достигает 70% [36].
Факторы риска неблагоприятного результата оперативного лечения ЧМТ разделяют на клинические и компьютерно-томографические (КТ) [37].
К клиническим относят снижение уровня сознания до 7 баллов и менее по ШКГ, присутствие анизокории или мидриаза с двух сторон, патологических познотонических реакций или диффузной мышечной гипо- или атонии, формирование острого отека и выбухания ГМ в момент операции, наличие тяжелых сочетанных экстракраниальных повреждений (40 баллов по шкале ISS и более), возраст пациента более 60 лет, а также признаки вторичного ишемического повреждения ГМ (артериальной гипотензии и гипоксемии).
К КТ-признакам неблагоприятного результата относят компрессию базальных цистерн (2 и более степень), кровоизлияние в ствол ГМ, присутствие острой субдуральной гематомы или множественных повреждений ГМ, объем очага повреждения ГМ более 100 см3, латеральная дислокация срединных структур более 10 мм, присутствие субарахноидального и/или внутрижелудочкового кровоизлияния, величина ВКК-2 8% и меньше [4, 9 , 12, 38].
Однако в настоящее время полностью не определена хирургическая тактика лечения двухсторонних МВЧГ [39].
Клинический пример
Далее приведем клинический пример комплексного лечения МВЧГ.
Пациент О., 1964 г. р., медицинская карта №3661, поступил в 17.04.2017 в
1 нейрохирургическое отделение ГБУЗ НО «Городская клиническая больница №39» (Нижегородский нейрохирургической центр имени А.П. Фраермана) г. Нижний Новгород с диагнозом: «Тяжелая сочетанная травма. Тяжелая открытая ЧМТ. Ушиб ГМ тяжелой степени. Острая внутримозговая гематома правой лобной доли. Острая субдуральная гематома правой лобно-височной области. Острая внутримозговая гематома левой лобной доли. Острые внутримозговые гематомы левых височной и теменной долей. Очаги геморрагических ушибов обеих височных долей. Травматическое субарахноидальное кровоизлияние. Линейный перелом левой височной кости с переходом на пирамиду височной кости и основание средней черепной ямки. Линейный перелом затылочной кости слева. Частичное травматическое расхождение ламбдовидного шва слева. Перелом пирамиды височной кости справа (клинически). Отогематорея справа (клинически). Гемосинус. Закрытый перелом VII– VIII ребер справа со смещением отломков».
В анамнезе: «Энцефалопатия смешанного генеза тяжелого течения».
Жалобы: не предъявляет по тяжести состояния.
Анамнез заболевания: пациент длительное время употреблял алкоголь, обстоятельства травмы выяснить невозможно. Со слов сопровождающих родственников больного - травма 14.04.2017 упал дома, ударился головой. За мед. помощью не обращался. С 15.04.2017
пациент перестал передвигаться по дому, а 17.04.2017 перестал вступать в контакт и открывать глаза.
Неврологический статус: Уровень сознания — кома-1 (7 по ШКГ). Глаза не открывает. Речевая продукция отсутствует. Локализует болевой раздражитель. Зрачки D=S, фотореакция ослабленная. Лицо симметричное. Слабые защитные движения во всех конечностях. Патологические стопные знаки с обеих сторон. Менингеальный синдром: ригидность затылочных мышц 5 см. Координаторные пробы не проводились из-за тяжести состояния.
Местно: отогематорея справа.
КТ головного мозга от 17.04.2017: Острая внутримозговая гематома правой лобной доли. Острая субдуральная гематома правой лобно-височной области. Острая внутримозговая гематома левой лобной доли. Острые внутримозговые гематомы левых височной и теменной долей. Очаги геморрагических ушибов обеих височных долей. Травматическое субарахноидальное кровоизлияние (Рисунок 1)
Травматолог: Закрытый перелом VII–VIII ребер справа со смещением отломков.
В экстренном порядке выполнены операции:
№1 «Резекционная трепанация черепа в правой лобно-височной области, удаление острой внутримозговой гематомы правой лобной доли объемом 80 мл и субдуральной гематомы правой лобно-височной области объемом 10 мл».
№2 «Резекционная трепанация черепа в левой височной теменной области, удаление внутримозговой гематомы левой теменной и височной долей объемом 30 мл».
КТ головного мозга на 1-е сутки после операции (Рисунок 2)
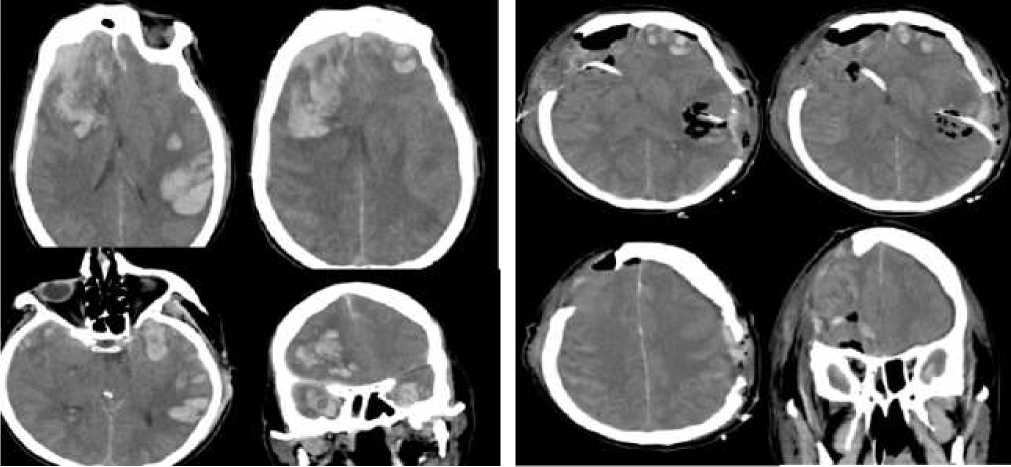
Рисунок 1. КТ ГМ при поступлении
Рисунок 2. КТ ГМ после операции
Пациент выписан на 44 сутки после операции. Шкала исходов Глазго — 2 балла.
В послеоперационном периоде данным пациентам проводилась респираторная поддержка, инфузионная терапия, коррекция гемодинамики и внутричерепной гипертензии [32].
Наряду с интенсивной терапией большое значение в лечении лиц с МВЧГ имела место нейропротекция (цитофлавин, магнезия сульфат, калия хлорид, аспаркам, аскорбиная кислота, эналаприл).
Проводились люмбальные пункции с лечебно-диагностической целью. После выписки из нейрохирургического стационара, было проведена реабилитация в условиях специализированных центров.
Заключение
Данные наблюдения показывают возможность выздоровления больных с МВЧГ острого течения при своевременном удалении всех очагов скопления крови, оказывающих объёмное воздействие и проведении своевременной наружной декомпрессии. Также не следует забывать о нейропротективной терапии в остром периоде ЧМТ и последующей реабилитации.
Список литературы Менеджмент пациента с множественными травматическими внутричерепными гематомами в нейрохирургической клинике: обзор литературы и клинический случай
- Потапов А. А., Крылов В. В., Гаврилов А. Г., Кравчук А. Д., Лихтерман Л. Б., Петриков С. С., Талыпов А. Э., Захарова Н. Е., Ошоров А. В., Солодов А. А. Рекомендации по диагностике и лечению тяжелой черепно-мозговой травмы. Ч. 1. Организация медицинской помощи и диагностика // Вопросы нейрохирургии им. Н.Н. Бурденко. 2015. Т. 79. №6. С. 100-106.
- Талыпов А. Э., Мятчин М. Ю., Куксова Н. С., Иоффе Ю. С., Кордонский А. Ю. Медикаментозная нейропротекция в остром периоде черепно-мозговой травмы средней степени тяжести // Медицинский совет. 2015. №10. С. 82-92.
- Талыпов А. Э., Мятчин М. Ю., Куксова Н. С., Кордонский А. Ю. Применение церебролизина у больных с ушибом головного мозга средней степени тяжести // Журнал неврологии и психиатрии им. C.C. Корсакова. 2014. Т. 114. №11. С. 98-106.
- Пурас Ю. В., Талыпов А. Э. Факторы риска развития неблагоприятного исхода в хирургическом лечении острой черепно-мозговой травмы // Нейрохирургия. 2013. №2. С. 8-16.
- Талыпов А. Э., Петриков С. С., Пурас Ю. В., Солодов А. А., Титова Ю. В. Лечение ушибов головного мозга // Медицинский совет. 2013. №4-1. С. 82-91.
- Крылов В. В., Петриков С. С., Талыпов А. Э., Пурас Ю. В., Солодов А. А., Левченко О. В., Григорьева Е. В., Кордонский А. Ю. Современные принципы хирургии тяжелой черепно-мозговой травмы // Журнал им. Н.В. Склифосовского Неотложная медицинская помощь. 2013. №4. С. 39-47.
- Крылов В. В., Талыпов А. Э., Пурас Ю. В. Хирургическое лечение тяжелой черепно-мозговой травмы // Нейрохирургия и неврология детского возраста. 2012. №2-3(32-33). С. 91-104.
- Пурас Ю. В., Талыпов А. Э., Кордонский А. Ю. Механизмы вторичного повреждения мозга и нейротрофическое действие церебролизина при черепно-мозговой травме // Нейрохирургия. 2012. №4. С. 94-102.
- Пурас Ю. В., Талыпов А. Э., Крылов В. В. Факторы риска развития неблагоприятного исхода в хирургическом лечении острой черепно-мозговой травмы // Журнал им. Н.В. Склифосовского Неотложная медицинская помощь. 2012. №2. С. 26-33.
- Пурас Ю. В., Талыпов А. Э., Крылов В. В. Декомпрессивная трепанация черепа в раннем периоде тяжелой черепно-мозговой травмы // Нейрохирургия. 2011. №3. С. 19-26.
- Талыпов А. Э., Петриков С. С., Пурас Ю. В., Солодов А. А., Титова Ю. В. Современные методы лечения ушибов головного мозга // Неврология, нейропсихиатрия, психосоматика. 2011. №1. С. 8-15.
- Фраерман А. П., Кравец Л. Я., Шелудяков А. Ю., Трофимов А. О., Балябин А. В. Сдавление головного мозга при изолированной и сочетанной черепно-мозговой травме. Поволжье. 2008. 328 с.
- Фраерман А. П. Травматическое сдавление головного мозга: современные аспекты проблемы, тактика лечения // Современные технологии в медицине. 2011. №4. С. 146-150.
- Тихомиров С. Е., Цыбусов С. Н., Кравец Л. Я., Фраерман А. П., Балмасов А. А. Пластика дефектов свода черепа и твердой мозговой оболочки новым полимерным материалом РЕПЕРЕН // Современные технологии в медицине. 2010. №2. С. 6-11.
- Пурас Ю. В., Кордонский А. Ю., Талыпов А. Э. Механизмы эволюции очагов ушиба головного мозга // Нейрохирургия. 2013. №4. С. 91-96.
- Крылов В. В., Иоффе Ю. С., Талыпов А. Э., Головко С. М. Некоторые показатели оказания нейрохирургической помощи больным с черепно-мозговой травмой в стационарах департамента здравоохранения г. Москвы. Ч. 1. // Нейрохирургия. 2008. №2. С. 54-59.
- Фраерман А. П., Сыркина Н. В., Железин О. В., Гомозов Г. И., Акулов М. С., Алейников А. В. Сочетанная черепно-мозговая травма. Поволжье, 2015. 204 с.
- Щербук А. Ю., Щербук Ю. А. Современная система организации нейротравматологической помощи в Санкт-Петербурге // Вестник хирургии им. И.И. Грекова. 2010. Т. 169. №1. С. 127-131.
- Dechant G., Neumann H. Neurotrophins // Molecular and Cellular Biology of Neuroprotection in the CNS. 2003. P. 303-334. https://doi.org/10.1007/978-1-4615-0123-7_11
- Щедренок В. В., Могучая О. В., Яковенко И. В., Калиничев А. Г., Орлов С. В., Хачатурова-Тавризян Е. В., Иванова Т. А., Соваков И. А. Особенности клиники сочетанной черепно-мозговой травмы // Вестник хирургии им. И.И. Грекова. 2008. Т. 167. №4. С. 40-42.
- Фраерман А. П., Кравец Л. Я., Шелудяков А. Ю., Балябин А. В. Ошибки в хирургии травматического сдавливания головного мозга и их предупреждение // Новости науки и техники. Серия: Медицина. Медицина катастроф. Служба медицины катастроф. 2007. №1. С. 236.
- Талыпов А. Э., Кордонский А. Ю., Крылов В. В. Международные многоцентровые исследования по лечению тяжелой черепно-мозговой травмы // Журнал неврологии и психиатрии им. C.C. Корсакова. 2016. Т. 116. №1. С. 113-121.
- Кравец Л. Я., Смирнов П. В., Кукарин А. Б. Выбор метода лечения при ушибах головного мозга // Нейрохирургия. 2017. №1. С. 8-14.
- Смирнов П. В., Кравец Л. Я., Якимов В. Н. Ранняя компьютерная томография при ушибах головного мозга // Нейрохирургия. 2017. №2. С. 21-28.
- Кравец Л. Я., Смирнов П. В., Лавренюк А. Н. Динамика очаговых травматических паренхиматозных повреждений головного мозга в остром периоде легкой черепно-мозговой травмы // Нейрохирургия. 2016. №2. С. 16-23.
- Яриков А. В., Ермолаев А. Ю., Леонов В. А., Калинкин А. А., Фраерман А. П., Астахов А. И., Руднев Ю. В. Комплексная нейровизуализация черепно-мозговой травмы: рентгенография и компьютерная томография // Наука и инновации в медицине. 2020. Т. 5. №3. С. 170-175. https://doi.org/10.35693/2500-1388-2020-5-3-170-175
- Яриков А. В., Смирнов П. В., Фраерман А. П., Леонов В. А., Хахин В. Б. Современные принципы лечения ушибов головного мозга // Врач. 2020. Т. 31. № 12. С. 20-25. https://doi.org/10.29296/25877305-2020-12-04
- Лавренюк А. Н., Кравец Л. Я., Смирнов П. В. Клинико-компьютерно-томографические параллели и расхождения при ушибах головного мозга // Российский нейрохирургический журнал им. профессора А.Л. Поленова. 2014. №6. С. 26.
- Яриков А. В., Фраерман А. П., Ермолаев А. Ю., Смирнов И. И., Руднев Ю. В., Тихомиров С. Е., Симонов А. Е., Яксаргин А. В., Макеев Д. А., Явкин М. Н. Черепно-мозговая травма: современное состояние проблемы, эпидемиология и аспекты хирургического лечения // Амурский медицинский журнал. 2020. №2 (30). С. 57-65. https://doi.org/10.24411/2311-5068-2020-11011
- Семенов А. В., Крылов В. В., Сороковиков В. А., Григорьева Е. В. Индекс травматических острых внутричерепных гематом и его значимость для объективизации показаний к их хирургическому лечению // Неотложная медицинская помощь. Журнал им. Н.В. Склифосовского. 2019. Т. 8. №4. С. 409-417.
- Суфианова Г. З., Витик А. А., Шапкин А. Г., Суфианов А. А., Реунов С. В., Масунов П. В. Клиническая и биохимическая оценка эффективности защитного действия аденозинтрифосфата в остром периоде черепно-мозговой травмы // Медицинская наука и образование Урала. 2015. Т. 16. № 4 (84). С. 134-139.
- Назаров И. П., Nazarov I. P. Интенсивная терапия тяжелой черепно-мозговой травмы (лекция 3) // Сибирское медицинское обозрение. 2008. №2 (50). С. 91-97.
- Суфианова Г. З., Суфианов А. А., Витик А. А., Немков А. Г., Кустов В. В. Новые перспективы нейропротекторной терапии ЧМТ // Медицинская наука и образование Урала. 2014. Т. 15. №2 (78). С. 155-158.
- Иванова Н. Е., Кондратьев С. А., Улитин А. Ю. Обзор по результатам исследования CAPTAIN II - эффективность и безопасность применения церебролизина для нейровосстановления после черепно-мозговой травмы средней и тяжелой степени // Российский нейрохирургический журнал имени профессора А.Л. Поленова. 2020. Т. 12. №2. С. 58-68.
- Каракулова Ю. В., Селянина Н. В., Ерошина О. А. Качество жизни больных в остром периоде черепно-мозговой травмы под влиянием нейротрофической терапии // Бюллетень сибирской медицины. 2011. Т. 10. №2. С. 122-126.
- Сафронова Е. С., Юнцев С. В., Белозерцев Ю. А. Нейропротекторный эффект ингибиторов ренин-ангиотензин-альдостероновой системы при диффузном аксональном повреждении мозга // Медицина и образование в Сибири. 2013. №3. С. 42.
- Сафронова Е. С., Юнцев С. В., Белозерцев Ю. А. НЕйропротекторное и мнемотропное действие ингибиторов АПФ при травматическом диффузном аксональном повреждении мозга // Вестник Бурятского государственного университета. 2013. №12. С. 160-166.
- Сафронова Е. С., Юнцев С. В., Белозерцев Ю. А. Эффективность нейропротекторного действия ряда препаратов при диффузном аксональном повреждении мозга // Забайкальский медицинский вестник. 2018. №4. С. 64-72.
- Гаибов С. С. Х., Воробьев Д. П., Захарчук Е. В. Некоторые аспекты черепно-мозговой травмы в условиях боевых действий // Академический журнал Западной Сибири. 2023. Т. 19. № 2 (99). С. 22-26. https://doi.org/10.32878/sibir.23-19-02(99)-22-26


