Место аналогов соматостатина в адъювантном лечении НЭО желудка CT1–2N0M0, GRADE I–II, 1-го клинико- морфологического типа: результаты одноцентрового ретроспективного исследования
Автор: Перегородиев И.Н., Мустафазаде Э.А., Малихова О.А., Богданова А.О., Федянин М.Ю., Иванов В.А., Делекторская В.В., Бохян В.Ю.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Оригинальные исследования
Статья в выпуске: 2 т.15, 2025 года.
Бесплатный доступ
Введение: Нейроэндокринные опухоли (НЭО) желудка 1 го клинико морфологического типа характеризуются относительно благоприятным течением и низкой частотой метастазирования. Основным методом лечения является эндоскопическая резекция слизистой (ЭРС), однако в ряде случаев применяется адъювантная терапия аналогами соматостатина (АС). Вопрос об эффективности такого подхода остаётся дискуссионным. Цель: Определить, как назначение АС у больных НЭО желудка 1 го типа (cT1–2N0M0, Grade I–II) влияет на частоту повторных ЭРС, выполняемых в связи с появлением метахронных опухолевых очагов. Материалы и методы: Проведено ретроспективное одноцентровое исследование, включавшее пациентов с НЭО желудка 1 го типа, перенёсших ЭРС в период с 2007 по 2024 годы. Для оценки влияния адъювантной терапии АС сформированы две группы: 1) получавшие АС после ЭРС; 2) динамическое наблюдение без противоопухолевого лечения. Для устранения групповых различий применён метод «псевдорандомизации» (propensity score matching) с использованием “cardinality matching”. Основным критерием эффективности служила частота повторных ЭРС. Статистический анализ выполнен с помощью t критерия Стьюдента. Результаты: В итоговый анализ вошли 104 пациента (52 в каждой группе), сбалансированные по полу, возрасту, Ki67, Grade, TNM стадии и другим факторам. Не выявлено статистически значимого снижения частоты повторных ЭРС в группе, получавшей АС, по сравнению с группой динамического наблюдения (р > 0,05). Также не отмечено достоверных различий в количестве выполняемых контрольных гастроскопий (р > 0,05). Выводы: Назначение аналогов соматостатина в адъювантном режиме у больных НЭО желудка 1 го типа статистически значимо не влияет на частоту повторных вмешательств. Таким образом, рутинное использование АС для профилактики метахронных очагов после ЭРС представляется нецелесообразным.
Нейроэндокринные опухоли желудка, аналоги соматостатина, опухоли желудка, нейроэндокринные неоплазии
Короткий адрес: https://sciup.org/140310765
IDR: 140310765 | DOI: 10.18027/2224-5057-2025-043
The role of somatostatin analogues in the adjuvant treatment of NETs of the stomach CT1–2N0M0, GRADE I–II, 1st clinical and morphological type: results of a single-center retrospective study
Background: Gastric type 1 neuroendocrine neoplasms (gNENs) are relatively indolent malignancies with low metastatic potential. Endoscopic resection (ER) is considered the primary treatment, while somatostatin analogs (SSAs) have proven anti-secretory and anti-proliferative effects. However, routine adjuvant SSA therapy after ER is not universally recommended. Objective: To determine whether adjuvant therapy with SSAs in patients with type 1 gNENs affects the rate of repeated endoscopic resections due to metachronous lesions. Methods: We conducted a retrospective, single-center study which included patients with gNENs cT1–2N0M0, Grade I–II who underwent ER from 2007 to 2024. Two groups were compared: one received SSAs in the adjuvant setting, the other remained under observation only. Propensity score matching using a “cardinality matching” approach ensured balanced cohorts. The primary endpoint was the frequency of repeated ER. Statistical analyses were performed using Student’s t-test. Results: After matching, there was no statistically significant reduction in repeated ER among patients receiving SSAs (p > 0.05). Furthermore, no significant difference in the number of endoscopic examinations was observed between the groups. Conclusion: Routine adjuvant SSA therapy after ER does not appear to reduce the frequency of repeated resections in patients with type 1 gastric NENs, suggesting that such practice may be unnecessary.
Текст научной статьи Место аналогов соматостатина в адъювантном лечении НЭО желудка CT1–2N0M0, GRADE I–II, 1-го клинико- морфологического типа: результаты одноцентрового ретроспективного исследования
-
[7,8,12]. Обосновывается это тем, что хотя терапия АС позволяет добиться высокой частоты ответа на лечение (25–100%), на фоне отмены приёма препаратов, как правило, отмечается рецидив заболевания [10]. Несмотря на отсутствие рекомендаций по адъювантному лечению АС пациентам после ЭРС, данный терапевтический подход остаётся популярным в среде специалистов онкологов.
МАТЕРИАЛЫ И МЕТОДЫ
Статистический анализ проводился при помощи набора программ R и RStudio. Псевдорандомизация пациентов проводилась с помощью пакета Matchit [4], был использован метод “cardinality matching”, позволяющий обеспечить наиболее точное сопоставление на уровне анализируемых групп, а не отдельных субъектов, в отличие от классических вариантов PSM [1]. Анализ влияния адъювантного лечения препаратами из группы АС на частоту ЭРС оценивалась с помощью t-критерия Стьюдента. Анализ выполнялся на популяции intention-to-treat (ITT).
РЕЗУЛЬТАТЫ
При проведении псевдорандомизации методом “cardinality” из 147 пациентов было исключено 43 пациента. В каждой группе оказалось по 52 пациента.
После проведения псведорандомизации оценены демографические характеристики групп пациентов. Анализ установления достоверности различий проводился методом однофакторного анализа с использованием критерия Пирсона для бинарных и дискретных переменных. Результаты анализа отражены в таблице 1. Медиана возраста в группе наблюдения составила 50 лет, в группе пациентов, получавших АС — 51 год (р = 0,326). Медиана индекса пролиферативной активности в обеих группах составила по 5% (р = 0,334), как и медиана максимального размера опухолевого узла — 6 мм (p = 0,566). Количество больных с высоко- и умереннодифференцированными опухолями составили 14 и 38 в группе пациентов, получавших АС, и 13 и 39-в группе контроля соответственно. В обеих группах подавляющее число пациентов были стадиро-ваны по системе TNM как cT1N0M0 (46 и 47 пациентов), и только у 6 и 5 пациентов стадия TNM была определена как cT2N0M0 (группа больных, получавших АС, и группа динамического контроля).
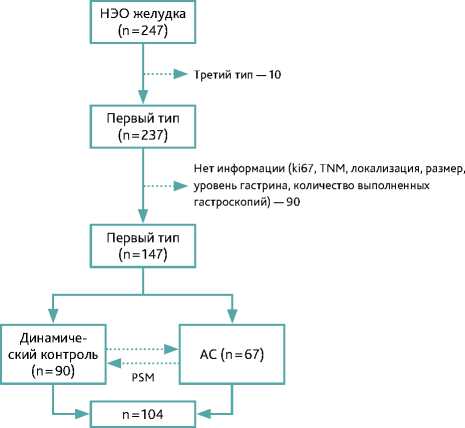
Рисунок 1. Отбор пациентов для проведения исследования
Figure 1. Selection of patients for the study
ОБСУЖДЕНИЕ
Анализ данных в нашем исследование был проведён с помощью метода «псевдорандомизации», что позволило нам обеспечить сбалансированность сравниваемых групп по ключевым факторам, влияющим на результат лечения, и, как следствие, повысить достоверность сделанных выводов.
Результаты проведённого исследования показали, что частота ЭРС одинакова и в группе пациентов, получавших АС, и в группе пациентов, находившихся на динамическом наблюдении. Для исключения влияния на результат фактора частоты выполнения контрольных гастроскопических исследований (поскольку в группе пациентов, получавших АС, чаще выполнялась гастроскопия), данный критерий был учтён при балансировке групп пациентов. Это являлось важным фактором, в виду того, что частота выполнения контрольных гастроскопий может напрямую влиять на частоту ЭРС, поскольку у пациентов, которым чаще выполняют гастроскопию, чаще обнаруживают метахронные очаги НЭО. В исходной группе (до проведения псевдорандомизации) среднее число гастроскопий в группе пациентов, получавших АС, было в два раза выше, чем в группе пациентов, находившихся на динамическом контроле (6 против 3).
Таблица 1. Демографические характеристики пациентов
Table 1. Demographic characteristics of patients


