Мета-анализ исследований эффективности добавления анти-PD1 антител к химиотерапии первой линии распространённого рака пищевода
Автор: Федянин М. Ю., Трякин А. А., Райс А. Б., Кононец П. В., Абу-хайдар О. Б., Гладилина И. А., Малихова О. А., Тюляндин С. А., Стилиди И. С.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Собственные исследования
Статья в выпуске: 2 т.13, 2023 года.
Бесплатный доступ
К 2022 году опубликованы результаты 6 рандомизированных исследований III фазы, которые посвящены изучению эффективности анти-PD1 антител при добавлении к химиотерапии первой линии при распространённом раке пищевода. При этом отсутствует четкий портрет пациента, у которого химио-иммунотерапия будет наиболее эффективна. В связи с этим проведение мета-анализа по изучению эффективности комбинированного подхода в отдельных подгруппах пациентов при совокупном анализе нескольких исследований поможет изменить клинические рекомендации.Материалы и методы: Нами проведен мета-анализ исследований комбинаций различных анти-PD1 антител и химиотерапевтических режимов в первой линии у больных распространённым раком пищевода с целью идентификации отдельных клинических групп с максимальным выигрышем от применения комбинации.Результаты: В мета-анализ были включены данные 6 рандомизированных исследований, в которых приняли участие 3813 пациентов. Выявлены достоверные различия в общей выживаемости в пользу анти-PD1 антител (ОР 0,69, 95% ДИ 0,63-0,75; p
Рак пищевода, мета-анализ, иммунотерапия, химиотерапия
Короткий адрес: https://sciup.org/140300125
IDR: 140300125 | DOI: 10.18027/2224-5057-2023-13-2-3
Meta-analysis of studies on the effectiveness of adding anti-PD1 antibodies to the first-line chemotherapy in advanced esophageal cancer
Introduction: The results of six randomized control trials have been published by 2022, which evaluated the efficacy of adding PD-1 inhibitors to the first-line chemotherapy in patients with metastatic esophageal cancer. However, it still remains unclear which patients derive the most clinical benefit from combined therapy. Therefore, it is necessary to evaluate the efficacy of the combination of anti-PD1 treatment with chemotherapy in different patient subgroups.Materials and methods: We conducted a meta-analysis of randomized controlled trials in patients with stage IV esophageal cancer who received anti-PD1 drugs with different chemotherapeutic regimens in the first-line setting to select patients who benefit the most from the combined therapy.Results: Six randomized trials were included in the analysis for a total of 3,813 patients. Patients who received combination therapy had significantly longer OS (HR = 0.69, 95% CI: 0.63-0.75; p
Текст научной статьи Мета-анализ исследований эффективности добавления анти-PD1 антител к химиотерапии первой линии распространённого рака пищевода
В 2020 году в мире было диагностировано свыше 604 тыс. новых случаев рака пищевода (РП), умерло 544 тыс. человек [15]. РП у многих пациентов диагностируется на поздних стадиях. Так, в Российской Федерации в 2020 году III и IV стадии были установлены у 30% и 33% больных соответственно [1]. РП представлен двумя основными морфологическими вариантами — аденокарциномой и плоскоклеточным раком. Первый вариант более распространен в странах Западной Европы и США, тогда как плоскоклеточный рак пищевода (пРП) остается преобладающим в странах Азии и в России. Долгие годы основой терапии метастатического пРП составляли комбинации цисплатина и фторурацила или таксанов и цисплатина, медиана общей выживаемости (ОВ) на которых обычно не превышает 10 месяцев [2,9]. Новый класс препаратов — анти-PD1 моноклональные антитела — впервые за многие годы позволил улучшить отдаленные результаты терапии пациентов с метастатическим пРП. В недавно опубликованных рандомизированных исследованиях было показано, что их добавление к химиотерапии первой линии увеличило выживаемость без прогрессирования (ВБП) и ОВ, однако данные по предиктивному значению ряда факторов, включая экспрессию PD-L1, были противоречивыми.
В связи с этим нами был проведен мета-анализ рандомизированных исследований по изучению комбинации анти-PD1 антител и химиотерапии с целью определения клинических групп, в которых данный подход был бы наиболее эффективен.
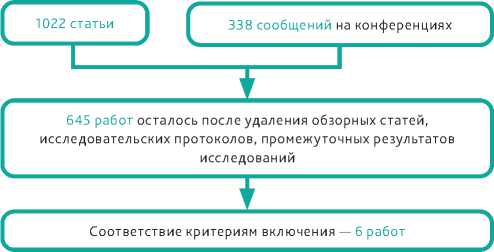
Рисунок 1. Диаграмма отбора исследований для мета-анализа.
МАТЕРИАЛЫ И МЕТОДЫ
Нами выполнен поиск статей в базе данных PubMed, в которых упоминаются сочетание анти-PD1 антител и химиотерапии в первой линии лечения распространённого рака пищевода. Компьютерный поиск был дополнен изучением списка литературы обзорных статей и оригинальных работ, а также тезисов, представленных на конференциях ASCO и ESMO за все время до июля 2022 года.
Критерии включения результатов исследования:
-
1. Проспективное рандомизированное исследование III фазы у пациентов с распространённым раком пищевода;
-
2. Первая линия терапии;
-
3. Химиотерапия в качестве группы контроля;
-
4. Представлены данные по сравнению ОВ и /или ВБП и/или объективный ответ (ОО).
Диаграмма отбора исследований для анализа представлена на рис. 1.
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Различия в ОВ представляли в виде отношения рисков смерти сравниваемых групп и 95% доверительного интервала (ДИ) к данному показателю. Различия в ВБП представляли в виде отношения рисков прогрессирования или смерти сравниваемых групп и 95% ДИ к данному показателю. Различия в частоте ОО, нежелательных явлений 3–4 степени и серьезных нежелательных явлений представляли в виде отношения шансов достижения изучаемого параметра сравниваемых групп и 95% ДИ к данному показателю. Анализ проводился во всей популяции больных, а также в подгруппах, для которых были представлены данные в статьях (пол, экспрессия
Таблица 1. Характеристика пациентов рандомизированных исследований, включенных в мета-анализ.
|
Исследование |
Checkmate 648 (6) |
Checkmate 648 (6) |
KEYNOTE-590 (7) |
ORIENT-15 (8) |
ESCORT-1st (9) |
JUPITER-06 (10) |
RATIONALE-306 (11) |
|
Кол-во пациентов в группе ИТ + ХТ/общее кол-во пациентов |
321/970 |
325/970 |
373/749 |
327/659 |
298/596 |
257/514 |
326/649 |
|
Иммунопрепарат |
Ниволумаб |
Ниволумаб с ипилимуму-мабом1 |
Пембролизумаб |
Синтилимаб |
Камрел изумаб |
Торипалимаб |
Тислелизумаб |
|
Химиотерапия 2 |
PF |
PF |
PF |
TP (93%), PF (7%) |
TP |
TP |
TP (55%) PF (45%) |
|
ОР ОВ (95% ДИ) |
0,74 (0,58–0,96) |
0,78 (0,62–0,98) |
0,73 (0,63–0,86) |
0,63 (0,51–0,78) |
0,7 (0,56–0,88) |
0,58 (0,43–0,78) |
0,66 (0,54–0.8) |
|
PD-L1 CPS ≥ 1 |
87% |
87% |
нд |
92% |
нд |
78% |
нд |
|
PD-L1 CPS ≥ 10 |
43% |
43% |
51% |
57% |
нд |
41% |
36% |
|
PD-L1 TPS ≥ 1 |
49% |
49% |
нд |
55% |
55% |
нд |
нд |
|
PD-L1 TPS ≥ 10 |
31% |
31% |
нд |
36% |
34% |
нд |
нд |
|
Антитело для оценки PD-L1 |
28–8 |
28–8 |
22C3 |
22C3 |
6E8 |
JS311 |
SP263 |
|
Женщины |
18% |
16% |
16% |
15% |
13% |
15% |
13% |
|
Не курильщики |
21% |
14% |
нд |
нд |
нд |
нд |
23% |
|
Возраст < 65 лет |
нд |
нд |
57% |
59% |
нд |
62% |
нд |
|
Статус ECOG1 |
54% |
54% |
60% |
77% |
77% |
75% |
67% |
|
Азиаты |
72% |
73% |
54% |
100% |
100% |
100% |
25% |
|
Ранее проводимая ЛТ |
нд |
нд |
нд |
19% |
16,0% |
14,0% |
12% |
|
Плоскоклеточный рак |
97% |
99% |
73% |
100% |
100% |
100% |
100% |
Стандартную ошибку вычисляли из 95% ДИ. Статистический анализ включал в себя тест χ2 для подтверждения однородности результатов включенных в анализ исследований. В отсутствие статистически значимой гетерогенности результатов исследований (р > 0,1) метод „generic inverse variance“ с фиксированным эффектом применяли для оценки отношения рисков прогрессирования и смерти и построения 95% ДИ. В другом случае применялась модель случайных эффектов. С целью исключения систематической ошибки, связанной с публикацией, проводилось построение воронкообразных графиков (со значениями стандартной ошибки (log OР) по оси ординат и отношением рисков (ОР).
Мета-анализ проводился с использованием программы Review Manager (RevMan, Computer program),
Version 5.3. Copenhagen: The Nordic Cochrane Centre, The Cochrane Collaboration, 2014.
РЕЗУЛЬТАТЫ
Исследования, включенные в мета-анализ
В мета-анализ были включены данные 6 рандомизированных исследований по изучению комбинаций ан-ти-PD1 антител и химиотерапии в первой линии терапии распространенного рака пищевода (рис. 1). Характеристика представлена в табл. 1.
В таблице с характеристиками исследований представлены данные исследования Checkmate-648, в котором пациенты были рандомизированы на 3 группы лечения: в первой группе пациенты получали иммунотерапию в комбинации с химиотерапией, во второй — комбинацию ипилимумаба с ниволумабом, в третьей — химиотерапию. В дальнейший анализ данное исследование не было включено, так как целью мета-анализа являлась оценка эффективности добавления анти-PD1 препаратов к химиотерапии.
Результаты мета-анализа
Общая выживаемость
В анализ результатов добавления ингибиторов иммунных контрольных точек к первой линии химиотерапии были включены данные 5 рандомизированных исследований: 1902 пациента получали лечение комбинацией и 1910 — только химиотерапией. Тест на однородность результатов исследований, включенных в мета-анализ,
|
Study or Subgroup |
log[Hazard Ratio] |
Anti-PD1 antibodies SE |
+ CT Total |
CT Total |
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|
|
Checkmate 648 (nivo_CF) |
-0.30111 |
0.096368 |
321 |
324 |
19.0% |
0.74 [0.61,0.89] |
-*- |
|
|
ESCORT-1 st (Camrelizumab_PC) |
-0.35667 |
0 115302 |
298 |
298 |
13.3% |
0.70 [0.56, 0.88] |
||
|
JUPITER-06 (Toripalimab_PC) |
-0.54473 |
0.155878 |
257 |
257 |
7.3% |
0.58 [0.43, 0.79] |
—— |
|
|
KEYNOTE-590 (pembro_CF) |
-0.31471 |
0.079391 |
373 |
376 |
28.0% |
0.73 [0.62, 0.85] |
||
|
ORIENT-15 (sintilimab_CF_PC) |
-0.46522 |
0.108408 |
327 |
332 |
15.0% |
0.63 [0.51,0.78] |
||
|
RATI 0 NALE- 3 0 6 (ti s I e I izu m a b_C F_P C) |
-0.41552 |
0.100266 |
326 |
323 |
17.5% |
0.66 [0.54, 0.80] |
||
|
Total (95% Cl) |
1902 |
1910 |
100.0% |
0.69 [0.63,0.75] |
||||
Test for overall effect: Z = 8 92 (P « 0.00001)
0.01 0.1
Anti-PD1 antibodies ♦ CT CT
Рисунок 2а. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител.
|
Study or Subgroup log[Hazard Ratio] |
SE |
Anti-PDI antibodies + CT Total |
CT Total |
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|||
|
Checkmate 648 (nivo_CF) -0.30111 |
0.096368 |
321 |
324 |
26.4% |
0.74 [0.61,0.89] |
■ |
|||
|
ESCORT-1 st (Camrelizumab_PC) -0.35667 |
0 115302 |
298 |
298 |
18.4% |
0.70 [0.56, 0.88] |
||||
|
JUPITER-06 (Toripalimab_PC) -0.54473 |
0.155878 |
257 |
257 |
10.1 % |
0.58 [0.43, 0.79] |
—■— |
|||
|
KEYNOTE-590 (pembro_CF) -0.31471 |
0.079391 |
373 |
376 |
0.0% |
0.73 [0.62, 0.85] |
||||
|
ORIENT-15 (sintilimab_CF_PC) -0.46522 |
0.108408 |
327 |
332 |
20.8% |
0.63 [0.51,0.78] |
||||
|
RATIONALE-306 (tislelizumab_CF_PC) -0.41552 |
0.100266 |
326 |
323 |
24.3% |
0.66 [0.54, 0.80] |
||||
|
Total (95% Cl) Heterogeneity: Chi== 2.44, df= 4 (P = 0.66); P = 0% |
1529 |
1534 |
100.0% |
0.67 [0.61,0.74] |
♦ |
||||
|
0.01 Anti-PD1 |
0'1 antibodies + CT |
CT |
10 |
100 |
|||||
|
Testfor overall effect: Z = 8.04 (P < 0.00001) |
|||||||||
Рисунок 2b. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) только при плоскоклеточном раке пищевода.
в отношении ОВ показал отсутствие значимых различий — р = 0,66 (I2 = 0 %). При этом выявлены достоверные различия в общей выживаемости в пользу анти-PD1 антител (ОР 0,69, 95 % ДИ 0,63–0,75; p < 0,001; рис. 2а). Аналогичные результаты были получены и при анализе исследований с плоскоклеточным гистотипом (рис. 2b).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 на опухолевых клетках < 1% доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал наличие значимых различий в данной подгруппе пациентов — р = 0,04 (I2 = 63%). При этом выявлены пограничные различия в ОВ в пользу ан-ти-PD1 антител (ОР 0,74, 95% ДИ 0,55–0,99; p = 0,05, рис. 3).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией
PD-L1 на опухолевых клетках ≥ 1% также доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,64 (I2 = 0%). При этом выявлены значимые различия в ОВ в пользу анти-PD1 антител (ОР 0,61, 95% ДИ 0,52–0,71; p < 0,001, рис. 4).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 в рамках CPS ≥ 1 доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,58 (I2 = 0%). При этом выявлены значимые различия в ОВ в пользу анти-PD1 антител (ОР 0,64, 95% ДИ 0,56–0,73; p < 0,001, рис. 5).
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
Weight |
Hazard Ratio IV, Random, 95% Cl |
Hazard Ratio IV, Random, 95% Cl |
||
|
Checkmate 648 (nivo_CF) ESCORT-1 st (Camrelizumab_PC) JUPITER-06 (Toripalimab_PC) ORIENT-15 (sintilimab_CF_PC) |
-0.0202 -0.23572 -0.4943 -0.59784 |
0.1 32984 0.17002 0.36406 0.1 60359 |
31.7% 27.5% 12.2% 28.6% |
0.98 [0.76, 1.27] 0.79 [0.57, 1.10] 0.61 [0 30, 1.25] 0.55 [0.40, 0.75] |
|||
|
-■- |
|||||||
|
Total (95% Cl) Heterogeneity: Tau== 0.05; ChP = Test for overall effect: Z = 2.00 (P = |
8.12, df= 3 (P = 0.04); I 0.05) |
100.0% |
0.74 [0.55, 0.99] |
♦ |
|||
|
= - 63% |
0.01 Anti-PD1 |
o'l antibodies + CT |
10 CT |
100 |
|||
Рисунок 3. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках < 1%.
Total (95% Cl)
Heterogeneity: Chi== 1.68, df= 3 (P = 0.64); l==0%
Test for overall effect: Z = 6.54 (P < 0.00001)
|
I------------------------------------------------------1------------------------------------------------------- 0.01 0.1 |
— 1 |
-------------------------------------------------------1 0 100 |
Anti-PD1 antibodies + CT CT
|
Study or Subgroup |
Hazard Ratio Hazard Ratio log[Hazard Ratio] SE Weight IV, Fixed, 95%Cl IV, Fixed, 95% Cl |
|
Checkmate 648 (nivo_CF) ESCORT-1 st (Camrelizumab_PC) JUPITER-06 (Toripalimab_PC) ORIENT-15 (sintilimab_CF_PC) |
-0.59784 0.133931 32.1% 0.55 [0.42,0.72] * -0.52763 0.158374 22.9% 0.59 [0.43,0.80] "■" -0.4943 0.173908 19.0% 0.61 [0.43,0.86] “^ -0.34249 0.148874 26.0% 0.71 [0.53,0.95] "■" |
100.0% 0.61 [0.52, 0.71] ♦
Рисунок 4. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках ≥ 1.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|
|
Checkmate 648 (nivo_CF) |
-0.37106 |
0.103435 |
46.7% |
0.69 [0.56, 0.85] |
■ |
|
|
JUPITER-06 (Toripalimab_PC) |
-0.4943 |
0.176823 |
16.0% |
0.61 [0.43, 0.86] |
||
|
ORIENT-15 (sintilimab_CF_PC) |
-0.52763 |
0.115795 |
37.3% |
0.59 [0.47, 0.74] |
<■ |
|
|
Total (95% Cl) |
100.0% |
0.64 [0.56, 0.73] |
Ф |
|||
|
Heterogeneity: Chi== 1.09, df= 2 (P = 0.58); l== 0% |
I--------------------------------- П ГИ |
—I---- n |
-----------------------------------------------------------------------------------1------------------------------------------------------------------------------------- 1 П 1 00 |
|||
|
Test for overall effect: Z= 6.35 (P < |
0.00001) |
anti-PD antobodies + CT |
CT |
|||
Рисунок 5. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 CPS ≥ 1.
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 в рамках CPS < 1 доступны были только в 3 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал наличие значимых различий в данной подгруппе пациентов — р = 0,09 (I2 = 58 %). При этом не выявлены различия в ОВ (ОР 0,58, 95 % ДИ 0,31–1,1, p = 0,1, рис. 6).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 на опухолевых клетках менее 10% доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,63 (I2 = 0%). При этом выявлены значимые различия в ОВ в пользу анти-PD1 антител (ОР 0,73, 95% ДИ 0,64–0,84; p < 0,001, рис. 7).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрес- сией PD-L1 на опухолевых клетках ≥ 10% доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,87 (I2 = 0 %). При этом выявлены значимые различия в ОВ в пользу анти-PD1 антител (ОР 0,58, 95% ДИ 0,48–0,7; p < 0,001, рис. 8).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 в рамках CPS ≥ 10 доступны были только в 3 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,99 (I2 = 0 %). При этом выявлены значимые различия в ОВ в пользу анти-PD1 антител (ОР 0,64, 95% ДИ 0,54–0,76; p < 0,001, рис. 9a). Аналогичные результаты получены и при плоскоклеточном гистотипе (рис. 9b).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экс-
Hazard Ratio
Hazard Ratio
Study or Subgroup
log[Hazard Ratio]SE Weight IV, Random, 95% Cl
IV, Random, 95% Cl
Checkmate 648 (nivo_CF)
JUPITER-06 (Toripalimab_PC)
ORIENT-15 (sintilimab_CF_PC)
-0.0202 0.347188 34.6%
-0.4943 0.366011 33.1%
-1.13943 0.377776 32.3%
0.98 [0.50,1.94]
0.61 [0.30,1.25]
0.32 [0.15, 0.67]

Total (95% Cl) 100.0%
0.58 [0.31,1.10]
I-----------------------1----------------------------------------------I—
0.01 0.1 10
Anti-PD1 antibodies * CT CT
Heterogeneity: Tau== 0.18; Chi= = 4.77, df= 2 (P = 0.09); l= = 58%
Test for overall effect: Z = 1.66 (P = 0.10)
Рисунок 6. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 CPS < 1.
Hazard Ratio
Hazard Ratio
|
Study or Subgroup log[Hazard Ratio] |
SE Weight IV, Fixed, 95% Cl IV, Fixed, 95% Cl |
|
Checkmate 648 (nivo_CF) -0.23572 ESCORT-1 st (Camrelizumab_PC) -0.24846 JUPITER-06 (Toripalimab_PC) -0.4943 ORIENT-15 (sintilimab_CF_PC) -0.39304 |
0.11 5302 37.3% 0.79 [0.63,0.99] ■• 0.139652 25.4% 0.78 [0.59,1.03] “^ 0.21 5235 10.7% 0.61 [0.40,0.93] -^ 0.136756 26.5% 0.68 [0.52,0.88] * |
Total (95% Cl)
|
100.0% 0.73 [0.64, 0.84] |
* |
|
|
0.01 0J |
10 1 00* |
|
Anti-PD1 antibodies + CT CT
Heterogeneity: Chi== 1.71, df= 3 (P= 0.63); l==0%
Test for overall effect: Z = 4.38 (P < 0.0001)
Рисунок 7. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT)
или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках < 10%.
Hazard Ratio Hazard Ratio
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
Weight |
IV, Fixed, 95% Cl |
IV, Fixed, 95% Cl |
|
|
Checkmate 648 (nivo_CF) |
-0.47804 |
0.1 73908 |
31.7% |
0.62 [0.44, 0.87] |
■ |
|
|
ESCORT-1 st (Camrelizumab_PC) |
-0.65393 |
0.207679 |
22.2% |
0.52 [0.35, 0.78] |
||
|
JUPITER-06 (Toripalimab_PC) |
-0.44629 |
0.241 288 |
16.5% |
0.64 [0.40,1.03] |
||
|
ORIENT-1 5 (sintilimab_CF_PC) |
-0.60331 |
0.180123 |
29.6% |
0.55 [0.38, 0.78] |
■ |
|
|
Total (95% Cl) |
100.0% |
0.58 [0.48, 0.70] |
Ф |
|||
|
Heterogeneity: Chi== 0.69, df= 3 (P |
= 0.87); F = 0% |
I-----------1— |
-----------------------------------------------------------1-----------------------------------------------------------1 1 П 1 ПП |
|||
|
Те st for overall effect: Z = 5.61 (P ■= 0.00001) |
Favours [experimental] |
Favours [control] |
||||
Рисунок 8. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках ≥ 10%.
прессией PD-L1 в рамках CPS < 10 доступны были только в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,26 (I2 = 26%). При этом выявлены различия в ОВ в пользу анти-PD1 антител (ОР 0,79, 95% ДИ 0,72–0,87, p < 0,001, рис. 10a). Аналогичные результаты получены и при плоскоклеточном гистотипе (рис. 10b).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов мужского пола
Hazard Ratio Hazard Ratio
|
Study or Subgroup log[Hazard Ratio] SE Weight IV, Fixed, 95% Cl |
IV, Fixed, 95% Cl |
||
|
Checkmate 648 (niVO_CF) -0.46204 0.1 481 3 34.9% 0.63 [0.47,0.84] KEYNOTE-590 (pembre_CF) -0.44629 0.1 1 4847 0.0% 0.64 [0.51,0.80] ORIENT-1 5 (sintilimab_CF_PC) -0.44942 0.1 451 77 36.3% 0.64 [0.48, 0.85] RATIONALE-306 (tislelizumab_CF_PC) -0.43078 0.1 6288 28.8% 0.65 [0 47,0.89] Total (95% Cl) 100.0% 0.64 [0.54, 0.76] Heterogeneity: Chi’- 0.02, df- 2 (P- 0.99); l=- 0% Те st for overall effect: Z = 5.13 (P < 0.00801) л |
-■- -■- -■- ♦ |
||
|
0.01 0'1 i 1 ti-PD1 antibodies + CT CT |
0 100* |
||
Рисунок 9a. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 CPS ≥ 10.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
|
Checkmate 648 (nivo_CF) |
-0.46204 |
0.14813 |
|
KEYNOTE-590 (pembro_CF) |
-0.44629 |
0.1 1 4847 |
|
ORIENT-15 (sintilimab_CF_PC) |
-0.44942 |
0.145177 |
|
RATIONALE-386 (tislelizumab_CF_PC) |
-0.43078 |
0.1 6288 |
Total (95% Cl)
Heterogeneity: Chi= = 0.02, df= 2 (P = 0.99); l= = 0%
Те st for overall effect: Z= 5.13 (P < 0.00001)
|
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|||
|
34.9% |
0.63 [0.47, 0.84] |
■ |
|||
|
0.0% |
0.64 [0.51, 0.80] |
||||
|
36.3% |
0.64 [0.48, 0.85] |
-e- |
|||
|
28.8% |
0.65 [0.47, 0.89] |
■ |
|||
|
100.0% |
0.64 [0.54, 0.76] |
♦ |
|||
|
0.01 |
0J |
10 |
100* |
||
|
Anti-P DI |
antibodies + CT |
CT |
|||
Рисунок 9b. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PDL на опухолевых клетках CPS ≥ 10 при плоскоклеточном гистотипе.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|
Checkmate 648 (nivo_CF) |
-0.24846 |
0.1 32851 |
12.7% |
0.78 [0.60,1.01] |
|
|
KEYNOTE-590 (pembre_CF) |
-0.1 7435 |
0.058269 |
66.0% |
0.84 [0.75, 0.94] |
■ |
|
ORIENT-1 5 (sintilimab_CF_PC) |
-0.48289 |
0.1637 |
8.4% |
0.62 [0.45, 0.85] |
|
|
RATIONALE-306 (tislelizumab_CF_PC) |
-0.34249 |
0.131239 |
13.0% |
0.71 [0.55, 0.92] |
-n- |
Total (95% Cl)
100.0% 0.79 [0.72, 0.87]♦
I-------------------1------------------II-
0.01 0.1 110
Anti-PD1 antibodies + CT CT
Heterogeneity: Chi= = 4.05, df= 3 (P = 0.26); l= = 26%
Test for overall effect: Z = 4.89 (P « 0.00001)
Рисунок 10a. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 CPS < 10.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
|
Checkmate 648 (nivo_CF) |
-0.24846 |
0.1 32851 |
|
KEYNOTE-590 (pembre_CF) |
-0.1 7435 |
0.058269 |
|
ORIENT-1 5 (sintilimab_CF_PC) |
-0.48289 |
0.1637 |
|
RATIONALE-306 (tislelizumab_CF_PC) |
-0.34249 |
0.131239 |
Total (95% Cl)
Heterogeneity: Chi== 1.24, df= 2 (P = 0.54); l= = 0%
Те st for overall effect: Z = 4.22 (P < 0.0001)
|
Hazard Ratio Weight IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
||
|
37.3% 0.78 [0.60,1.01] 0.0% 0.84 [0.75, 0.94] 24.5% 0.62 [0.45, 0.85] 38.2% 0.71 [0.55, 0.92] 100.0% 0.71 [0.61,0.83] |
■ ♦ |
||
|
0.01 0'1 Anti-PD1 antibodies + CT |
1 CT |
0 100* |
|
Рисунок 10b. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PDL на опухолевых клетках CPS < 10 при плоскоклеточном гистотипе.
доступны были во всех 6 исследованиях. Тест на однородность результатов исследований, включенных в метаанализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,52 (I2 = 0%). При этом выявлены значимые различия в общей выживаемости в пользу анти-PD1 антител (ОР 0,66, 95% ДИ 0,6–0,72, p < 0,001, рис. 11a). Аналогичные результаты были получены и при плоскоклеточном гистотипе (рис. 11b).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов женского пола доступны были во всех 6 исследованиях. Тест на однородность результатов исследований, включенных в метаанализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,45 (I2 = 0%). При этом выявлены значимые различия в общей выживаемости в пользу анти-PD1 антител (ОР 0,78, 95% ДИ 0,62–0,98, p = 0,03, рис. 12a). При плоскоклеточном гистотипе значимых различий в общей выживаемости не получено (рис. 12b).
Была выявлена схожая эффективность в отношении ОВ комбинации иммунотерапии и химиотерапии в подгруппах пациентов азиатской и неазиатской рас: ОР 0,66, 95% ДИ 0,6–0,73 и ОР 0,71, 95% ДИ 0,62–0,81 соответственно (рис. 1, 2 приложения).
Достоверный выигрыш в отношении ОВ в группе иммунотерапии и химиотерапии отмечался вне зависимо- сти от применяемого режима химиотерапии — цисплати-на/фторурацила и паклитаксела/цисплатина: ОР 0,67, 95% ДИ 0,58–0,77 и ОР 0,68, 95% ДИ 0,59–0,77 соответственно (рис. 3, 4 приложения).
На выигрыш в отношении ОВ в группе иммунотерапии и химиотерапии также не влияли такие факторы как наличие или отсутствие метастазов в печени (ОР 0,6,95% ДИ 0,44–0,81 и ОР 0,7,95% ДИ 0,6–0,83 соответственно (рис. 5, 6 приложения)), функциональный статус по шкале ECOG 0 или 1 (ОР 0,62, 95% ДИ 0,53–0,71 и ОР 0,7, 95% ДИ 0,63–0,77 соответственно (рис. 7, 8 приложения)), возраст младше или старше 65 лет (ОР 0,73, 95% ДИ 0,65–0,81, p < 0,001 и ОР 0,62, 95% ДИ 0,54–0,72 соответственно (рис. 9, 10 приложения)), вес менее или более 60 кг (ОР 0,72, 95% ДИ 0,59–0,88 и ОР 0,6, 95% ДИ 0,47–0,76 соответственно (рис. 11, 12 приложения)).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с поражением менее 2 органов доступны были в 2 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,44 (I2 = 0%). При этом отмечена тенденция к различиям в ОВ в пользу анти-PD1 антител (ОР 0,81, 95% ДИ 0,66–1,0, p < 0,001, рис. 13).
|
Hazard Ratio Hazard Ratio Study or Subgroup log[Hazard Ratio] SE Weight IV, Fixed, 95% Cl IV, Fixed, 95% Cl |
||
|
Checkmate 648 (niVO_CF) -0.35667 0.1 04922 1 8.4% 0.70 [0.57, 0.86] "■" ESCORT-1 st (Camrelizumab_PC) -0.37106 0.1 1 9899 1 4.1% 0.69(0.55,0.87] "^ JUPITER-06 (Toripalimab_PC) -0.69315 0.1 69637 7.0% 0.50(0.36,0.70] -— KEYNOTE-590 (pembro_CF) -0.46204 0.08857 25.8% 0.63 [0.53,0.75] » ORIENT-1 5 (sintilimab_CF_PC) -0.44006 0.1 1 5077 1 5.3% 0.64(0.51,0.81] — RATIONALE-306 (tislelizumab_CF_PC) -0.3285 0.1 01 99 1 9.4% 0.72(0.59,0.88] * Total (95% Cl) 100.0% 0.66 [0.60,0.72] ♦ Heterogeneity: Chi= = 4.18, df= 5 (P= 0.52); l= = 0% H------- t+---------- Testfor overall effect: Z = 9.27 (P = 0.00001) Anti-PD1 antibodies + CT |
1 CT |
b 0 |
Рисунок 11a. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у мужчин.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
|
Checkmate 648 (nivo_CF) |
-0.35667 |
0.1 04922 |
|
ESCORT-1 st (Camrelizumab_PC) |
-0.37106 |
0.1 1 9899 |
|
JUPITER-06 (Toripalimab_PC) |
-0.69315 |
0.1 69637 |
|
KEYNOTE-590 (pembro_CF) |
-0.46204 |
0.08857 |
|
ORIENT-1 5 (sintilimab_CF_PC) |
-0.44006 |
0.1 1 5077 |
|
RATIONALE-306 (tislelizumab_CF_PC) |
-0.3285 |
0.10199 |
Total (95% Cl)
Heterogeneity: Chi= = 3.83, df= 4 (P = 0.43); l= = 0%
Те st for overall effect: Z= 7.68 (P < 0.00001)
|
Hazard Ratio Hazard Ratio Weight IV, Fixed, 95% Cl IV, Fixed, 95% Cl |
||
|
24.8% 0.70 [0 57, 0.86] * 19.0% 0.69[0.55,0.87] "■" 9.5% 0.50 [0.36, 0.70] “^ 0.0% 0.63 [0.53, 0.75] 20.6% 0.64(0.51,0.81] -" 26.2% 0.72 [0.59, 0.88] * 100.0% 0.67 [0.60, 0.74] ♦ |
||
|
0.01 0J Anti-PD1 antibodies + CT |
1 CT |
0 1 oo1 |
Рисунок 11b. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у мужчин при плоскоклеточном гистотипе.
Hazard Ratio Hazard Ratio
|
Study or Subgroup log[Hazard Ratio] SE Weight IV, Fixed, 95% Cl |
IV, Fixed, 95% Cl |
||
|
Checkmate 648 (nivo_CF) 0.01 9803 0.238487 24.9% 1.02 [0.64,1.63] ESCORT-1 st (Camrelizumab_PC) -0.1 3926 0.37266 1 0.2% 0.87 [0.42,1.81] JUPITER-06 (Toripalimab_PC) 0.336472 0.433334 7.5% 1.40 [0.60,3.27] KEYNOTE-590 (pembro_CF) -0.30111 0.21 0887 31.8% 0.74(0.49,1.12] ORIENT-15 (sintilimab_CF_PC) -0.55687 0.342069 1 2.1% 0.57 [0.29,1.12] RATIONALE-306 (tislelizumab_CF_PC) -0.77653 0.322601 1 3.6% 0.46 [0.24,0.87] Total (95% Cl) 100.0% 0.78 [0.62, 0.98] Heterogeneity: Chi’- 6.73, df- 5 (P - 0.24); l=- 26% Те st for overall effect: Z = 2.12 (P= 0.03) Ar |
|||
|
♦ |
|||
|
0.01 0J i 1 ti-PD1 antibodies + CT CT |
0 |
||
Рисунок 12a. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) у женщин.
|
Hazard Ratio Study or Subgroup log[Hazard Ratio] SE Weight IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
||
|
Checkmate 648 (nivo_CF) 0.01 9803 0.238487 36.4% 1.02 [0.64,1.63] ESCORT-1 st (Camrelizumab_PC) -0.1 3926 0.37266 1 4.9% 0.87 [0.42,1.81] JUPITER-06 (Toripalimab_PC) 0.336472 0.433334 1 1.0% 1.40 [0.60, 3.27] KEYNOTE-590 (pembro_CF) -0.30111 0.21 0887 0.0% 0.74 [0.49,1.12] ORIENT-15 (sintilimab_CF_PC) -0.55687 0.342069 1 7.7% 0.57 [0.29,1.12] RATIONALE-306 (tislelizumab_CF_PC) -0.77653 0.322601 1 9.9% 0.46 [0.24,0.87] Total (95% Cl) 100.0% 0.79 [0.60,1.05] Heterogeneity: Chi’- 6.65, df- 4 (P- 0.16); l=- 40% Те st for overall effect:Z=1.60 (P= 0.11) Ar |
|||
|
0.01 0J ti-PD1 antibodies + CT |
1 CT |
0 100 |
|
Рисунок 12b. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у женщин при плоскоклеточном гистотипе.
Hazard Ratio
Hazard Ratio
Study or Subgroup log [Hazard Ratio]SE Weight ГУ, Fixed, 95% Cl
Checkmate 648 (nivo_CF) -0.27444 0.138961 60.2% 0.76 [0.58,1.00]
ESCORT-1 st (Camrelizumab_PC) -0.10536 0.170773 39.8% 0.90 [0.64,1.26]
IV, Fixed, 95% Cl
Total (95% Cl)
Heterogeneity: Chi= = 0.59, df= 1 (p = 0.44); l==0%
Test for overall effect: Z = 1.92 (P = 0.05)
100.0% 0.81 [0.66,1.00]♦
I---------------------------1-------------------------I---------------------------11
0.01 0.1 1 10100
Anti-PD1 antibodies + CT CT
Рисунок 13. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у пациентов с поражением менее 2 органов.
Hazard Ratio Hazard Ratio
Study or Subgroup log [Hazard Ratio]SE Weight ГУ, Fixed, 95% Cl
Checkmate 648 (nivo_CF) -0.21072 0.130313 59.5% 0.81 [0.63,1.05]
ESCORT-1 st (Camrelizumab_PC) -0.56212 0.157918 40.5% 0.57 [0.42, 0.78]
IV, Fixed, 95% Cl
Total (95% Cl)
Heterogeneity: Chi= = 2.95, df= 1 (P = 0.09); l== 66%
Test for overall effect: Z = 3.51 (P = 0.0004)
100.0% 0.70 [0.58, 0.86]♦
I------------------------------------------------------1--------------------------------------------------------------------------------------------------------------11
0.01 0.1 1 10100
Anti-PD1 antibodies + CT CT
Рисунок 14. Форест-график мета-анализа исследований, в которых проводилось сравнение ОВ: химиотерапии (CT)
или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у пациентов с поражением 2 и более органов.
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с поражением 2 и более органов доступны были в 2 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, выявил наличие различий в данной подгруппе пациентов — р = 0,08 (I2 = 66%). При этом отме- чено значимое различие в ОВ в пользу анти-PD1 антител (ОР 0,7, 95% ДИ 0,58–0,86, p < 0,001, рис. 14).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с локорегионар-ным прогрессированием доступны были в 5 исследованиях. Тест на однородность результатов исследований, вклю-
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
|
Checkmate 648 (nivo_CF) |
0.1 22218 |
0.34799 |
|
ESCORT-1 st (Camrelizumab_PC) |
-0.1 7435 |
0.25208 |
|
JUPITER-06 (Toripalimab_PC) |
-0.69315 |
0.41 9683 |
|
ORIENT-1 5 (sintilimab_CF_PC) |
-0.26136 |
0.32047 |
|
RATIONALE-306 (tislelizumab_CF_PC) |
-0.82098 |
0.290264 |
Total (95% Cl)
Heterogeneity: Chi= = 5.70, df= 4 (P = 0.22); l= = 30%
Те st for overall effect:Z= 2.51 (P = 0.01)
|
Hazard Ratio Weight IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
||
|
16.1% 1.13 [0.57, 2.24] 30.7% 0.84(0.51,1.38] 11.1% 0.50 [0 22,1.14] 19.0% 0.77 [0.41,1.44] 23.1% 0.44 [0.25, 0.78] 100.0% 0.70 [0.54, 0.93] Ar |
|||
|
0.01 0J i 1 ti-PD1 antibodies + CT CT |
0 100* |
||
Рисунок 15. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у пациентов с локорегионарным прогрессированием.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
|
Checkmate 648 (nivo_CF) |
-0.28768 |
0.124186 |
|
ESCORT-1 st (Camrelizumab_PC) |
-0.41552 |
0.1 33296 |
|
JUPITER-06 (Toripalimab_PC) |
-0.52763 |
0.1 67765 |
|
ORIENT-1 5 (sintilimab_CF_PC) |
-0.47804 |
0.1 1 5302 |
|
RATIONALE-306 (tislelizumab_CF_PC) |
-0.3285 |
0.10199 |
Total (95% Cl)
Heterogeneity: Chi= = 2.33, df= 4 (P= 0.67); l== 0%
Те st for overall effect: Z = 7.09 (P = 0.00001)
|
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|||
|
19.8% |
0.75 [0.59, 0.96] |
-1- |
|||
|
17.2% |
0.66 [0.51, 0.86] |
■ |
|||
|
10.8% |
0.59 [0.42, 0.82] |
||||
|
22.9% |
0.62 [0.49, 0.78] |
■ |
|||
|
29.3% |
0.72 [0.59, 0.88] |
-■- |
|||
|
100.0% |
0.68(0.61,0.75] |
1 |
|||
|
0.01 |
0J |
10 |
1 oo1 |
||
|
Anti-PD1 |
antibodies + CT |
CT |
|||
Рисунок 16. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у пациентов с отдаленными метастазами.
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
Weight |
Hazard Ratio IV, Fixed, 95% Cl |
Hazard Ratio IV, Fixed, 95% Cl |
|
Checkmate 648 (nivo_CF) |
-0.30111 |
0.1 06254 |
42.6% |
0.74 [0.60, 0.91] |
* |
|
ESCORT-1 st (Camrelizumab_PC) |
-0.37106 |
0.1 55987 |
19.8% |
0.69 [0.51, 0.94] |
|
|
RATIONALE-306 (tislelizumab_CF_PC) |
-0.43078 |
0.1 1 3063 |
37.6% |
0.65 [0.52, 0.81] |
* |
|
Total (95% Cl) |
100.0% |
0.70 [0.61,0.80] |
♦ |
0.01
0.1
Heterogeneity: Chi= = 0.70, df= 2 (P = 0.70); l== 0%
Те st for overall effect: Z = 5.24 (P < 0.00001)
Anti-PD1 antibodies + CT CT
Рисунок 17. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) у пациентов, курящих или куривших табак в анамнезе.
ченных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,22 (I2 = 30%). При этом отмечены различия в общей выживаемости (ОР 0,7, 95% ДИ 0,54–0,93, p = 0,01, рис. 15).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с отдаленными метастазами доступны были в 5 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, не выявил различий в данной подгруппе пациентов — р = 0,67 (I2 = 0%). При этом отмечено значимое различие в общей выживаемости в пользу анти-PD1 антител (ОР 0,68, 95% ДИ 0,61–0,75, p < 0,001, рис. 16).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов, курящих или куривших табак в анамнезе, доступны были в 3 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, не выявил различий в данной подгруппе пациентов — р = 0,7 (I2 = 0%). При этом отмечено значимое различие в общей выживаемости в пользу ан-ти-PD1 антител (ОР 0,7, 95% ДИ 0,61–0,8, p < 0,001, рис. 17).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов без факта курения табака в анамнезе доступны были в 2 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,63 (I2 = 0%). При этом не отмечено различий в ОВ (ОР 0,86, 95% ДИ 0,67–1,1, p = 0,23, рис. 18).
Сводные результаты мета-анализа факторов в отношении ОВ представлены в табл. 2 (в приложении).
Hazard Ratio Hazard Ratio
|
Study or Subgroup |
log[Hazard Ratio] SE Weight IV, Fixed, 95% Cl IV, Fixed, 95% Cl |
|
Checkmate 648 (nivo_CF) ESCORT-1 st (Camrelizumab_PC) RATIONALE-306 (tislelizumab_CF_PC) |
0.00995 0.21 4486 35.2% 1.01(0.66,1.54] HH -0.22314 0.225775 31.7% 0.80(0.51,1.25] “»“ -0.26136 0.221 1 99 33.1% 0.77(0.50,1.19] -*" |
Total (95% Cl)
Heterogeneity: Chi= = 0.91, df= 2 (P = 0.63); l== 0%
Те st for overall effect: Z = 1.21 (P = 0.23)
100.0% 0.86(0.67,1.10] ♦
I-----------------------------------------------------1--
0.01 0.1 1
Anti-PD1 antibodies + CT CT
H------------1
10 100
Рисунок 18. Форест-график мета-анализа исследований, в которых проводилось сравнение общей выживаемости (ОВ): химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) у пациентов без факта курения табака в анамнезе.
|
Study or Subgroup log[Hazard Ratio] |
SE |
anti-PD1 antibodies *CT Total |
CT Total |
Weight |
Hazard Ratio IV, Random, 95% Cl |
Hazard Ratio IV, Random, 95% Cl |
|
Checkmate 648 (nivo_CF) -0.21072 |
0 123854 |
321 |
324 |
12.9% |
0.81 [0.64,1.03] |
|
|
ESCORT-1 st (Camrelizumab_PC) -0.57982 |
0.099711 |
298 |
298 |
17.2% |
0.56 [0.46, 0.68] |
|
|
JUPITER-06 (Toripalimab_PC) -0.54473 |
0.120037 |
257 |
257 |
13.5% |
0.58 [0.46, 0.73] |
|
|
KEYNOTE-590 (pembro_CF) -0.40048 |
0.08778 |
373 |
376 |
20.0% |
0.67 [0.56, 0.80] |
|
|
ORIENT-15 (sintilimab_CF_PC) -0.5834 |
0.097652 |
327 |
332 |
17.7% |
0.56 [0.46, 0.68] |
|
|
RATIONALE-306 (tislelizumab_CF_PC) -0.47804 0.09343 Total (95% Cl) Heterogeneity: Tau2= 0.01; ChP= 7.95, df= 5 (P = 0.16); F= 37% Test for overall effect: Z= 8.99 (P < 0.00001) |
326 1902 |
323 1910 |
18.6% 100.0% |
0.62 [0.52, 0.74] 0.62 [0.56,0.69] I------------------------------------------------------------------------------ 8.81 Anti-PD1 |
♦ ----1----------------------H 8.1 10 antibodies + CT CT |
|
Рисунок 19a. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT).м
|
Study or Subgroup log[Hazard Ratio] |
SE |
anti-PD1 antibodies + CT Total |
CT Total |
Weight |
Hazard Ratio IV, Random, 95% Cl |
Hazard Ratio IV, Random, 95% Cl |
|
Checkmate 648 (nivo_CF) -0.21072 |
0 123854 |
321 |
324 |
16.5% |
0.81 [0.64,1.03] |
-^ |
|
ESCORT-1 st (Camrelizumab_PC) -0.57982 |
0.099711 |
298 |
298 |
21.4% |
0.56 [0.46, 0.68] |
|
|
JUPITER-06 (Toripalimab_PC) -0.54473 |
0.120037 |
257 |
257 |
17.2% |
0.58 [0.46, 0.73] |
|
|
KEYNOTE-590 (pembro_CF) -0.40048 |
0.08778 |
373 |
376 |
0.0% |
0.67 [0.56, 0.80] |
|
|
ORIENT-15 (sintilimab_CF_PC) -0.5834 |
0.097652 |
327 |
332 |
21.9% |
0.56 [0.46, 0.68] |
|
|
RATIONALE-306 (tislelizumab_CF_PC) -0.47804 0.09343 Total (95% Cl) Heterogeneity: Tau2 = 0.01; ChP= 7.01, df= 4 (P = 0.14); F= 43% Test for overall effect: Z = 7.82 (P < 0.00001) |
326 1529 |
323 1534 |
22.9% 100.0% |
0.62 [0.52, 0.74] 0.61 [0.54,0.69] I------------------------------------------------------------------------------ 9.91 Anti-PD1 |
* ----1----------------------H 9.1 19 antibodies + CT CT |
|
Рисунок 19b. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) при плоскоклеточном раке.
Hazard Ratio Hazard Ratio
|
Study or Subgroup |
log[Hazard Ratio] |
SE |
Weight |
IV, Fixed, 95% Cl |
IV, Fixed, 95% Cl |
|||
|
Checkmate 648 (nivo_CF) ESCORT-1 st (Camrelizumab_PC) JUPITER-06 (Toripalimab_PC) ORIENT-15 (sintilimab_CF_PC) |
-0.43078 -0.67334 -0.54473 -0.57982 |
0.176823 0.138044 0.136046 0.099711 |
13.4% 22.0% 22.6% 42.1% |
0.65 [0.46, 0.92] 0.51 [0.39, 0.67] 0.58 [0.44, 0.76] 0.56 [0.46, 0.68] |
-■- -■-e |
|||
|
Total (95% Cl) Heterogeneity: Chi== 1.22, df= 3 (P = 0.75); l= = 0% Test for overall effect: Z= 8.85 (P < 8.00001) |
100.0% |
0.56 [0.50, 0.64] |
♦ |
|||||
|
0.01 Anti-PD1 |
antibodies +CT |
CT |
10 |
100* |
||||
Рисунок 20. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT)
или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках ≥ 1%.
Выживаемость без прогрессирования
В рамках сравнения химиотерапии с или без ингибиторов иммунных контрольных точек была также оценена выживаемость без прогрессирования (ВБП) в первой линии лечения.
Тест на однородность результатов исследований, включенных в мета-анализ в отношении ВБП, показал отсутствие различий — р = 0,16 (I2 = 37 %). При анализе данных всех включенных в 6 рандомизированных исследований пациентов выявлены достоверные различия в ВБП в пользу анти-PD1 антител (ОР 0,62, 95% ДИ 0,56–0,69, p < 0,001, рис. 19a). Аналогичные результаты были получены и при плоскоклеточном гистотипе (рис. 19b).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 на опухолевых клетках ≥ 1% доступны были в 4 исследо-
Hazard Ratio Hazard Ratio
|
Study or Subgroup log[Hazard Ratio] SE Weight IV, Random, 95% Cl |
IV, Random, 95% Cl |
|||
|
Checkmate 648 (nivo_CF) -0.051 29 0.1 351 59 28.9% 0.95 [0.73, 1.24] ESCORT-1 st (Camrelizumab_PC) -0.47804 0.1 50561 27.4% 0.62 [0.46, 0.83] JUPITER-06 (Toripalimab_PC) -0.41 552 0.29801 2 1 5.5% 0.66 [0.37,1.18] ORIENT-1 5 (sintilimab_CF_PC) -0.65393 0.1 41 823 28.2% 0.52 [0.39, 0.69] Total (95% Cl) 100.0% 0.67 [0.50,0.91] Heterogeneity: Tau=- 0.06; Chi=- 1 0.08, df- 3 (P- 0.02); l=-70% Test for overall effect: Z = 2.58 (P = 0.010) ar |
■ |
|||
|
■ |
||||
|
0.01 0'1 i 1 ti-PD1 antibodies * CT CT |
0 100 |
|||
Рисунок 21. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках < 1%.
Study or Subgroup log[Hazard Ratio]
Hazard Ratio IV, Fixed, 95% Cl
Hazard Ratio SE Weight IV, Fixed, 95% Cl
|
ESCORT-1 st (Camrelizumab_PC) -0.67334 0.176823 20.0% 0.51 [0.36, 0.72] JUPITER-06 (Toripalimab_PC) -0.43078 0.1 8243 18.8% 0.65 [0.45,0.93] KEYNOTE-590 (pembro_CF) -0.63488 0.129065 37.6% 0.53 [0.41,0.68] ORIENT-1 5 (sintilimab_CF_PC) -0.61619 0.163394 23.5% 0.54 [0.39, 0.74] Total (95% Cl) 100.0% 0.55 [0.47, 0.64] Heterogeneity: Chi=- 1.12, df- 3 (P- 0.77); l=-0% |
■ ■ ♦ |
|||
Test for overall effect: Z = 7.57 (P < 0.00001)
Anti-PD1 antibodies + CT CT
Рисунок 22. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках ≥ 10%.
|
Hazard Ratio Hazard Ratio |
|
|
Study or Subgroup |
log[Hazard Ratio] SE Weight IV, Random, 95% Cl IV, Random, 95% Cl |
|
ESCORT-1 st (Camrelizumab_PC) JUPITER-06 (Toripalimab_PC) KEYNOTE-590 (pembro_CF) ORIENT-15 (sintilimab_CF_PC) |
-0.52763 -0.57982 -0.2231 4 -0.57982 |
0.1 24706 0.1 64065 0.1 1 6387 0.1 22064 |
26.1 % 19.3% 27.9% 26.7% |
0.59 [0.46, 0.75] 0.56 [0.41, 0.77] 0.80 [0.64, 1.00] 0.56 [0.44, 0.71] |
■ |
|||
|
Total (95% Cl) Heterogeneity: Tau== 0.02; Chff = 5.93, df= Test for overall effect: Z = 5.11 (P « 0.00801) |
3 (P = 0.12); |
= = 49% |
100.0% |
0.63 [0.52, 0.75] |
♦ |
|||
|
0.01 Anti-PD1 |
antibodies * CT |
CT |
10 |
1Oo' |
||||
Рисунок 23. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 на опухолевых клетках < 10%.
ваниях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,75 (I2 = 0%). При этом выявлены значимые различия в ВБП в пользу ан-ти-PD1 антител (ОР 0,56, 95% ДИ 0,5–0,64; p < 0,001, рис. 20).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 на опухолевых клетках < 1 % доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, выявил наличие значимых различий в данной подгруппе пациентов — р = 0,02 (I2 = 70 %). При этом выявлены значимые различия в ВБП в пользу анти-PD1 антител (ОР 0,67, 95% ДИ 0,5–0,91; p = 0,01, рис. 21).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрес- сией PD-L1 на опухолевых клетках ≥ 10% доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,77 (I2 = 0 %). При этом выявлены значимые различия в ВБП в пользу анти-PD1 антител (ОР 0,55, 95% ДИ 0,47–0,64; p < 0,001, рис. 22).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 на опухолевых клетках менее 10% доступны были в 4 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал различия в данной подгруппе пациентов — р = 0,12 (I2 = 49%). При этом выявлены значимые различия в ВБП в пользу анти-PD1 антител (ОР 0,63, 95% ДИ 0,52–0,75; p < 0,001, рис. 23).
Hazard Ratio
Hazard Ratio
Study or Subgroup log[Hazard Ratio]SE Weight IV, Fixed, 95% Cl IV, Fixed, 95% Cl
JUPITER-06 (Toripalimab_PC) -0.54473 0.134077 37.3%
ORIENT-15 (sintilimab_CF_PC) -0.61619 0.103435 62.7%
0.58 [0.45, 0.75]
0.54 [0.44, 0.66]
Total (95% Cl)
Heterogeneity: ChP = 0.1 8, df= 1 (P = 0.67); l== 0%
Test for overall effect: Z= 7.20 (P < 0.00001)
100.0% 0.55(0.47,0.65]♦
I-------------------------------------------------------1---------------------------------------------------------------------------------------------------------------11
0.01 0.1 1 10100
anti-PD1 antibodies + CT CT
Рисунок 24. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1- антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 CPS ≥ 1%.
Hazard Ratio
Hazard Ratio
Study or Subgroup log [Haza rd Ratio]SE Weight IV, Fixed, 95% Cl
JUPITER-06 (Toripalimab_PC) -0.41552 0.297797 51.9% 0.66 [0.37,1.18]
ORIENT-1 5 (sintilimab_CF_PC) -0.27444 0.309613 48.1% 0.76 [0.41,1.39]
IV, Fixed, 95% Cl
Total (95% Cl)
Heterogeneity: Chi= = 0.11, df = 1 (P = 0.74); P = 0%
Test for overall effect: Z= 1.62 (P = 0.11)
100.0% 0.71 [0.46,1.08]♦
I-------------------------------------------------------1---------------------------------------------------------------------------------------------------------------11
0.01 0.1 1 10100
anti-PD1 antibodies + CT CT
Рисунок 25. Форест-график мета-анализа исследований, в которых проводилось сравнение ВБП: химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при экспрессии PD-L1 CPS < 1%.
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 CPS ≥ 1 % доступны были в 2 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие значимых различий в данной подгруппе пациентов — р = 0,67 (I2 = 0%). При этом выявлены значимые различия в ВБП в пользу анти-PD1 антител (ОР 0,55, 95% ДИ 0,47–0,65; p < 0,001, рис. 24).
Данные по эффективности комбинации иммунотерапии и химиотерапии в подгруппе пациентов с экспрессией PD-L1 CPS менее 1 % доступны были в 2 исследованиях. Тест на однородность результатов исследований, включенных в мета-анализ, показал отсутствие различий в данной подгруппе пациентов — р = 0,74 (I2 = 0 %). При этом не выявлены значимые различия в ВБП (ОР 0,71, 95% ДИ 0,46–1,08; p = 0,11, рис. 25).
Достоверный выигрыш в отношении ВБП в группе иммунотерапии и химиотерапии отмечался вне зависимости от пола пациента: мужской ОР 0,57, 95% ДИ 0,52– 0,63 и женский ОР 0,72, 95% ДИ 0,55–0,94 (рис. 13, 14 приложения), возраста младше или старше 65 лет: ОР 0,62, 95% ДИ 0,55–0,7 и ОР 0,56, 95% ДИ 0,48–0,66 соответственно (рис. 15, 16 приложения), принадлежности к азиатской или неазиатской этнической группе: ОР 0,57, 95% ДИ 0,52–0,63 и ОР 0,7, 95% ДИ 0,56–0,88 соответственно (рис. 17 приложения), функционального статуса по шкале ECOG 0 или 1: ОР 0,56, 95% ДИ 0,47–0,67 и ОР 0,61, 95% ДИ 0,54–0,68 соответственно (рис. 18, 19 приложения), локорегионарного или отдаленного метастазирования: ОР 0,62, 95% ДИ 0,46–0,83 и ОР 0,55, 95% ДИ 0,48–0,62 соответственно (рис. 20, 21 приложения), наличия или отсутствия метастазов в печени: ОР 0,61, 95% ДИ 0,46–0,79 и ОР 0,55, 95% ДИ 0,47–0,64 соответственно
(рис. 22, 23 приложения), режима химиотерапии — циспла-тина/фторурацила и паклитаксела/цисплатина: ОР 0,71, 95% ДИ 0,62–0,81 и ОР 0,56, 95% ДИ 0,5–0,63 соответственно (рис. 24, 25 приложения).
Сводные результаты мета-анализа факторов в отношении ВБП представлены в табл. 3 (в приложении).
Частота объективных ответов
Также нами было проведено сравнение частоты объективных ответов на фоне различных вариантов терапии. Общее число включенных пациентов составило 1901 в группе комбинации и 1910 — в группе химиотерапии. Добавление анти-PD1 антител к химиотерапии значимо, практически в 2 раза, повышает шанс достижения объективного эффекта (значимые различия в однородности исследований отсутствуют — р = 0,5, (I2 = 0%); ОШ 2,12, 95% ДИ 1,85–2,42; p < 0,001; 6 исследований, рис. 26a). Аналогичные результаты были получены и в группе плоскоклеточного гистотипа (рис. 26b).
Токсичность лечения
Нами было проведено сравнение частоты нежелательных явлений на фоне различных вариантов терапии. Добавление анти-PD1 антител к химиотерапии незначимо повышало шанс развития нежелательных явлений 3–4 степени (имеются различия в однородности исследований– р = 0,19, (I2 = 33%); ОШ 1,15, 95% ДИ 0,98–1,36; p = 0,1; 6 исследований, рис. 27a). Аналогичные результаты были получены и в группе плоскоклеточного гистотипа (рис. 27b).
Добавление анти-PD1 антител к химиотерапии значимо повышало шанс развития серьезных нежелательных явлений (отсутствуют различия в однородности иссле-дований– р = 0,81, (I2 = 0 %); ОШ 1,43, 95% ДИ 1,18–1,73; p < 0,001; 5 исследований, рис. 28).
|
anti-PD antibodies Study or Subgroup Events |
+ CT Total |
CT Events |
Total |
Weight |
Odds Ratio M-H, Fixed, 95% Cl |
Odds Ratio M-H, Fixed, 95% Cl |
|
|
Checkmate 648 (nivo_CF) 151 |
321 |
87 |
324 |
15.3% |
2.42 [1.74, 3.36] |
||
|
ESCORT-1 st (Camrelizumab_PC) 215 |
298 |
1 85 |
298 |
17.2% |
1.58 [1.12, 2.23] |
—■— |
|
|
JUPITER-06 (Toripalimab_PC) 178 |
25? |
1 34 |
257 |
13.7% |
2.07 [1.44, 2.97] |
■ |
|
|
KEYNOTE-590 (pembro_CF) 168 |
372 |
110 |
376 |
20.0% |
1.99 [1.47, 2.69] |
||
|
ORIENT-15 (sintilimab_CF_PC) 216 |
327 |
1 51 |
332 |
1 7.0% |
2.33 [1.70, 3.20] |
||
|
RATIONALE-306 (tislelizumab_CF_PC) 207 |
326 |
1 37 |
323 |
16.8% |
2.36 [1.72, 3.24] |
||
|
Total (95% Cl) Total events 1135 Heterogeneity: Chi= = 4.37, df= 5 (P = 0.50); F = 0% |
1901 |
884 |
1910 |
100.0% |
2.12 [1.85, 2.42] |
* |
|
|
0.01 |
OJ CT |
10 too1 anti-PD antibodies + CT |
|||||
|
Test for overall effect: Z = 11.06 (P = 0.00001) |
|||||||
Рисунок 26a. Форест-график мета-анализа исследований, в которых проводилось сравнение шанса достижения объективного эффекта при применении химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT).
|
anti-PD antibodies Study or Subgroup Events |
+ CT Total |
CT Events |
Total |
Weight |
Odds Ratio M-H, Fixed, 95% Cl |
Odds Ratio M-H, Fixed, 95% Cl |
|
|
Checkmate 648 (nivo_CF) 151 |
321 |
87 |
324 |
19.1% |
2.42 [1.74, 3.36] |
-■— |
|
|
ESCORT-1 st (Camrelizumab_PC) 215 |
298 |
1 85 |
298 |
21.5% |
1.58 [1.12, 2.23] |
■ |
|
|
JUPITER-06 (Toripalimab_PC) 178 |
25? |
1 34 |
257 |
17.2% |
2.07 [1.44, 2.97] |
■ |
|
|
KEYNOTE-590 (pembro_CF) 168 |
372 |
110 |
376 |
0.0% |
1.99 [1.47, 2.69] |
||
|
ORIENT-15 (sintilimab_CF_PC) 216 |
327 |
1 51 |
332 |
21.2% |
2.33 [1.70, 3.20] |
||
|
RATIONALE-306 (tislelizumab_CF_PC) 207 |
326 |
1 37 |
323 |
21.0% |
2.36 [1.72, 3.24] |
||
|
Total (95% Cl) Total events 967 Heterogeneity: ChP= 4.17, df= 4 (P = 0.38); F = 4% |
1529 |
694 |
1534 |
100.0% |
2.15 [1.85, 2.49] |
* |
|
|
0.01 |
OJ CT |
10 too1 anti-PD antibodies + CT |
|||||
|
Test for overall effect: Z = 10.12 (P = 0.00001) |
|||||||
Рисунок 26b. Форест-график мета-анализа исследований, в которых проводилось сравнение шанса достижения объективного эффекта при применении химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT) при плоскоклеточном раке.
|
Study or Subgroup |
Anti-PDI antibodies * CT |
CT Events |
Total |
Weight |
Odds Ratio M-H, Random, 95% Cl |
Odds Ratio M-H, Random, 95% Cl |
||
|
Events |
Total |
|||||||
|
Checkmate 648 (nivo_CF) |
151 |
321 |
117 |
324 |
17.8% |
1.57 [1.15, 2.15] |
■ |
|
|
ESCORT-1 st (Camrelizumab_PC) |
189 |
298 |
201 |
298 |
16.2% |
0.84 [0.60,1.17] |
||
|
J U PITER- 0 6 (To ripa Ii m a b_P C) |
188 |
25? |
1 80 |
257 |
13.6% |
1.1? [0.79,1.71] |
||
|
KE YN OTE- 5 9 0 (p e m b ro_C F) |
266 |
373 |
252 |
376 |
18.1 % |
1.22 [0.90,1.67] |
||
|
ORIENT-15 (sintilimab_CF_PC) |
222 |
327 |
219 |
332 |
17.1% |
1.09 [0.79,1.51] |
||
|
RATI 0 N ALE- 3 0 6 (ti s I e I Izu m a b_C F_P C) |
217 |
326 |
208 |
323 |
17.2% |
1.1 0 [0.80,1.52] |
||
|
Total (95% Cl) Total events Heterogeneity’: Tau= = 0.01; Chi== 7.49, df |
1233 = 5 (P = 0.19); l= = 33% |
1902 |
11 77 |
1910 |
100.0% |
1.15 [0.98,1.36] |
I |
|
|
0.01 |
o!i CT |
10 1 oo' Anti-PD1 antibodies + CT |
||||||
|
Test for overall effect: Z= 1.66 (P = 0.10) |
||||||||
Рисунок 27a. Форест-график мета-анализа исследований, в которых проводилось сравнение шанса развития нежелательных явлений 3–4 степени при применении химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT).
|
Ant Study or Subgroup |
-PD1 antibodies* CT |
CT Events |
Total |
Weight |
Odds Ratio M-H, Fixed, 95% Cl |
Odds Ratio M-H, Fixed, 95% Cl |
||
|
Events |
Total |
|||||||
|
Checkmate 648 (nivo_CF) |
29 |
321 |
16 |
324 |
6.6% |
1.91 [1.02, 3.59] |
||
|
ESCORT-1 st (Camrelizumab_PC) |
90 |
298 |
69 |
297 |
22.1% |
1.43 [0.99, 2.06] |
||
|
J U PITER- 0 6 (T о r i p a I i rn a b_ P C) |
93 |
257 |
75 |
257 |
21.9% |
1.38 [0.95,1.99] |
||
|
ORIENT-15 (Sintilimab_CF_PC) |
124 |
327 |
103 |
332 |
29.1% |
1.36 [0.98,1.87] |
||
|
RATIONALE-306 (tislelizumab_CF_PC) |
94 |
326 |
62 |
323 |
20.3% |
1.71 [1.18,2.46] |
||
|
Total (95% Cl) |
1529 |
1533 |
100.0% |
1.49 [1.25,1.76] |
♦ |
|||
|
Total events |
438 |
325 |
||||||
|
Heterogeneity: Chi== 1.66, df= 4 (P = 0.80); l= = |
0% |
ooi— |
---ГМ--------- |
------L-----H |
||||
|
Test for overall effect: Z = 4.55 (P < 0.00001) |
CT |
Anti-PD1 antibodies * CT |
||||||
Рисунок 28. Форест-график мета-анализа исследований, в которых проводилось сравнение шанса развития серьезных нежелательных явлений при применении химиотерапии (CT) или комбинации химиотерапии и анти-PD1 антител (Anti-PD1 antibodies + CT).
ОБСУЖДЕНИЕ ПОЛУЧЕННЫХ РЕЗУЛЬТАТОВ
Долгие годы лечение распространенного плоскоклеточного рака пищевода ограничивалось лишь одной химиотерапией на основе препаратов платины, фторурацила и таксанов, и лишь появление анти-PD1 моноклональных антител позволило сделать значимый прогресс. В 5 рандомизированных исследованиях сравнивалась эффективность и безопасность добавления анти-PD1 антител к химиотерапии первой линии у пациентов преимущественно с плоскоклеточным раком пищевода. В них были достигнуты достаточно однородные результаты — улучшение ОВ (все исследования), ВБП (5 исследований из 6) и частоты ОО (все исследования). [6,8,10–12,14] Выигрыш в отношении ОВ и ВБП достигался практически во всех подгруппах больных вне зависимости от возраста, пола, расы, распространенности опухолевого процесса, статуса по шкале ECOG.
Тем не менее, у подавляющего числа пациентов в ближайший год развивается прогрессирование заболевания, а сама химио-иммунотерапия сопряжена с высокой стоимостью и большей токсичностью, что диктует необходимость выделения больных, имеющих наибольший шанс ответа на нее. Наиболее распространенным предиктором ответа является экспрессия PD-L1, определяемая на опухолевых клетках (TPS) или на опухолевых клетках и микроокружении (CPS). В данном мета-анализе было показано, что выигрыш в отношении ОВ от добавления иммунотерапии был схож вне зависимости от экспрессии PD-L1, ОР варьировало от 0,58 до 0,83. Данные результаты об отсутствии предиктивной роли экспрессии PD-L1 не совпадают со схожими по дизайну исследованиями, проведенными при других плоскоклеточных раках. Так, в исследованиях KEYNOTE-826 (рак шейки матки) и KEYNOTE-048 (опухоли головы и шеи) добавление пембролизумаба к химиотерапии первой линии увеличивало продолжительность жизни пациентов только при экспрессии PD-L1 CPS ≥ 1 [3,5]. Интересно, что именно для пембролизумаба при раке пищевода (исследование Keynote-590) также прослеживалась тенденция к выигрышу у пациентов с высокой экспрессией PD-L1 (CPS ≥ 10 ОР 0,64 против CPS < 10 ОР 0,84). Может ли это быть связано с особенностями тестирования PD-L1? Вряд ли, так как во всех исследованиях мы видим схожую частоту выявления различной экспрессии PD-L1 как на опухолевых клетках, так и на микроокружении. Кроме того, в исследованиях ORIENT-15 и Keynote-590 использовался одинаковый диагностический клон 22C3, несмотря на это предиктивное значение экспрессии в первом исследовании не удалось продемонстрировать.
Другим возможным объяснением различий между исследованиями мог стать химиотерапевтический партнер для антитела. В исследованиях KEYNOTE-590 и CheckMate-648 все пациенты получали стандартную для стран Запада комбинацию цисплатина и фторурацила, тогда как для исследований из Азии допускалось применение более удобного режима паклитаксел плюс цисплатин. Несмотря на раз- личие в режимах, улучшение ОВ от добавления иммунотерапии было практически идентичным в обеих группах химиотерапии.
Другим потенциальным предиктивным фактором чувствительности опухоли к иммунотерапии является факт курения табака. Как и при немелкоклеточном раке легкого (НМРЛ), для плоскоклеточного рака пищевода курение является одним из наиболее важных факторов риска его развития. Мета-анализ исследований по иммунотерапии при НМРЛ показал, что достоверный выигрыш в отношении ОВ от ее добавления отмечался только у бывших или настоящих курильщиков [7]. В нашем мета-анализе были получены схожие данные: достоверное улучшение ОВ отмечалось лишь у курильщиков (ОР 0,7, 95% ДИ 0,61–0,8) в отличие от некурильщиков (ОР 0,86, 95% ДИ 0,67–1,1). Влиянием курения на эффективность иммунотерапии при плоскоклеточном раке пищевода можно объяснить и несколько меньшую чувствительность к ней женщин (ОР в отношении ОВ 0,79, 95% ДИ 0,6–1,05) по сравнению с мужчинами (ОР 0,67, 95% ДИ 0,6–0,74), что обычно объясняется большей долей курильщиков среди последних. К сожалению, из данных опубликованных исследований, включенных в мета-анализ, невозможно провести анализ взаимосвязи курения с другими прогностическими и предиктивными факторами.
Очевидно, что необходим поиск новых маркеров, позволяющих отбирать кандидатов для проведения иммунотерапии при плоскоклеточном раке пищевода. Перспективным направлением видится идентификация специфических экспрессионных профилей опухоли [4,13].
Ограничением этого мета-анализа является невозможность включения в него индивидуальных данных пациентов и отсутствие в оригинальных публикациях поданализов в зависимости от различных границ экспрессии PD-L1.
ЗАКЛЮЧЕНИЕ
В проведенном мета-анализе 6 рандомизированных исследований мы продемонстрировали, что добавление анти-PD1 антител к химиотерапии в первой линии достоверно увеличивает показатели ОВ, ВБП и частоту ОО у пациентов с плоскоклеточным раком пищевода. Имеющиеся данные не позволяют уверенно выделить подгруппу пациентов с наибольшим выигрышем от применения химио-иммунотерапии, что диктует необходимость поиска новых маркеров.
Список литературы Мета-анализ исследований эффективности добавления анти-PD1 антител к химиотерапии первой линии распространённого рака пищевода
- А.Д. Каприн, В.В. Старинский, А.О. Шахзадова Состояние онкологической помощи населению России в 2020 году [Электронный ресурс]. URL: https://oncology-association.ru/wp-content/uploads/2021/10/pomoshh-2020-el.-versiya.pdf.
- Bleiberg H. [и др.]. Randomised phase II study of cisplatin and 5-fluorouracil (5-FU) versus cisplatin alone in advanced squamous cell oesophageal cancer // European journal of cancer (Oxford, England : 1990). 1997. № 8 (33). C. 1216-1220.
- Burtness B. [и др.]. Pembrolizumab Alone or With Chemotherapy for Recurrent / Metastatic Head and Neck Squamous Cell Carcinoma in KEYN0TE-048 : Subgroup Analysis by Programmed Death Ligand-1 Combined Positive Score // Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2022. № 21 (40). C.
- Chen Y. P. [m gp.]. Identification and validation of novel microenvironment-based immune molecular subgroups of head and neck squamous cell carcinoma : implications for immunotherapy. // Annals of Oncology : Official Journal of the European Society for Medical Oncology. 2019. № 1 (30). C. 68-75.
- Colombo N. [m gp.]. Pembrolizumab for Persistent, Recurrent, or Metastatic Cervical Cancer // The New England journal of medicine. 2021. № 20 (385). C. 1856-1867.
- Doki Y. [m gp.]. Nivolumab Combination Therapy in Advanced Esophageal Squamous-Cell Carcinoma // The New England journal of medicine. 2022. № 5 (386). C. 449-462.
- Kim J. H., Kim H. S., Kim B. J. Prognostic value of smoking status in non-small-cell lung cancer patients treated with immune checkpoint inhibitors : a meta-analysis // Oncotarget. 2017. № 54 (8). C. 93149-93155.
- Lu Z. [и др.]. Sintilimab versus placebo in combination with chemotherapy as first line treatment for locally advanced or metastatic oesophageal squamous cell carcinoma (ORIENT-15) : multicentre, randomised, double blind, phase 3 trial // BMJ (Clinical research ed.). 2022. (377).
- Lu Z. [и др.]. Paclitaxel and cisplatin with or without cetuximab in metastatic esophageal squamous cell carcinoma : a randomized, multicenter phase II trial // The Innovation. 2022. № 3 (3). C. 100239.
- Luo H. [и др.]. Effect of Camrelizumab vs Placebo Added to Chemotherapy on Survival and Progression-Free Survival in Patients With Advanced or Metastatic Esophageal Squamous Cell Carcinoma : The ESCORT-1st Randomized Clinical Trial // JAMA. 2021. № 10 (326). C. 916.
- Sun J. M. [и др.]. Pembrolizumab plus chemotherapy versus chemotherapy alone for first-line treatment of advanced oesophageal cancer (KEYN0TE-590) : a randomised, placebo-controlled, phase 3 study // Lancet (London, England). 2021. № 10302 (398). C. 759-771.
- Wang Z. X. [и др.]. Toripalimab plus chemotherapy in treatment-naive, advanced esophageal squamous cell carcinoma (JUPITER-06) : A multi-center phase 3 trial // Cancer cell. 2022. № 3 (40). C. 277-288.e3.
- Xu J. [и др.]. 79 Tumor-immune signatures associated with response or resistance to tislelizumab (Anti-PD-1) in esophageal squamous cell carcinoma (ESCC) // Journal for ImmunoTherapy of Cancer. 2020. № Suppl 3 (8). C. A49.1-A49.
- Yoon H. [и др.]. RATI0NALE-306 : Randomized, global, placebo-controlled, double-blind phase 3 study of tislelizumab plus chemotherapy versus chemotherapy as first-line treatment for advanced or metastatic esophageal squamous cell carcinoma (ESCC) 2022.
- Global Cancer Observatory [Электронный ресурс]. URL: https://gco.iarc.fr/ (дата обращения : 05.11.2022).
- Investigation of PD-L1 expression and tislelizumab efficacy in gastroesophageal adenocarcinoma using a novel tumor and immune cell score with VENTA... | OncologyPRO [Электронный ресурс]. URL : https : // oncologypro.esmo. org / meeting-resources / esmo-virtual-congress-2020 / investigation-of-pd-l1-expression-and-tislelizumab-effica-cy-in-gastroesophageal-adenocarcinoma-using-a-novel-tumor-and-immune-cell-score-with-venta.


