Метод анализа динамических изображений нефросцинтиграфии
Автор: Гайдель Андрей Викторович, Капишников Александр Викторович, Пышкина Юлия Сергеевна, Колсанов Александр Владимирович, Храмов Александр Григорьевич
Журнал: Компьютерная оптика @computer-optics
Рубрика: Обработка изображений, распознавание образов
Статья в выпуске: 4 т.42, 2018 года.
Бесплатный доступ
Предложен метод автоматической обработки динамических нефросцинтиграмм, основанный на приближении кривой ренограммы экспоненциальной функцией. Метод позволяет получить объективные параметры состояния почек. Работа метода изучена на наборе радионуклидных изображений ренотрансплантата. Представлены результаты клинических исследований, подтверждающие диагностическую эффективность разработанного подхода. Анализ кинетики нефротропного индикатора обеспечивает точную оценку функционального состояния пересаженной почки. Выявлено два числовых параметра, показывающих более высокую диагностическую эффективность при их вычислении по построенной модели, чем при их вычислении по исходной ренограмме.
Обработка изображений, распознавание образов, сцинтиграфия, нефрология, трансплантация
Короткий адрес: https://sciup.org/140238430
IDR: 140238430 | DOI: 10.18287/2412-6179-2018-42-4-688-694
Method of nephroscintigraphic dynamic images analysis
We propose a method for automatic processing of dynamic nephroscintigrams based on fitting the renogram curve by an exponential function. The method makes it possible to obtain objective parameters of the kidney condition. The performance of the method is studied on a set of radionuclide images of a transplant. Results of clinical studies confirming the diagnostic efficiency of the developed approach are presented. Analysis of the kinetics of the nephrotropic indicator provides an accurate assessment of the functional status of the transplanted kidney. Two numerical parameters are revealed that offer a higher diagnostic efficiency when calculated from the constructed model compared to when they are calculated from the original renogram.
Текст научной статьи Метод анализа динамических изображений нефросцинтиграфии
Диагностика состояния пересаженной почки – одна из основных задач ведения пациентов в посттрансплантационном периоде [1, 2]. Неинвазивным способом изучения функции и морфологии органов человека является радионуклидный метод [3], развитие которого тесно связано с совершенствованием методов компьютерной обработки изображений [4].
Динамическая сцинтиграфия почек (реносцинти-графия) – метод радионуклидной визуализации, заключающийся в получении на гамма-камере серии изображений после введения меченого нефротропно-го индикатора (радиофармпрепарата, РФП) [3]. Меченый нефротропный индикатор – это разрешенное для введения человеку с диагностической целью химическое соединение, тропное к тканям почки, в молекуле которого содержится радионуклид. Диагностическое значение имеют изменения топографии и формы почки, характер накопления и выведения индикатора (рис. 1). Объективное суждение о функции органа основывается на количественной оценке динамики яркости радионуклидного изображения, отражающей трансфер меченого индикатора в различных зонах интереса нефросцинтиграмм. Нефросцин-тиграмма – это изображение почек пациента, полученное посредством регистрации на гамма-камере излучения, испускаемого инкорпорированным радионуклидом.
Решающее значение для определения тактики ведения реципиента имеет получение объективной инструментальной информации о формировании патологии ренотрансплантата, что определяет актуальность совершенствования информационных технологий для анализа динамической сцинтиграфии почек [5, 6].
Время, мин.
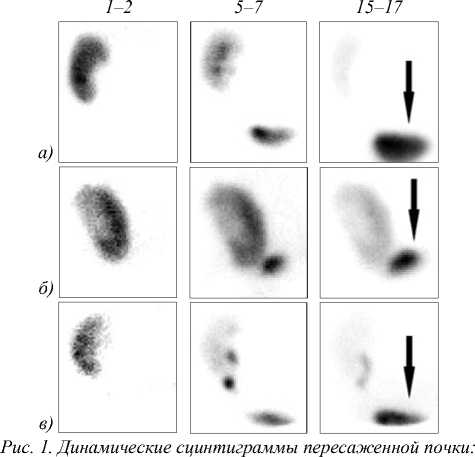
норма (a); замедленное накопление и выведение индикатора из паренхимы (б) и полостной системы почки (в).
Стрелка – РФП, поступивший в мочевой пузырь
Популярным подходом для анализа ренограмм является деконволюционный метод. Он применяется при анализе ренограмм для получения импульсной характеристики функции паренхимы почки и вычисления паренхиматозного транзитного времени, а также для определения скорости клубочковой фильтрации [7]. Принцип деконволюции (deconvolution – обратная свёртка) состоит в определении функции задержки РФП почкой при введении (фаза секреции) и выведении (экскреция) индикатора при динамической нефросцинтиграфии [8]. Указанный метод применим для анализа кинетики клубочковых или канальцевых радиофармпрепаратов при условии формирования компактного болюса РФП [7].
Преимуществом деконволюционного анализа является возможность получения следующих объективных параметров динамической реносцинтиграфии: среднее транзитное время; эффективный почечный отток; относительное и абсолютное почечное поглощение; начальное накопление; время максимальной активности ( T max ); активность на 20-й минуте – индекс ретенции ( T 20 ); T 80 – время, когда максимальное значение кривой уменьшается на 20% [9, 10] и более точная коррекция фоновой активности [7]. Применение деконволюционного метода возможно посредством различных математических моделей: матричного метода, преобразующего метода и метода, основанного на дифференциации участка Ратленд – Патлака. Для оценивания их параметров используют преобразование Лапласа, матричный метод, модификацию Фурье, метод наименьших квадратов (МНК) [11] и метод Карлсена.
Ранее для диагностики нефрологических патологий исследовались текстурные признаки изображений, полученных при ультразвуковых исследованиях [12]. Для распознавания нефросцинтиграмм использовались яркостные и геометрические признаки [13]. Однако такие подходы не учитывают динамику изменений этих изображений во времени.
Цель работы – разработка метода анализа динамической сцинтиграфии почек и оценка его диагностической информативности при распознавании постре-нотрансплантационных осложнений.
1. Признаки, основанные на модели ренограммы
Исходные динамические нефросцинтиграммы представляют собой трёхмерные цифровые изображения ю ( m , n , к ): D m x Z ^ Q , где D юс Z 2 - множество отсчётов изображения, Q = [0; Q -1] n Z - множество уровней яркости, соответствующих уровням активности РФП, Q – количество уровней яркости, Z – множество целых чисел, а третья координата k отвечает за время. На этих кадрах медицинским специалистом вручную выделяется три области: D 1 ( k ) с D ю - весь ренотрансплантат, D2(к ) с D 1 ( к ) - область паренхимы, D Z с D и - небольшой участок фона. Области D 1 и D 2 исследуются отдельно, из всего изображения вычитается средний уровень фона, так что вместо изображений и ( m , n , к ) рассматриваются изображения
и(m, n,к) = ю(m, n,к) — ]—^ ю(m, n,к), (1) DZI (m,n )еDZ где |A| означает количество элементов в конечном множестве A. Это правомерно, поскольку при лучевом исследовании на интенсивность излучения в конкретной точке влияет не только исследуемый орган, но и окружающие его ткани [3].
На практике изображения регистрируются в секреторной и экскреторной фазах с шагом дискретизации A t = 30 с. Секреторная фаза - фаза преимущественного накопления РФП в канальцах нефрона почки.
Экскреторная фаза – фаза, обусловленная выведением РФП из почки [14]. Начальный участок сосудистой фазы продолжительностью T 0 =40 с не учитывается при оценивании параметров [15].
Отсчёты ренограммы ук ( к е [0; N -1] n Z ) получаются усреднением отсчётов изображений (1) в заданной области D j ( j = 1 или j =2) [3]:
У к = 1 Е ю ( m , n , к ) . (2)
D j ( к ) ( m , n ) е D j ( к )
Для анализа ренограммы (2) строится экспоненциальная модель y ( t ) = A exp (-a( t - tmax )) + B’ t eE tmax; tstop J " (3)
Такая модель выбрана, поскольку на практике участок кривой ренограммы, соответствующий фазе выведения РФП из области паренхимы, действительно убывает экспоненциально [9].
Параметр B – это постоянная составляющая, соответствующая фоновому значению на наблюдаемом участке ренограммы, ( t stop – t max ) – продолжительность секреторной фазы, момент времени t max – момент времени максимального накопления РФП, A – амплитуда сигнала, a - затухание.
На рис. 2 пунктирной линией изображён пример реальной ренограммы, полученной по формуле (2), а сплошной линией – построенная модель (3) для неё. Также отмечены время максимального накопления t max и значение параметра B .
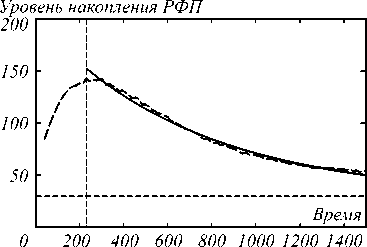
Рис. 2. Реконструированная ренограмма на основе разработанной математической модели
Алгоритм оценивания параметров модели включает следующие этапы. Предварительное сглаживание для устранения шумовых выбросов производится по семи точкам с помощью интерполяционного многочлена третьей степени. Уточнённое значение у’ получается по соседним значениям y i + k по формуле
У к = 21 ( 7 y i + 6 ( y i + 1 + y i - 1 ) + 3 ( y i + 2 + y i - 2 ) -- 2 ( y i + 3 + y i - 3 ) ) , i e [ 3; N - 4 ] n Z .
Граничные отсчёты обрабатываются отдельно:
y 0 =
39 y о + 8 y 1 - 4( y 2 + y з - y 4 ) + y 6 - 2 y 6
y ‘ =
8 y 0 + 19 y 1 + 16 y 2 + 6 y 3 - 4 y 4 - 7 y 6 + 4 y 6 .
- 4 y о + 16 y + 19 y 2 + 12 y з + 2 y 4 - 4 y 6 + y 6 ;
у N - 3 = 42 ( y N - 7 - 4 y N - 6 + 2 y N - 5 + 12 y N - 4 + 19 y N - 3 + + 16 y N - 2 - 4 y N - 1 ) ;
y N - 2 = — ( 4 y N - 7 - 7 y N - 6 - 4 y N - 5 + 6 y N - 4 + 16 y N - 3 + 42
+ 19 y N - 2 + 8 y N - 1 ) ;
y N - 1 = —( - 2 N - 7 + y N - 6 + 4 y N - 5 - 4 y N - 4 - 4 y N - 3 + 42
+ 8 y N - 2 + 39 y N - 1 ) .
Предварительно найденный максимум ренограм-мы i max уточняется с использованием МНК [11] при аппроксимации параболой y ( k ) = ak 2 + bk + c в окрестности ± M точек предварительно найденного максимума. Параметры a , b и c находятся из системы уравнений
M a £ k2 k=-M
M
+ £ 1
k =- M
M b £ k2 k=-M
M M a £ k4 + c £ k2
k =- M k =- M
M
= £ y,+k, k=-M
M
= £ kyi+k , k=-M
M
= £ k2 yi+k , k=-M после чего находится уточнённая точка максимального накопления РФП imax = imax - b / (2a).
На рис. 3 вертикальными пунктирными линиями отмечены время максимального накопления РФП по ренограмме и по параболе, аппроксимирующей точки ренограммы, соседствующие с точкой максимума. Сплошной линией изображена сама аппроксимирующая парабола.
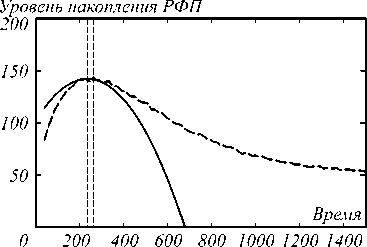
Рис. 3. Уточнение максимума ренограммы путём аппроксимации параболой
Непосредственно применение метода наименьших квадратов для аппроксимации отсчётов ренограммы (2) экспоненциальной кривой (3) приводит к вычислительно сложной и, возможно, неоднозначной нели- нейной задаче с тремя неизвестными: istop 2
J1 = £ A exp |-a( k - imax )A)+ В - yk ^ min. , C \ v v ' Z / A, B ,а k =i max
Если считать параметр B заданным, то решается линейная задача в логарифмическом пространстве, то есть параметры A и а находятся из соображений минимизации логарифмического показателя качества istop 2
J 2 = £ ( A-а( k - imax )A t - Zk ) ^ min, k- C v A,“
Л = max
где A = In A , z k = ln ( y k - B ) .
Система линейных уравнений для оценивания параметров A и а имеет вид is top is top is top
A £ 1 -а £ k = £ Zk, k = i max k=i max k = imax is top is top is top
A £ k -а £ k 2 = £ kz k . k = i max k = i max k = i max
Так как значение параметра B не известно, можно найти минимальное значение критерия (5), подбирая параметр B на отрезке
0; ˆ min yk kel imax; is top I^Z например, с помощью одной из модификаций метода Ньютона, и на каждом шаге заново решая линейную задачу (5).
Другой подход к вычислению параметра B может быть применён, если значения (2) не сильно зашумлены или предварительно сглажены. Выбрав три не слишком близкие значения аргумента k0, k1 = k0 – K и k2 = ko+K из диапазона l imax;istop ЮZ, можно полу- чить систему ykо - B = A exP(-аk0),
1 y k , - B = A exp ( -а k 1 ) , [ y k 2 - B = A exp ( -а k 2 ) ;
или
J y k 1 - B = ( y k 0 - B ) exp ( +а K ) , [ y k 2 - B = ( y k 0 - B ) exp ( -а К ) .
Перемножение двух уравнений последней системы приводит к уравнению
(yk! - B)(yk2 - B) = (yk0 - B)2, откуда выражается параметр B:
yk 0 - Kyk 0 + K yk 0
B =--------------------- .
y k 0 - К + y k 0 + К - 2 y k 0
Целесообразно
выбрать, например,
k0 = (imax + istop ) / 2 , K = (istop imax ) / 4 . Полученное значение параметра B используется непосредственно при решении задачи (5) или в качестве начального приближения для процедуры итерационного уточнения, описанной выше.
Требуемые диагностические параметры находятся по формулам:
- среднее транзитное время MTT = 1/ а [с];
– период полувыведения
1 A - B T 1/2 = —in [с];
а 2 A
включающей весь ренотрансплантат (рис. 6 б ); Т 80 зоны, включающей весь ренотрансплантат; б) при хронической трансплантационной нефропатии существенно удлиняется T max зоны интереса, включающей весь ренотрансплантат; снижается Т 20 паренхиматозной зоны.
– время максимального накопления РФП
т -Т
T max = To + t max
[с].
2. Результаты клинического использования разработанных методов анализа сцинтиграмм
Проверка разработанного метода анализа динамических радионуклидных изображений выполнена на наборе реносцинтиграмм (размер матрицы 128×128). Радионуклидное исследование пересаженных почек выполнялось на планарной гамма-камере с 99mTc «Технемаг». Ренограммы были получены и прошли предварительную обработку с помощью программного пакета GoldRada.
Выполнена постпроцессинговая обработка результатов 192 динамических сцинтиграфий, каждая из которых представляла собой серию из 40 изображений пересаженных почек пациентов Самарского центра трансплантации органов и тканей клиник Самарского государственного медицинского университета (рис. 4, 5). Количественный анализ данных динамических сцинти-грамм проведен квалифицированными врачами-радиологами, при этом определялись и оценивались амплитудно-временные характеристики ренографических кривых с зон интереса пересаженного органа.
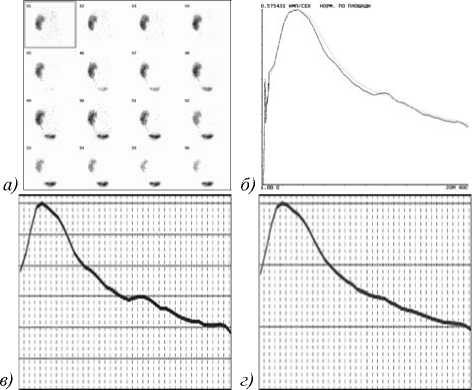
Рис. 4. Исходная сцинтиграмма ренотрансплантата с нормальной гистологической картиной (a и б) и сглаженная с помощью формулы (4) ренограмма: только для области паренхимы (в), для всего ренотрансплантата (г)
Сцинтиграфическая семиотика нарушения функции почечного трансплантата (ПТ) имеет следующие особенности: а) при остром отторжении почечного трансплантата характерно значительное увеличение: T max, времени полувыведения РФП ( Т 1/2), Т 80 паренхиматозной зоны; T max, Т 1/2 (рис. 6 а ), Т80 медуллярной (средней) зоны (СПТ); Т 20 медуллярной зоны и зоны,
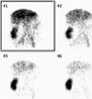

* *
а)
в)
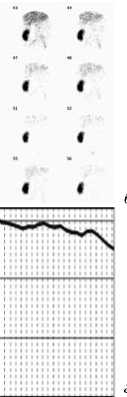
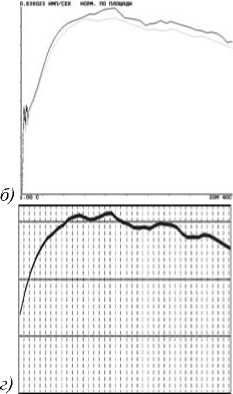
Рис. 5. Исходная сцинтиграмма при остром отторжении ренотрансплантата (a и б) и сглаженная с помощью формулы (4) ренограмма: только для области паренхимы (в), для всего ренотрансплантата (г)

Анализ диагностической эффективности радионуклидных параметров выявил, что площадь под характеристической кривой (AUROC) времени максимального накопления РФП всего почечного трансплантата при остром отторжении составила 0,96±0,001; при хронической нефропатии ПТ – AUROC=0,95±0,002 (рис. 7).
Tш средней зоны 4000 3500 3000 2500 2000 1500 1000 500
О
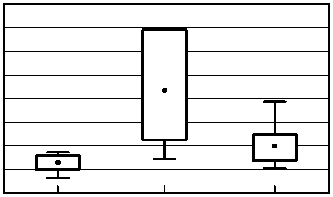
норма острое хроническая отторжение нефропатия
а)
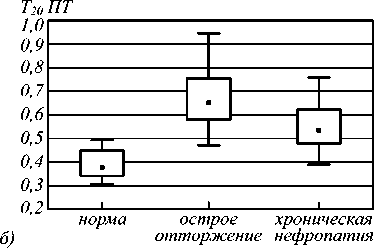
Рис. 6. Параметры динамической реносцинтиграфии у реципиентов в постренотрансплантационном периоде: T1/2 СПТ (а); Т20 ПТ (б). Уровень доверия для доверительных интервалов: 0,95 (* p < 0,05)
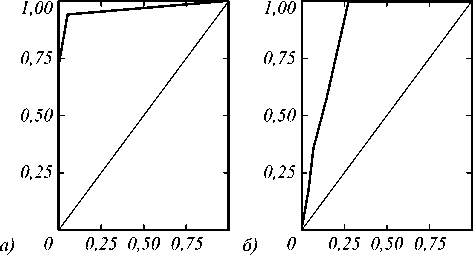
Рис. 7. Характеристические кривые Tmax ренотрансплантата при выявлении острого отторжения (а) и хронической трансплантационной нефропатии (б) ренотрансплантата у реципиентов Комбинированное использование предложенных показателей повысило диагностическую информативность радионуклидного метода. Так, например, при выявлении острого отторжения ренотрансплантата площадь под ROC-кривой Т max для области паренхимы с 0,86±0,006 повысилась до 0,93±0,002; Т max для всего ренотрансплантата с 0,82±0,006 повысилась до 0,96±0,001; Т 1/2 для области паренхимы с 0,84±0,002 повысилась до 0,90±0,001. При выявлении ХТН площадь под ROC-кривой Т max для области паренхимы с 0,84±0,006 повысилась до 0,87±0,002; Т max для всего ре-нотрансплантата с 0,74±0,006 повысилась до 0,95±0,002; Т 1/2 для области паренхимы с 0,55±0,004 повысилась до 0,95±0,002. Значения операционных характеристик теста (чувствительности и специфичности) также повысились. Полученные данные свидетельствуют о возможности использования параметров предложенного метода при описании состояния пересаженной почки.
Заключение
Анализ кинетики нефротропного индикатора способствует определению функционального состояния пересаженной почки. Применение разработанного метода обеспечивает надёжный количественный анализ трансфера РФП при радионуклидном исследовании ренотрансплантата. Включение радионуклидной визуализации в план обследования реципиентов позволяет оптимизировать применение биопсии почечного трансплантата путем использования параметров предложенного анализа реносцинтиграмм в качестве тестов-идентификаторов или теста дискриминаторов в зависимости от этапа мониторинга пациента.
Параметры, вычисленные по предложенной экспоненциальной модели участка ренограммы, позволяют эффективно описывать поведение ренотрансплантата и прогнозировать его состояние. В особенности это касается уточнённого времени максимального накопления РФП и времени полувыведения РФП, вычисленных по области паренхимы почечного ренотрансплантата. Для подтверждения этого заключения требуется провести более масштабное клиническое исследование.
Работа выполнена при поддержке гранта РФФИ № 16-41-630761 р_а, а также Министерства науки и высшего образования в рамках выполнения работ по Государственному заданию ФНИЦ «Кристаллография и фотоника» РАН (соглашение № 007-ГЗ/Ч3363/26).
Список литературы Метод анализа динамических изображений нефросцинтиграфии
- Столяревич, Е.С. Морфологические особенности позднего отторжения трансплантированной почки и их влияние на течение и прогноз нефропатии/Е.С. Столяревич, Л.Ю. Артюхина, И.Г. Ким, Л.Г. Куренкова, Н.А. Томилина//Нефрология и диализ. -2012. -Т. 14, № 4. -С. 242-252.
- Крайник, Н.А. Интраоперационный ультразвуковой мониторинг состояния почечного аллотрансплантата/Н.А. Крайник, В.А. Сандриков, В.И. Садовников, М.М. Каабак, Е.Н. Платова//Ультразвуковая и функциональная диагностика. -2016. -№ 3. -С. 11-24.
- Радионуклидная диагностика для практических врачей/под ред. Ю.Б. Лишманова, В.И. Чернова. -Томск: STT, 2004. -394 с. -ISBN: 5-93629-166-9.
- Котина, Е.Д. Обработка данных в радионуклидной диагностике/Е.Д. Котина, Д.А. Овсянников, В.А. Плоских, А.В. Бабин, О.Ф. Тузикова//Ульяновский медико-биологический журнал. -2014. -№ 1. -С. 174-175.
- Williams, D.L. Improvement in quantitative data analyses by numerical deconvolution techniques/D.L. Williams//The Journal of Nuclear Medicine. -1979. -Vol. 20, Issue 6. -P. 568-557.
- Lee, S. Generalized image deconvolution by exploiting the transmission matrix of an optical imaging system/S. Lee, K. Lee, S. Shin, Y. Park//Scientific Reports. -2017. -Vol. 7, Issue 1. -8961. - DOI: 10.1038/s41598-017-07937-8
- Chaiwatanarat, T. Deconvolution analysis of renal blood flow: evaluation of postrenal transplant complications/T. Chaiwatanarat, S. Laorpatanaskul, M. Poshyachinda, S. Boonvisut, V. Buachum, A. Krisanachinda, R. Suvanapha//The Journal of Nuclear Medicine. -1994. -Vol. 35, Issue 11. -P. 1792-1796.
- Cosgriff, P.S. The urinary tract/P.S. Cosgriff. -In book: Practical nuclear medicine/ed. by P.F. Sharp, H.G. Gemmell, A.D. Murray. -Part 11. -London: Springer, 2005. -P. 205-230. - DOI: 10.1007/1-84628-018-4_11
- Durand, E. International scientific committee of radionuclides in nephrourology (ISCORN) consensus on renal transit time measurements/E. Durand, M.D. Blaufox, K.E. Britton, O. Carlsen, P. Cosgriff, E. Fine, J. Fleming, C. Nimmon, A. Piepsz, A. Prigent, M. Samal//Seminars in Nuclear Medicine. -2008. -Vol. 38, Issue 1. -Р. 82-102. - DOI: 10.1053/j.semnuclmed.2007.09.009
- Bajén, M.T. MAG3 renogram deconvolution in kidney transplantation: utility of the measurement of initial tracer uptake/M.T. Bajén, R. Puchal, A. González, J.M. Grinyó A. Castelao, J. Mora, J. Martin-Comin//The Journal of Nuclear Medicine. -1997. -Vol. 38, Issue 8. -P. 1295-1299.
- Knesaurek, K. Comparison of three deconvolution techniques in renography/K. Knesaurek, S. Spaventi//European Journal of Nuclear Medicine. -1984. -Vol. 9, Issue 6. -Р. 254-256.
- Гайдель, А.В. Исследование текстурных признаков для диагностики нефрологических заболеваний по ультразвуковым изображениям/А.В. Гайдель, С.Н. Ларионова, А.Г. Храмов//Вестник Самарского государственного аэрокосмического университета им. академика С.П. Королёва (национального исследовательского университета). -2014. -№ 1(43). -С. 229-237. - DOI: 10.18287/1998-6629-2014-0-1(43)-229-237
- Гайдель, А.В. Метод анализа цифровых нефросцинтиграмм на основе яркостных и геометрических характеристик изображений/А.В. Гайдель, А.Г. Храмов, А.В. Капишников, А.В. Колсанов, Ю.С. Пышкина//Компьютерная оптика. -2017. -Т. 41, № 1. -С. 103-109. - DOI: 10.18287/2412-6179-2017-41-1-103-109
- Веснина, Ж.В. Радионуклидная диагностика в нефрологии и урологии/Ж.В. Веснина. -В кн.: Радионуклидная диагностика для практических врачей/под ред. Ю.Б. Лишманова, В.И. Чернова. -Томск: STT. -2010. -Т. 2. -С. 195.
- Kuyvenhoven, J.D. Optimal time window for measurement of renal output parameters/J.D. Kuyvenhoven, H.R. Ham, A. Piepsz//Nuclear medicine review. Central & Eastern Europe. -2002. -Vol. 5, Issue 2. -Р. 105-108.


