Метод оценки радиационных рисков заболеваемости солидными злокачественными новообразованиями, учитывающий возможные ошибки в постановке и регистрации диагнозов
Автор: Горский А.И., Чекин С.Ю., Максютов М.А., Щукина Н.В., Кочергина Е.В., Зеленская Н.С., Лашкова О.Е.
Рубрика: Научные статьи
Статья в выпуске: 4 т.31, 2022 года.
Бесплатный доступ
Одной из причин смещения оценок радиационных рисков в эпидемиологических исследованиях могут быть ошибки в постановке диагнозов. В данной работе исследованы оценки радиационного риска в таблице сопряжённости 2´2 случаев заболеваний и облучения с учётом показателей чувствительности и специфичности методов диагностики. Радиационный риск оценивали метриками отношения шансов (OR) и относительного риска (RR). Показано, что оценка радиационного риска в метрике RR не зависит от показателя чувствительности диагностики, и поэтому является предпочтительной по сравнению с метрикой OR. При уменьшении специфичности диагностики оценка RR увеличивается по сравнению с оценкой, получаемой непосредственно по наблюдаемому числу случаев заболеваний, без учёта специфичности. В качестве числового примера использованы данные о случаях заболеваний злокачественными новообразованиями (ЗНО) трахеи, бронхов и лёгкого в когорте российских ликвидаторов последствий аварии на Чернобыльской АЭС, сформированной по данным наблюдений Национального радиационно-эпидемиологического регистра (НРЭР) с 1992 по 2020 гг. За этот период наблюдения в исследованной когорте численностью 67587 человек было зарегистрировано 2222 случая заболеваний. Члены когорты были разделены на 2 группы: с дозами облучения менее 0,1 Гр, которые считались не облучёнными, и остальные, которые считались облучёнными. Если показатель специфичности принять равным 100%, то оценка RR=1,07 при 95% доверительном интервале (ДИ) (1,02; 1,13). Оценки радиационных рисков ЗНО, получаемые непосредственно по наблюдаемому числу случаев заболеваний в облучённой и необлучённой группах лиц, без учёта показателей специфичности и чувствительности диагностики, являются нижними оценками радиационного риска. При увеличении вероятности ошибок диагностики (при уменьшении показателей специфичности и чувствительности диагностики) и при учёте этих ошибок оценки радиационных рисков увеличиваются. При уменьшении специфичности до 98,7% оценка радиационного риска ЗНО трахеи, бронхов и лёгкого среди ликвидаторов увеличивается до RR=1,13, но находится в пределах 95% ДИ оценки RR при специфичности 100%. Использованный в данном исследовании метод оценки радиационного риска, основанный на сравнении облучённой и необлучённой групп лиц в метриках OR или RR, накладывает высокие требования на показатель специфичности комплекса методов диагностики ЗНО трахеи, бронхов и лёгкого (Sp>98,7%) для того, чтобы получить не смещённые оценки радиационных рисков при дозах облучения ликвидаторов менее 1 Зв. Эти требования не обеспечиваются известными методами скрининговых исследований и могут быть выполнены только в рамках долгосрочных медицинских наблюдений, выполняемых в системе НРЭР.
Радиационный риск, таблица сопряжённости 2´2, отношение шансов, относительный риск, методы диагностики, чувствительность, специфичность, чернобыльская авария, ликвидаторы, злокачественные новообразования, трахея, бронхи, лёгкое
Короткий адрес: https://sciup.org/170196134
IDR: 170196134 | УДК: 616-006.04-02:614.876 | DOI: 10.21870/0131-3878-2022-31-4-53-63
Method for assessing the radiation risks of the solid cancer incidence accounting for possible diagnostic errors
A bias in radiation risk estimates may be caused by diagnostic errors. In this paper radiation risk estimates are examined with the use of the contingency table 2´2 of irradiated cancer cases with account of sensitivity and specificity indicators of diagnostic methods accuracy were examined. Radiation risk is estimated by metrics of the odds ratio (OR) and relative risk ratio (RR). It is shown that the estimation of radiation risk in the RR metric did not depend on the diagnostic sensitivity indicator, and therefore is preferable, compared to the OR metric. When the specificity of the diagnosis is reduced, the RR value increases, compared to the risk estimated with the use of observed number of cancer cases regardless of the specificity. As a numerical example, data on trachea, bronchus and lung cancers in a cohort of the Chernobyl cleanup workers of Russia formed by using data monitored within frames of the National Radiation Epidemiological Register (NRER) from 1992 to 2020. During this period, 2,222 cancer cases were reported in the cohort of 67,587 people. The cohort members were divided into two groups, those who were unexposed to radiation (radiation doses less than 0.1 Gy) and other, exposed to radiation. If the specificity indicator is taken to be 100%, then the RR=1.07 at 95% CI (1.02; 1.13). The estimates of radiation risks of malignant neoplasms obtained directly from the observed number of cancer cases in exposed and unexposed groups of people, excluding the specificity and sensitivity indicators of diagnosis accuracy, are the lower estimates of radiation risk. As the probability of diagnostic errors increases (as the specificity and sensitivity of diagnostic tests decrease), and when these errors are taken into account, the estimates of radiation risks increase. If the specificity is reduced to 98.7% CI radiation risk estimates for trachea, bronchus and lung cancer among cleanup workers of the Chernobyl accident increase to RR=1.13, but it is within 95% CI of the RR estimate if specificity is 100%. The radiation risk assessment approach used in the study, based on the comparison of exposed and unexposed groups of cleanup workers in OR or RR metrics, imposes high requirements to the specificity indicator of the complex of diagnostic methods in trachea, bronchus and lung (Sp>98.7%) in order to obtain unbiased estimates of radiation risks of cancer in the cleanup workers received dose below 1 Sv. These requirements are not supported by current screening methods, they can be fulfilled as a result of long-term medical monitoring within the system of the NRER.
Текст научной статьи Метод оценки радиационных рисков заболеваемости солидными злокачественными новообразованиями, учитывающий возможные ошибки в постановке и регистрации диагнозов
Одной из причин смещения оценок риска в эпидемиологических исследованиях могут быть ошибки в постановке диагнозов. В современной научной литературе сравнительно редко встречаются работы, в которых проводятся эпидемиологические исследования с учётом возможных ошибок диагностики. В данной работе исследованы свойства оценок радиационных рисков, принимающих во
Горский А.И.* – вед. науч. сотр., к.т.н.; Чекин С.Ю. – зав. лаб.; Максютов М.А. – зав. отд., к.т.н.; Щукина Н.В. – ст. науч. сотр.; Кочергина Е.В. – зав. лаб., к.м.н.; Зеленская Н.С. – науч. сотр.; Лашкова О.Е. – науч. сотр. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
внимание величину показателей чувствительности и специфичности диагностики злокачественных новообразований (ЗНО). Влияние возможных ошибок в постановке и регистрации диагнозов заболеваний на оценку радиационного риска иллюстрируется на простом примере оценок отношения шансов (OR) и относительного риска (RR) в таблице сопряжённости 2 x 2 с использованием фактических данных о дозах облучения и заболеваемости ЗНО трахеи, бронхов и лёгкого среди российских участников ликвидации последствий аварии на Чернобыльской АЭС (ликвидаторов).
Материалы и методы
В исследовании использованы данные о заболеваемости ЗНО трахеи, бронхов и лёгкого в когорте российских ликвидаторов последствий аварии на Чернобыльской АЭС, сформированной по данным наблюдений Национального радиационно-эпидемиологического регистра (НРЭР) с 1992 по 2020 гг. За этот период наблюдения в исследованной когорте мужчин-ликвидаторов 1986-1987 гг. въезда в чернобыльскую зону, общей численностью 67587 человек, было зарегистрировано 2222 верифицированных случая заболеваний. Полное описание когорты приведено авторами ранее [1].
Медицинская информация о лицах, включённых в систему НРЭР, собирается в каждом из 85 субъектов Российской Федерации, а также в 4-х ведомственных подрегистрах. Источниками медицинской информации являются первичные медицинские документы, утверждённые Минздравом России, заполнение которых происходит по результатам проведённой спецдиспансери-зации, медицинского наблюдения и лечения, а в случае смерти лица, состоящего на учёте в НРЭР, – посмертные документы. Кроме того, используются протоколы различных медицинских специальных диагностических исследований, копии бланков с результатами гистологического (цитологического) исследования, заключения Межведомственных экспертных советов, заключения консультантов, копии документов ЗАГС и др.
Ответственными медицинскими организациями (МО), осуществляющими медицинское обслуживание лица по месту проживания, на основании источников медицинской информации указанной выше, заполняются формы НРЭР, посредством внесения в них необходимой информации о заболеваемости и причинах смерти, в соответствии с «Международной статистической классификацией болезней и проблем, связанных со здоровьем» 10-го пересмотра (МКБ-10). Заполненные формы НРЭР на бумажном носителе и (или) в электронном виде из МО передаются в уполномоченные организации за ведение региональных сегментов (РС) НРЭР в субъектах Российской Федерации. Затем из РС НРЭР каждого субъекта Российской Федерации данные в виде компьютерных файлов передаются на федеральный уровень НРЭР в МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России для окончательной верификации и включения (загрузки) в единую федеральную базу данных (ЕФБД) НРЭР.
Для проведения верификации медицинской информации на федеральном уровне НРЭР уполномоченными организациями вместе с формами НРЭР представляются копии всех первичных документов, использованных при заполнении этих форм. В тех случаях, когда документы содержат неполную информацию, неточности, некорректные формулировки или несоответствия между различными первичными документами, с федерального уровня НРЭР отправляются запросы в РС НРЭР о предоставлении дополнительных данных (справки с информацией из медицинских карт, результаты гистологических заключений, протоколы вскрытия и т.д.). Все недочёты и ошибки, выявленные в заполненных формах НРЭР, по окончании работ по верификации медицинской информации систематизируются и анализируются как по каждому отдельному субъекту
Российской Федерации, так и в целом по ЕФБД НРЭР. Из прошедших экспертную проверку форм НРЭР формируются подрегистр смертности и канцер-подрегистр ЕФБД НРЭР, уже без ошибок и недочётов. Протоколы верификации передаются в уполномоченные организации по ведению РС НРЭР в субъектах Российской Федерации для исправления имеющихся ошибок в представленных формах НРЭР и восполнения недостающих сведений. Процесс верификации медицинской информации на уровне ЕФБД НРЭР по времени может занимать до года, а в редких случаях может длиться до двух лет и более. Статистический анализ процесса верификации диагнозов солидных ЗНО за последние 10 лет показывает, что к настоящему времени менее 1% случаев солидных ЗНО могут оставаться окончательно не верифицированными. При этом доля некорректно заполненных диагнозов в формах НРЭР год от года постоянно уменьшается.
В данном исследовании оценку радиационных рисков ЗНО трахеи, бронхов и лёгкого среди ликвидаторов проводили по полностью верифицированным диагнозам, внесённым в ЕФБД НРЭР.
Общие основы анализа влияния ошибок в постановке диагнозов на оценки радиационных рисков изложены в монографиях [2, 3]. В соответствии с общепринятыми подходами к такому анализу введём следующие обозначения для состояния субъекта (человека): X=1 – облучён, X=0 – не облучён, D=1 – болен (истинный случай заболевания), D=0 – здоров (истинный контроль), D*=1 – классифицирован как случай заболевания (наблюдаемый случай), D*=0 – классифицирован как здоровый (наблюдаемый контроль).
Рассмотрим таблицы сопряжённости 2 x 2 между облучением и заболеванием. Табл. 1 представляет наблюдаемое число случаев и контролей, а табл. 2 – истинное число больных субъектов (случаев заболеваний) и здоровых (контролей).
Таблица 1
Таблица сопряжённости 2x2 для наблюдаемого числа случаев заболеваний и контролей
|
Состояние здоровья |
Число облучённых лиц (X=1) |
Число необлучённых лиц (X=0) |
Всего |
|
Случаи (D*=1) |
A 1 * |
A 0 * |
M 1 * |
|
Контроли (D*=0) |
B 1 * |
B 0 * |
M 0 * |
|
Всего |
N 1 |
N 0 |
K |
Таблица 2
Таблица сопряжённости 2x2 для истинного числа случаев заболеваний и контролей
|
Состояние здоровья |
Число облучённых лиц (X=1) |
Число необлучённых лиц (X=0) |
Всего |
|
Случаи (D=1) |
A 1 |
A 0 |
M 1 |
|
Контроли (D=0) |
B 1 |
B 0 |
M 0 |
|
Всего |
N 1 |
N 0 |
K |
По табл. 1 и 2 определяются наблюдаемое и истинное отношение шансов (OR) обнаружить облучённый случай (по отношению к шансам обнаружить необлучённый случай) [3]:
OR* = Ai* x Bo*/ (Bi* x Ao*),(1)
OR = Ai x Bo / (Bi x Ao).(2)
Аналогичным образом определяется наблюдаемый и истинный относительный радиационный риск (RR):
RR* = Ai* x No / (Ao* x Ni),(3)
RR = Ai x No / (Ao x Ni).(4)
Определим следующие вероятности.
-
1. Вероятность, что здоровый человек классифицирован как контроль (показатель специфичности): Sp=Pr(D*=0|D=0).
-
2. Вероятность, что больной человек классифицирован как случай заболевания (показатель чувствительности): Se=Pr(D*=1|D=1).
-
3. Вероятность, что здоровый человек классифицирован как случай заболевания (ошибка первого рода, или ложноположительный диагноз): Fp=Pr(D*=1|D=0)=1–Sp.
-
4. Вероятность, что больной человек классифицирован как здоровый (ошибка второго рода, или ложноотрицательный диагноз): Fn=Pr(D*=0|D=1)=1–Se.
Тогда наблюдаемое число лиц, классифицированных как случаи:
A i * = Se х A i + Fp x B i = Se x A i + (1 - Sp) x B i , (5)
и наблюдаемое число лиц, классифицированных как контроли:
B i * = Sp x B i + Fn x A i = Sp x B i + (1 - Se) x A i , (6)
где значение индекса i =0 соответствует не облучённым лицам (X=0), а значение индекса i =1 – облучённым (X=1).
Здесь следует заметить, что суммарное число облучённых N 1 и необлучённых N 0 лиц в табл. 1 и 2 должны совпадать, в то время как соотношение между истинным числом случаев и контролей в табл. 2 (M 1 /M 0 ) будет меняться в зависимости от предполагаемых вероятностей ошибок диагностики, а именно – в зависимости от предполагаемых показателей чувствительности и специфичности применявшихся методов диагностики и верификации диагнозов [3].
Из уравнений (5) и (6) определим истинное число больных (A i ) и здоровых (B i ) лиц через наблюдаемое число случаев (A i *) и контролей (B i *) и предполагаемые вероятности различных вариантов постановки (и регистрации) диагнозов, перечисленные в пунктах 1-4 выше. С учётом того, что B i *=N i – A i * и B i =N i – A i , получим следующие выражения:
Ai = (Ai* - Fp x Ni) / (Sp - Fn) = [Ai* - (1 - Sp) x Ni] / (Sp + Se - 1),(7)
Bi = (Bi* - Fn x Ni) / (Sp - Fn) = [Bi* - (1 - Se) x Ni] / (Sp + Se - 1).(8)
Таким образом, истинное значение отношения шансов:
OR = (A 1 * - Fp x N 1 ) x (Se x N o - A o *) / [ (A o * - Fp x N0) x (Se x N 1 - A 1 *) ] =
= [A1* - (1 - Sp) x N1 ] x (Se x No - Ao*) / [(Ao* - (1 - Sp) x No) x (Se x N1 - A1*)].(9)
Как нетрудно видеть, при единичной специфичности (Sp=1–Fp=1, т.е. Fp=0) и чувствительности (Se=1–Fn=1, т.е. Fn=0), выражение (9) для истинного значения OR переходит в его исходное выражение (2). В другом крайнем случае, когда специфичность и чувствительность нулевые (Sp=0, Fp=1, Se=0, Fn=1), истинное значение OR переходит в обратное по отношению к наблюдаемому значению (OR=1/OR*).
Аналогичным образом, истинное значение относительного риска RR задаётся выражением:
RR = [ A 1 *- (1 - Sp) x N 1 ] x N o / [ (A o *- (1 - Sp) x N o ) x N 1 ] . (10)
Как следует из формул (9) и (10), оценка истинного отношения шансов OR зависит от чувствительности Se и специфичности Sp, а оценка истинного RR – только от специфичности Sp. В этом смысле оценка истинного радиационного риска в метрике RR является предпочтительной по сравнению с метрикой OR.
Доверительные пределы для оценок OR и RR определим с использованием приближений, приведённых в [4].
Дисперсии (Var) логарифмов оценок OR и RR определяется следующими формулами:
Var(ln(OR)) = 1/A 0 + 1/A 1 + 1/B 0 + 1/B 1 , (11)
Var(ln(RR)) = 1/A 1 + 1/B 1 – 1/N 1 – 1/N 0 . (12)
Границы доверительных интервалов (ДИ) для оценок OR и RR определяются, исходя из приближения, что статистики TOR=[ln(OR)]2/Var(ln(OR)) и TRR=[ln(RR)]2/Var(ln(RR)) асимптотически имеют распределение хи-квадрат ( х 2) с одной степенью свободы [4]. Для оценок наблюдаемых OR* и RR* доверительные интервалы определяются аналогичным образом.
Результаты и обсуждение
Рассмотрим пример влияния ошибок в постановке и регистрации диагнозов на оценки радиационного риска. Данные о ликвидаторах, входивших ранее в когортное исследование ЗНО трахеи, бронхов и лёгкого [1], разделим на две дозовые группы (меньше или равно 0,1 Гр и больше 0,1 Гр). Данные такой выборки представлены таблицей сопряжённости 2 x 2 (табл. 3).
Таблица 3
Наблюдаемое число случаев и контролей для заболеваемости ликвидаторов ЗНО трахеи, бронхов и лёгкого
|
Состояние здоровья |
Число облучённых лиц (X=1) |
Число необлучённых лиц (X=0) |
Всего |
|
Случаи (D*=1) |
1241 |
981 |
2222 |
|
Контроли (D*=0) |
35310 |
30055 |
65365 |
|
Всего |
36551 |
31036 |
67587 |
В соответствии с формулами (1), (3), (11) и (12) оценки наблюдаемых по табл. 3 величин отношения шансов OR* и относительного риска RR*, с их 95% ДИ, равны OR*=1,08 (0,99; 1,17) и RR*=1,07 (1,02; 1,13).
На рис. 1 приведена зависимость истинного значения относительного риска RR (наблюдаемого RR*, откорректированного с учётом показателя специфичности Sp) от величины показателя специфичности, выраженного в %. Как показано на рис. 1, истинное значение RR возрастает при уменьшении показателя специфичности. При уменьшении специфичности до 98,7% оценка радиационного риска увеличивается до RR=1,13. При этом она достигает верхней границы 95% ДИ оценки RR*, полученной по наблюдаемому числу случаев и контролей из табл. 1.
Оценка истинного отношения шансов OR зависит как от показателя специфичности Sp, так и от показателя чувствительности Se. При Se=1 общий вид зависимости OR от показателя специфичности Sp практически совпадает с зависимостью RR от этого показателя. С другой стороны, в диапазоне значений Sp от 0,98 до 1 (от 98% до 100% в процентном выражении) оценка OR, в соответствии с формулой (9), практически не зависит от показателя чувствительности Se: первая производная OR по переменной Se в формуле (9) близка к нулю.
На рис. 2 приведена зависимость истинного значения отношения шансов OR (наблюдаемого OR*, откорректированного с учётом показателя чувствительности Se) от величины показателя чувствительности, выраженного в %. Как показано на рис. 2, при уменьшении показателя чувствительности оценка истинного значения OR возрастает, однако, даже при снижении показателя чувствительности Se со 100% до 6%, оценка отношения шансов увеличивается только до OR=1,17, достигая верхней границы 95% ДИ оценки OR*, полученной по наблюдаемому числу случаев и контролей из табл. 1.
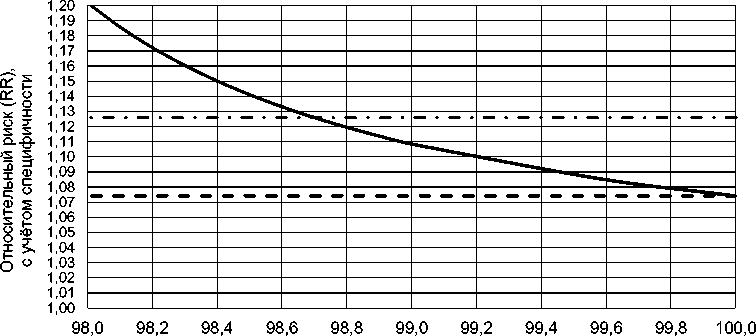
Показатель специфичности, %
RR RR* Верх. гран. 95%ДИ RR*
Рис. 1. Истинное значение относительного риска RR (наблюдаемого RR*, откорректированного с учётом показателя специфичности Sp) в зависимости от величины показателя специфичности.
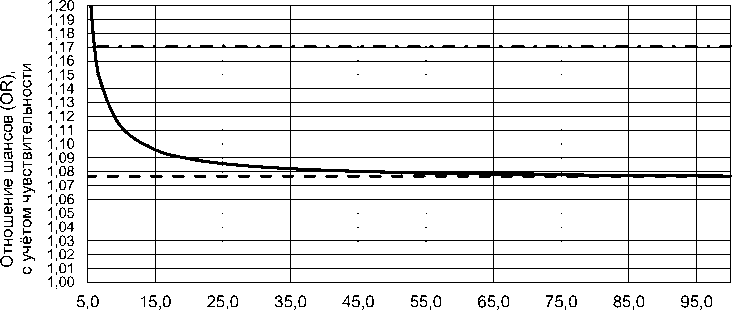
Показатель чувствительности, %
OR OR* Верх. гран. 95%ДИ OR*
Рис. 2. Истинное значение отношения шансов OR (наблюдаемого OR*, откорректированного с учётом показателя чувствительности Se) в зависимости от величины показателя чувствительности.
В разобранном выше численном примере табл. 3 содержит только полностью верифицированные диагнозы ЗНО трахеи, бронхов и лёгкого, включённые в ЕФБД НРЭР, что обеспечивает оценку минимально возможных (при данных наблюдаемых случаях и контролях) радиационных рисков в относительных метриках OR и RR. Как показывают формулы (9) и (10), наличие ошибок в постановке и регистрации диагнозов ЗНО и учёт этих ошибок при оценках OR и RR увеличивало бы последние. Однако, данные методы оценки радиационных рисков очень устойчивы к ошибкам в диагнозах. Например, даже если 38,8% из 2222 указанных в табл. 3 диагнозов были бы ложноположительными (864 ложноположительных диагнозов: для 465 облучённых и 396 необлучённых членов выборки), показатель специфичности Sp=98,7%, и оценка RR=1,13 не выходила бы за верхнюю границу 95% ДИ для исходной не откорректированной оценки RR*=1,07 с 95% ДИ (1,02; 1,13).
В противоположность долговременному медицинскому наблюдению когорты, осуществляемому в системе НРЭР, для раннего выявления ЗНО лёгкого в выделенных группах риска в последнее время рекомендуется скрининговое обследование методом низкодозной компьютерной томографии (НДКТ). Основное преимущество НДКТ – способность анатомически наиболее точно оценить расположение опухоли в грудной клетке, что даёт возможность планировать прицельную биопсию с целью установки гистопатологического диагноза и стадирования опухоли [5]. Преимуществом является также высокая разрешающая способность, позволяющая диагностировать центральный рак ещё до появления признаков нарушения вентиляции ткани лёгкого, а также выявлять начальные формы рака, в том числе и расположенные на поверхности бронхов. Основное ограничение НДКТ грудной клетки заключается в низкой точности идентификации метастазов средостения. При подозрении на опухоли средостения, за исключением крупных образований, как правило, требуются дополнительные исследования. Показатели чувствительности и специфичность НДКТ по отношению к диагностике ЗНО лёгкого оценивались как Se=55% и Sp=80% [5]. Более сложные алгоритмы диагностики, основанные на трёхстадийном скрининговом обследовании методом НДКТ, при определённых условиях позволяли достичь показателя специфичности диагностики около 95% [6].
Одним из достаточно информативных современных методов диагностики ЗНО лёгкого считается совместное применение позитронно-эмиссионной томографии (ПЭТ) и НДКТ (ПЭТ/КТ). Преимущество ПЭТ, в частности, заключается в высокой чувствительности, позволяющей с высокой степенью точности визуализировать как первичный опухолевый очаг, так и регионарные и отдалённые метастазы. Также с помощью ПЭТ можно оценивать эффективность лечения ЗНО лёгкого [7]. Недостатки ПЭТ прежде всего связаны с отсутствием возможности чёткого отображения анатомических структур и пространственного расположения изменений по отношению к окружающим тканям. Их можно компенсировать путём совмещения ПЭТ/КТ, что позволяет повысить точность диагностики. Показатели чувствительности и специфичности диагностики при применении ПЭТ достигают значений Se=80% и Sp=88%, а при совместном применении ПЭТ/КТ – Se=62% и Sp=90% [7]. В ещё одном масштабном обзоре, изучавшем результаты 56 исследований с участием 8699 пациентов [8], было показано, что чувствительность и специфичность ПЭТ/КТ при стадировании опухолей средостения составила 72% и 91%, внутригрудных опухолей – 78% и 90%, при обнаружении отдалённых метастазов – 77% и 95%, а метастазов в кости – 91% и 98%. Данные метаанализа также подтвердили, что при стадировании не мелкоклеточного рака лёгкого чувствительность и специфичность ПЭТ/КТ гораздо выше, чем КТ с контрастированием, а чувствительность выше, чем ПЭТ [8].
Обзор современных методов диагностики ЗНО лёгкого, включая биомаркеры, различные анализы крови, мочи и метаболомические анализы, показывает, что для отдельно взятых методов диагностики показатели специфичности Sp не превышают 98% и, в основном, находятся в диапазоне от 70% до 95% [9].
В то же время, с общетеоретической точки зрения ранее было показано, что при значениях Sp<90% адекватно могут быть оценены величины отношения шансов OR>3 [10]. Кроме того, были показаны существенные ограничения на вероятности ошибок диагностики и при использовании традиционных методов оценки рисков, основанных на параметрах в моделях логистической регрессии [10].
Выводы
В данном исследовании показано, что оценки радиационных рисков ЗНО, получаемые непосредственно по наблюдаемому числу случаев заболеваний в облучённой и необлучённой группах лиц, без учёта показателей специфичности и чувствительности диагностики, являются нижними оценками радиационного риска. При увеличении вероятности ошибок диагностики (при уменьшении показателей специфичности и чувствительности диагностики) и при учёте этих ошибок оценки радиационных рисков увеличиваются.
Оценка радиационного риска в метрике относительного риска (RR) зависит только от показателя специфичности (Sp) диагностики и не зависит от показателя чувствительности (Se), в то время как оценка отношения шансов (OR) зависит и от Sp и от Se. Поэтому метрика радиационного риска RR является предпочтительной по сравнению с метрикой отношения шансов OR.
Использованный в данном исследовании метод оценки радиационного риска, основанный на сравнении облучённой и необлучённой групп лиц в метриках отношения шансов (OR) или относительного риска (RR), накладывает довольно высокие требования на показатель специфичности комплекса методов диагностики ЗНО трахеи, бронхов и лёгкого (Sp>98,7%) для того, чтобы получить не смещённые оценки радиационных рисков при дозах облучения менее 1 Зв. Эти требования не обеспечиваются известными методами скрининговых исследований и могут быть выполнены только в рамках долгосрочных медицинских наблюдений, выполняемых в системе НРЭР.
Список литературы Метод оценки радиационных рисков заболеваемости солидными злокачественными новообразованиями, учитывающий возможные ошибки в постановке и регистрации диагнозов
- Кащеев В.В., Чекин С.Ю., Карпенко С.В., Максютов М.А., Туманов К.А., Кочергина Е.В., Глебова С.Е., Иванов С.А., Каприн А.Д. Оценка радиационных рисков злокачественных новообразований среди российских участников ликвидации последствий аварии на Чернобыльской АЭС //Радиация и риск. 2021. Т. 30, № 1. C. 58-77.
- Rothman K., Greenland S. Modern epidemiology. Part 19. Basic methods for sensitivity analyses and external adjustment. Publ. Lippincott Williamce & Wilkins, 1998. P. 343-358.
- Альбом А., Норрел С. Введение в современную эпидемиологию /пер. с англ. Таллинн, 1996.
- Breslow N.E., Day N.E. Statistical methods in cancer research. Volume I: The analysis of case-control studies. IARC Scientific Publication 32. Lyon: IARC, 1980. 346 p.
- Silvestri G.A., Gonzalez A.V., Jantz M.A., Margolis M.L., Gould M.K., Tanoue L.T., Harris L.J., Detterbeck F.C. Methods for staging non-small cell lung cancer: Diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines //Chest. 2013. V. 143, N 5 (Suppl.). P. e211S-e250S.
- Pinsky P.F., Gierada D.S., Black W., Munden R., Nath H., Aberle D., Kazerooni E. Performance of Lung-RADS in the National Lung Screening Trial: a retrospective assessment //Ann.Intern. Med. 2015. V. 162, N 7. P. 485-491.
- De Wever W., Ceyssens S., Mortelmans L., Stroobants S., Marchal G., Bogaert J., Verschakelen J.A. Additional value of PET-CT in the staging of lung cancer: comparison with CT alone, PET alone and visual correlation of PET and CT //Eur. Radiol. 2007. V. 17, N 1. P. 23-32.
- Wu Y., Li P., Zhang H., Shi Y., Wu H., Zhang J., Qian Y., Li C., Yang J. Diagnostic value of fluorine 18 fluorodeoxyglucose positron emission tomography/computed tomography for the detection of metastases in non-small-cell lung cancer patients //Int. J. Cancer. 2013. V. 132, N 2. P. 37-47.
- Nooreldeen R., Bach H. Current and future development in lung cancer diagnosis //Int. J. Mol. Sci. 2021. V. 22, N 16. P. 8661.
- Pepe M.S., Janes H., Longton G., Leisenring W., Newcomb P. Limitations of the odds ratio in gauging the performance of a diagnostic, prognostic, or screening marker //Am. J. Epidemiol. 2004. V. 159, N 9. P. 882-890.


