Метод определения электропроводности растворов кислот и оснований
Автор: Балданова Д.М., Танганов Б.Б.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Статья в выпуске: 4 (43), 2013 года.
Бесплатный доступ
В рамках плазменно-гидродинамической теории растворов электролитов предложена теоретическая модель оценки электропроводности кислот и оснований, учитывающая радиусы гидратированных ионов. Полученные результаты хорошо коррелируют с экспериментальными данными.
Электропроводность, радиус, гидратированные ионы, кислоты, основания
Короткий адрес: https://sciup.org/142142722
IDR: 142142722 | УДК: 544.35.03:537.311
Method for electrical conductivity determination of acids and bases solutions
Theoretical evaluation model of electrical conductivity of acids and bases, taking into account the radii of hydrated ions is proposed in the framework of the plasma hydrodynamic theory of electrolyte solutions. The obtained results are in good agreement with the experimental data.
Текст научной статьи Метод определения электропроводности растворов кислот и оснований
Исследование электропроводности имеет большое значение при изучении процессов сольватации и транспортных свойств ионов в растворах электролитов. Особенно интересными являются растворы кислот и оснований, так как ионы гидроксония и гидроксила движутся по эстафетному механизму, а механизм движения противоионов неэстафетный:
H 3 O + + H 2 O о H 2 O + H 3 O + . (1)
OH - + H 2 O о H 2 O + OH - . (2)
В процессе (1) ионы H 3 O + группируют 4 молекулы воды [1]. При этом отрицательные заряды диполей воды направлены к H 3 O + , что облегчает туннельный переход протона H + в H 3 O + к молекулам воды и далее.
В случае процесса (2) ионы OH - ориентируют 2 молекулы H 2 O положительными зарядами диполей. Тогда за счет туннельного эффекта ионы H + из H 2 O переходят к иону OH - .
Эти процессы и объясняют аномально высокую электропроводность растворов кислот и оснований.
Метод определения электропроводности растворов кислот и оснований
На кафедре «Неорганическая и аналитическая химия» ВСГУТУ разработана плазменно-гидродинамическая концепция состояния ионов в растворах электролитов. В рамках данной теории получено уравнение для теоретических оценок электропроводности водных растворов электролитов [2]:
NAe 2 exp( — — ) • 1,11 • 10 —12
A Э 7 T7 ’ 7 17
Л =___________ k B ___________, Ом - см моль - .
6nnRs (1 + R s -)
rD
Для кислот и оснований остается неформализованной величина Rs . Обзор литературы показал, что значения радиусов гидратированных ионов H 3 O + и OH — вообще отсутствуют. Приемлемых методов теоретических оценок этих величин, соответствующих данным Стокса, нет.
Эффективные радиусы этих гидратированных ионов формализуются известной задачей механики [3] о системе, состоящей из одной частицы с массой M и n частиц с одинаковыми массами m .
Если исключить движение центра инерции, то проблема сводится к задаче движения n частиц с M - массой ионов H 3 O + или OH — ; m - массой молекул воды; n s - гидратным числом.
^
Рассматривается гидратный комплекс, в котором R - радиус-вектор H 3 O + или
OH ; R a a = (1,2,3,..., n ) - радиус вектор
комплексе. Расстояние от H 3 O + или OH
гидратированных молекул воды в гидратном до молекул в этом комплексе обеспечивается
выражением:
^ ^
r a = R a
^
— R ,
а начало координат в центре инерции формализуется равенством:
^
^
M • R + m У R a = 0.
a
Очевидно, введение в уравнение (5) значения Ra из [4] дает безразмерное равенство в оригинальной постановке задачи
R
m
У ra M + n s • m
a
— ■
.
Гидратированные ионы имеют центрально-симметричное распределение вещества и заряда, и при их движении под действием внешнего поля меняется система отсчета. Тогда возможно умножение левой и правой частей уравнения (6) на величину R a • M . Далее в левую часть уравнения (6) вводится значение ra из выражения (4), что приводит к следующему уравнению:
^ ^
^
У Г =У1 Ra — R | = n • Ra as
^
— R .
a
a
В этом случае
^ ^
R • R a
^ n s • R a
—
M • m ^ — • M =-- R a .
r M + ns • m
Наглядная трансформация векторных величин к их скалярам в виде модулей можна в виде
^ ^ ^ ^ ^ ^
R • R a • M =-- ( nsR a • R a — R • R a ).
M + ns • m
^ ^ о ^ ^
Угол между векторами Ra и Ra равен a = 180 , а между векторами R и Ra — воз-
a
00. Тогда, согласно правилам векторного анализа, скалярное произведение двух векторов равно произведению их модулей на cos а (где a - угол между направлениями этих век-
→→ →→ торов). Поэтому R⋅ Ra = -R ⋅ Ra, так как cos1800 = -1 и R⋅Ra=R⋅R ввиду того, что cos00 = 1.
Приведенные факты дают основание следующему представлению
R ⋅ R a = M ⋅ m ⋅ R a . (8)
R + ns ⋅ Ra M + ns ⋅ m M
Таким образом, приведенная симметричная форма выражения (8) в скалярных ар-
M⋅m гументах с учетом приведенной массы системы, равной , показывает, что
M + ns ⋅ m
R⋅R a = r есть эффективный приведенный радиус системы. R+ns ⋅Ra
8 см [5],
Радиус молекулы воды в жидком состоянии при 298 K равен R = 1,15 ⋅ 10
радиус R + =1,35 ⋅ 10 - 8 см и радиус R H 3 O OH
- 8 H O +
=1,53 ⋅ 10 8 см [4]. Далее гидратное число nsH 3 O = 4
[1] и nsOH - = 2,2 из уравнения (8) при ri =1,53 ⋅ 10 - 8
При этих значениях R , Ra и ns эффективные радиусы ионов H 3 O + и OH - равны:
R s ( H 3 O + )
1,35 ⋅ 10 - 8 ⋅ 1,15 ⋅ 10 - 8
1,34 ⋅ 10 - 8 + 4 ⋅ 1,15 ⋅ 10 - 8
= 0,261 ⋅ 10 - 8
см,
R s ( OH ) =
1,53 ⋅ 10 - 8 ⋅ 1,53 ⋅ 10 - 8
1,53 ⋅ 10 - 8 + 2,2 ⋅ 1,15 ⋅ 10 - 8
= 0,43 ⋅ 10 - 8
см.
Результаты исследования
Полученные значения радиусов гидратированных ионов H 3 O + и OH - могут быть использованы при оценке электропроводности водных растворов кислот и оснований. Результаты теоретических оценок эквивалентных электрических проводимостей растворов электролитов в рамках плазменно-гидродинамической модели по уравнению (3) приведены в таблицах 1, 2 и на рисунках 1, 2. Литературные значения Λ лит взяты из [6].
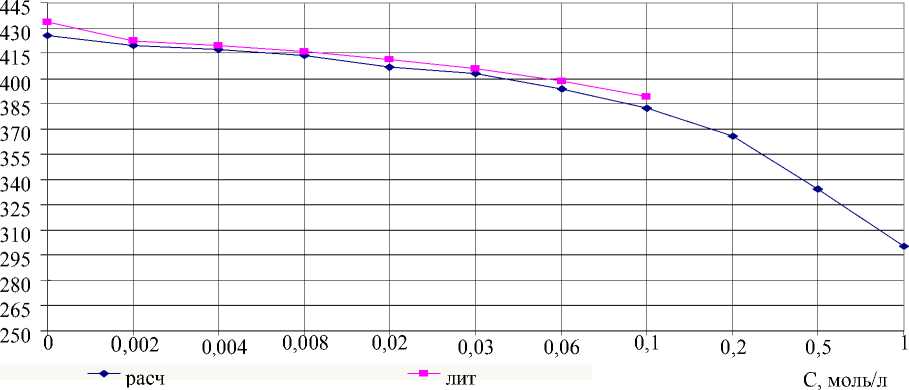
Рис. 1. Графическая зависимость электропроводности Λ водного раствора HBr от концентрации при 298K
Λ, Ом-1∙см2∙моль-1
|
•--------------< |
.—__: |
1---— |
|||||||||||
|
^------■ |
|||||||||||||
|
- |
|||||||||||||
0,5 1
0,001 0,002 0,005 0,01 0,02 0,03 0,05 0,1 0,2 0,3
расч
—■— лит
С, моль/л
Рис. 2. Графическая зависимость электропроводности Λ водного раствора KOH от концентрации при 291К
Таблица 1
Концентрационная зависимость эквивалентной электропроводности ( Λ , Ом - 1 ⋅ см2 ⋅ моль - 1) HCl при 291K
µ = 9,24; rs Kt = 0,26 ⋅ 10 - 8см; rs An = 1,34 ⋅ 10 - 8см; rs прив = 0,22 ⋅ 10 - 8см
|
C, моль/л |
0 |
0,001 |
0,01 |
0,1 |
5 |
10 |
|
Х = ( z kt z an ⋅ С / µ )1/2 |
0,000 |
0,010 |
0,033 |
0,104 |
0,736 |
1,040 |
|
exp( - 0,84 ⋅ X ) |
1,000 |
0,991 |
0,973 |
0,916 |
0,539 |
0,418 |
|
rD = 0,02814( ε T / C )1/2 |
∞ |
48,50 |
15,34 |
48,50 |
6,85 |
4,85 |
|
Λ теор |
372 |
367 |
361 |
340 |
146 |
91 |
|
Λ лит |
378 |
377 |
370 |
351 |
150 |
66 |
Таблица 2
Концентрационная зависимость эквивалентной электропроводности (Λ , Ом - 1 ⋅ см2 ⋅ моль - 1) NaOH при 291K
µ = 9,75; r s Kt = 1,75 ⋅ 10 - 8 см; r s An =0,43 ⋅ 10 - 8см; r s прив = 0,345 ⋅ 10 - 8см
|
C , моль/л |
0 |
0,001 |
0,01 |
0,1 |
10 |
|
Х = ( z kt z an ⋅ С / µ )1/2 |
0,000 |
0,010 |
0,32 |
0,319 |
1,011 |
|
exp( - 0,82 ⋅ X ) |
1,000 |
0,992 |
0,973 |
0,764 |
0,427 |
|
rD = 0,02814 ⋅ ( ε T / С )1/2 |
∞ |
136,5 |
43,16 |
4,315 |
1,3647 |
|
Λ теор |
226 |
223 |
216 |
159 |
18,000 |
|
Λ лит |
220 |
208 |
200 |
160 |
20,0 |
Заключение
Таким образом, полученные значения электропроводности кислот и оснований на основе плазменно-гидродинамической модели состояния ионов в растворах электролитов, учитывающие теоретически оцененные радиусы гидратированных ионов H3O+ и OH-, имеющих центрально-симметричное распределение вещества и заряда, хорошо коррелируют с литературными данными.


