Методика комбинированного хирургического лечения гнойного лактационного мастита
Автор: Котов Игорь Игнатьевич, Бублейник Оксана Алексеевна, Кацовский А.М.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.10, 2015 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140188432
IDR: 140188432
Текст статьи Методика комбинированного хирургического лечения гнойного лактационного мастита
Лечение острого гнойного лактационного мастита (ОГЛМ) остается сложной задачей в неотложной хирургии. Частота возникновения послеродового мастита (ПМ) составляет 0,5–6% от общего числа родов [7]. При этом в деструктивную форму переходит от 10 до 19% всех случаев ПМ [1]. В структуре послеродовых гнойно-воспалительных осложнений у родильниц мастит составляет 26–67% [10]. В последние годы наметился рост заболеваемости острым маститом, а количество деструктивных форм ПМ не имеет тенденции к уменьшению [8].
Некоторые аспекты хирургического лечения ОГЛМ на сегодня окончательно не решены и остаются диску-табельными, это: объем иссечения пораженных тканей; открытое или закрытое ведение ран; первичный или вторичный шов; разные варианты дренажных систем при первичном шве; дренирование пассивное или с вакуумной аспирацией; составы лаважных растворов при промывном дренировании; степень разряжения при активной аспирации; сроки удаления дренажей; тактика лечения и способы устранения молочных фистул и ряд других.
Современные требования к хирургическому лечению ПМ включают следующие положения: купирование воспалительного процесса в кратчайшие сроки; максимальное сохранение функции молочной железы; максимальное сохранение эстетического состояния молочной железы [9].
Объективные трудности лечения деструктивного послеродового мастита связанны с необходимостью санации гнойного очага в функционально активной железе, поэтому в ряде случаев возникают показания для прекращения лактации [2, 5, 7]. Согласованная тактика по этому важному вопросу пока не выработана.
Цель работы заключается в улучшении результатов лечения больных с острым гнойным лактационным маститом (ОГЛМ) с приоритетным сохранением лактации.
Материалы и методы
Представлены результаты лечения 216 больных с ОГЛМ, поступивших в отделении гнойной хирургии БУ-ЗОО ГК БСМП № 1 г. Омска за период с 2006 по ноябрь 2014 гг. Пациентки обследованны физикально, с применением УЗИ на аппарате «LOGIQ P6/PRC» GE Healhcare с линейным датчиком 11 МГц, бактериологическими исследованиями гноя и молока, общепринятыми клиническими анализами.
На базе ГКБСМП № 1 г. Омска с 2001 года функционирует единый городской центр по оказанию неотложной хирургической помощи беременным и родильницам.
Возраст больных колеблется от 17 до 42 лет. До 20 лет была 21 (9,7%) пациентка, наибольшее количество женщин 137 (63,4%) наблюдалось в возрасте от 21 года до 30 лет, от 31 года до 40 лет было 56 (25,9%) больных и старше 41 года всего – 2 (0,9%).
Воспалительный процесс в молочной железе возникал в послеродовом периоде в первые 3 недели у 34 (15,7%) больных, в период с 4 по 6 недели у 124 (57,4%), в более поздние сроки у 58 (26,9%) пациенток. Родильниц было 158 (73,1%) из 216 больных ОГЛМ.
Период с момента заболевания до госпитализации составил до 7суток у 145 (67,1%) больных, до 14 суток у 53 (24,5%) пациенток, остальные 18 (8%) обратились позже.
У всех пациенток гнойной деструкции в молочной железе предшествовал лактостаз, у 32 (14,8%) – наблю-

далась патология соска молочной железы (трещины, мацерация, втянутый сосок).
Наиболее часто гнойный воспалительный процесс локализовался в верхнем наружном (ВН) квадранте молочной железы в 74 (33,5%) случаях. В верхнем внутреннем (ВВ) в – 22 (10%); в нижнем наружном (НН) в – 20 (9,0%); в нижнем внутреннем (НВ) в – 7 (3,2%); субареолярно в – 32 (14,5%). В смежных зонах или с захватом двух зон: ВН-ВВ у 32 (14,5%) больных, ВН-НН у 15 (6,8%), ВВ-НВ у 4 (1,8), НВ-НН у 15 (6,8%) пациенток. Практически одинаково в правой и левой молочных железах. У 5 больных гнойники были с двух сторон. Следует отметить, что с учетом поражения смежных квадрантов в верхней наружной части молочной железы гнойники локализовались в 121 (54,8%) случаев.
До 2011 года большинство больных лечили по традиционной методике. Под в/в обезболиванием гнойную полость вскрывали и санировали, далее вели открыто на тампонах с мазью на водорастворимой основе, с ежедневными перевязками до появления грануляций (7–8 сутки), после чего накладывали вторичные швы, если пациентки не выписывались раньше.
Таким способом лечено 170 (78,7%) пациенток из них: вторичный шов на рану наложен 31 (14,3%), выписаны на амбулаторное лечение с гранулирующей раной 139 (64,3%), в связи с этим у трети больных лактация была прервана искусственно.
У 7 (3,2%) больных выполняли иссечение гнойника в пределах здоровых тканей с первичным швом кожной раны и пассивным промывным дренированием. Из-за формирования остаточной полости в МЖ и по ряду других причин лактация была прервана у 4 пациенток. Еще у двух женщин отмечена значительная деформация молочной железы.
На современном этапе развития медицины, результаты лечений ОГЛМ можно и нужно улучшать, путем внедрения современных технологий.
Для достижения поставленной цели нами была разработана методика лечения ОГЛМ с приоритетным сохранением лактации (патент РФ № 2471434), основанная на двухэтапной тактике хирургического лечения, с применением аргонно-плазменной санации и коагуляции, промывного вакуумного дренирования, первично отсроченного кожного шва. Методика с 2011 года применена у 39 пациенток и заключается в следующем.
При поступлении больным после обследования и соответствующей подготовки производят вскрытие гнойника радиарным или дугообразным разрезом с традиционной хирургической обработкой деструктивной полости.
Выполняют общепринятую санацию, при этом удаляют только явные некрозы и тампонируют полость марлевой салфеткой с мазью на водорастворимой основе.
На следующие сутки в операционной под в/в наркозом выполняют повторную хирургическую обработку раны. После удаления тампона и обработки полости раствором 3% перекиси водорода вновь оценивают жизнеспособность тканей. Как правило, они жизнеспособны. С помощью АПК удаляют оставшиеся мелкие очаги некроза. Тщательно сцеживают молоко, отмечают места расположения молочных фистул (рис. 1). Рану высушивают и обрабатывают все поверхности плазменным потоком до образования тонкой коагуляционной пленки с целью санации гнойной полости. Места устьев млечных фистул подвергают более глубокой АПК, что приводит к денатурации белков и их «завариванию» (рис. 2). Для этого используют аппарат («С-350РЧ-АРГОН» производства РФ) (рис. 3).
Через отдельный кожный прокол в рану вводят перфорированный силиконовый дренаж с внутренним диаметром 5–6 мм, к которому подвязан микроирригатор
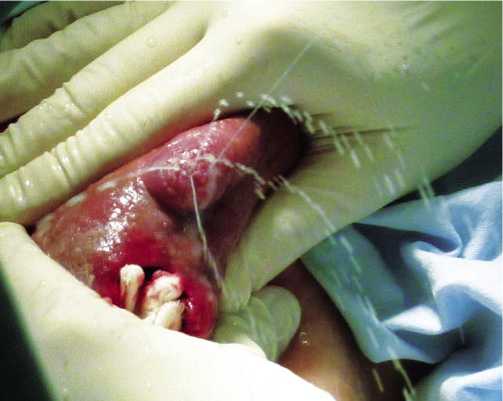
Рис. 1. Тщательно сцеживают молоко на операционном столе
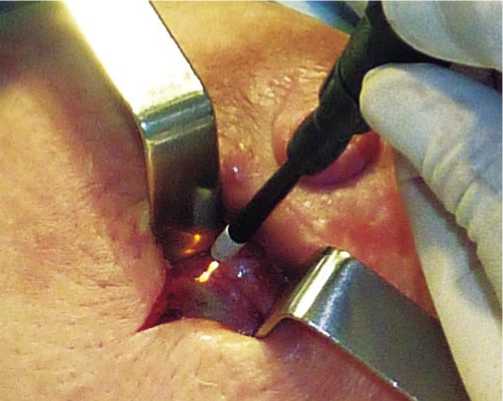
Рис. 2. Аргоновой плазмой обрабатывают стенки полости и заваривают фистулы молочных протоков

Рис. 3. Аппарат для аргоно-плазменной коагуляции С-350РЧ-АРГОН
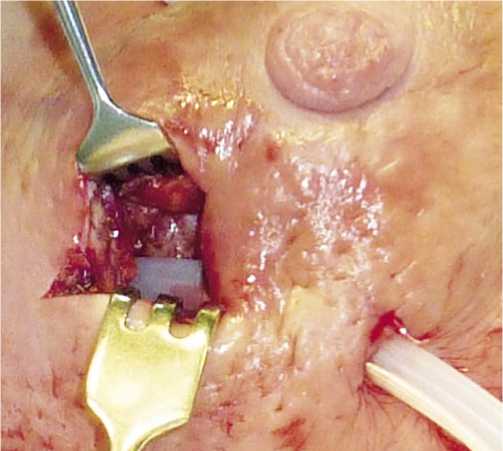
Рис. 4. В рану укладывают промывной вакуумный дренаж типа Каншина.
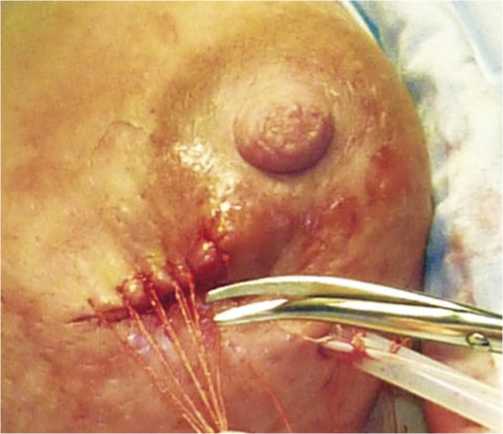
Рис. 5. Кожную рану ушивают наглухо узловыми швами
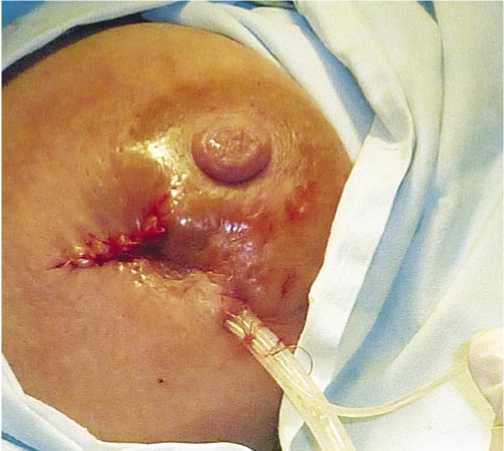
Рис. 6. При подключении активной аспирации к дренажу стенки полости спадаются
из подключичного катетера, таким образом, чтобы конец микроирригатора был в просвете дренажа у самого начала, но не выступал из него (дренаж типа Каншина) (рис. 4). Кожную рану ушивают наглухо узловыми швами (рис. 5). При подключении активной аспирации к дренажу стенки полости спадаются (рис. 6). На всех этапах лечения берут материала для бактериологического исследования.
В послеоперационном периоде осуществляют медленное капельное введение в микроирригатор 0,9% изотонического раствора натрия хлорида, а силиконовый дренаж подключают к центральному вакууму через аппарат Боброва с разряжением 120–140 см вод. ст. В комплекс лечения входит 4–6 кратное сцеживание молока в течение суток с предварительным в/м введением 2 мл но-шпы, 0,5 мл окситоцина три раза в сутки.
Течение заболевания в послеоперационном периоде оценивают по купированию системной воспалительной реакции, регрессии местных симптомов, пальпацией и УЗИ контролем уплотнений в молочной железе после сцеживания, бактериологическим исследованием молока из обеих желез, промывной жидкости, по состоянию ушитой кожной раны. Активное промывное дренирование проводят в течение 5–6 суток с удалением дренажей на 6–7 сутки.
Результаты
При бактериальном исследовании посевов из гнойного очага доминирующим возбудителем заболевания является St.Aureus, который наблюдался в 77,7% как моноинфекция и еще в 12,4% в ассоциации с другими микроорганизмами. Интраоперационные посевы молока из соска дали аналогичные результаты.
У большинства больных в ближайшие 2–3 суток после повторной обработки нормализовались показатели температуры тела, количества лейкоцитов, стихали боли. Женщины активно сцеживали молоко. На 5–6 сутки вакуумное промывное дренирование прекращали. Если дренажная трубка стояла на глубину более 6 см, то ее извлекали и вводили более короткую на глубину 3–4 см с продолжением активной аспирации еще на одни сутки. После чего дренаж извлекали окончательно, кожную рану от него не ушивали. Такая методика способствует полному закрытию дренажного хода изнутри кнаружи. Только у двух пациенток с инфильтративно-гнойным маститом (по типу пчелиных сот) местные и общие воспалительные явления не стихали, что потребовало медикаментозного прекращения лактации и дополнительного пункционного лечения под УЗ контролем. После этого гнойный процесс удалось купировать.
Все пациентки были выписаны на 7–8 сутки, кожные швы сняты на 8–9 сутки в стационаре или амбулаторно. Кожные раны зажили первичным натяжением у всех женщин, но у 2-х на пятые сутки произошло частичное прорезывание швов в результате активного сцеживания молока, что потребовало наложения дополнительных швов. В двух случаях в зоне швов на 3 и 4 сутки сформировались серо-галактомы, которые были ликвидированы дренированием резиновыми выпускниками. Формирования остаточной полости в молочной железе при контрольном УЗ исследовании не отмечено. У одной пациентки в течение трех недель функционировал молочный свищ через рану от дренажа, который закрылся самостоятельно.
Лактация в стационаре была прекращена медикаментозно у 4 больных. В одном случае во время повторной хирургической обработки при субареолярной локализации гнойной полости было обнаружено повреждение нескольких крупных центральных молочных протоков, что в послеоперационном периоде сопровождалось интенсивным отделением молока по промывному дренажу без тенденции к уменьшению. У двух женщин с «сотовым» гнойным маститом с вовлечением двух квадрантов железы процесс удалось купировать с помощью нескольких лечебных пункций под УЗ навигацией. Еще одна пациентка 42 лет с фиброзно-кистозной мастопатией в анамнезе попросила прекратить лактацию в связи малым количеством молока до заболевания маститом и отказом ребенка сосать грудь.
Обсуждение
Локализацию гнойников в верхне-наружной части молочной железы в 54,8% случаев предположительно мож- но объяснить особенностями оттока лимфы из молочной железы, наличием добавочной доли и особенностями опорожнения молочной железы при вскармливании.
Дугообразный разрез на молочной железе совпадает с линиями Лангера и оставляет менее заметный рубец, поэтому он предпочтительнее с эстетической точки зрения. Но при радиарном разрезе меньше вероятность повреждения крупных молочных протоков, поэтому при субареолярных гнойниках лучше использовать этот доступ, а в остальных случаях – дугообразный.
Одномоментная эксцизия патологического очага в пределах здоровых тканей ведет к потере большого объема железистой паренхимы, пересечению молочных ходов в оставшихся пограничных долях с обильным истечением молока в рану в послеоперационном периоде, заметной деформации железы в отдаленном периоде, образовании обширного интрамаммарного рубца с вовлечением в склеротический процесс протоковой системы и вероятным нарушением последующей лактации.
Двухэтапная хирургическая тактика более приемлема по следующим соображениям. При первой операции на фоне еще не устраненного лактостаза в прилегающих долях трудно определить границы инфильтрата. Инфицированное молоко с гноем оказывает значительное давление на стенки полости деструкции и внешне после вскрытия гнойника объем девитализированных тканей выглядит более массивно, чем на самом деле. Учитывая, что на сегодняшний день нет четких критериев нежизнеспособности ткани молочной железы, на этом этапе удаляют только явные некрозы, придерживаясь принципа бережного отношения к железистой ткани и особенно к протоковой системе.
Сцеживание молока на операционном столе под наркозом позволяет полностью разрешить перифокальный лактостаз в прилегающих долях, что значительно облегчают полноценное сцеживание в послеоперационном периоде. На повторной операции в результате восстановления микроциркуляции объем истинно девитализированных тканей значительно уменьшается или их нет совсем. Поэтому удалять приходится незначительное количество пристеночных плоскостных некрозов. Для этого действия наилучшим образом подходит применение аргоноплазменной коагуляции (АПК).
Плазменная коагуляция девитализированных тканей и устьев молочных фистул, поверхностная обработка стенок раневой полости, наряду с воздействием высокой температуры плазменного потока, ультрафиолетового облучения выделяемого аргоновой плазмой и озона, который образуется из атмосферного кислорода в плазменном потоке в целом является комплексным средством обладающим мощным бактерицидным эффектом с тройным действием, независящим от вида возбудителя, его чувствительности к антибиотикам, типа дыхания или других культуральных свойств.
Наличие промывного дренирования с вакуумной аспирацией в данной методике считаем принципиально
важным по следующим соображениям. В первые 2–3 суток небольшое количество молока, все равно, попадает в рану при достаточно интенсивном ручном сцеживании, также туда происходит выделение воспалительного раневого экссудата и поступление остаточной микрофлоры из небольших заворотов и карманов при сложной конфигурации полости, что может привести к ее нагноению. Но этого не происходит, потому что наличие отрицательного давления внутри полости и трубках дренажной системы с одновременным промыванием 0,9% изотоническим раствором натрия хлорида способствует активному отведению из раны указанных жидкостей и микрофлоры. Кроме того, оно обеспечивает сближение стенок полости. Учитывая низкий уровень бактериальной обсемененно-сти раны после плазменной обработки и постоянное вымывание оставшихся микробов, такое сближение способствует заживлению полости в паренхиме железы по типу первичного натяжения с тонким внутренним рубцом и закрытием молочных свищей молодой соединительной тканью параллельно резорбции коагуляционной пленки и струпа, что так же способствует репарации кожной раны первичным натяжением.
При лечении по предлагаемой методике к плюсам закрытого ведения добавляется максимально возможное в данной ситуации сохранения ткани молочной железы, низкая вероятность формирования молочных свищей. В итоге пациентки соглашаются потерпеть возникшие временные неудобства, связанные с наличием промывного дренажа, и сохранить лактацию. Еще их привлекает отсутствие грубого рубца после лечения и сохранение объема молочной железы.
Выводы
-
1) аргоноплазменная обработка гнойной полости позволяет выполнить ее качественную санацию и коагуляцию молочных фистул, что предотвращает развитие молочных свищей;
-
2) промывное дренирование с вакуумной аспирацией способствует скорейшему заживлению раны в паренхиме железы без формирования остаточной полости и позволяет наложить первичный глухой шов на кожную рану с заживлением первичным натяжением;
-
3) комбинированное применение указанных методик позволят сократить сроки лечения, в большинстве случаев сохранить лактацию, получить хороший косметический результат.


