Методы и критерии формирования групп радиационного риска среди населения загрязнённых областей Российской Федерации и Республики Беларусь
Автор: Чекин С.Ю., Максютов М.А., Меняйло А.Н., Власов О.К., Щукина Н.В., Корело А.М., Туманов К.А., Иванов В.К.
Рубрика: Научные статьи
Статья в выпуске: 1 т.24, 2015 года.
Бесплатный доступ
Настоящая работа рассматривает проблему оптимизации мер контроля за состоянием здоровья населения в ситуациях существующего облучения. В исследовании представлен метод формирования групп радиационного риска среди облучённого населения, основанный на вычислении годовой атрибутивной доли радиации в заболеваемости злокачественными новообразованиями (ЗНО). Показано, что для заданной истории существующего облучения и для каждой локализации ЗНО существует половозрастная группа населения, имеющая максимальный радиационный риск. На примере населения загрязнённых районов Брянской области Российской Федерации и Гомельской области Республики Беларусь определены группы радиационного риска в 2014 г. Риски ЗНО щитовидной железы, молочной железы и лейкозов выбраны в качестве основных индикаторных радиационных рисков населения. Выделение групп риска разработанным методом по вышеперечисленным ЗНО позволяет оптимизировать меры контроля за здоровьем населения и мероприятия по ранней диагностике, ежегодно выбирая для этих мероприятий около 10-12% лиц из населения загрязнённых районов.
Существующее облучение, чернобыльская аэс, загрязнённая радионуклидами территория, население, злокачественные новообразования щитовидной железы, злокачественные новообразования молочной железы, лейкозы, атрибутивная доля радиации, группы риска
Короткий адрес: https://sciup.org/170170189
IDR: 170170189
Methods and criteria of formation of groups of radiation risk among the population of the contaminated regions of the Russian Federation and Republic of Belarus
The paper considers a problem of optimization of control measures on population health in existing exposure situations. The method of formation of groups of radiation risk among the exposed population based on calculation of an annual attributable radiation fraction (ARF) for cancer incidence is presented. It is shown that for the given history of the existing exposure and for each localization of cancer there is a gender and age group of the population having the maximum radiation risk. Definition of groups of radiation risk in 2014 is shown on the example of the population of the contaminated arias of the Bryansk region of the Russian Federation and the Gomel region of the Republic of Belarus. Risks of a thyroid cancer, a breast cancer and leukemia are chosen as the main indicator radiation risks of the population. Allocation of groups of risk by the developed method on above-mentioned cancers allows to optimize control measures on population health and action for early diagnostics, annually choosing for these actions about 10-12% of persons from the population of the contaminated areas.
Текст научной статьи Методы и критерии формирования групп радиационного риска среди населения загрязнённых областей Российской Федерации и Республики Беларусь
Облучение населения, обусловленное радиоактивным загрязнением территорий в результате аварии на Чернобыльской АЭС, современной системой радиологической защиты [1, 2] классифицируется как ситуация существующего облучения, к которой относится ряд требований Основных норм безопасности (ОНБ) МАГАТЭ [1].
В частности, Требование 47 ОНБ [1] устанавливает ответственность национальных Правительств по обеспечению оценки ситуаций облучения населения, требующих внимания с точки зрения радиационной защиты, а также по распределению обязанностей регулирующего органа и других компетентных органов, касающихся разработки и осуществления стратегий защиты. В ситуациях существующего облучения соответствующими полномочиями могут быть наделены органы здравоохранения.
Стратегия защиты должна включать информирование облучённых лиц «о потенциальных рисках для здоровья» ([1], п. 5.4). После завершения восстановительных мероприятий компетентные органы должны также установить тип, масштабы и продолжительность мер контроля «с надлежащим учётом остаточных радиационных рисков» ([1], п. 5.15).
Рекомендованные контрольные уровни в ситуациях существующего облучения выражаются в терминах эффективной дозы и составляют 1-20 мЗв/год [1]. Однако, эффективная доза не может использоваться для оценки реальных радиологических последствий (радиационных рисков) в конкретной облучённой популяции [2]. Эффективная доза вычисляется путём усреднения эквивалентных доз (с весами тканевых факторов) по несуществующей референсной по-
Чекин С.Ю.* - зав. лаб.; Максютов М.А. - зав. лаб., к.т.н.; Меняйло А.Н. - ст. научн. сотр., к.б.н.; Власов О.К. - зав. лаб., д.т.н.; Щукина Н.В. – научн. сотр.; Корело А.М. – ст. научн. сотр.; Туманов К.А. – зав. лаб., к.б.н.; Иванов В.К. – Председатель РНКРЗ, зам. директора по научн. работе, чл.-кор. РАН. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИРЦ» Минздрава России.
пуляции. Радиационный риск облучённого индивидуума зависит не только от дозы облучения, но и от его пола, возраста при облучении, достигнутого возраста, динамики накопления дозы облучения. Поэтому для учёта существующих в конкретной популяции радиационных рисков требуется выбрать подходящую метрику радиационного риска.
Для осуществления мер контроля за здоровьем населения соответствующие контрольные уровни могут быть выражены целым рядом метрик риска: годовой избыточный абсолютный риск (EAR) [1], годовая атрибутивная доля радиации (ARF, для этой величины используются также термины атрибутивный риск, AR, или вероятность причинной обусловленности, PC) [3], пожизненный атрибутивный риск (LAR) [1], пожизненная атрибутивная доля радиации (LARF) [4], потерянные годы жизни (YLL) [4], потерянные годы жизни на радиационно-индуцированный случай смерти (YLLRIC) [4].
Для вычисления пожизненных метрик радиационных рисков (LAR, LARF, YLL, YLLRIC) используется прогноз показателей заболеваемости и смертности в конкретной рассматриваемой популяции на длительный период – порядка 100 лет [4], что означает формальность этих метрик и существенную неопределённость их связи с будущими реальными радиологическими последствиями.
В настоящей работе рассматривается годовая атрибутивная доля радиации (ARF) в качестве метрики, в терминах которой могут формулироваться текущие контрольные уровни осуществления мер ранней диагностики злокачественных новообразований (ЗНО), т.е. критерии формирования групп радиационного риска для населения загрязнённых областей России и Белоруссии.
По данным НКДАР ООН [4], лейкозы, а также ЗНО щитовидной железы при облучении за счёт радиоизотопов йода в детском возрасте являются основными индикаторными рисками воздействия на человека ионизирующей радиации. ЗНО молочной железы – самая распространённая локализация ЗНО среди женщин в большинстве стран мира. Зависимость «доза – эффект» для этой локализации устойчиво обнаруживается и имеет линейный вид в широком диапазоне доз. Гомельская область Белоруссии и Брянская область России в наибольшей степени подверглись радиационному воздействию в результате чернобыльской катастрофы, поэтому в настоящей работе рассмотрены группы радиационного риска по вышеперечисленным локализациям ЗНО на этих территориях.
Материалы и методы
Загрязнёнными районами в Брянской области в настоящее время считаются следующие: Гордеевский, Злынковский, Климовский, Клинцовский, Красногорский, Новозыбковский, (Старо-дубский); в Гомельской области: Брагинский, Буда-Кошелевский, Ветковский, Добрушский, Ель-ский, Кормянский, Наровлянский, Хойникский, Чечерский. Численность населения представлена в табл. 1.
Таблица 1
Численность населения загрязнённых районов Брянской и Гомельской областей в 2013 г.
|
Пол |
Население загрязнённых районов Брянской обл., чел. |
Население загрязнённых районов Гомельской обл., чел. |
|
Муж. |
97376 |
92380 |
|
Жен. |
114753 |
106768 |
|
Всего |
212129 |
199148 |
Методы вычисления радиационных рисков
Для прогноза радиационных рисков заболеваемости ЗНО использовались два типа моделей: 1) модель Рекомендаций Международной комиссии по радиологической защите 2007 г. (Публикация 103 МКРЗ) [2] – в дальнейшем тексте эта модель будет называться «модель МКРЗ»; 2) модель Научного комитета по действию атомной радиации при Организации Объединённых Наций (НКДАР ООН) [4] – в дальнейшем тексте эта модель будет называться «модель НКДАР».
Обе модели радиационных рисков записываются через интенсивные показатели радиационно-обусловленной заболеваемости.
В отсутствии облучения основным показателем риска является показатель фоновой или спонтанной онкологической заболеваемости Л о , т.е. частота заболеваний в год. Воздействие радиации приводит к увеличению Л 0 на дополнительную величину X R . Полный показатель риска Л является суммой фонового показателя и радиационной добавки:
Л = Л о + Л R . (1)
Модели МКРЗ и НКДАР используют фоновые показатели для локализации l , зависящие от достигнутого возраста а и пола s : т.е. Ло = Л о ( / , a, s) . Радиационный риск при этом зависит от локализации l , пола s , эквивалентной дозы d , возраста на момент облучения g и достигнутого возраста a :
Л ( g , a , /, s, d ) = Л о ( a , /, s ) + A R ( g , a , /, s, d ) .
Радиогенный риск Л R вносит вклад в полный риск в двух формах: аддитивной и мультипликативной. В аддитивной модели полный риск есть:
Л = Ло + EAR
(2а)
где Л R = EAR - избыточный абсолютный риск (Excess Absolute Risk), обусловленный радиационным облучением.
В мультипликативной модели полный риск записывается в виде:
Л = Ло ■ ( 1 + ERR ) , (2б)
где Л/ ?= Л о ^ ERR , ERR - избыточный относительный риск (Excess Relative Risk) или отношение избыточного абсолютного риска к фоновому показателю:
EAR
ERR = ---
Л о
.
После облучения радиационный риск, как EAR , так и ERR , могут диагностироваться только через определённое время – латентный период T LS . В настоящее время принято модельное приближение, в котором T LS не зависит от типа используемой модели – EAR или ERR.
Для получения модели риска в МКРЗ использовалась в основном когорта LSS ([2] A108). Для переноса модели рисков на другие популяции величина избыточного абсолютного риска заболеваемости солидными ЗНО в модели МКРЗ получается как взвешенное среднее аддитивной и мультипликативной моделей. Аддитивная модель даёт величину риска в форме EAR, а мультипликативная модель даёт величину риска в форме ERR:
EAR inc = p ■ ERR mult ■ Ло + ( 1 - p ) ■ EAR add или по-другому, с учётом (3):
EAR inc = p ■ EAR mult + ( 1 - p ) ■ EAR add . (4)
Здесь p – весовой множитель, зависящий от локализации опухоли ([2] A140), абсолютный избыточный риск аддитивной модели МКРЗ:
R .. (I Y я A Ю add ( 1 )
EAR add ( g, a, l, s , D ) =■ D ■ в add s ) ■[ — I ■ exp [ a add ( l ) ■ ( g - 30 ) ] , (5)
10 4 V 70 J абсолютный избыточный риск мультипликативной модели МКРЗ 2007:
innc V mmult ( ' )
EAR mult ( g , a , l , s , D ) = ^ ( ' ’ s ’ a ) ■ D ■ в ™» ( ' , s ) ■ I — I ■ exp [ a ( ' ) ■ ( g - 30 ) ] • (6)
10 5 V 70 J
В формулах (5) и (6): l – локализация ЗНО; s – пол; g – возраст при облучении; a – возраст дожития; D - доза облучения; p mult , romult , amult - параметры мультипликативной модели; padd , гоadd , aadd - параметры аддитивной модели.
В Рекомендациях МКРЗ [2] параметры a тик и aadd непосредственно не приводятся. Однако там приведены величины, которые ниже обозначены /mult и yadd . Эти параметры даются в виде процента изменения ERR mult и EAR add соответственно, при увеличении возраста при облучении на десятилетие ([2] таблицы A4.6, A4.7). Исходя из этого и вида формул (5) и (6), параметры amult и aadd можно вычислить по следующим формулам:
(1 In Г 1 m mult ( l )1 ■ (i\ 1 In fl Y add ( l )1
a mult ( l ) = ■ ln I 1 + I ; a add ( l ) = ■ ln I 1 + I •
10 V 100 J 10 V 100 J
Параметры p mwt , ® mU lt , y muk , в add , ® add , y add для ЗНО молочной железы и щитовидной железы приведены ниже в табл. 2.
Латентный период для солидных ЗНО, T LS , в модели МКРЗ равен 10-ти годам. То есть, в течение 10 лет после облучения избыточные риски, как по мультипликативной, так и по аддитивной моделям, принимаются равными нулю.
Таблица 2
Параметры модели радиационного риска заболеваемости для ЗНО молочной железы и щитовидной железы по модели МКРЗ 2007 [2]
|
Локализация опухоли |
Пол |
P mult |
Y mult |
COmuit |
P add |
Y add |
COadd |
|
Молочная железа |
Жен. |
0,87 |
0 |
-2,26 |
10,9 |
-39 |
3,5 |
|
Щитовидная железа |
Муж. Жен. |
0,53 1,05 |
-56 |
0,00 |
0,69 2,33 |
-24 |
0,01 |
Избыточный абсолютный риск возникновения ЗНО локализации l после однократного облучения EARS с учётом (4) можно записать в виде:
EARS ( g , a , l , s , D ) = p ( l ) ■ EAR mult ( g , a , l , s , D ) + ( 1 - p ( l )) ■ EAR add ( g , a , l , s , D ) .
Здесь p - весовой множитель, равный 0 для ЗНО молочной железы и 1 - для ЗНО щитовидной железы ([2] A140).
Сравнивая модели МКРЗ [2] и НКДАР [4] для щитовидной железы, следует отметить, что риск заболеваемости ЗНО щитовидной железы по модели НКДАР в возрасте при облучении 0 стремится к бесконечности, т.е. риск в возрасте до 1 года имеет большую неопределённость. Поэтому модель НКДАР риска ЗНО щитовидной железы в дальнейшем использоваться не будет.
Процедура переноса риска на другие популяции, в соответствии с рекомендациями МКРЗ [2], в моделях НКДАР не используется. Аддитивная модель риска НКДАР для ЗНО молочной железы при однократном облучении записывается следующим образом:
EARS ( a , g , D ) = D • а • exp [ к 1 • In ( a - g ) ]
а = 1,94038 x 10 - 5 • Зв - 1 • год - 1 (7)
г, = 1,086
где a - достигнутый возраст; g - возраст на момент облучения, D - доза облучения в возрасте g ; абсолютный риск EAR имеет размерность 1/100 тыс. чел.-лет.
Вычисления показывают, что модель риска НКДАР для ЗНО молочной железы является более консервативной, чем модель МКРЗ, поэтому в дальнейшем для ЗНО молочной железы будет использоваться модель НКДАР.
При пролонгированном облучении полный избыточный абсолютный риск EAR в достигнутом возрасте a будет складываться из рисков в этом возрасте, обусловленных однократными облучениями в каждом году проживания на загрязнённой территории:
Д a - T LS
EAR ( g , a , l , s , D ) = ----------- У EARS ( e , a , l , s , De ) ; a > e ,
DDREF e e = g где g - возраст начала облучения; a - достигнутый возраст; De - доза облучения, полученная жителем в возрасте e; D - накопленная доза облучения; l - локализация опухоли; s - пол; DDREF- коэффициент эффективности дозы и мощности дозы, учитывающий уменьшение риска в случае хронического облучения или облучения в малой дозе, DDREF=2 для модели МКРЗ и DDREF=1 для модели НКДАР.
Избыточный абсолютный риск (EAR) для лейкозов в заданном достигнутом возрасте вычисляется суммированием вкладов в EAR от облучений в предшествовавших возрастах по аддитивной модели доклада НКДАР 1994 г. [5] (стр. 48, ф-ла 14):
-
a - 2
EAR( s, a, g ,D) = y {a s (t) • D t (1 + 0,79 • D) • exp( в (t) • (a - t - 25))} , (9) t=g где a - достигнутый возраст; g - возраст на начало облучения; t - возраст на момент облучения Dt - доза облучения в возрасте t; абсолютный риск EAR имеет размерность 1/100 тыс. чел.-лет и зависит от времени t=a–g, прошедшего после облучения; латентный период для лейкозов принят равным 2 (двум) годам.
Для лейкозов зависимость от дозы является линейно-квадратичной. Наибольшие риски наблюдаются по истечении латентного периода. В табл. 3 приведены значения параметров a и
β . В данной модели риски зависят от времени, прошедшего после облучения. Риски после облучения со временем уменьшаются – параметр β входит в (9) с отрицательным знаком. Так, у мужчин характерное время спада риска τ составляет от 6-14 лет, у женщин – 14-33 года. Кроме того, зависимость риска от возраста при облучении g аппроксимируется ступенчатой зависимостью (табл. 3).
Таблица 3
Значения параметров избыточного абсолютного риска EAR заболеваемости лейкозами
|
Возраст t , лет |
Мужчины |
Женщины |
||||
|
а , Зв-1 |
β , год-1 |
τ , год |
а , Зв-1 |
β , год-1 |
τ , год |
|
|
0-19 |
3,3 |
-0,17 |
5,9 |
6,6 |
-0,07 |
14,3 |
|
20-39 |
4,8 |
-0,13 |
7,9 |
9,7 |
-0,03 |
33,3 |
|
> 39 |
13,1 |
-0,07 |
14,3 |
26,4 |
0,03 |
33,3 |
Обозначим наблюдаемые в облучённой группе лиц возрастные показатели заболеваемости следующим образом:
OIR(a,g,D)= X ( a ) +EAR(a,g,D) , (10)
где a – достигнутый возраст (возраст здорового дожития); g – возраст на начало облучения; a > g ; D - доза, Гр; X ( a) - фоновый показатель заболеваемости в достигнутом возрасте а .
Годовая атрибутивная доля радиации в риске (атрибутивный риск), ARF , является отношением:
ARF
EAR (a , g , D )
( a , g , D ) = ---------------------,
OIR ( a, g, D )
где обозначения соответствуют (9).
Метод определения групп радиационного риска среди населения областей России и Белоруссии, подвергшихся радиационному загрязнению
Определение групп радиационного риска проводится ежегодно, по следующим шагам:
-
1) Наблюдавшиеся для населения загрязнённых областей России и Белоруссии возрастные показатели заболеваемости ЗНО на текущий год (или на год, ближайший к текущему, если на текущий год показатели не доступны) OIR ( a,g,D ) находятся по доступным национальным статистическим данным для этих областей. Если по доступным национальным данным ширина возрастных групп по достигнутому возрасту a превышает один год, внутри каждой такой возрастной группы показатель заболеваемости считается постоянным. Важно отметить, что эти наблюдаемые показатели не являются фоновыми ( X ( a ) ) и уже содержат избыточный абсолютный риск, зависящий от дозы D и возраста на начало облучения g .
-
2) Набор показателей OIR ( a,g,D ) применяется проспективно в календарном году, следующем за текущим (в прогнозируемом году).
-
3) В прогнозируемом году каждой возрастной группе населения ставится в соответствие годовая атрибутивная доля радиации в заболеваемости:
EAR ( a , g , D ) ARF ( a, g, D ) = ---------------,
OIR ( a, g, D )
где a - средний достигнутый возраст в возрастной группе в прогнозируемом году; g - возраст на начало облучения в возрастной группе; D - накопленная доза в возрастной группе для возраста на начало облучения g ; EAR ( a,g,D ) - избыточный радиационный риск.
-
4) Проводится усреднение величины ARF ( a,g,D ) по возрасту на начало облучения g и дозе D :
1 N
ARF ( a ) = —- 2 ARF ( a- g, - D ,) , N / .1
где i - индекс, соответствующий отдельному человеку; N - численность возрастной группы a .
-
5) В качестве критерия определения групп радиационного риска выбирается достигнутый возраст в прогнозируемом году.
-
6) Значения критерия определения групп радиационного риска устанавливаются следующим образом.
6а) Группу радиационного риска (ГР) в прогнозируемом году представляют те возрастные группы населения, для которых сопоставленные им усреднённые годовые атрибутивные доли { ARF ( a ) } (12) составляют более 50% от глобального максимума усреднённой величины ARF ( a ) на всём интервале достигнутых в прогнозируемом году возрастов a :
a е {ГР}: { ARF ( a )} > O,5-Max a ( ARF ( a )) . (14)
6б) Группу повышенного радиационного риска (ГПР) в прогнозируемом году представляют те возрастные группы населения, для которых сопоставленные им усреднённые годовые атрибутивные доли { ARF ( a ) } (12) составляют более 80% от глобального максимума усреднённой величины ARF s ( a ) на всём интервале достигнутых в прогнозируемом году возрастов a :
a е {ГПР}: { ARF ( a )} > O,8-Max a ( ARF ( a )) . (15)
Контрольные уровни ARF ( a ) 50% и 80% определяют ширину диапазона достигнутых возрастов для ГР и ГПР и установлены для населения загрязнённых районов Брянской и Гомельской областей таким образом, чтобы ширина этих возрастных групп не превышала 20 лет и 5 лет соответственно. Контрольные уровни ARF ( a ) могут корректироваться, исходя из конкретных практических возможностей проведения медицинского скрининга по той или иной локализации ЗНО.
-
7) С изменением текущего календарного года находятся новые актуальные значения OIR ( a,g,D ) по данным национальной статистики, величины EAR ( a,g,D ) вычисляются заново и шаги 1) - 6а, б) повторяются.
Результаты
На рис. 1 приведён пример расчёта прогнозной величины годовой атрибутивной доли радиации ARF ( a ) (13) в риске заболеваемости ЗНО щитовидной железы, на 2014 г., по данным о населении загрязнённых районов Гомельской области в 2013 г. Дозы на щитовидную железу для населения Гомельской области основаны на данных каталога [7].
В качестве ГР в 2014 г. выбираются группы населения с годовой атрибутивной долей >34,6%:
а е {ГР}: { ARF ( a )} > 0,5-Maxa( ARF ( a ))=0,5-69,2%=34,6%, т.е.:
мужчины в возрасте от 28 лет (ARF=54,9%) до 32 лет (ARF=34,6%) - 5961 чел., женщины в возрасте от 28 лет (ARF=54,9%) до 35 лет (ARF=36,8%) - 10817 чел.;
в качестве ГПР в 2014 г. выбираются возрастные группы населения с годовой атрибутивной долей >55,4%:
а е {ГПР}: { ARF ( a )} > 0,8-MaX a ( ARF ( a ))=0,8-54,9%=55,39%=55,4%, т.е.:
мужчины в возрасте 28 лет (ARF=54,9%) - 985 чел., женщины в возрасте от 28 лет (ARF=54,9%) до 31 года (ARF=57,4%) - 5319 чел.
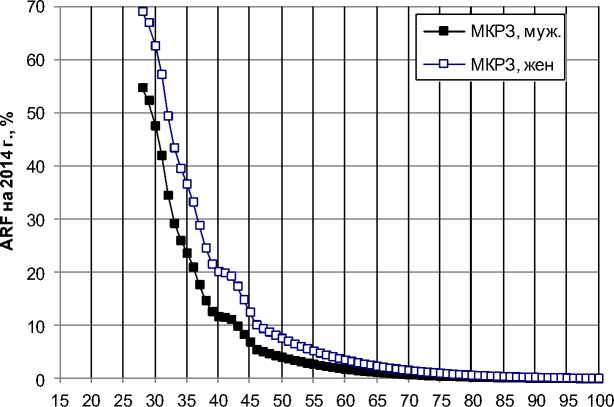
Возраст в 2014 г., лет
Рис. 1. Прогнозная величина годовой атрибутивной доли радиации ARF(a) в риске заболеваемости ЗНО щитовидной железы для населения загрязнённых районов Гомельской области, на 2014 г.; Maxa( ARF ( a ))=69,2%, женщины в возрасте 28 лет.
Численность ГР и ГПР рассчитана по табл. 4, где приведён половозрастной состав населения загрязнённых районов Брянской и Гомельской областей в 2013 г.
Аналогичные вычисления дают состав и численность групп радиационного риска (ГР) для населения загрязнённых районов Брянской и Гомельской областей на 2014 г., по заболеваемости ЗНО щитовидной железы (РЩЖ), ЗНО молочной железы (РМЖ) и по лейкозам (табл. 5). По данным НКДАР [6], риски ЗНО щитовидной железы, молочной железы и лейкозов являются основными индикаторными радиационными рисками населения.
Таблица 4
Половозрастной состав населения загрязнённых районов Брянской и Гомельской областей в 2013 г. (15-44 года)
Состав и численность групп радиационного риска (ГР) для населения загрязнённых районов Брянской и Гомельской областей на 2014 г., по локализациям ЗНО
|
Возраст, лет |
Население загрязнённых районов Брянской обл., чел. |
Население загрязнённых районов Гомельской обл., чел. |
||
|
муж. |
жен. |
муж. |
жен. |
|
|
15 |
1452 |
1490 |
1495 |
1217 |
|
16 |
1452 |
1490 |
1495 |
1217 |
|
17 |
1452 |
1490 |
1495 |
1217 |
|
18 |
1452 |
1490 |
1495 |
1217 |
|
19 |
1452 |
1490 |
1495 |
1217 |
|
20 |
1371 |
1399 |
1421 |
1266 |
|
21 |
1371 |
1399 |
1421 |
1266 |
|
22 |
1371 |
1399 |
1421 |
1266 |
|
23 |
1371 |
1399 |
1421 |
1266 |
|
24 |
1371 |
1399 |
1421 |
1266 |
|
25 |
1458 |
1488 |
985 |
1265 |
|
26 |
1458 |
1488 |
985 |
1265 |
|
27 |
1458 |
1488 |
985 |
1265 |
|
28 |
1458 |
1488 |
985 |
1265 |
|
29 |
1458 |
1488 |
985 |
1265 |
|
30 |
1491 |
1477 |
1331 |
1395 |
|
31 |
1491 |
1477 |
1331 |
1395 |
|
32 |
1491 |
1477 |
1331 |
1395 |
|
33 |
1491 |
1477 |
1331 |
1395 |
|
34 |
1491 |
1477 |
1331 |
1395 |
|
35 |
1498 |
1411 |
1379 |
1314 |
|
36 |
1498 |
1411 |
1379 |
1314 |
|
37 |
1498 |
1411 |
1379 |
1314 |
|
38 |
1498 |
1411 |
1379 |
1314 |
|
39 |
1498 |
1411 |
1379 |
1314 |
|
40 |
1631 |
1609 |
1445 |
1316 |
|
41 |
1631 |
1609 |
1445 |
1316 |
|
42 |
1631 |
1609 |
1445 |
1316 |
|
43 |
1631 |
1609 |
1445 |
1316 |
|
44 |
1631 |
1609 |
1445 |
1316 |
Таблица 5
|
Локализация ЗНО |
Состав ГР |
Загрязнённые районы Брянской обл., чел. |
Загрязнённые районы Гомельской обл., чел. |
Всего |
||
|
муж. |
жен. |
муж. |
жен. |
|||
|
РЩЖ |
Возраст, лет Численность, чел. |
28-29 2917 |
28-31 5931 |
28-32 5961 |
28-35 10817 |
25626 |
|
РМЖ |
Возраст, лет Численность, чел. |
16-19 5959 |
16-24 11200 |
17159 |
||
|
Лейкозы |
Возраст, лет Численность, чел. |
26-44 28933 |
27-39 18903 |
26-44 24709 |
27-44 23918 |
96463 |
Выводы
Показано, что для заданной истории существующего облучения и для каждой локализации ЗНО существует половозрастная группа населения, имеющая максимальный радиационный риск (годовую атрибутивную долю радиации, ARF) в заданном календарном году.
На основании вышесказанного предложены следующие критерии формирования групп радиационного риска в ситуациях существующего облучения:
-
■ Группу радиационного риска (ГР) в данном году представляют те возрастные группы населения, для которых сопоставленные им годовые атрибутивные доли ARF составляют более 50% от максимума величины ARF на всём интервале достигнутых в этом году возрастов.
-
■ Группу повышенного радиационного риска (ГПР) в данном году представляют те возрастные группы населения, для которых сопоставленные им годовые атрибутивные доли ARF составляют более 80% от максимума величины ARF на всём интервале достигнутых в этом году возрастов.
Для населения загрязнённых районов Брянской области России и Гомельской области Белоруссии:
-
■ Группы радиационного риска (ГР) по заболеваемости ЗНО молочной железы (рак молочной железы, РМЖ) и по заболеваемости ЗНО щитовидной железы (рак щитовидной железы, РЩЖ) не пересекаются и имеют разный возрастной состав: для РМЖ – суммарно от 16 до 24 лет, а для РЩЖ – суммарно от 28 до 35 лет.
-
■ Общая численность ГР РМЖ и ГР РЩЖ для населения загрязнённых районов Брянской области России и Гомельской области Белоруссии на 2014 г. составила 42785 человек, т.е. 10,4% от общей численности населения 411277 человек.
-
■ ГР по лейкозам для населения загрязнённых районов Брянской области России и Гомельской области Белоруссии включает ГР по РЩЖ.
-
■ Хотя общая численность ГР по лейкозам на 2014 г. составила 96463 человека, т.е. 23,5% от общей численности населения, годовая атрибутивная доля радиации (ARF) в риске заболеваемости лейкозами для населения загрязнённых районов Брянской области России не превышает 5% (максимальное значение ARF – 4,8%), что не позволяет статистически значимо связать избыточный риск с радиационным воздействием.
-
■ Таким образом, ГР по лейкозам может быть сужена до 48627 человек, проживающих в Гомельской области (11,8% от общей численности населения загрязнённых районов).
Выделение ГР разработанным методом по вышеперечисленным ЗНО позволяет оптимизировать меры контроля за здоровьем населения и мероприятия по ранней диагностике, ежегодно выбирая для этих мероприятий около 10-12% лиц из населения загрязнённых районов, имеющих максимальные радиационные риски.
Работа выполнена в рамках Программы совместной деятельности по преодолению последствий чернобыльской катастрофы в рамках Союзного государства на период до 2016 г. в 2014 г. по теме «Оценка радиационных рисков и прогнозирование медицинских радиологических последствий для граждан России и Беларуси, подвергшихся радиационному воздействию вследствие чернобыльской катастрофы, на базе Единого чернобыльского регистра России и Беларуси».
Список литературы Методы и критерии формирования групп радиационного риска среди населения загрязнённых областей Российской Федерации и Республики Беларусь
- Радиационная защита и безопасность источников излучения: Международные основные нормы безопасности. Промежуточное издание. Общие требования безопасности. Серия норм МАГАТЭ по безопасности № GSR Part 3 (Interim). Вена: МАГАТЭ, 2011. 311 с.
- Публикация Международной комиссии по радиационной защите (МКРЗ): пер. с англ./Под общей ред. М.Ф. Киселёва и Н.К. Шандалы. М.: Изд. ООО ПКФ «Алана», 2009. 312 с.
- Methods for estimating the probability of cancer from occupational radiation exposure, IAEA-TECDOC-870. Vienna: IAEA, 1996. 55 p.
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR) 2006 report. Effects of ionizing radiation. Volume I: Report to the General Assembly, Scientific annexes A and B. New York: United Nations, 2008. 383 p.
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR) 1994 Report to the General Assembly, with Scientific Annexes. Sources and effects of ionizing radiation. New York: United Nations, 1994. 272 p.
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR) 2013 report. Sources, effects and risks of ionizing radiation. Volume I: Report to the General Assembly, Scientific annex A, Levels and effects of radiation exposure due to the nuclear accident after the 2011 great east-Japan earthquake and tsunami. New York: United Nations, 2014. 311 p.
- Каталог годовых эффективных доз облучения в 2004 г. (ГЭДкр-2004) жителей населённых пунктов Республики Беларусь, отнесённых к зонам радиоактивного загрязнения по Постановлению Совета Министров Республики Беларусь № 714 от 30.05.2003 г. «О внесении изменений и дополнений в Постановление СМ Республики Беларусь от 8.08.2002 г. № 1076» (для целей зонирования).


