Методы ультрафильтрации как способ регуляции гидробаланса при коррекции транспозиции магистральных артерий у новорожденных детей
Автор: Фуражков Денис Александрович, Свалов Алексей Игоревич, Захаров Евгений Витальевич, Булдакова Татьяна Львовна, Левит Александр Львович, Казанцев Константин Борисович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Органопротекция
Статья в выпуске: 3 т.18, 2014 года.
Бесплатный доступ
Коррекция врожденных пороков сердца у новорожденных детей в условиях искусственного кровообращения сопровождается перегрузкой жидкостью. Для устранения этого патологического состояния используется метод ультрафильтрации. Представлен анализ коррекции в 2009-2012 гг. 20 новорожденных с транспозицией магистральных артерий с использованием двух методов ультрафильтрации во время искусственного кровообращения: I группа (n = 10) - ультрафильтрация, модифицированная ультрафильтрация после остановки искусственного кровообращения - II группа (n = 10). Полученные данные свидетельствуют, что в группе, где выполнялась модифицированная ультрафильтрация, индекс инотропной поддержки, потребность в проведении гемотрансфузии в ближайшем послеоперационном периоде, время нахождения пациента на ИВЛ достоверно ниже, чем в группе с ультрафильтрацией.
Транспозиция магистральных артерий, ультрафильтрация, модифицированная ультрафильтрация
Короткий адрес: https://sciup.org/142140616
IDR: 142140616 | УДК: 616
Ultrafiltration as a method for regulating the volume balance during correction of transposition of great vessels in newborns
Correction of congenital heart disease in newborns under extracorporeal circulation is accompanied by fluid overload. To eliminate this pathological state, the method of ultrafiltration is commonly used. The paper presents a comparative analysis of two methods of ultrafiltration in the arterial switch procedure in 20 newborns with transposition of the great vessels. In group I (n = 10) we conducted conventional ultrafiltration during cardiopulmonary bypass; and in group II (n = 10), modified ultrafiltration after completing the cardiopulmonary bypass was used. The data obtained indicate that the inotropic support, the need in blood transfusion during the immediate follow-up and the mechanical ventilation duration were significantly lower during modified ultrafiltration as compared to conventional one.
Текст научной статьи Методы ультрафильтрации как способ регуляции гидробаланса при коррекции транспозиции магистральных артерий у новорожденных детей
Коррекция врожденных пороков сердца у новорожденных детей в условиях искусственного кровообращения сопровождается перегрузкой жидкостью. Для устранения этого патологического состояния используется метод ультрафильтрации. Представлен анализ коррекции в 2009–2012 гг. 20 новорожденных с транспозицией магистральных артерий с использованием двух методов ультрафильтрации во время искусственного кровообращения: I группа (n = 10) – ультрафильтрация, модифицированная ультрафильтрация после остановки искусственного кровообращения – II группа (n = 10). Полученные данные свидетельствуют, что в группе, где выполнялась модифицированная ультрафильтрация, индекс инотропной поддержки, потребность в проведении гемотрансфузии в ближайшем послеоперационном периоде, время нахождения пациента на ИВЛ достоверно ниже, чем в группе с ультрафильтрацией. Ключевые слова: транспозиция магистральных артерий; ультрафильтрация; модифицированная ультрафильтрация.
Во всем мире ежегодно возрастает количество операций, проведенных по поводу врожденных пороков сердца (ВПС), в том числе выполненных в периоде новорож-денности. В Российской Федерации в 2012 г. выявлено 1 380 ВПС на 100 тыс. населения детского возраста [1].
Одной из основных интраоперационных проблем, стоящих перед анестезиологом и перфузиологом, является нарушение гидробаланса у ребенка и его коррекция. Причинами перегрузки жидкостью могут быть физиологические особенности детей (физиологическая гидрофильность тканей, несовершенность функций почек, а также их послеоперационное повреждение), проведение искусственного кровообращения (ИК) (несоответствие объема циркулирующей крови (ОЦК) ребенка и первичного объема заполнения контура аппарата ИК, введение экзогенных жидкостей, несовместимость материалов контура ИК и крови пациента, что, в свою очередь, может запустить ферментативный каскад, приводящий к развитию синдрома капиллярной утечки) [3].
Устранить это патологическое состояние можно двумя методами ультрафильтрации: ультрафильтрацией (УФ) во время ИК и модифицированной ультрафильтрацией (МУФ) [6, 8].
Положительными эффектами ультрафильтрации, по данным литературы, являются: уменьшение отека миокарда, повышение артериального давления, уменьшение частоты сердечных сокращений, снижение центрального венозного давления, уменьшение потребности в инотропах [7], улучшение оксигенации и уменьшение внесосудистой воды в легких [4], уменьшение выраженности постперфузионной системной воспалительной реакции (снижение содержания в плазме провоспалительных цитокинов), повышение клиренса креатинина и уменьшение общего содержания воды в организме [2, 7], повышение гематокрита (Ht) и факторов свертывания в плазме, тем самым – снижение использования трансфузионных сред [5].
В настоящее время продолжается активное изучение использования ультрафильтрации в практике детской кардиоанестезиологии. Нам представляется интересным оценить эффективность ультрафильтрации в комплексе анестезиологического обеспечения при проведении коррекции транспозиции магистральных артерий (ТМА) у новорожденных детей в условиях ОКБ № 1. Цель исследования – оценить эффективность двух методов ультрафильтрации при коррекции транспозиции магистральных артерий у новорожденных детей.
Таблица 1
Распределение детей по возрасту и массе тела
Таблица 2
Интраоперационная динамика гемоглобина и гематокрита, темп дренажных потерь первых послеоперационных суток
|
Показатель |
Группа УФ, n = 10 |
Группа МУФ, n = 10 |
р |
|
Гемоглобин, г/л |
|||
|
исходный |
144,5 (123; 156) |
127 (123; 143) |
>0,05 |
|
после ИК |
90,5 (89; 110) |
137 (113,5; 155,0) |
<0,05 |
|
Гематокрит, % |
|||
|
исходный |
40,5 (34; 46) |
39,5 (37,5; 39,5) |
>0,05 |
|
после ИК |
27,5 (23; 30) |
39,5 (32,5; 43,0) |
<0,05 |
|
Темп дренажных потерь, мл/кг/ч |
0,73 (0,52; 1,97) |
0,58 (0,46; 1,04) |
>0,05 |
Таблица 3
Влияние методов ультрафильтрации на течение периопераци-онного периода
|
Показатель |
Группа УФ, n = 10 |
Группа МУФ, n = 10 |
р |
|
Длительность пережатия аорты, мин |
50,5 (44,5; 53,0) |
61 (49; 69) |
>0,05 |
|
Длительность ИК, мин |
85,5 (79,5; 138,0) |
107 (99; 119) |
>0,05 |
|
Длительность ИВЛ, ч |
244,5 (213; 336) |
124,5 (90,5; 229,5) |
<0,05 |
|
Длительность в ОАР, ч |
288 (260; 333) |
190 (128,5; 318,0) |
0,067 |
|
Показатель |
Группа УФ, n = 10 |
Группа МУФ, n = 10 |
р |
|
Возраст, сутки |
13,5 (11,5; 15,0) |
5,0 (4,5; 12,5) |
<0,05 |
|
Масса тела, кг |
3,28 (2,9; 3,87) |
3,33 (2,97; 3,49) |
>0,05 |
Материал и методы
В исследование включены 20 новорожденных пациентов с транспозицией магистральных артерий, оперированных в ГБУЗ «СОКБ № 1» с 2006 по 2012 г. Все дети разбиты на две группы. Первую группу составили 10 пациентов, которым проводилась УФ во время искусственного кровообращения, вторую группу – пациенты, которым проводилась МУФ после остановки ИК.
Методика проведения УФ во время ИК: забор крови из аорты в гемофильтр путем создания разрежения в нем до 40 мм вод. ст., со скоростью 20–50 мл/мин; возврат крови осуществлялся в венозный резервуар. Объем ультрафильтрата составил в первой группе 52,7 (33,1; 77,6) мл/кг. Процедуру УФ проводили до достижения Ht 30%.
Методика проведения МУФ: после остановки ИК забор крови из аорты в гемофильтр путем создания разрежения в нем до 40 мм вод. ст., со скоростью 100–250 мл/мин; возврат крови осуществлялся в полую вену. Время МУФ составило 13,5 (11; 15) мин. Объем ультрафильтрата – 64,8 (50,0; 94,5) мл/кг. Процедуру МУФ прекращали при достижении Ht 40%.
Всем пациентам выполнено артериальное переключение магистральных артерий в условиях искусственного кровообращения (с перфузионным индексом 2,5–3,0 л/мин/м2) и умеренной гипотермией (32 (31; 32) °С) с окклюзией аорты, кровяной фармакохолодовой кардиоплегией. Во всех случаях проводилась тотальная внутривенная анестезия (мидазолам 0,2 мг/кг на индукцию и 0,1 мг/кг/ч поддержание, фентанил 10 мкг/кг/ч, ардуан 0,05 мг/кг на индукцию и 0,02 мг/кг/ч поддержание). В периопе-рационном периоде – стандартный анестезиологический мониторинг.
Динамику показателей кровообращения и лабораторные данные оценивали на восьми этапах: I – до операции (исходные данные); II – перед ИК; III – после ИК; IV – после МУФ; V – после операции; VI – через 6 ч после операции; VII – через 24 ч после операции; VIII – через 48 ч после операции.
Статистическую обработку данных проводили с помощью пакета статистических программ StatPlus Professional 5.8. При межгрупповых сравнениях использовали T-тест Вилкоксона, U-тест Манна – Уитни. Достоверными считали результаты при достижении уровня значимости p <0,05. Результаты представлены в виде медианы (М) и процентилей (25; 75).
Результаты и обсуждение
Исследуемые группы были сопоставимы по массе пациентов, но достоверно отличались по возрасту (табл. 1). В инотропной поддержке до операции нуждались 50% пациентов второй группы, в отличие от 10% в первой. Для оценки потребности пациента в инотропных препаратах мы использовали индекс инотропной поддержки (IS) – сумма доз кардиотонических препаратов, мкг/кг/мин, умноженных на поправочный коэффициент, который для допамина и добутамина – 1, адреналина и норадреналина – 100. После проведения коррекции ТМА IS был достоверно выше в группе ультрафильтрации сразу после операции и сохранялся высоким к концу вторых суток после операции ( рисунок ).
Объем ультрафильтрации и гидробаланс на момент окончания ИК рассчитывали в мл/кг. Объем ультрафильтрата между группами достоверно не различался, составив в первой группе 52,7 (33,1; 77,6) мл/кг, во второй 64,8 (50,0;
Индекс инотропной поддержки: 1 – исходно;
-
2 – до ИК; 3 – после ИК;
-
4 –после МУФ; 5 – п/о;
-
6 – через 6 ч; 7 – через 24 ч; 8 – через 48 ч.
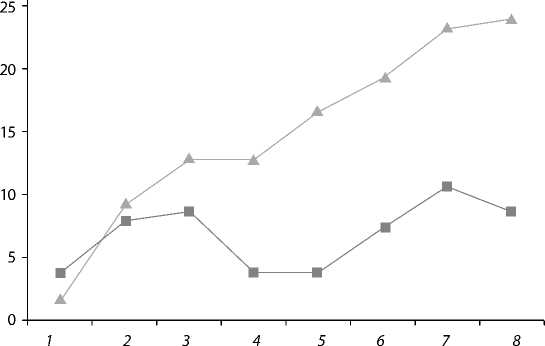
-*- УФ
—■— МУФ
-
94,5) мл/кг. При окончании ИК в группе МУФ получен отрицательный гидробаланс, а в группе УФ положительный. Гидробаланс к окончанию первых послеоперационных суток в обеих группах был положительным и не различался между группами. Инфузионная терапия в течение первых суток достоверно отличалась и составила в первой группе 11,3 (7,23; 14,45) мл/кг/ч, во второй – 7,77 (6,67; 9,61) мл/кг/ч.
Группы не отличались между собой по уровню гемоглобина и гематокрита до ИК. После окончания ИК и проведения процедуры МУФ во второй группе гемоглобин и гематокрит были достоверно выше в сравнении с пациентами первой группы (табл. 2). Темп дренажных потерь достоверно не отличался между группами (табл. 2). Потребность в трансфузии эритроцитарной массы в первые сутки после операции составила 90% в первой группе и 20% – во второй.
Группы не отличались между собой по длительности ИК и пережатия аорты, однако во второй группе достоверно меньше, чем в первой группе, длительность искусственной вентиляции легких (ИВЛ). Отмечена тенденция меньшей длительности нахождения пациентов второй группы в отделении реанимации и анестезиологии (ОАР) (табл. 3).
Выявлено, что в группе МУФ пациенты поступают в операционную с клиникой сердечной недостаточностью, проявляющейся большей потребностью в инотропных препаратах, а значит, пациенты исходно тяжелее. После радикальной коррекции ТМА IS в группе МУФ достоверно ниже, чем в первой группе, где более выражена клиника сердечной недостаточности. По данным литературы, это связано с уменьшением отека миокарда после проведения МУФ и отрицательным гидробалансом [7].
По нашим данным, использование процедуры МУФ достоверно способствует повышению гемоглобина и гемо-токрита, тем самым уменьшая потребность трансфузии эритроцитарной массы. При этом в нашем исследовании достоверной разницы темпа дренажных потерь не обнаружено [5].
Полученные результаты достоверного сокращения длительности ИВЛ во второй группе, по-видимому, связаны с уменьшением внесосудистой воды в легких, уменьшением общей воды в организме, а, следовательно, улучшением оксигенации [2, 4]. На этом фоне удается в более ранние сроки адаптировать пациентов к самостоятельному дыханию.
Выводы
-
1. Оба метода регуляции гидробаланса при коррекции ТМА в условиях ИК у новорожденных эффективны и позволяют устранить анемию, но, используя МУФ после ИК, удается достичь исходного уровня гемоглобина и гематокрита, уменьшить потребность трансфузии эритроцитарной массы.
-
2. Использование МУФ способствует уменьшению послеоперационной сердечной недостаточности, снижению потребности в кардиотонических препаратах, уменьшению длительности послеоперационной ИВЛ и длительности пребывания в ОРИТ.


