Миастения с ранним и поздним началом заболевания
Автор: Романова Т.В., Повереннова И.Е.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Неврология
Статья в выпуске: 2 т.12, 2016 года.
Бесплатный доступ
Цель: проверка гипотезы о существовании двух клинически различных групп больных миастенией с разным возрастом начала заболевания на большой популяции пациентов с помощью методов многомерной группировки. Материал и методы. Анализировали показатели 444 пациентов, включенных в регистр больных миастенией Самарской области, длительность заболевания которых составила более 1 года. Статистическая обработка результатов исследования проводилась с использованием многомерной группировки методом кластерного анализа. Проверка качества классификации осуществлялась с использованием дискриминантного анализа. Результаты. Переходный возраст между двумя группами был определен в 40 лет. Наиболее существенные критерии различия групп пациентов с началом до 40 лет и после 40 лет: пол пациента и наличие гиперплазии тимуса. Заключение. Полученные клинико-иммунологические паттерны миастении с ранним и поздним началом заболевания могут служить основой формирования модели прогноза течения миастении и создания алгоритма ведения пациентов.
Возраст начала, гиперплазия тимуса, клинико-иммунологический паттерн, миастения
Короткий адрес: https://sciup.org/14918308
IDR: 14918308
Early and late myasthenia gravis
The aim: the hypothesis testing of the existence of two different groups of patients with different age at disease onset in a large population of patients with methods multidimensional constellation. Materials and Methods. Analysis of 444 patients enrolled in the register of patients with myasthenia in the Samara region. The duration of disease was more than 1 year. Statistical results of the study was carried out using a multi-dimensional grouping by cluster analysis Checking the quality of the classification was carried out using discriminant analysis. Results. Transient age between the two groups was defined as 40 years. The most important criteria of distinction patients group was sex of the patient and the presence of thymic hyperplasia. Conclusion. These clinical and immunologic patterns of early-onset and late-onset myasthenia gravis can serve as a basis of formation flow forecast model of myasthenia gravis and to create an algorithm of patient management.
Текст научной статьи Миастения с ранним и поздним началом заболевания
-
1Введение. Миастения относится к аутоиммунным болезням нервной системы. При этом заболевании нарушается нервно-мышечная передача. Патогенез болезни связан с образованием аутоантител к целому ряду антигенных мишеней нейромоторного аппарата [1–3]. В последние годы отмечен рост числа больных миастенией во всех возрастных группах [4, 5]. Число больных миастенией в мире ежегодно увеличивается на 5-10% [4]. Распространенность миастении в популяции колеблется от 4 до 39,5 случаz на 100000 населения [5, 6].
На протяжении последних десятилетий ведется активный разнонаправленный поиск новых подходов к лечению миастении, основанный на углубленном изучении различных аспектов этиологии, патогенеза и клинико-эпидемиологических особенностей заболевания [2, 6, 7]. В настоящее время доказана патогенетическая неоднородность миастении [2, 6, 8].
В литературе, посвященной классификационным подходам к миастении, утвердилось разделение на миастению с ранним началом и миастению с поздним началом [7, 9, 10]. Два варианта заболевания, по мнению большинства авторов, имеют различные клинико-иммунологические паттерны и, возможно, отличаются ответом на терапию. Ранний и поздний варианты заболевания отличаются по гендерному составу, частоте встречаемости глазных форм миастении, степени тяжести генерализованной формы, преобладанию бульбарных симптомов, распространенности серонегативной по антителам к ацетилхолиновым рецепторам (АХР) формы болезни, наличию изменений тимуса [9–11]. Однако среди исследователей до сих пор нет единой точки зрения по поводу возрастной границы раннего и позднего варианта течения болезни. Большинство ученых склоняются к мнению, что граница дебюта заболевания должна определяться возрастом 40–50 лет [9, 11].
Цель : проверка гипотезы о существовании двух клинических групп больных миастенией с ранним и поздним возрастом начала заболевания на большой популяции пациентов с помощью методов многомерной группировки.
Материал и методы. В Самарской области на базе областной клинической больницы им. В. Д. Се-
редавина с 1999 г. работает областной миастенический центр. К 2009 г. был создан электронный регистр больных миастенией Самарской области. Данный регистр позволяет быстро вносить, изменять и обрабатывать информацию, а также осуществлять длительное наблюдение за большой группой больных. К настоящему моменту база данных содержит информацию более чем о 500 пациентах. Данное исследование основано на анализе показателей 444 пациентов, включенных в регистр, длительность заболевания которых составила более одного года.
Среди обследованных больных было 317 женщин (71,4%) и 127 мужчин (28,6%). Длительность заболевания к моменту анализа составила от 1 года до 45 лет, средняя продолжительность 8,8±7,6 года; для мужчин 7,3±6,3; для женщин 9,4±8,0 года.
Верификация диагноза осуществлялась на основании клинического обследования, прозериновой пробы, исследования нервно-мышечной передачи, определения титра антител к АХР, компьютерной или магнитно-резонансной томографии средостения и гистологического исследования вилочковой железы в случаях проведения тимэктомии.
Статистическая обработка результатов исследования проводилась в операционной системе Windows XP с использованием программы Microsoft Excel, Statistica 10.0 и SPSS 16.0. Проверка выборки на нормальность распределения осуществлялась несколькими способами с использованием критериев, включенных в пакет Statistica 10.0 и SPSS 16.0. Распределение выборки соответствует нормальному.
Средние значения показателей представлены co стандартными ошибками (М±m). Предположение о существенности различий пациентов по «возрасту начала» проверяли с помощью многомерной группировки методом кластерного анализа (мера близости — евклидова метрика; иерархическое объединение кластеров проводили методом Уорда). Проверка качества классификации осуществлялась с использованием дискриминантного анализа.
Результаты. Первоначально проверялась гипотеза о существовании двух групп пациентов, различающихся по возрасту начала заболевания, и определялся «переходный» возраст. Была построена гистограмма распределения всей популяции больных по возрасту начала заболевания (рис. 1).
Как демонстрирует график, популяция больных разделилась на две подгруппы с пиками заболева-
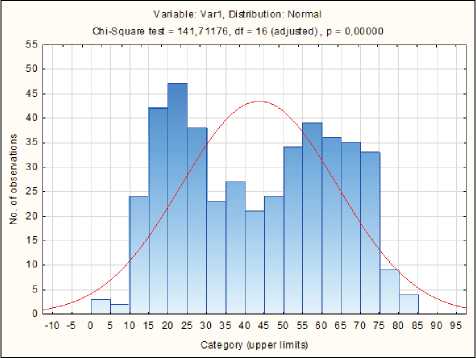
Рис. 1. Гистограмма распределения пациентов по возрасту начала заболевания емости в 20–25 лет и 55–60 лет. В период от 40 до 45 лет отмечается значительный спад частот, причем наибольшее снижение приходится на возраст 40 лет. Таким образом, было получено предварительное подтверждение гипотезы о том, что возраст 40 лет является границей разделения двух клинических форм болезни. Проверка гипотезы была проведена с помощью статистических методов: кластерного и дискриминантного анализа, методов непараметрической статистики.
Сложность кластерного анализа заключается в том, что реальные объекты (в данном случае пациенты) являются многомерными, то есть описываются не одним, а несколькими параметрами. В нашем исследовании мы выбрали следующие параметры, которые могут иметь значение для кластеризации пациентов: возраст начала заболевания, пол, форма заболевания (глазная, генерализованная), первые симптомы болезни, изменения тимуса, максимальная тяжесть заболевания, выраженность бульбарных симптомов. Общий объем выборки 444 человека; кластеризация включила 416 пациентов, имеющих все данные по анализируемым параметрам. Параметр «антитела к ацетилхолиновым рецепторам» исключен из критериев кластеризации, поскольку данный показатель имелся не у всех пациентов, но в дальнейшем мы добавили его в описание кластеров.
Логика кластерного анализа состоит в том, что число кластеров заранее не задается, а определяется эмпирическим путем, исходя из представления о мере близости объектов друг к другу. В решении этой задачи помогает графическое представление классификации в виде дендрограммы (дерева объединения). В результате расчетов и анализа дендрограммы выборка оказалась разбита на два больших кластера. Данные кластеры имели наибольшие различия по средним характеристикам и показали са-
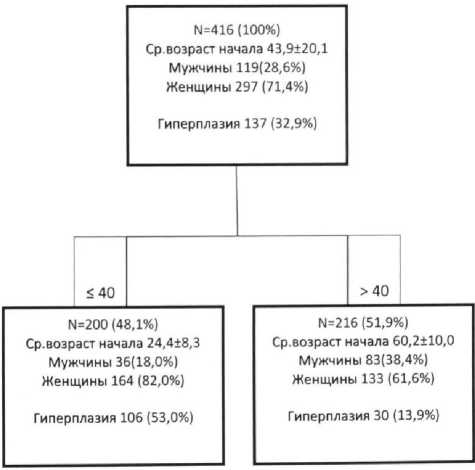
Рис. 2. Классификация пациентов по возрасту начала миастении мые важные факторы, по которым произошло разделение на кластеры.
Для более детальной проверки качества классификации и выявления «вклада» отдельных факторов в различия пациентов по возрасту применен дискриминантный анализ. В анализ были введены основные параметры, относящиеся к состоянию больного, чтобы выяснить, какие из них наиболее различаются у пациентов указанных групп. Результаты дискриминации представлены в табл. 1.
В первом столбце итоговой таблицы приведены значения статистики «лямбда» Уилкса, являющиеся важным результатом включения данной переменной в модель (интервал возможных значений от 0 до 1). Чем больше значение λ, тем более желательно присутствие этой переменной в процедуре дискриминации. В результате построения дискриминационной функции значимыми оказались два параметра: пол пациента и гиперплазия тимуса. Это означает, что именно они являются решающими факторами различий возраста начала миастении до 40 лет и после 40 лет.
Рассмотрены характеристики полученных кластеров. На рис. 2 показана классификация пациентов по возрасту начала миастении.
Кластер 1 вместил в себя 200 больных с возрастом начала до 40 лет включительно. Средний возраст начала миастении составил 24,4±8,3 года. Кластер 2 состоял из 216 пациентов, заболевших в возрасте 41 года и старше. Средний возраст начала заболевания был 60,2±10,0 лет.
Таблица 1
Итоговые показатели дискриминантного анализа пациентов по возрасту начала заболевания
|
N = 416 |
Discriminant Function Analysis Summary 2 grps Wills’s Lambda: 77332 approx. F (2,413) = 60,530 p < 0,0000 |
|||||
|
Wills’s Lambda |
Partial Lambda |
F-remove (1,413) |
p-valid |
Toler |
1-Toler (R-Sqr) |
|
|
Пол |
0,82468 |
0,93771 |
27,4328 |
0,00000 |
0,99326 |
0,00673 |
|
Гиперплазия |
0,94337 |
0,81937 |
90,8192 |
0,00000 |
0,99326 |
0,00673 |
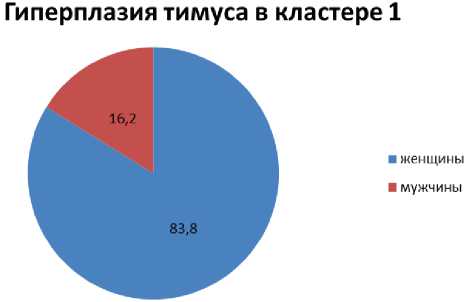
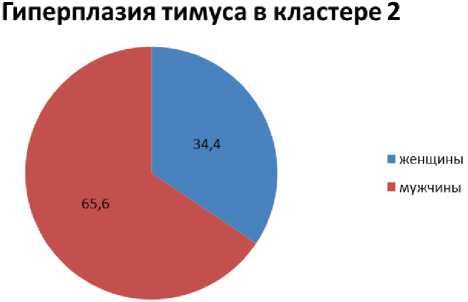
Рис. 3. Соотношение пациентов с гиперплазией тимуса по полу в кластерах
Первым значимым фактором разделения кластеров явилось соотношение пациентов по полу внутри кластера. У пациентов с ранним началом заболевания соотношение М:Ж составило 1:4,6, а в группе пациентов с поздним началом 1:1,6.
Вторым значимым фактором явился характер изменений тимуса. В группе с ранним началом заболевания изменения тимуса выявлены у 71,5% больных. Гиперплазия тимуса встречается более чем у половины пациентов (в три раза чаще, чем тимомы). В группе с поздним началом миастении изменения тимуса выявлены только у 39,8% больных, при этом тимома встречалась в два раза чаще, чем гиперплазия тимуса.
Представляет интерес распределение по полу среди пациентов с гиперплазией вилочковой железы в каждом кластере (рис. 3).
При раннем начале миастении гиперплазия тимуса встречалась почти исключительно у женщин, в то время как при начале заболевания после 40 лет большую часть пациентов с гиперплазией тимуса представляли лица мужского пола. При рассмотрении соотношения пола пациентов с наличием тимомы обнаруживается сходная закономерность в обоих кластерах, характерная для всей популяции больных миастенией: соотношение женщин и мужчин представлено как 3:1.
Количество пациентов с глазной формой миастении в кластере 1 составило 12,5%, в кластере 2-13,9%. В отношении генерализованной формы заболевания между кластерами существовали расхождения по максимальной тяжести проявлений миастении. Кластер 1 — это более легкая по тяжести течения заболевания группа. В ней преобладают легкая и среднетяжелая формы заболевания (72,1 %). В кластере 2 преобладают среднетяжелая и тяжелая формы, доля которых составила 61,8%. Средневзвешенная степень максимальной тяжести в кластерах заметно отличается (соответственно 2,75 и 3,28). Тем не менее, модальным значением в обоих кластерах является среднетяжелая миастения (37,2% в кластере 1 и 38,2% в кластере 2). Выраженность бульбарных симптомов в кластерах также существенно различается. Так, в кластере 1 клинически значимые бульбарные симптомы отмечены у 46,9% больных, в кластере 2 — у 69,3%.
По характеру первых симптомов кластеры также имеют существенные различия. Доминирующий удельный вес принадлежит глазным, бульбарным и скелетным симптомам. Во втором кластере значительно выше удельный вес дебюта, проявляющегося глазными симптомами. В первом кластере значимо чаще, чем во втором, отмечено начало заболевания с общей слабостью и утомляемостью.
Редкие варианты дебютных симптомов, такие как миастенический криз, внезапные падения, изолированные дыхательные расстройства и слабость мышц шеи, значительно чаще отмечены в кластере 1. Здесь их общая доля составляет 9,0%, а в кластере 2-1,9%. Во втором кластере вообще не были отмечены такие варианты дебюта, как внезапные падения и изолированная слабость мышц шеи.
По характеру течения и темпам нарастания симптомов также можно отметить различия. У пациентов с ранним началом по сравнению с группой позднего начала заболевания отмечено больше эпизодических форм (9,5 и 2,8% соответственно), меньше прогрессирующих и злокачественных форм миастении (25,0 и 36,3%), чаще представлено течение по типу «обострение — ремиссия» (24,0 и 18,5%). К моменту
Таблица 2
Клинико-иммунологические паттерны миастении с ранним и поздним началом заболевания
|
Показатель / группа |
Начало до 40 лет |
Начало после 40 лет |
|
М: Ж |
1: 4,6 |
1: 1,6 |
|
Изменения тимуса (%) |
71,5 |
39,8 |
|
Гиперплазия: тимома |
3:1 |
1: 2 |
|
Начальные симптомы |
Общая слабость и утомляемость |
Поражение экстраокулярных мышц |
|
Бульбарные нарушения (%) |
46,9 |
69,3 |
|
Доминирующая тяжесть заболевания (%) |
Легкая + среднетяжелая 72,1 |
Среднетяжелая + тяжелая 61,8 |
|
Ср. титры АТ к АХР (нмоль/л) |
13,7 |
15,8 |
|
Ремиссия заболевания (%) |
33,0 |
10,6 |
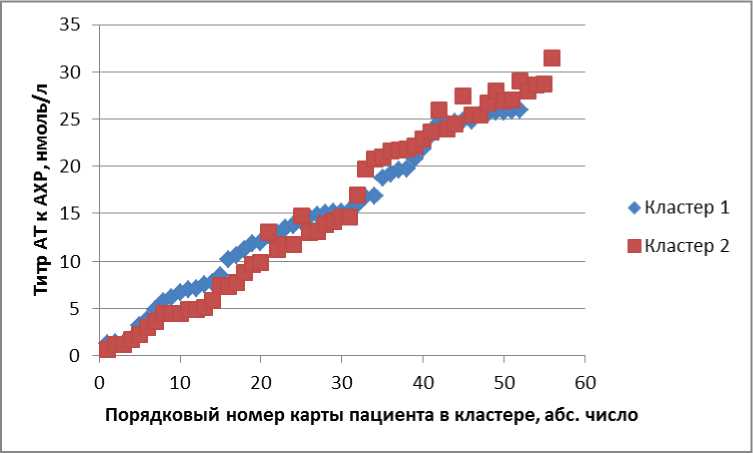
Рис. 4. Распределение пациентов по титрам антител к АХР в кластерах
анализа пациенты из группы с ранним началом в три раза чаше находились в состоянии ремиссии (33,0 и 10,6%), в два раз реже находились в состоянии декомпенсации и прогрессирования заболевания (6,0 и 15,3%). Различия кластеров по основным клиникоиммунологическим характеристикам представлены в табл. 2.
Последний параметр — титр антител к АХР — был исключен из классификации, но добавлен в описание кластеров. В кластере 2 его значения в среднем больше, чем в кластере 1: половина пациентов имеют антитела к АХР выше 15,2 нмоль/л. Во втором кластере 12,5% пациентов имеют значения титра антител к АХР больше, чем максимальное значение в кластере 1. Среднее значение в кластере 2 составило 15,8±8,6 нмоль/л, в кластере 1–13,7±8,1 нмоль/л. Также во втором кластере разброс значений данного показателя более широкий: от 0,6 до 31,5 (в первом кластере от 1,3 до 26,1), как это видно на рис. 4.
Серонегативные по антителам к АХР формы миастении в первом кластере составили 9,6%, во втором 5,4%.
Обсуждение. Предположение о существовании двух клинически различающихся групп пациентов с ранним и поздним началом заболевания проверено на нашей популяции больных с помощью методов многомерной группировки. Переходный возраст между двумя группами определен в 40 лет. Наиболее существенными критериями различия группы пациентов с началом до 40 лет и после 40 лет являлись пол пациента и наличие гиперплазии тимуса. Получены клинико-иммунологические паттерны раннего и позднего вариантов заболевания с возрастной границей дебюта в 40 лет.
Для миастении с началом заболевания до 40 лет характерны следующие особенности: женский пол; гиперплазия тимуса; начало заболевания со слабости и утомляемости любой группы мышц, но чаще с общей скелетной слабости; более легкое доброкачественное течение; меньшая представленность бульбарных нарушений и частоты глазной формы миастении; средние титры антител к АХР; меньшая вероятность злокачественного прогрессирующего течения; большее число благоприятных исходов лечения и достижения ремиссии.
Миастения с началом после 40 лет имеет сглаженные гендерные особенности, изменения тимуса встречаются у трети пациентов, при этом гиперплазия тимуса характерна для мужчин; начало болезни чаще всего с глазных и бульбарных симптомов; доминирование бульбарных нарушений у большинства больных; высокие титры антител; часто прогрессирующее, достаточно тяжелое течение; во многих случаях недостаточная эффективность терапии.
Заключение. Полученные клинико-иммунологические паттерны миастении с ранним и поздним началом заболевания могут служить основой формирования модели прогноза течения миастении и создания алгоритма ведения пациентов с целью достижения наилучшего результата в каждом конкретном случае.
Список литературы Миастения с ранним и поздним началом заболевания
- Ланцова В.Б., Сепп Е.К. Антигенные мишени при миастении. Иммунология и аллергия 2004; 5 (1): 196-198
- Meriggioli MN, Sanders DB. Autoimmune myasthenia gravis: emerging clinical and biological heterogeneity. Lancet Neurol 2009; 8 (5): 475-490
- Vincent A. Autoantibodies at the neuromuscular junction -link to the central nervous system. Re Neurol (Paris) 2014; 170 (10): 584-586
- Пономарева E.H. Миастения: Клиника, патогенез, дифференциальная диагностика, тактика ведения. Минск: МЕТ, 2002; 175 с.
- Романова Т.В. Эпидемиологическое исследование миастении гравис в Самарской области. Саратовский научно-медицинский журнал 2012; 1 (08): 91-95
- Romi F, Gilhus NE, Aarli JA. Myasthenia gravis: clinical, immunological and therapeutic advances. Acta Neurol Scand 2005; 111 (2): 134-141
- Санадзе А.Г. Миастения и миастенические синдромы. М: Литтерра, 2012; 255 с.
- Санадзе А.Г. Миастения. В кн.: Аутоиммунные заболевания в неврологии: клин. рук. М.: РООИ Здоровье человека, 2014; с. 101-128
- Akaishi Т, Yamaguchi Т, Suzuki Y, et al. In sightsinto the classification of myasthenia gravis. PLoS One 2014; 9 (9):e106757.
- Barbaud A, Carlander B, Pagns M. Late onset forms of myasthenia gravis. Comparison with early-onset myasthenia gravis. Rev Neurol 2006; 162 (10): 990-996
- Chan KH, Cheung RT, Mak W, et al. Nonthymoma early-onset-and late-onset-generalized myasthenia gravis: a retrospective hospital-based study. Clin Neurol Neurosurg 2007; 109 (8): 686-691.


