Микробиологический анализ торфяной лечебной грязи месторождения Таборли-3
Автор: Гафарова Л.Ф., Курди У., Яковлева Г.Ю., Колпаков А.И., Ильинская О.Н.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2025 года.
Бесплатный доступ
Торфяные грязи (пелоиды) представляют собой природные органоминеральные комплексы, образованные при разложении органических остатков в болотистой местности в условиях недостатка кислорода. Они обладают высокой теплоемкостью и содержат биологически активные вещества (соли, газы, биостимуляторы, метаболиты организмов и пр.), а также живые микроорганизмы. Однако микробный состав пелоидов практически не изучен. Цель работы заключалась в анализе микробного состава торфяных пелоидов месторождения Таборли-3 (Республика Татарстан) согласно санитарно- бактериологическим характеристикам, спектру культивируемых микроорганизмов, молекулярно- генетическому определению прокариотического метагенома и его функционального потенциала. В течение 2021-2023 гг. изучены 7 образцов таборлинских пелоидов. Санитарно-бактериологический анализ осуществляли согласно программе производственного контроля санаториев, применяющих данную грязь. Таксономическую идентификацию выделенных культур микроорганизмов проводили методом времяпролетной масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией MALDI-TOF MS. Молекулярно-генетический анализ сообщества микроорганизмов выполняли секвенированием 16S рРНК с помощью Illumina MiSeq, дальнейщий анализ последовательностей проводили с использованием пакета программного обеспечения Mothur на платформе Galaxy. Охарактеризованы бактериальные сообщества пелоидов, в которых преобладали представители филумов Firmicutes (22%) и Proteobacteria (36%). На уровне семейств доминировали Streptococcaceae, Ruminicoccaceace, Lactobacillaceae, Comamondaceae и Sphingomonadaceae. Функциональный потенциал сообществ подтверждает, что бактерии пелоидов содержат основные гены метаболизма углеводов, липидов, витаминов, аминокислот и нуклеотидов, а также способны утилизировать ксенобиотики. Впервые охарактеризован микробиом лечебных грязей месторождения Таборли-3. Мониторинг состава микробных сообществ лечебных грязей является важной составляющей для оценки вклада микроорганизмов и их метаболитов в оздоровительный эффект пелоидотерапии.
Пелоиды, торфяные грязи, санитарно-бактериологический анализ, микробиом, метагеном, функциональный профиль
Короткий адрес: https://sciup.org/147251161
IDR: 147251161 | УДК: 581.522 | DOI: 10.17072/1994-9952-2025-1-21-31
Microbiological analysis of peat therapeutic mud from the Taborli-3 deposit
Peat mud (peloids) are natural organomineral complexes formed during the decomposition of organic residues in swampy areas under conditions of lack of oxygen. They have a high heat capacity and contain biologically active substances (salts, gases, biostimulants, metabolites of organisms, etc.), as well as living microorganisms. However, the microbial composition of peloids is practically unknown. The purpose of the work was to analyze the microbial composition of peat peloids from the Taborli-3 deposit (Tatarstan Republic) according to sanitary and bacteriological characteristics, the range of cultivated microorganisms, molecular-genetic determination of the prokaryotic metagenome and its functional potential. During 2021-2023 7 samples of peloids from the Taborli-3 deposit were studied. Sanitary and bacteriological analysis was carried out in accordance with the control program of sanatoriums using this mud. Taxonomic identification of the isolated microorganism cultures was carried out using time-of-flight mass spectrometry with matrix-assisted laser desorption/ ionization MALDI-TOF MS. Molecular-genetic analysis of the microbial community was performed by sequencing 16S rRNA using Illumina MiSeq, subsequent sequence analysis was carried out using the Mothur software package on Galaxy platform. Bacterial communities of peloids were characterized, the dominance of representatives of the phyla Firmicutes (22%) and Proteobacteria (36%) was established. At the family level, Streptococcaceae, Ruminicoccaceae, Lactobacillaceae, Comamondaceae and Sphingomonadaceae were dominant. The functional potential of the communities confirms that peloid bacteria contain the main genes for the metabolism of carbohydrates, lipids, vitamins, amino acids and nucleotides, and are also capable to utilize xenobiotics. The microbiome of therapeutic mud from the Taborli-3 deposit was characterized for the first time. Monitoring the composition of microbial communities of therapeutic mud is an important component for assessing the contribution of microorganisms and their metabolites to the healing effect of peloid therapy.
Текст научной статьи Микробиологический анализ торфяной лечебной грязи месторождения Таборли-3
Под лечебными грязями (пелоидами) понимаются природные коллоидальные органоминеральные образования (иловые, торфяные, сопочные), обладающие высокой пластичностью, теплоемкостью и медленной теплоотдачей, содержащие биологические активные вещества (соли, газы, витамины, ферменты, гормоны и др.) и живые микроорганизмы1.
Торфяные грязи образуются вследствие разложения высших растений в местностях, подвергающихся заболачиванию, чаще вблизи пресных водоемов2. Они представляют собой болотные отложения торфов высокой степени разложения (более 40%), преимущественно органического состава (более 50% от сухого вещества)3. Провинция торфяных грязей на севере граничит с тундрой, на юге ‒ с лесостепной и степной зонами, охватывает более 80% территории России. Практически в любой области этой территории можно выявить месторождения торфяных грязей. Это, как правило, пресноводный бессульфидный торф, лечебная значимость которого обуславливается высокими тепловыми свойствами и большим количеством органических веществ, в том числе признающихся терапевтически активными ‒ гуминовых кислот, липидов, битумов [Ялтанец и др., 2004]. Данные о торфяных лечебных грязях, приведенные в литературе, подтверждают ее терапевтическую эффективность в отношении хронических неспецифических заболевания легких, астмы и заболевания верхних отделов ЖКТ [Антипова и др., 2012]; также применяются при реабилитации пациентов после операций на позвоночнике [Гайдукова и др., 2023].
Таборли-3 ‒ действующее месторождение торфяных шламов (грязей), находится на пойменной террасе р. Чаж в Агрызском р-не Республики Татарстан (рис. 1) [Таборли: Российский федеральный геологический фонд, 2023]. Грязи используются в Татарстане – в санатории «Шифалы-Су Ижминводы» [Tatarica: Татарская энциклопедия, 2023], спортивно-оздоровительном комплексе санатория-профилактория «Ян» (Альметьевский р-н), и также в санаториях Удмуртии «Варзи-Ятчи» и «Металлург» [Перспективы развития…, 2020]. Запасы таборлинского месторождения лечебной грязи значительны, что обусловливает возможность развития сети грязелечебниц в прилегающих и удаленных регионах. В Республике Татарстан известно 8 месторождений лечебной грязи с запасами около 900 тыс. м3 [Tatarica: Татарская энциклопедия, 2023]. Наиболее крупные – это месторождение торфяных грязей Таборли-3 (Агрызский р-н) и Верхняя Мочажина (Лениногорский р-н). Разрабатываются месторождения сапропе- левых грязей (Бугульминский р-н) и иловых лечебных грязей (Азнакаевский р-н). На сегодня наиболее изученными являются грязи Сакского месторождения (Крым), которые характеризуются наличием гипса, галита, кальцита, арагонита и бассанита [Максимов и др., 2021], а жидкая фаза представлена поровым раствором, содержащим хлориды и магниево-натриевые растворимые соли вместе с комплексом органических веществ [Антипова и др., 2012]. К сожалению, о составе пелоидов Татарстана практически ничего не известно; также отсутствуют данные о химических, физических, радиологических и микробиологических характеристиках торфяной грязи месторождения Таборли-3, не опубликованы и результаты, подтверждающие ее терапевтические эффекты. Однако, в соответствии с информацией на официальном сайте санатория «Шифалы-Су Ижминводы», лечебные грязи месторождения Таборли-3 с успехом применяются для лечения и профилактики широкого круга заболеваний опорно-двигательного аппарата, нервной системы, органов малого таза, а также кожных и ряда других заболеваний [Санаторий Шифалы Су Ижминводы, 2023]. В результате жизнедеятельности микроорганизмов в грязь попадают биологически активные вещества: сероводород, липиды, каротиноиды, ферменты оксидоредуктазы и гидролазы, витамины, гормоноподобные вещества.
Рис. 1 . Местоположение месторождения торфяной грязи Таборли-3 [Паспорт месторождения …, 2023] [Location of the Taborli-3 peat mud deposit [Taborli-3 field passport, 2023]
В связи с вышеизложенным, целью настоящей работы стал анализ микробного состава торфяных пе-лоидов месторождения Таборли-3 в соответствии с рекомендуемыми нормами санитарнобактериологического исследования параллельно с характеристикой таксономического спектра культивируемых микроорганизмов, молекулярно-генетическому определению прокариотического метагенома и его функционального потенциала.
Материалы и методы
Подготовка образцов пелоидов и микробиологическое исследования
В 2021 г. проведен анализ проб лечебной грязи (п = 7) месторождения Таборли-3, расположенного в Агрызском р-не Республики Татарстан (рис. 1), Санитарно-бактериологический анализ пелоидов проводили в соответствии с Методическими указаниями4.
Отобранные образцы пелоидов гомогенизировали и отбирали 1 г влажной массы, готовили серию последовательных разведений в стерильной дистиллированной воде и высевали на рекомендованные среды для подсчета колониеобразующих единиц (КОЕ). Общее количество микроорганизмов определяли на неселективной среде – мясопептонном агаре (компания BioMedia, РФ). Для выявления энтеробактерий использовали лактозопептонную среду Эйкмана (ООО Биотехновация); для выделения и грамотрица-тельных микроорганизмов кишечной группы производили высев на среду Эндо (Микролаб, представи- тель Laboratorios Conda в РФ). Для обнаружения грибов медицинского значения применяли среду Сабуро (BioMedia) для солеустойчивых микроорганизмов, в том числе коагулазоположительных стафилококков ‒ желточно-солевой агар производства ВНИИМС (ФГБНУ «ФНЦ пищевых систем им. В.М. Горбатова» РАН), для синегнойной палочки ‒ цетримидный агар (BioMedia). Результаты представляли как среднеарифметическое число со стандартным отклонением по исследованным 7 образцам. Таксономическую идентификацию чистых культур всех выделенных микроорганизмов проводили методом времяпролетной масс-спектрометрии с матрично-активированной лазерной десорбцией/ионизацией MALDI-TOF-MS на масс-спектрометре Vitek MS (производства БиоМерье (bioMerieux), Франция).
Метагеномный анализ сообщества бактерий
Из поступивших образцов пелоидов выделяли общую ДНК с использованием набора Miniprep Kit (Axygen, США) согласно протоколу производителя. Полученную ДНК нормализовали до концентрации 10 нг/мкл. Для подтверждения качественного выделения ДНК проводили амплификацию гена 16S рРНК, по области V3—V4 гена 16s рРНК бактерий с помощью полимеразной цепной реакции и гель-электрофореза. С помощью Illumina MiSeq была проведена подготовка библиотеки и секвенирование. Выбор оперативной таксономической единицы (OTU) осуществляли при пороге идентичности 97% и классифицировали по справочной базе данных Greengenes 13-8-99 [DeSantis et al., 2006]. Оценку функциональных профилей сообществ осуществляли на платформе iVikodak с использованием инструмента Global Mapper [Nagpal et al., 2019].
Результаты
Стандартный санитарно-бактериологический анализ образцов пелоидов месторождения Таборли-3 выявил присутствие 12 основных видов культивируемых бактерий (табл. 1). Только одна из 7 проб не соответствовала гигиеническим нормативам по показателю Pseudomonas aeruginosa , обнаружение которой недопустимо в грязях, готовых к применению. Данный факт свидетельствует о важности и необходимости соблюдения регламента термообработки при пробоподготовке грязи перед ее использованием.
Таблица 1
Таксономическая идентификация и количественный состав культивируемых бактерий торфяной лечебной грязи месторождения Таборли-3, поступающей в санатории Республики Татарстан.
Представлены средние значения 7 образцов
[Taxonomic identification and quantitative composition of cultivated bacteria of peat medicinal mud from the Taborli-3 deposit, supplied to sanatoriums of the Republic of Tatarstan. The average values of 7 samples are presented]
|
№ |
Идентифицированные микроорганизмы |
Σ колоний микроорганизмов, выросших из 7 образцов пелоидов (×104/г пелоида) |
% |
|
1 |
Bacillus firmus |
245±15 |
87.7 |
|
2 |
Lysinibacillus fusiformis |
10±2 |
3.6 |
|
3 |
Micrococcus luteus |
3±1 |
1.1 |
|
4 |
Rhizobium radiobacter |
3±1 |
1.1 |
|
5 |
Brevibacillus spp |
3±1 |
1.1 |
|
6 |
Staphylococcus hominis |
3±1 |
1.1 |
|
7 |
Paracoccus yeei |
3±1 |
1.1 |
|
8 |
Bacillus megarerium |
2±1 |
0.7 |
|
9 |
Staphylococcus warneri |
2±1 |
0.7 |
|
10 |
Staphylococcus pasteuri |
2±1 |
0.7 |
|
11 |
Brevundimonaa diminuta |
2±1 |
0.7 |
|
12 |
Pseudomonas aeruginosa* |
1 |
0.4 |
|
Итого |
279 |
Примечание: * обнаружен только в одном образце.
Как видно из данных табл. 1, среди выделенных микроорганизмов доминировал вид Bacillus firmus , часто встречающийся в различных почвах. Этот вид включает штаммы, умеренно устойчивые к щелочам (pH от 6.5 до 8.5), и алкалофильные (pH до 10.5) [Guffanti et al., 1980]. B. firmus может участвовать в ассоциативной азотфиксации [Злотников и др., 2007], которая способствует более гибкому реагированию на экологические факторы, позволяет полнее использовать потоки энергии и глубже утилизировать субстраты по сравнению с чистыми культурами [Вавилин, 1986].
Также относительно часто встречались изоляты Lysinibacillus fusiformis . По данным литературы, различные штаммы L. fusiformis выделяются из сельскохозяйственных почв и производственных сточных вод. Некоторые штаммы проявляют высокую протеолитическую активность в отношении казеина, обладают высокой липолитической активностью [Нагызбеккызы и др., 2022] Штаммы L. fusiformis проявляют антагонистическую активность в отношении других бактерий [Марданова и др., 2015] и могут использоваться в биоремидиации [Mehta et al., 2015].
Перечисленные выше свойства B. firmus и L. fusiformis иллюстрируют их участие в процессах биоремедиации и повышении лечебных свойств грязей.
Метагеномный анализ позволил установить, что в пелоидах доминируют бактерии филумов Proteobacteria (36%) и Firmicutes (22%) (рис. 2 А). Стоит отметить, что в пелоидах присутствуют и цианобактерии (11%), являющиеся наиболее сложно организованными и морфологически дифференцированными прокариотами, способными к оксигенному фотосинтезу.
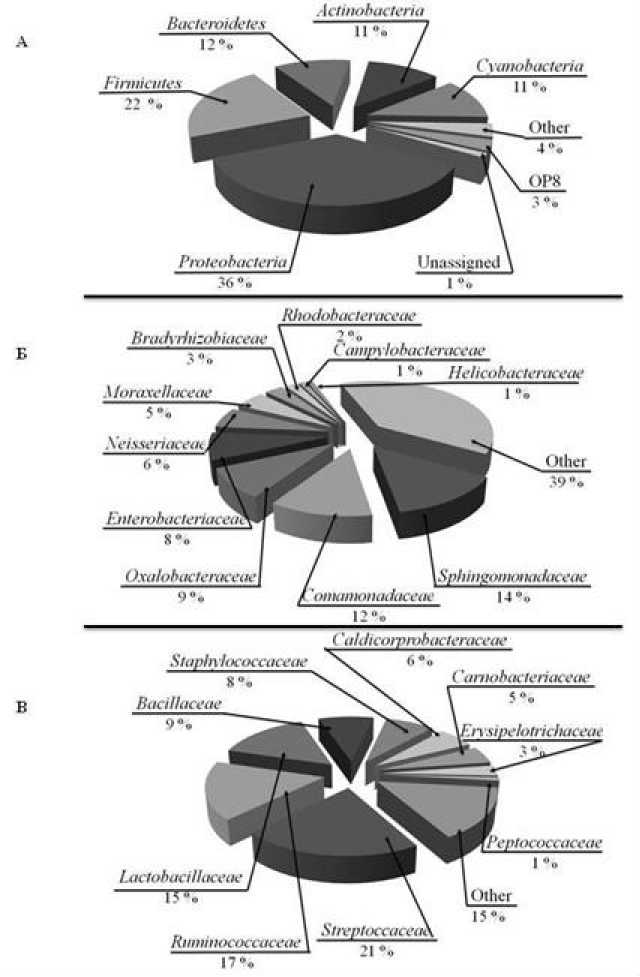
Рис. 2 . Таксономическая идентификация бактерий пелоидов месторождения Таборли-3: А – согласно филумам, Б – внутри филума Firmicutes , В – внутри филума Proteobacteria
[Taxonomic identification of bacteria from peloids of the Taborli-3 deposit:
A – according to phyla, Б – within the Firmicutes phylum, В – within the Proteobacteria phylum]
Внутри филума Firmicutes преобладали представители семейства Sphingomonadaceae (14%) (рис. 2Б), – грамотрицательные бактерии, содержащие гликозилцерамиды в своей внешней мембране [Kawahara et al., 2002]. Они являются многочисленными в окружающей среде, но не в кишечнике человека, и не являются патогенными [Nandy et al., 2013]. Второе место по численности занимает семейство Comamonadaceae (12%), аэробные грамотрицательные оксидазоположительные палочки, которые обычно встречаются в почве, воде и на растениях, но редко вызывают инфекции у человека.
Среди филума Proteobacteria выявлено высокое содержание стрептококков, руминикокков и лактобацилл (рис. 2В). Семейство Streptococcaceae включает шаровидные аспорогенные грамположительные хемоорганотрофные факультативно-анаэробные бактерии, присутствующие у человека в составе нормальной микрофлоры верхних дыхательных путей; также стрептококки, родственные Streptococcus sanguis , представляют собой основной сегмент бактериальной флоры некоторых почв. Стрептококки имеют сложные питательные потребности и погибают при пастеризации, что косвенно подтверждается отсутствием культивируемых форм этих бактерий в пелоидах. Руминококки – семейство грамположи-тельных неподвижных анаэробных аспорогенных бактерий, которые расщепляют целлюлозу, заселяют рубец жвачных и толстую кишку травоядных животных, а также входят в состав резидентной микрофлоры толстой кишки человека. Присутствие лактобацилл в пелоидах имеет особое значение, поскольку они участвуют в сбраживании травянистой биомассы с образованием спектра органических кислот, включая молочную, тем самым препятствуют развитию в пелоидах плесневых грибов.
Оценка функционального потенциала микробиома пелоидов подтверждает многообразие процессов, которые осуществляют бактерии. Очевидно, что большинство генетических детерминант относится к основным метаболическим процессам, таким как обмен углеводов, витаминов, аминокислот, нуклеотидов, терпеноидов, поликетидов (табл. 2). В то же время не исключена возможность продукции факторов устойчивости к антибиотикам, например, ферментов бета-лактамаз, разрушающих пенициллиновое кольцо, или генов, участвующих в развитии бактериальных инфекций. Метагеномный и функциональный анализы существенно расширяют наши познания о спектре микроорганизмов пелоидов, однако классический санитарно-бактериологический анализ по-прежнему имеет решающее значение для определения безопасности применения лечебных грязей.
Таблица 2 Функциональная активность бактериальных сообществ лечебной грязи месторождения Таборли-3
[Functional activity of bacterial communities in therapeutic mud of the Taborli-3 deposit]
|
Число генов |
Функции |
|
32113,89 |
Углеводный обмен |
|
9254,55 |
Метаболизм терпеноидов и поликетидов |
|
7289,53 |
Биодеградация и метаболизм ксенобиотиков |
|
5300,23 |
Устойчивость к антибиотикам |
|
6398,43 |
Инфекционные заболевания бактериальные |
|
6109,62 |
Липидный обмен |
|
10077,31 |
Метаболизм кофакторов и витаминов |
|
8651,81 |
Энергетический обмен |
|
14671,70 |
Аминокислотный обмен |
|
10007,93 |
Нуклеотидный метаболизм |
|
8285,88 |
Биосинтез вторичных метаболитов |
|
611,28 |
Экологическая адаптация |
|
12296,82 |
Репликация |
|
2434,72 |
Мембранный транспорт |
Обсуждение
Проведенные исследования выявили преобладание в пелоиде грамотрицательных бактерий филумов Proteobacteria (36%) и грамположительных бактерий филума Firmicutes (22%). За ними с примерно равными долями следовали бактероиды, актиномицеты и цианобактерии (рис. 2А). Мы сочли возможными приводить принятые ранее номенклатурные названия филумов, поскольку использование новой номенклатуры 2021 г. (соответственно, Bacillota, Pseudomonadota, Bacteroidota, Actinomycetota и Cyanobacteriota) оспаривается многими авторами [Oren et al., 2022]. Естественно, что выделение и определение метаболического потенциала разнообразных микроорганизмов из пелоидов не входит в протоколы санитарно-бактериологического анализа и представляет собой отдельную масштабную задачу, требующую использования широкого спектра разнообразных сред и подбора условий культивирования. На основе анализа метагенома пелоидов можно сделать определенный вывод о вкладе доминирующих филумов в физиологическую активность лечебных грязей. В частности, обнаружение стрептококков косвенно свидетельствует о наличии в пелоиде их внеклеточных метаболитов, таких как стрептолизин, стрептокиназа, лейкоцидин, бактериоцины (рис. 2В). Наличие руминококков вследствие их метаболической активности вносит вклад в расщепление остатков целлюлозы в пелоиде с образованием метана. Лактобациллы – известные продуценты не только молочной, но и других органических кислот, считаются наиболее значимой группой пробиотических бактерий.
В то же время анализ культивируемых бактерий, определенных нами в составе пелоида месторождения Таборли-3, показывает практически абсолютное доминирование двух видов – Bacillus firmus и Lysinibacillus fusiformis (см. табл. 1).
-
B. firmus не обладает риском для здоровья человека и используется в некоторых биологических процессах, в частности, для энзиматического гидролиза целлюлозосодержащих субстратов [Teeravivattanakit et al., 2022]. Этот вид также обладает высокой ксиланолитической активностю, улучшая доступ целлюлолитических ферментов к целлюлозе [Teeravivattanakit et al., 2022], что важно для разложения растительных остатков при созревании пелоида.
Более того, B. firmus эффективен в процессе биодеградации ксенобиотиков, в частности, ди-2-этилгексилфталата (ДЭГФ), который используется в качестве пластификатора при производстве пластмасс и выбрасывается на свалки. Так, штамм B. firmus MP04 использует ДЭГФ в качестве единственного источника углерода при pH 7, концентрации соли 5%, температуре от 20 до 37°C [Rashmi et al., 2023]. Описан гипертолерантный к мышьяку штамм B. firmus L-148, который может переносить концентрацию мышьяка более 3М и окислять 75 мМ арсенита [As(III)], в том числе в присутствии тяжелых металлов [Bagade et al., 2020]. B. firmus способен разлагать краситель Reactive Blue 160 (RB160), используемый в текстильной красильной промышленности и попадающий в воду и почвы (в бассейне р. Нойял, штат Тамил Наду, Индия), с образованием нетоксичных продуктов разложения [Barathi et al., 2019]; способен метаболизировать фипронил, который широко используется против различных насекомых-вредителей и создает серьезные проблемы для окружающей среды [Mandal et al., 2014].
-
B. firmus оказался сильным поликлональным активатором В-лимфоцитов мыши, влияющим на все изотипы Ig и повышающим синтез IFN-гамма и IL-10. Учитывая стимулирующий эффект на образование IgA и стимуляцию макрофагов, B. firmus представляется перспективным адъювантом слизистой оболочки и/или пробиотиком [Prokesová et al., 2002].
Данные литературы об различных биологических активностях Lysinibacillus fusiformis свидетельствуют, что этот вид способен к деградации ксенобиотиков [Adefiranye et al., 2023]; например, гербицида диурона, что делает его перспективным участником процессов биоремедиации участков, загрязненных диуроном [Reyes-Cervantes et al., 2021]. Штамм L. fusiformis B30 эффективно удаляет азотистые загрязнения посредством гетеротрофной нитрификации и аэробной денитрификации без накопления нитритов, переводя аммонийный азот в газообразный [Wu et al., 2023]. Штамм L. fusiformis MK559526 продуцирует биосурфактант с высоким потенциалом эмульгирования и значительным снижением поверхностного натяжения, что определяет значение штамма в процессе биоремедиации почв [John et al., 2021].
Эндофитные бактерии L. fusiformis B27, выделенные из Rhizophora mucronata , являются перспективным продуцентом L-аспарагиназы, которая применяется как противоопухолевое цитостатическое средство в терапии некоторых лейкозов [Prihanto et al., 2019]. Штамм L. fusiformis S4C11, выделенный из корней яблони в северной Италии, обладает противогрибковой активностью в отношении различных возбудителей и способен препятствовать прорастанию конидий Botrytis cinerea , а также ингибировать ее рост за счет продукции летучих органических молекул [Passera et al., 2021].
Таким образом, доминантные культивируемые бактерии пелоидов месторождения Таборли-3 имеют высокий потенциал полезных свойств, подтверждающих их вклад в детоксифицикацию возможных промышленных загрязнений пелоидов, а также в их оздоравливающий эффект.
Заключение
Впервые охарактеризован микробиом торфяных грязей (пелоидов) месторождения Таборли-3 (Республика Татарстан), применяющихся в санаториях Татарстана для лечения и профилактики широкого круга заболеваний опорно-двигательного аппарата, нервной системы, органов малого таза, а также кожных и ряда других заболеваний. Органоминеральные комплексы пелоидов содержат продукты разложения органических веществ, соли, газы, биостимуляторы, метаболиты организмов, а также живые микроорганизмы, вносящие вклад в оздоравливающий эффект пелоидов.
Согласно полученным санитарно-бактериологическим характеристикам, исследованные пелоиды в основном удовлетворяют требованиям безопасности: только в одной пробе из 7-и была обнаружена единственная колония Pseudomonas aeruginosa . Молекулярно-генетический анализ сообщества микроорганизмов на основе секвенирования 16S рРНК показал, что в сообществе преобладают бактерии филумов
Firmicutes (22%) и Proteobacteria (36%). Среди семейств доминировали представители Streptococcaceae , Ruminicoccaceace, Lactobacillaceae, Comamondaceae и Sphingomonadaceae . Анализ функционального потенциала прокариотического метагенома выявил, что бактерии пелоидов содержат основные гены метаболизма углеводов, липидов, витаминов, аминокислот и нуклеотидов, а также способны утилизировать ксенобиотики.
Важно отметить, что доминирующими культивируемыми микроорганизмами были безопасные для человека бактерии двух видов – Bacillus firmus и Lysinibacillus fusiformis , для которых подтверждена способность к деструкции ксенобиотических загрязнений и антифунгицидный потенциал. Выявление структуры и функций микробных сообществ пелоидов представляет собой современное перспективное направление, которое позволит во многом объяснить полезные свойства лечебных грязей.


