Микробное разнообразие в глинисто-солевых шламах калийного предприятия (г. Березники, Пермский край)
Автор: Корсакова Е.С., Шестакова Е.А., Одинцова Т.А., Бачурин Б.А., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2017 года.
Бесплатный доступ
Из глинисто-солевых шламов предприятия БКПРУ-2 ПАО «Уралкалий» (г. Березники, Пермский край) выделено 138 штаммов бактерий, которые на основании морфологических и генетических особенностей были объединены в 28 морфогеномогрупп. Представители каждой группы были идентифицированы на основе анализа нуклеотидных последовательностей гена 16S рРНК, сравни-тельное исследование которых показало принадлежность штаммов к классам Alphaproteobacteria, Gammaproteobacteria и Actinobacteria. Все обнаруженные бактерии являются галотолерантными, т.к. способны к росту на средах без добавления NaCl и с повышенной концентрацией соли (до 150 г/л). Большинство штаммов росли в щелочных условиях (рН 9.0) и использовали в качестве един-ственного источника углерода ряд моно- и полиароматических соединений, в том числе полицик-лические ароматические углеводороды, фталаты.
Глинисто-солевые шламы, филогенетическое разнообразие, бактерии-деструкторы, аромати-ческие соединения, фталаты
Короткий адрес: https://sciup.org/147204813
IDR: 147204813 | УДК: 579.695:579.262:579.222.2
Microbial diversity in clay-salt sludge of the potash enterprise (Berezniki, Perm krai)
From clay-salt sludge of the enterprise Berezniki-2 of OJSC "Uralkali" (Berezniki, Perm Territory) 138 bacterial strains were isolated and basing on morphological and genetic features have been combined in 28 morpho(genomo)groups. Representatives of each group have been identified while analyzing the nu-cleotide sequences of 16S rRNA gene, and comparative analysis showed that those strains belonged to the classes Alphaproteobacteria, Gammaproteobacteria and Actinobacteria. All the bacteria studied are halotolerant, because they are capable of growing on media without NaCl supplementation and with in-creased salt concentration (up to 150 g/l). Most strains grew in alkaline conditions (pH 9.0) and utilized several mono- and polyaromatic compounds as a sole source of carbon, including polycyclic aromatic hy-drocarbons, phthalates.
Текст научной статьи Микробное разнообразие в глинисто-солевых шламах калийного предприятия (г. Березники, Пермский край)
Верхнекамское месторождение калийно-маг-ниевых и натриевых солей (ВМКМС) Пермского края является одним из крупнейших среди разрабатываемых в мире. В результате деятельности калийных комбинатов предприятий ПАО «Уралкалий» (г. Соликамск и Березники, Пермский край) образуются значительные объемы глинисто-солевых шламов и избыточных рассолов, которые хранятся в специальных гидротехнических сооружениях - шламохранилищах. Формирование состава шламов определяется, в первую очередь, составом добываемого сырья, а также технологическими факторами последующей рудоподготовки и обогащения, что обусловливает присутствие в них, наряду7 с легкорастворимыми хлоридными минералами, широкого спектра тяжелых металлов и органических соединений [Бачурин, Одинцова, 2009]. Основным источником последних являются используемые технологические химические реагенты и продукты их трансформации, главными вещест ве Корсакова Е. С. Шестакова Е. А., Одинцова Т. А., Бачурин Б. А., Плотникова Е. Г., 2017
вами преобразования которых являются полиэток-сильные соединения (полигликоли, полиоксиалканолы и ИХ эфиры, диоксоланы, диоксаны И Др.)к гетероциклы углеводородные структуры. включая полициклическую ароматику7 и фталаты [Бачурин. 2008: Бачурин, Одинцова, Первова. 2014].
По результатам эколого-геохимических исследований было обнаружено, что аккумулированные в глинисто-солевых шламах органические поллютанты служат мощными источниками 'загрязнения природных экосистем благодаря их высокой геохимической подвижности и могут рассматриваться как потенциальные вторичные источники контаминации гидросферы - высвобождение их из связанного состояния может происходить при выщелачивании отходов атмосферными осадками [Бачурин, Одинцова, 2006; Бачурин, 2012; Бачурин, Сметанников, Хохрякова, 2014]. В связи с этим при такой комплексной нагрузке абиотических факторов на территории шламохра-нилищ возникают условия для формирования уникальных сообществ галофильных и галотолерангных микроорганизмов, в том числе способных разлагать экотоксиканты.
Ранее из шламов района солеразработок ВМКМС были выделены и охарактеризованы бак- терии-дестру кторы полицикли ческих ароматических углеводородов и фталатов родов Rhodococ-cus^ Pseudomonas, Arthrobacter, Bacillus [Плотникова и др.. 200 L 2 011; Ястребова и др., 2009: Пастухова и др., 2010: Корсакова, Пьянкова. Плотникова. 2013; Кандаурова, Ястребова, Плотникова. 2016]. Описаны новые таксоны архей и прокариот, выделенные из продуктов флотационного обогащения калийных минералов и техногенных вод шла мохра нилища П АО « Ура лка лий» [ Реутских, Сара лов. 2012: Саралов и др.. 2012а. 20126; Saratov et al., 2013].
Цель настоящей работы - изучение бактериального сообщества глинисто-солевых шламов калийного предприятия БКПРУ-2 ПАО «Уралкалий» в г. Березники (Пермский край).
Материалы и методы исследования
Образцы шламов. В качестве материала для исследования были выбраны пять образцов, отобранных из шла мохра нилища калийного предприятия БКПРУ-2 ПАО «Уралкалий» (г. Березники) (табл. 1).
Таблица 1
Характеристика образцов глинисто-солевых шламов
|
№ образца шлама |
Регистрационный № |
Точка отбора, глубина отбора |
Минерализация, мг/кг |
ХБА\ мг/кг |
Н1Г\ мг/кг |
|
1 |
219/1 |
И [дам из шурфа № 1, о.3 м |
2641MJ |
902.5 |
312.5 |
|
2 |
220/2 |
Шлам из шурфа № 1, 0.5 м |
26400 |
817.5 |
265.0 |
|
3 |
221/3 |
Шлам из шурфа № 2, 0,2 м |
22650 |
932.5 |
340.0 |
|
4 |
222/4 |
Шлам из шурфа № 3. 0.2 м |
35800 |
1111.0 |
349.0 |
|
5 |
222/5 |
11 [лам из шурфа Яо 3, 0.4 м |
43000 |
но/** |
но. |
Примечание. ХБА - хлороформенный битумоид (компонент органического вещества, извлекаемый из горной породы органическим растворителем - хлороформом, без предварительной обработки соляной кисло гой). НП -нефтепродукты; и,о, - не определяли [Бачурин, Одинцова, 2009],
Для выделения и роста микроорганизмов была использована минеральная среда Раймонда (МСР) (Raymond, 1961) с добавлением NaCl (50 г/л). Агаризованные среды получали при добавлении агара («Sigma». США) в концентрации 15 г/л. Для приготовления богатой среды Раймонда (Б СР) в МСР добавляли 5 г/л триптона («Fluka», США) и 2.5 г/л дрожжевого экстракта («Difco», США) в качестве ростовых субстратов
Микробиологический анализ образцов шламов проводили общепринятыми методами посева почвенной суспензии на агаризованную БСР с последующим подсчетом колоний микроорганизмов (колониеобразующих единиц, КОЕ) и выделением бактерий из единичных колоний для идентификации [Методы ..., 1991]. Биоразнообразие и плотность видов бактерий -деструкторов оценивали с помощью индексов Шеннона-Уивера. Симпсона и Менхиника. используя дифференцированный подсчет колоний, принадле жащих к разным морфо(геномо)типам [Широких и др.. 2013; Орлова, 2013].
Способность бактерий разлагать ароматические углеводороды оценивали путем культивирования на агаризованной МСР (30 г/л NaCl) при 28°С с добавлением моно( полихроматических углеводородов («Fluka», США) в качестве единственного источника углерода и энергии. Нафталин, бифенил, бензол, толуол, фенол и дибутилфталат помещали на крышку перевернутой чашки Петри; орто- фталевую кислоту (у-ФК), бензойную (БК), цйрт-гидроксибензойную кислоты (ПГБК) вносили в среду до конечной концентрации 1 г/л, салициловую кислоту7 - до 0.5 г/л. Рост колоний бактерий на агаризованных средах с углеводородами оценивали по сравнению с ростом на агаризованных средах того же состава без субстратов (контрольный вариант). Колонии диаметром менее 1 мм оценивали как «+». 1-2 мм - «++», более 3 мм - «+++».
Рост микроорганизмов при изменении осмолярности среды. Изучение устойчивости микроорганизмов к NaCl (0-200 г/л) проводили на ага-ризованной среде БСР. оценивая размер выросших колоний.
Рост при разных значениях pH определяли при концентрации Na' 0.8-0.85 М в буферных системах, приготовленных на основе БСР. Штаммы культивировались на чашках Петри на агаризо-ванной среде при pH 5.0, 6.0, 7.0. 8.0, 9.0. Рост учитывали на седьмой день культивирования [Герхардт и др.. 1983].
Рост при разных температурах. Штаммы культивировали на агаризованной БСР (30 г/л NaCl) при 10, 20. 28. 37 и 45°С. Рост учитывали на седьмой день культивирования.
ДНК-тонирование полученных бактериальных изолятов проводили методом ВОХ-ПЦР (полимеразная цепная реакция повторяющихся ВОХ-элементов) с использованием праймера BOXA1R (5 -CTACGGCAAGGCGACGCTGACG-3’) в соответствии с методикой [Versalovic et al, 1994]. Продукты реакции разделяли электрофорезом в 1.5%-ном агарозном геле на 1 х ТВЕ буфере (89 мМ Трис-НО, 89 мМ борная кислота. 2,5 мМ ЭДТА, pH 8.2) в течение 2 ч. при напряжённости электрического поля 5.7 V/см и анализировали полученные фрагменты.
Филогенетический анализ полученных изо-лятов был основан на определении нуклеотидных последовательностей гена 16S рРНК с применением набора реактивов Big Dye Terminator Cycle Se quencing Kit на автоматическом секвенаторе Genetic Analyser 3500XL («Applied Biosystems», США) в Пермском государственном национальном исследовательском университете (кафедра ботаники и генетики растений). Полученные нуклеотидные последовательности были проанализированы с использованием программ CLUSTAL W, Sequence Scanner v. 2.0. Mega v. 7.0. Поиск гомологичных последовательностей проводили по базам данных GenBank и EzTaxon (http://www. .
Результаты и их обсуждение
Методом прямого высева на агаризованную БСР с содержанием 50 г/л NaCl из образцов шламов было выделено 138 штаммов бактерий. Отбор осуществлялся на основе различий в морфологии колоний микроорганизмов, растущих на агаризованной среде. В результате были сформированы 34 морфологические группы, представители которых были взяты для проведения дальнейших исследований.
Проведена сравнительная характеристика представителей наиболее сходных морфогрупп с применением метода ВОХ-ПЦР. Анализ полученных ВОХ-ПЦР профилей фрагментов геномной ДНК исследуемых бактерий показал, что 22 штамма, близких по морфологическим признакам, принадлежат к 16 геномогруппам (рис. 1). Согласно полученным результатам, выделенные штаммы бактерий были объединены в 28 морфогеномогрупп, далее обозначенных как репрезентативные операционные таксономические единицы (ОТЕ).
М12345678 9 10 11 М 12 13 14 15 16 17 18 19 20 М 21 22
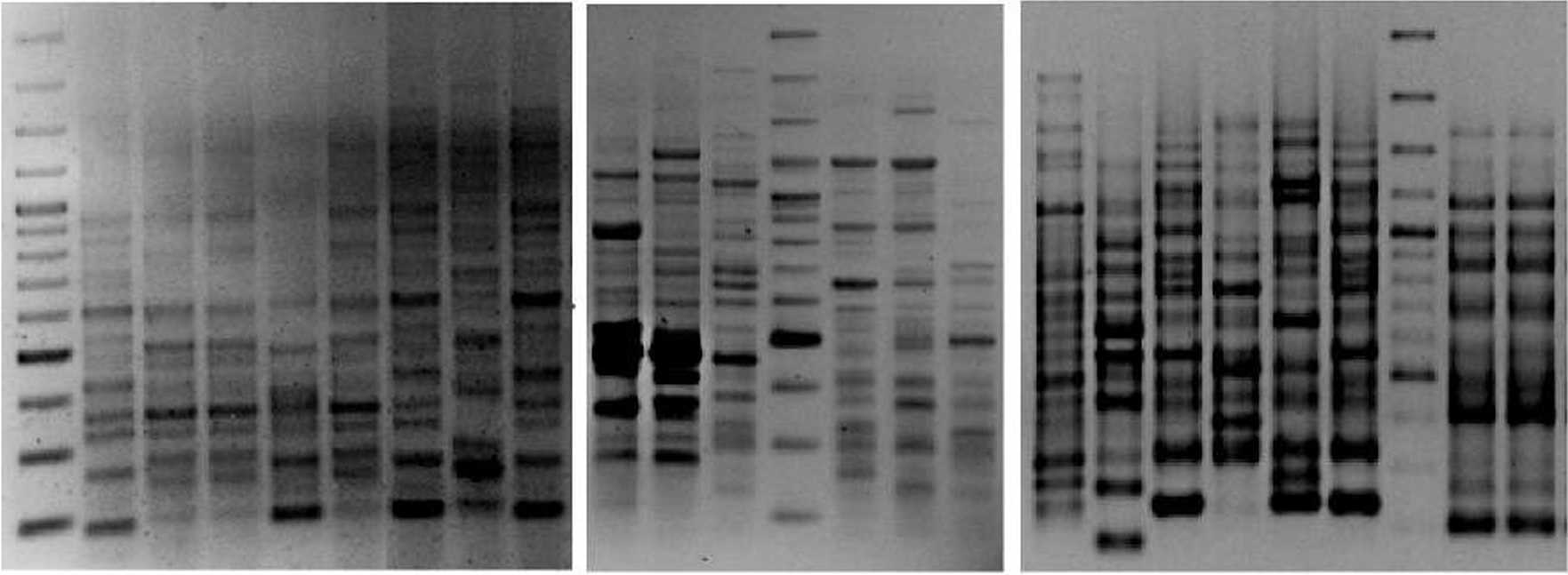
'—у—' 4—у—'
1 11 111 II 1 IV 1 V VI Vil VIII IX X XI XII XIII XIV XV XIII XVI
Рис. 1. Электрофореграмма продуктов ВОХ-ПЦР штаммов бактерий, изолированных из образцов шламов:
М
- маркер O’GeneRuler™ 100 bp Plus DNA Ladder («Fermentas», Литва), 7 - ВОЮ;
2
- ВОН;
3
- ВО 14:
4 -
ВО22;
5
- ВО26:
6 -
ВО36; 7 - ВО23; 5 - ВО8;
9
- ВОЮ;
10
- ВО34-1; 7 7 - ВО25; 7 2 - ВО9:
13 -
ВО20;
14 -
ВО35; 75 - ВО13;
16
- ВО27;
17 -
ВО28; 719 - ВОЗО; 20 - ВОЗ 1; 21 - ВО 1; 22 - Rhodococcus sp. КТ723 (штамм-деструктор нафталина из рабочей коллекции Лаборатории молекулярной микробиологии и биотехнологии ИЭГМ УрО РАН)
Была проведена статистическая оценка альфа-разнообразия представленных микробных сообществ с использованием индесов Шеннона-Уивера (придает большее значение уникальным ОТЕ) и Симпсона (общим ОТЕ), показавшая примерно равные показатели биоразнообразия и выравнен-ности сообществ в исследуемых пробах. Однако, согласно проведенному анализу, образец шлама № 5 характеризуется гораздо большим биоразнообразием уникальных ОТЕ по индексу Шеннона-Уивера (Н'=1.316) и меньшим значением общих ОТЕ (D=0.319) при сравнении с пробами № W. Большое количество морфогеномогрупп, низкая численность изолированных бактерий и высокий уровнь минерализации (43000 мг/кг) данной пробы могут быть непосредственно связаны с присутст вием галотолерантных и галофильных форм микроорганизмов (табл. 1). Расчет плотности видов (видового богатства) в сообществе по индексу Менхиника (DMn) показал, что наибольшее значение данного параметра выявлено в образце шлама № 2, в котором, в свою очередь, была обнаружена высокая численность бактерий (7.84 хЮ1) и малое количество представленных морфотипов (табл. 2). Вероятно, что такие особенности связаны с параметрами данной пробы, а именно с отбором с глубины 0.5 м. на котором воздействие неблагоприятных биотических факторов снижается (в том числе вымывание бактерий из образца шлама атмосферными осадками), что обусловливает высокую численность обнаруженных бактерий
Таблица 2
Анализ разнообразия микробных сообществ образцов шламов
|
Номер образца |
Количество ОТЕ |
Общая численность бактерий, КОЕ/1 г шлама |
Индекс Менхиника (Dwn) |
Индекс 111енно-на-Уивсра (1Г) |
Индекс Симпсона (D) |
|
1 |
13 |
6.35*10° |
0.005 |
0.839 |
0.463 |
|
2 |
10 |
7.84*10" |
0.011 |
1.077 |
0.469 |
|
3 |
15 |
7.35*10° |
0.006 |
1.047 |
0.475 |
|
4 |
13 |
2.72*10° |
0.008 |
0.996 |
0.482 |
|
5 |
14 |
2.27*10° |
0 009 |
1.316 |
0.319 |
В результате сравнения последовательностей гена 16S рРНК (у 28 изолятов. представителей каждой морфогеномогруппы) с типовыми видами из базы данных EzTaxon (http://www.ezbiocloud. net) установлено, что 7 культур являются представителями класса Bacilli, 8 штаммов относятся к классу
Crnnmuproteobcctenck 11 штаммов - к классу А cli-nobacteria и 2 штамма - к классу' Alphaproteobac-lena. Уровень сходства 16S рДНК изолятов с типовыми штаммами узаконенных видов находился в пределах 98.1-100% (табл. 3).
Таблица 3
Анализ нуклеотидных последовательностей генов 16S рРНК изолированных бактерий
|
№ штамма |
Типовой штамм |
№ GenBank |
Сходство, % |
Количество нуклеотдов |
|
ВО1 |
Rhodococcus wradslaviensisMCMB 13082т |
Z37138 |
99.9 |
800 |
|
ВО2 |
Rhodococcus fascians DSM 20669т |
X79186 |
100 |
819 |
|
ВОЗ |
Bacillus pumilus ATCC 7061T |
ABRX01000007 |
99.9 |
1426 |
|
ВО4 |
Bacillusfmrms NCIMB 9366T |
X60616 |
99.3 |
908 |
|
ВОЗ |
Bacillus thiiringiensis AICC 107921 |
ACNF01000156 |
100 |
915 |
|
ВО6 |
Bacillus safens is РО-ОЗбЬ1 |
AF234854 |
99.9 |
935 |
|
BOS |
Pseudomonas xanthomarina KMM 14471 |
.ABI 76954 |
987 |
1401 |
|
ВО9 |
Dietzia mans DSM 436721 |
X79290 |
99 8 |
904 |
|
BOI 1 |
Pseudomonas xanthomarina KMM I4471 |
AB 176954 |
990 |
1434 |
|
BOIS |
Stenotrophomonas maltophiho ATCC 136371 |
AB008509 |
100 |
930 |
|
BOIS |
Bacillus safensis FO-ОЗбЬ1 |
AF234854 |
100 |
923 |
|
BO19 |
ArthrobacTer oxydans DSM 201191 |
X83408 |
100 |
1233 |
|
BO20 |
DiOzia mans DSM 436721 |
X79290 |
99.9 |
887 |
|
BO21 |
Anhrobacter oxydans DSM 201191 |
X83408 |
99.2 |
1388 |
|
BO22 |
Pseudomonas xanthomanna KMM 14471 |
AB 176954 |
99.0 |
1438 |
|
BO23 |
Pseudomonas xanthomarbta KMM 14471 |
AB 176954 |
99.2 |
1404 |
|
BO24 |
Pseudomonas xauthomanna KMM 14471 |
AB 176954 |
99.2 |
1421 |
|
BO25 |
Arthrobacter nicotianae DSM 20123T |
X80739 |
99.1 |
1387 |
|
BO27 |
Stenotrophomonas maiiophdia ATCC 136371 |
AB008509 |
99.2 |
769 |
|
BO28 |
Paracoccus beibnensrs ЛЛ’1284Т |
EU65OI96 |
98.1 |
1330 |
|
возо |
Paracoccus beibnensis JI Л 1284T |
EU650196 |
98.2 |
1330 |
|
BO32 |
Pseudomonas mon lei Id CIP 104883T |
AF064458 |
99.5 |
927 |
|
возз |
Bacillus vietnamensis 15-lT |
AB099708 |
99.0 |
604 |
Окончание табл. 3
|
№ штамма |
Типовой штамм |
№ GenBank |
Сходство, % |
Количество нуклеотидов |
|
ВО34-1 |
Arthrobacter oxydems DSM 20119 1 |
X83408 |
100 |
1401 |
|
ВО35 |
Kocuria rosea DSM 204471 |
X87756 |
99 7 |
972 |
|
ВО37 |
Micrococcus luteus NCTC 26651 |
CP001628 |
100 |
414 |
|
ВО38 |
StrepTomyces somaiiensis NBRC 129161 |
AB 184243 |
100 |
1392 |
|
ВО141 |
Bacillus plexus IFO 157151 |
AB021185 |
100 |
722 |
Согласно полученным результатам, преимущественным значением среди выделенных бактериальных штаммов обладали представители классов Aciinobacieria и Gammaproieobacteria, а именно -бактерии родов Dietzia (31.77%) и Stenotrophomo-nas (46Л%), соответственно (рис. 2). Что характерно. наибольшим многообразием таксономических групп характеризовались микроорганизмы класса Actinobacteria. среди которых доминирующее положение занимали изоляты, филогенетически близкородственные к бактериям рода Dietzia. Менее многочисленными были бактерии родов Аг-throbactey Кос uh а, Micrococcus, Rhodococcus и Streptomyces (в порядке уменьшения количества КОЕ/1 г шлама).
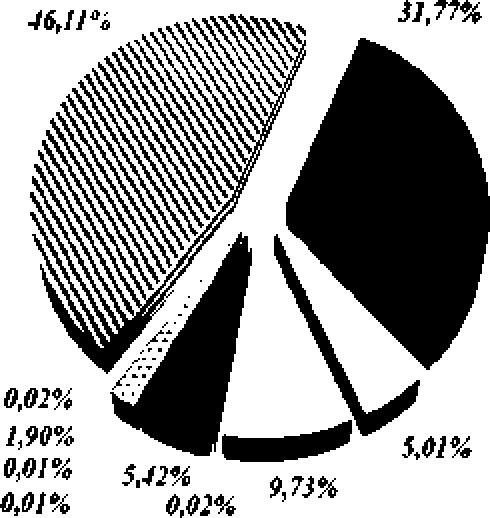
7, RhodOCOCCHS sp.
«BociHus sp.
’frSfenotrophomcmfis sp.
■ №№ sp.
Arthrobader sp.
Pseudomonas sp.
■ Porncoccus sp.
• Micrococcus sp.
•Streptomyces sp.
* Kocuria sp.
Рис. 2, Относительное содержание различных филогенетических групп (родов) бактерий классов A ct / по ba с ten а ,А Iphaproteob ас teri а.
Bacilli и Gammaproteobacteha
В результате изучения биодеградационных свойств 28 штаммов (представителей сформированных ОТЕ) было выявлено семь наиболее активных штаммов-деструкторов VArthrobacter spp. BOI 9, BO25t Bacillus spp. BO4, BO33, Kocuria sp. BO35, Paracoccus sp. BO28 и Rhodococcus sp. BOI), обладающих широкой субстратной специфичностью и способных использовать в качестве единственного источника углерода и энергии такие соединения, как нафталин, бифенил, орто- фталевую. бензойную, и^^-гидроксибензойную. салициловую кислоты, а также фенол, толуол и бензол. Стоит отметить, что большинство штаммов росли на моно- и полиароматических соединениях, но были также обнаружены бактерии (штаммы Rhodococcus sp. BOL Dietzia sp. BO9, Arthro-bacter spp. БО25, BO34-1, Bacillus sp. ВОЗЗ). использующие в качестве субстрата широко используемое в химической промышленности, труднораз-лагаемое и токсичное соединение - дибутилфталат (табл. 4).
Кроме того, было установлено, что все изолированные бактериальные культуры способны к росту на агаризованной среде как без добавления NaCl, так и с повышенной концентра дней соли (30-150 г/л), т.с. являются галотолсрантными организмами [Кашнер, 1981]. Среди них присутст-в>ют штаммы, обладающие способностью к росту при особенно высоких концентрациях хлорида натрия -до 150 г/л, а именно спорообразующис бактерии рода Bacillus (табл. 5).
Таблица 4
Рост бактерий на ароматических углеводородах на агаризованной МСР
|
Штамм |
Субстрат |
|||||||||
|
Фен. |
Бен, |
Тол. |
Наф, |
Биф, |
О-ФК |
БК |
СК |
ПГБК |
ДБФ |
|
|
Rhodococcus sp. BOI |
+++ |
++ |
+ |
+++ |
++ |
+44 |
+ |
++ |
++4 |
++ |
|
Rhodococcus sp. BO2 |
- |
+++ |
++ |
++ |
++ |
44 |
+ |
++ |
++4 |
4 |
|
Bacillus sp. BO3 |
+ |
+ |
+ |
+ |
4 |
44 |
+ |
+ |
4 |
+ |
|
Bacillus sp. BO4 |
+++ |
++ |
+4 |
+++ |
444 |
+44 |
++ |
+++ |
++ |
— |
|
Bacillus sp. BO5 |
+ |
+ |
— |
+ |
4 |
4 |
— |
— |
— |
— |
|
Bacillus sp. BO6 |
44 |
+ |
+ |
4 |
4 |
44 |
4 |
4 |
— |
|
|
Pseudomonas sp. BOS |
+ |
++ |
4 |
4 |
4 |
4 |
4 |
4 |
||
|
Dictzia sp. BO9 |
+ |
-И- |
4 |
4 |
+44 |
4+4 |
4 |
++ |
||
|
Pseudomonas sp. BO11 |
44 |
++ |
+ |
++ |
++ |
+44 |
4+4 |
++ |
||
|
Stenotrophomouas sp. BO 13 |
44 |
+ |
— |
++ |
++ |
44 |
4 |
++ |
||
|
Bacillus sp. BOIS |
4 |
+ |
+ |
++ |
++ |
44 |
4 |
4 |
||
|
Arthrobacter sp. BOW |
44 |
+ |
+ |
++ |
4 |
+44 |
++ |
++ |
++ |
|
|
Dietzia sp, BO20 |
44 |
++ |
+ |
4 |
4 |
4+4 |
++ |
4 |
||
|
Arthrobacter sp. BO21 |
44 |
++ |
+ |
4 |
44 |
4 |
4+4 |
4+ |
4+ |
— |
Окончание табл. 4
|
Штамм |
Субстрат |
|||||||||
|
Фен. |
Бен, |
Тол. |
Наф. |
Биф. |
о-ФК |
БК |
СК |
ПГБК |
ДБФ |
|
|
Pseudomonas sp. БО22 |
++ |
— |
+ |
++ |
+4- |
+ |
++ |
+ |
— |
|
|
Рдегк/утунил’ sp. BO23 |
+ |
++ |
— |
++ |
++ |
— |
+++ |
+ |
+ |
— |
|
Pseudomonas sp. BO24 |
+ |
++ |
— |
4-4- |
4- |
— |
+4-4- |
4+ |
+ |
— |
|
Arthrobacter sp. BO25 |
+++ |
+++ |
+++ |
+++ |
++4- |
+4- |
+++ |
++ |
+++ |
+++ |
|
Sfenotraphomonas sp. BO27 |
-н- |
++ |
+ |
4- |
4- |
4- |
+ |
+ |
+ |
— |
|
Paracoccus sp. B02S |
+++ |
+++ |
+ |
-Н- |
-Н- |
+4- |
4-Н- |
4-Н- |
+ |
+ |
|
Paracoccus sp. BO 30 |
+ |
+ |
+ |
4- |
+ |
4- |
+ |
+ |
— |
|
|
Pseudomonas sp. BO32 |
-н- |
++ |
-Н- |
-Н- |
4- |
+ |
+ |
4-Н- |
— |
|
|
Bad Hus sp. BO33 |
-н- |
+++ |
+ |
4- |
4- |
-Н- |
+ |
+ |
+ |
+++ |
|
Arthrobacter sp. BO34-1 |
— |
+ |
4- |
-Н- |
+4- |
+ |
+ |
4-Н- |
+++ |
|
|
Коси ria sp, BO35 |
+++ |
++ |
++ |
-Н- |
-Н- |
+4- |
+ |
+ |
+ |
— |
|
Micrococcus sp, BO37 |
+++ |
+ |
-Н- |
-Н- |
+4- |
+ |
+ |
+ |
— |
|
|
Streptomvces sp, B03S |
+++ |
+ |
-Н- |
-Н- |
+4- |
4-Н- |
++ |
-н- |
— |
|
|
Bacillus sp. BO141 |
++ |
— |
— |
4-4- |
-НН- |
4-Н- |
++ |
++ |
-н- |
— |
Примечание. Фен. - фенол; Бен. - бензол; Тол. - толуол; Наф. - нафталин; Биф. - бифенил; о-ФК - орто- фталевая кислота; БК - бензойная кислота; СК - салициловая кислота; ПГБК - нстрл-гидрокеибензойная кислота; ДБФ - дибутил фталат.
Таблица 5
Рост бактерий в присутствии различных концентраций NaCl
|
Штамм |
Концентрация NaCl (г/л)} среда БСР |
|||||||||
|
Без NaCl |
30 |
50 |
60 |
70 |
S0 |
90 |
100 |
120 |
150 |
|
|
Rhodococcus sp. BOI |
+++ |
+++ |
+++ |
+++ |
+++ |
++ |
++ |
+ |
||
|
Rhodococcus sp. BO2 |
++ |
+++ |
+ |
+ |
— |
- |
— |
— |
- |
- |
|
Bacillus sp. BO3 |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+ |
|
Bacillus sp. BO4 |
+++ |
+++ |
+++ |
+++ |
++ |
++ |
+ |
++ |
+ |
- |
|
Bacillus sp. BO 5 |
+++ |
+++ |
+++ |
+++ |
+ |
- |
— |
— |
- |
- |
|
Bacillus sp. BOO |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
++ |
+ |
|
Pseudomonas sp. BOS |
+++ |
+++ |
++ |
+ |
+ |
+ |
+ |
— |
- |
- |
|
Dietzia sp. BO9 |
+ |
4-Н- |
++ |
++ |
4-Н- |
+ |
+ |
— |
||
|
Pseudomonas sp. BO 11 |
-НН- |
4-Н- |
-НН- |
-НН- |
+4 |
4-4 |
+ |
+ |
||
|
Stenotrophomonas sp. BO13 |
-НН- |
4-Н- |
-нн- |
+ |
+ |
+ |
+ |
— |
||
|
Bacillus sp. BOIS |
-НН- |
4-Н- |
-нн- |
-нн- |
4-Н- |
4-Н- |
4-Н- |
4-Н- |
-НН- |
+ |
|
Arthrobacter sp. BO 19 |
-НН- |
4-Н- |
++ |
+ |
+ |
+ |
+ |
— |
||
|
Dietzia sp BO20 |
4- |
4-Н- |
-н- |
-н- |
+ |
+ |
+ |
— |
||
|
Arthrobacter sp. BO2 1 |
-нн- |
4-Н- |
++ |
+ |
— |
|||||
|
Pseudomonas sp, BO22 |
-н- |
4-Н- |
++ |
++ |
+ |
+ |
+ |
— |
||
|
Pseudomonas sp, BO23 |
-н- |
4-Н- |
++ |
++ |
+4 |
4-4 |
+ |
+ |
||
|
Pseudomonas sp, BO24 |
-н- |
4-Н- |
++ |
++ |
+4 |
4-4 |
+ |
+ |
||
|
Arthrobacter sp, BO25 |
-нн- |
4-Н- |
-нн- |
-нн- |
4-Н- |
4-Н- |
4-Н- |
4-Н- |
4-+ |
— |
|
Stenotrophomonas sp. BO27 |
+++ |
+++ |
+ |
— |
— |
— |
— |
— |
— |
— |
|
Patacoccus sp. BO28 |
+++ |
+++ |
++ |
++ |
++ |
+ |
+ |
— |
— |
— |
|
Paracoccus sp. BO30 |
+++ |
+++ |
+ |
+ |
— |
- |
— |
— |
- |
|
|
Pseudomonas sp, BO32 |
+++ |
+++ |
++ |
+ |
— |
- |
— |
— |
- |
|
|
Bacillus sp, BO33 |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+ |
|
Arthrobacter sp. BO34-1 |
+++ |
+++ |
++ |
+ |
— |
- |
— |
— |
- |
- |
|
Kocuria sp. BO35 |
+++ |
+++ |
+++ |
+++ |
+++ |
++ |
+ |
+ |
- |
- |
|
Micrococcus sp. BO37 |
+++ |
+++ |
+++ |
+++ |
+++ |
++ |
+ |
+ |
+ |
- |
|
Streptomvces sp. BO38 |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
++ |
- |
|
Bacillus sp. BO141 |
+++ |
+++ |
+++ |
+++ |
+++ |
++ |
++ |
++ |
++ |
- |
Примечание. «+» - слабый роет, «++» - средний рост; «+++» - хороший рост; «-» - отсутствие роста бактерий,
Также был исследован диапозон роста бактерий при различных значениях pH в среде культивирования и при различной температуре. Установлено, что значительная часть изолятов (Bacillus spp.
ВОЗ? ВО4, ВОЗ, ВО IX, Rhodococcus Sp, ВО2, Arthrobacter sp, BO25, Pseudomonas sp. BO32) способна к эффективному росту при pH среды от 6,0 до 9,0. Штамм Rhodococcus sp. ВО1 характерно- вался ростом в более широком диапазоне значений pH среды (от 5,0 до 9,0).
У ряда исследуемых штаммов (Bacillus spp. ВОЗ. ВО18, ВО141, Pseudomonas spp. BOIL BO14, BO26, Paracoccus sp. ВОЗО и Kocuria sp. BO35) была отмечена способность к росту в диапазоне температур от +10°С до 45°С (с оптимумом роста 28°С). относящая их к термотолерантным микроорганизмам. При температуре ниже 10°С рост культуры не наблюдался или был незначительным.
Интересен тот факт, что среди изолированных бактерий встречаются штаммы, сходные по филогенетическому положению с одним и тем же типовым штаммом бактерий, но отличающиеся по ВОХ-ПЦР профилям фрагментов геномной ДНК. субстратной специфичности, а также способности к росту на средах с различными значениями pH и концентрации NaCL Так, например, выявлено 5 штаммов (ВО8. BOIL ВО22. ВО23. ВО24). которые имеют наибольший процент сходства по нуклеотидной последовательности гена 16S рРНК с типовым видом Pseudomonas xanthomarina КММ 1447Т. но при этом существенно различаются по утилизации ароматических соединений (табл. 4), а штамм Pseudomonas sp. ВОН может эффективно использовать в качестве единственного источника углерода орто-фталевую кислоту.
Заключение
В результате исследования микробного сообщества образцов глинисто-солевых шламов из шла-мохранилища БКПРУ-2 ПАО «Уралкалий» (г. Березники, Пермский край) получены новые данные по филогенетическому разнообразию культивируемых бактерий района Верхнекамского месторождения солей. Выделено 138 штаммов бактерий-деструкторов различных ароматических углеводородов, в том числе фталатов филогенетический анализ показал принадлежность изо лированных штаммов к трем классам: Alphaproteobacteria. Gammaproteobacteria и Actinobacteria: десяти родам: Arthrobacter. Bacillus. Dietzia, Kocuria. M i crococcus, Pa racoccus, Pseudomona s. Rhodococcus, Stenotrophomonas и Streptomyces. При изучении их биодеградационных свойств выявлено семь наиболее активных штаммов-деструкторов, способных использовать в качестве ростового субстрата различные углеводороды: нафталин, бифенил. фенол, толуол и бензол, бензойную . пара -гидроксибензойную, салициловую кислоты, а также ([палаты (орто-фталат, дибутил-фталат), Кроме того, показано, что все изоляты являются галотолерантами (растут в присутствии 100-150 г/л NaCl), а ряд из них - алкалафилами (растут в диапазоне значений pH до 9.0).
Таким образом. установлено, что в районах шламохранилищ сформированы уникальные мик робные сообщества, в состав которых входят солеустойчивые бактерии-деструкторы ароматических соединений, являющихся одними из характерных экотоксикантов отходов калийного производства. Выявленные активные галотолерантные бактерии-деструкторы фталатов, моно(поли)ароматических углеводородов перспективны для дальнейшего изучения и использования при создании новых биотехнологий ремедиации территорий с высокой минерализацией и контаминацией стойкими органическими загрязнителями.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 16-44-590968 р_а и Программами УрО РАН «Молекулярная и клеточная биология» (проект №15-4-4-13) и «Фундаментальный базис инновационных технологий оценки, добычи и глубокой комплексной переработки стратегического минерального сырья» (проект №15-11-5-24).
Список литературы Микробное разнообразие в глинисто-солевых шламах калийного предприятия (г. Березники, Пермский край)
- Бачурин Б.А. Эколого-геохимическая характеристика отходов калийного производства//Горный журнал. 2008. Т. 10. С. 88-91
- Бачурин Б.А. Эколого-геохимические аспекты выщелачивания техногенно-минеральных образований горного производства//Материалы Всероссийской конференции с участием иностранных ученых «Геологическая эволюция взаимодействия воды с горными породами». 2012. С. 199-202
- Бачурин Б.А., Одинцова Т.А. Органическая геохимия техногенеза горнопромышленного профиля//Минералогия техногенеза. 2006. Т. 7. С. 265-284
- Бачурин Б.А., Одинцова Т.А. Отходы горнообогатительного производства как источники эмиссии органических поллютантов//Горный информационно-аналитический бюллетень. 2009. Вып. 7. С. 374-380
- Бачурин Б.А., Одинцова Т.А., Первова Е.С. Эколого-геохимическая характеристика флотореагентов//Материалы II-й Всероссийской научной виртуальной онлайн-конференции «Химическая наука: современные достижения и историческая перспектива». 2014. С. 17-22
- Бачурин Б.А., Сметанников А.Ф., Хохрякова Е.С. Эколого-геохимическая оценка продуктов переработки глинисто-солевых шламов калийного производства//Современные проблемы науки и образования. 2014. № 6. С. 1-8
- Герхардт Ф. и др. Методы общей бактериологии. М.: Мир. 1983. Т. 1-3
- Кандаурова Ю.М., Ястребова О.В., Плотникова Е.Г. Бактерии-деструкторы орто-фталевой кислоты, выделенные из района добычи и переработки калийных солей (г. Березники, Пермский край)//Материалы ХIV Всероссийской научнопрактической конференции с международным участием «Биодиагностика состояния природных и природно-техногенных систем». Киров, 2016. С. 329-332.
- Кашнер Д. Жизнь микробов в экстремальных условиях. М.: Мир. 1981. 365 с
- Корсакова Е.С., Пьянкова А.А., Плотникова Е.Г. Бактерии-деструкторы стойких органических загрязнителей -эфиров фталевой кислоты, как основа для создания новых экобиотехнологий//Известия Самарского научного центра РАН. 2013. Т. 15, № 3 (5). С. 1633-1636
- Методы почвенной микробиологии и биохимии: учеб. пособие/под ред. Д.Г. Звягинцева. М.: Изд-во МГУ, 1991. 304 с
- Орлова Ю.С. Использование индексов биологического разнообразия для анализа альгофлоры бассейна р. Алатырь//Вестник Мордовского университета. 2013. Т. 3/4. С. 53-57
- Пастухова Е.С. и др. Бактерии-деструкторы ортофталевой кислоты, выделенные из отходов калийного производства//Вестник Пермского университета. Сер. Биология. 2010. Вып. 3. С. 24-29
- Плотникова Е.Г. и др. Бактерии-деструкторы полициклических ароматических углеводородов, выделенные из почв и донных отложений района солеразработок//Микробиология. 2001. Т. 70, № 1. С. 61-69
- Плотникова Е.Г. и др. Галотолерантные бактерии рода Arthrobacter -деструкторы полициклических ароматических углеводородов//Экология. 2011. № 6. С. 459-466
- Реутских Е.М. Саралов А.И. Exiguobacterium sp. RS34 -галоалкалотолерантная факультативно анаэробная неспорообразующая бактерия порядка Bacillales из шламохранилища калийного рудника//Вестник Пермского университета. Сер. Биология. 2012. Вып. 3. С. 49-53
- Саралов А.И. и др. Arhodomonas recens sp. nov. -умеренно галофильная гаммапротеобактерия из рассолов флотационного обогащения калийных минералов//Микробиология. 2012а. Т. 81, № 5. C. 630-637
- Саралов А.И. и др. Halarchaeum solikamskense sp. nov. -термо-толерантный нейтрофильный галоархаеон из пенных продуктов флотационного обогащения калийных минералов//Микробиология. 2012б. Т.81, № 5. C. 638-644
- Широких И.Гидр. Численность и структура комплексов почвенных актиномицетов в районе возможного влияния химически опасного объекта//Почвоведение. 2013. Т. 7. С. 860-866
- Ястребова О.В. и др. Разнообразие бактерий, выделенных из района разработок месторождения калийных солей Верхнекамья//Bестник Пермского университета. 2009. Вып. 10 (36). Биология. С. 124-129
- Raymond R.L. Microbial oxidation of nparaffinichydrocarbons.//Developments in Industrial Microbiology. 1961. Vol. 2, № 1. P. 23-32
- Saralov A.I. et al. Haloferax chudinovii sp. nov., a halophilic archaeon from Permian potassium salt deposits//Extremophiles. 2013. Vol. 17(3). P. 499-504
- Versalovic J. et al. Genomic fingerprinting of bacteria using repetitive sequence-based polymerase chain reaction//Methods in Molecular and Cellular Biology. 1994. Vol. 5(1). P. 25-40


