Микробное сообщество техногенно загрязненного грунта района солеразработок (г. Березники)
Автор: Ястребова О.В., Воронина А.О., Ананьина Л.Н., Корсакова Е.С., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2018 года.
Бесплатный доступ
С использованием молекулярно-генетических методов проведено исследование структуры микробного сообщества грунта, расположенного вблизи солеотвала БКПРУ-3 предприятия ПАО «Уралкалий» (г. Березники, Пермский край). Методом ПЦР-РВ фрагментов гена 16S рРНК в тотальной ДНК исследуемого образца грунта выявлено наличие бактериальных генов 16S рРНК в количестве 6.6 х 1011 (±8.87 х 107) копий гена на 1 г грунта, а также доминирование грамотрицательных бактерий. ДГГЭ-анализ генов 16S рРНК, амплифицированных с тотальной ДНК, выявил, что бактериальные сообщества накопительных культур, полученных на бифениле и ортио-фталате, существенно различаются между собой, а также отличаются от исходного сообщества образца грунта как по составу, так и наличием доминирующих видов. Установлено, что в полученных НК доминировали грамотрицательные бактерии классов Gammaproteobacteria и Acidobacteria. Методом ДГГЭ-анализа в исследуемом микробном сообществе выявлены «некультивируемые» бактерии рода Halomonas, ранее не обнаруженные культуральны-ми методами.
Денатурирующий градиентный гель-электрофорез, ген 16s ррнк, некультивируемые бактерии, ортио-фталат, бифенил
Короткий адрес: https://sciup.org/147227017
IDR: 147227017 | УДК: 579.695:579.262:579.222.2
Microbial community of the technogenically polluted soil of salt-mining region (Berezniki)
With the use of molecular-genetic methods a study of the structure of microbial community from the soil located near the BKPRU-3 salt separator of PAO Uralkali (Berezniki, Perm Territory) enterprise was carried out. The presence of 16S rRNA bacterial genes in the amount of 6,6 х 1011 (±8,87 х 107) copies of the gene per gram of soil and the Gram-negative bacteria dominance were detected by the real-time-PCR of the 16S rRNA gene fragments in the total DNA of the soil sample. The DGGE-analysis of 16S rDNA genes, amplified from total DNA, revealed that the bacterial communities of enrichment cultures, obtained on biphenyl and ortAo-phthalate, differed significantly from each other, as well as from the original community of the soil sample, both in composition and in the presence of dominant species. It was established that gram-negative bacteria of Gammaproteobacteria and Acidobacteria classes dominated in the derived enrichment cultures. By the method of DGGE-analysis "uncultivated" bacteria of the genus Halomonas were detected in the investigated microbial community.
Текст научной статьи Микробное сообщество техногенно загрязненного грунта района солеразработок (г. Березники)
Верхнекамское месторождение калийно-магни-евых и натриевых солей (ВМКМС) Пермского края представляет собой многопластовую толщу соленосных отложений и является одним из крупнейших среди разрабатываемых в мире. Обогащение и переработка калийных руд на комбинатах предприятия ПАО «Уралкалий» (г. Соликамск и Березники, Пермский край) сопровождается образованием значитель- ных объемов глинисто-солевых шламов и избыточных рассолов, сбрасываемых в шламохранилища и содержащих более 90% хлорида натрия. Растворение и вынос солей отвалов и шламохранилищ приводит к появлению зон засоления, а также водоемов с соленой водой (рассолосборники), в которых происходит осаждение солей.
В образующихся галитовых отвалах и рассолос-
борниках зафиксирован широкий спектр поллютантов, включая тяжелые металлы и органические соединения, что обусловлено технологическими факторами рудоподготовки и обогащения добываемого сырья [Бачурин, 2008; Бачурин, Одинцова, 2009]. Продуктами трансформации химических реагентов, используемых в данных технологических процессах, являются полиэтоксильные соединения (полигликоли, полиоксиалканолы и их эфиры, диоксоланы, диоксаны и др.), гетероциклы, углеводородные структуры, включая полициклическую ароматику и фталаты [Бачурин, Одинцова, 2009; Бачурин, Одинцова, Пер-вова, 2014].
Сложившиеся условия являются основой для формирования в экосистемах данного района сообществ микроорганизмов, устойчивых к высокому содержанию соли в среде и способных при этом проявлять биодеградационные свойства. Из исследований микробных сообществ различных экосистем известно, что доля микроорганизмов, культивируемых в лабораторных условиях, составляет не более 0.1–1%, большую же часть природных микробных консорциумов представляют некультиви-руемые микроорганизмы [Puspita et. al., 2012; Dickinson et. al., 2016]. В связи с этим необходимы новые методические подходы для выявления и описания некультивируемых бактерий, изучения генетического разнообразия и структуры микробных консорциумов, понимания их экологической роли. Одним из методических подходов при изучении микробного разнообразия является использование метода денатурирующего градиентного гель-электрофореаза (ДГГЭ), который позволяет с высокой точностью проследить изменения состава микробных сообществ разных экосистем под действием различных факторов, определить филогенетическую принадлежность всех представителей сообщества, в том числе некультивируемых микроорганизмов [Назаров и др., 2010; Feris et. al., 2004].
Материалы и методы исследования
Образцы исследования. В районе промышленных разработок Верхнекамского месторождения солей (Пермский край) в весенне-летний период 2016 г. были отобраны образцы почв, шламов, донных отложений рассолосборника, а также грунта на расстоянии 5 м от солеотвала предприятия БКПРУ-3 ПАО «Уралкалий» (г. Березники).
Химический анализ отобранных проб показал высокую степень их засоленности, а также содержание таких органических загрязнителей, как алканы, фталаты, моно- и полиароматические углеводороды [Корсакова и др., 2015].
Оценка количества бактерий грунта была проведена методом полимеразной цепной реакции в реальном времени (ПЦР-РВ). При амплификации бактериальных генов 16S рРНК были использованы праймеры Eub338 (5'-ACTCCTACGGGAGGCAGCAG-3') и Eub518 (5'-ATTACCGCGGCTGCTGG-3') [Fierer et. al., 2005].
ПЦР-РВ проводили в присутствии красителя Sybr Green I в наборе реактивов 2X Maxima SYBR Green/ROX qPCR Master Mix («Thermo Scientific», США) на приборе «CFX96 Touch™ Real-Time PCR Detection Systems» («Bio-Rad Laboratories», США). Для стандартной калибровочной кривой, а также для анализа кривых плавления ДНК (температуры плавления (Tm) дуплекса ДНК) был использован образец очищенной геномной ДНК штамма Pseudomonas sp. SN11. Эффективность ПЦР определяли методом серийных разведений с построением калибровочной кривой.
Накопительное культивирование. Образец грунта был использован для получения двух накопительных культур (НК). В 250 мл колбы с минеральной средой (100 мл) и ароматическим субстратом помещали 1 г образца. НК1 получена с использованием минеральной среды К1 [Zaitsev et. al., 1991] с бифенилом в качестве субстрата. НК2 получена на минеральной среде Раймонда [Розанова, Назина, 1982] с добавлением NaCl (30 г/л) и 1 г/л орто- фталевой кислоты ( орто- ФК) в качестве субстрата.
Выделение тотальной ДНК из образца грунта и накопительных культур проводили с использованием коммерческого набора реактивов «MP Biomedicals» (США). Выделение ДНК из НК1 и НК2 проводили через 1 и 7 месяцев соответственно, с начала культивирования. Концентрацию ДНК определяли на приборе QubitTM Fluorometer («Invi-trogen», США) с использованием реактивов производителя.
Денатурирующий градиентный гель электрофорез (ДГГЭ ). Структуру микробных сообществ исследовали методом ДГГЭ фрагментов гена 16S рРНК, составляющих приблизительно 500 п.н., амплифицированных с использованием эу-бактериальных праймеров 27F (5`-AGAGTTTGATC(A/C)TGGCTCAG-3`) и 518R 518R (5`-ATTACCGCGGCTGCTGG-3`) [Tiirola et al., 2002]. Праймер 27F включал на 5`-конце 40 п.н. GC-хвост (5`-CGCCCGCCGCGC CCCGCGCCCGTCCCGCCGCCCCCGCCCG-3`).
Амплификацию l мкл очищенной геномной ДНК проводили в 50 мкл смеси, содержащей 0,25 мM дНТФ, 0,3 мкM праймера (каждого), 1,5 мМ MgCl 2 , 1х буфер для Taq -полимеразы («Син-тол», Россия), 2 ед. акт. Taq -полимеразы («Син-тол», Россия). Процедура ПЦР включала начальный денатурирующий шаг при 95°С в течение 5 мин. и 30 циклов: 94°С в течение 30 сек., 55°С в течение 1 мин. и 72°С в течение 3 мин.; затем 72°С в течение 10 мин.
Электрофорез был выполнен в 6% полиакриламидном геле, содержащем линейный денатури- рующий химический градиент от 30 до 60%, где 100% составляет 7М мочевина и 40% – формамид, согласно протоколу [Muyzer, de Waal E.C., Uitter-linden, 1993]. Разгонку проводили в течение 16 ч. при 45 V и 60°С на DcodeTM Universal Mutation System («Bio-Rad Laboratories», США). ДНК была визуализирована после окрашивания бромистым этидием (0,5 мкг/мл) UV-трансиллюминацией и документирована системой Gel Doc XR («Bio-Rad Laboratories», США).
Элюирование ДНК осуществляли в стерильной деионизированной воде в течение 24 ч. при температуре 4°С. Элюированную ДНК использовали в качестве матрицы для ПЦР-реам-плификации гена 16S рРНК. Амплификацию гена 16S рРНК проводили с использованием бактериальных праймеров 27F (5`-AGAGTTTGATC(A/C)TGGCTCAG-3`) и 1492R (5`-АСGG(C/T)TACCTTGTTACGACTT-3`) на ам-плификаторе «My Cycler» («Bio-Rad Laboratories», США).
Определение нуклеотидных последовательностей гена 16S рРНК осуществляли с применением набора реактивов Big Dye Terminator Cycle Sequencing Kit на автоматическом секвенаторе Genetic Analyser 3500XL («Applied Biosystems», США) в молекулярно-генетической (ПЦР) лаборатории кафедры ботаники и генетики растений Пермского государственного национального исследовательского университета.
Филогенетический анализ полученных нуклеотидных последовательностей 16S рДНК проводили с использованием программ MEGA 7.0, Sequence Scanner v. 2.0. Поиск гомологичных последовательностей осуществляли при использовании баз данных GenBank и EzTaxon .
Результаты и их обсуждение
С использованием метода ПЦР-РВ в тотальной ДНК, выделенной из образца грунта, отобранного у солеотвала БКПРУ-3, было выявлено наличие бактериальных генов 16S рРНК в количестве 6,6 х 10 11 (±8.87 х 107) копий гена на 1 г грунта. Методом анализа кривых плавления ДНК была установлена Tm исследуемой ДНК, равная 82.5°С, что всего на один градус превышает Tm геномной ДНК штамма Pseudomonas sp. SN11. Основываясь на полученных данных, можно предположить, что нуклеотидный состав анализируемой ДНК незначительно отличается составом GC-пар, что указывает на предполагаемое доминирование грамотри-цательных бактерий в микробном сообществе образца исследуемого грунта.
Проведен ДГГЭ-анализ генов 16S рРНК, ам-плифицированных с тотальной ДНК образца грун-
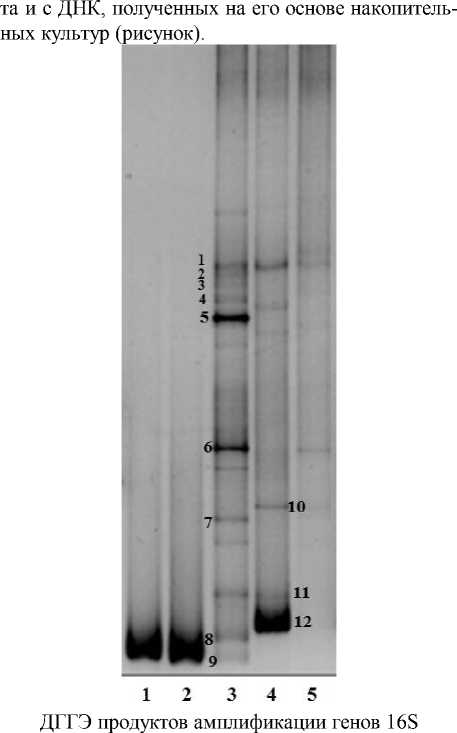
рРНК с препаратов суммарной ДНК техно-геннозагрязненного грунта, отобранного около солеотвала, накопительных культур (НК) и штаммов бактерий.
1 – Rhodococcus sp. PP22-1; 2 – Rhodococcus sp. KBB16; 3 – НК1 с бифенилом в качестве субстрата; 4 – НК2 с орто -ФК в качестве субстрата и присутствием 30 г/л NaCl; 5 – образец грунта
Как показал ДГГЭ-анализ генов 16S рРНК тотальной ДНК образца грунта, исследуемое бактериальное сообщество характеризовалось таксономическим разнообразием. Бактериальные сообщества накопительных культур, полученных на бифениле и орто -фталате, существенно различались между собой, а также отличались от сообщества исходного образца как по составу, так и наличием мажорных (доминантных) полос на ДГГЭ-профиле (рисунок). В ряде работ показано, что при загрязнении почвенных экосистем ароматическими углеводородами менялась видовая структура микробных сообществ, при этом не снижалось бактериальное разнообразие [Feris et. al., 2004; Vin˜as et. al., 2005]. Из других исследований известно, что загрязнение почвы нефтепродуктами приводит к снижению видового разнообразия микробных сообществ при увеличении общей численности бактерий [Панов и др., 2013; Castle, Montgomery, Kirchman, 2006].
|
Фрагменты гена 16S рДНК, отличающиеся цированы. У 12 фрагментов 16S рДНК были опре-электрофоретической подвижностью при разгонке делены нуклеотидные последовательности (рису-(ДГГЭ), были элюированы из геля и реамплифи- нок, таблица). Результаты филогенетического анализа элюированных из геля фрагментов гена16S рРНК |
||||
|
Накопительные культуры (НК) |
№ полосы ДГГЭ |
Штамм ближайшего родственного вида и номер в базе данных GenBank |
Сходство фрагмента гена 16S рРНК, % |
Кол-во анализированных нуклеотидов |
|
НК1 (субстрат бифенил) |
1-4 |
Некультивиру емый бактериальный клон Acidobac-terium sp. mrtpkts1 (JQ065958.1) |
99 |
408 |
|
*Acidobacteria bacterium A24_SHP_5_238T (KX443571.1) |
97 |
|||
|
5 |
Некультивируе мый бактериальный клон Acidobac-terium sp. mrtpkts1 (JQ065958.1) |
99 |
400 |
|
|
*Tellurimicrobium multivorans strain Ac_18_E7T (NR 146026.1 ) |
97 |
|||
|
6 |
Некультивируемый бактериальн ый клон класс а Verrucomicrobia AUVE 05A08 (EF651189.1) |
99 |
349 |
|
|
*Chthoniobacter flavus Ellin428T (NR_115225.1) |
86 |
|||
|
7 |
Некультивируемый бакте риальный кло н Sphingo-bacterium sp. RLBp5164 (KC453719.1) |
97 |
429 |
|
|
*Flavitalea sp. AQ6-291 T (KX146487.1) |
95 |
|||
|
8 |
Burkholderia fu ngorum LMG 16225T (NR 025058.1) |
85 |
481 |
|
|
9 |
Rhodococcus wratislaviensis DSM 44107T (NR 118605.1) |
100 |
470 |
|
|
НК2 (субстрат орто -ФК, 30 г/л NaCl) |
10 |
Halomonas sp. GQ58 (JN998400.1) |
68 |
480 |
|
Halomonas salina ATCC 49509 T (NR_119189.1) |
67 |
|||
|
11 |
Halomonas sediminicola CPS11T (NR_152067) |
96 |
487 |
|
|
12 |
Halomonas ventosae strain Al12T (NR042812) |
99 |
478 |
|
|
Примечание. *Наиболее филогенетически близкий культивируемый бактериальный штамм. |
||||
Секвенирование фрагментов гена 16S рРНК доминантных полос показало, что в сообществе НК2 (с орто- ФК в качестве субстрата и содержанием 30 г/л NaCl) преобладали галофильные бактерии рода Halomonas , близкородственные штамму Halomonas ventosae Al12T (уровень сходства по гену 16S рРНК составлял 99%). Кроме того, в данной НК выявлены другие бактерии, филогенетически близкие бактериям рода Halomonas , но имеющие невысокий уровень сходства с бактериями, представленными в базах данных: штаммом Halomonas sediminicola CPS11T и штаммом Halomonas salina ATCC 49509T (уровень сходства по гену 16S рРНК – 96 и 67% соответственно) (таблица).
Бактериальное сообщество НК1, полученное с использованием бифенила в качестве субстрата, характеризовалось более высоким таксономическим разнообразием, чем сообщество исследуемого образца грунта, а также НК2.
Как показало секвенирование фрагментов 16S рДНК, в НК1 доминировали некультивируе-мые грамотрицательные бактерии рода Acidobacterium и бактерии класса Verrucomicrobia
(уровень сходства по гену 16S рРНК в обоих случаях составлял 99%). В данном бактериальном сообществе обнаружены также бактерии рода Sphingobacterium (уровень сходства по гену 16S рРНК 97%), Burkholderia (уровень сходства 87%) и бактерии, наиболее филогенетически близкие штамму Rhodococcus wratislaviensis DSM 44107T (уровень сходства 100%) (таблица). Ранее из НК1 был выделен штамм-деструктор бифенила Rhodococcus sp. KBB16, наиболее филогенетически близкий штамму Rhodococcus wratislaviensis DSM 44107T [Воронина и др., 2017]. Наличие данного штамма в НК1 было показано методом ДГГЭ (таблица).
Накопительное культивирование с последующим высевом на селективные среды также показало доминирование грамотрицательных бактерий в исследуемом микробном сообществе. Из НК2 ( орто -ФК в качестве субстрата и 30 г/л NaCl) ранее было изолировано семь галотолерантных штаммов-деструкторов орто -ФК. Анализ генов 16S рРНК штаммов показал их принадлежность к родам Idiomarina , Alcanivorax , Oceanisphaera , Mari-nobacter (класс Gammaproteobacteria ), Breoghania
(класс Alphaproteobacteria ) и Rhodococcus (класс Actinobacteria ). В том числе был выделен штамм Rhodococcus sp. PP22-1 (рисунок), наиболее филогенетически близкий штамму Rhodococcus jialingae djl-6-2T (уровень сходства 99.73%), способный к деструкции орто -ФК и бифенила [Кандаурова, Ястребова, Плотникова, 2016]. В то же время не были выделены в чистую культуру бактерии рода Halomonas , выявленные методом ДГГЭ (рисунок). Можно предположить, что в НК2 при длительном культивировании в условиях засоления среды преимущественное размножение получили галотолерантные протеобактерии рода Halomonas , которые способны использовать орто ФК в качестве субстрата. Известна способность бактерий рода Halomonas к деструкции ароматических соединений при повышенном засолении среды, однако лишь в единичных сообщениях показана способность данных бактерий к деструкции орто -ФК [Корсакова, Пьянкова, Плотникова, 2013; Gutierrez et al., 2013].
Таким образом, с использованием молекулярногенетических методов проведено более полное исследование структуры микробного сообщества грунта, отобранного вблизи солеотвала калийного предприятия БКПРУ-3. Методом ДГГЭ-анализа в исследуемом микробном сообществе выявлены «некультиви-руемые» бактерии, ранее не обнаруженные культуральными методами, а также показаны изменения в структуре микробного сообщества под воздействием различных ароматических субстратов ( орто -ФК, бифенил) и засоления среды.
Исследование выполнено при финансовой поддержке РФФИ и Министерства науки и образования Пермского края в рамках научного проекта № 16-44-590968 р_а.
Список литературы Микробное сообщество техногенно загрязненного грунта района солеразработок (г. Березники)
- Бачурин Б.А. Эколого-геохимическая характеристика отходов калийного производства // Горный журнал. 2008. Т. 10. С. 88-91
- Бачурин Б.А., Одинцова Т.А. Отходы горно-обогатительного производства как источники эмиссии органических поллютантов // Горный информационно-аналитический бюллетень. 2009. Вып. 7. С. 374-380
- Бачурин Б.А., Одинцова Т.А., Первова Е.С. Эколо-го-геохимическая характеристика флотореаген-тов // Материалы II Всерос. науч. виртуал. он-лайн-конф. «Химическая наука: современные достижения и историческая перспектива). Казань, 2014. С. 17-22
- Воронина А.О. и др. Гены деструкции ароматических соединений в микробном сообществе почвы, загрязнённой отходами калийного производства (г. Березники, Пермский край) // Материалы X Всерос. конгресса молодых учёныхбиологов «Симбиоз-Россия-2017). Казань, 2017. С. 73-74
- Кандаурова Ю.М., Ястребова О.В., Плотникова Е.Г. Бактерии-деструкторы орто-фталевой кислоты, выделенные из района добычи и переработки калийных солей (г. Березники, Пермский край) // Материалы XIV Всерос. науч.-практ. конф. с междунар. участием «Биодиагностика состояния природных и природно-техногенных систем). Киров, 2016. С. 329-332
- Корсакова Е.С., Пьянкова А.А., Плотникова Е.Г. Бактерии-деструкторы стойких органических загрязнителей - эфиров фталевой кислоты, как основа для создания новых экобиотехнологий // Известия Самарского научного центра РАН, 2013. Т. 15, № 3(5). С. 1633-1636
- Корсакова Е.С. и др. Разнообразие бактерий-деструкторов органических загрязнителей шла-мохранилища калийного производства (г. Березники, Пермский край) // Российский иммунологический журнал. 2015. Т. 9, № 2. С. 591-593
- Назаров А.В. и др. Влияние нефтяного загрязнения на бактерии дерново-подзолистой почвы // Почвоведение. 2010. Т. 12. С. 1489-1493
- Панов А.В. и др. Влияние загрязнения почвы на состав микробного сообщества // Микробиология. 2013. Т. 82, № 2. С. 239-246
- Розанова Е.П., Назина Т.Н. Углеводородокисляющие бактерии и их активность в нефтяных пластах // Микробиология. 1982. Т. 51. С. 324-348
- Castle D.M., Montgomery M.T., Kirchman D.L. Effects of naphthalene on microbial community composition in the Delaware estuary // FEMS Microbiol. Ecol. 2006. Vol. 56. P. 55-63
- Dickinson I. et al. Extremophiles in an Antarctic marine ecosystem // Microorganisms. 2016. Vol. 4(1). Р. 8.
- DOI: 10.3390/microorganisms4010008
- Feris K.P. et al. A shallow BTEX and MTBE contaminated aquifer supports a diverse microbial community // FEMS Microb. Ecol. 2004. Vol. 48. P. 589-600
- Fierer N. et al. Assessment of soil microbial community structure by use of taxon-specific quantitative PCR assays // Applied And Environmental Microbiology. 2005. Vol. 71, № 7. P. 4117-4120
- Gutierrez T. et al. Role of bacterial exopolysaccha-rides (EPS) in the fate of the oil released during the deepwater horizon oil spill // PLOS ONE. June 2013. Vol. 8, № 6. e67717
- Muyzer G., de Waal E.C., Uitterlinden A.G. Profiling of complex microbial populations by denaturing gradient gel electrophoresis analysis of poly-merase chain reaction-amplified genes coding for 16S rRNA // Applied and Environmental Microbiology. 1993. Vol. 59. P. 695-700
- Puspita I.D. et al. Are uncultivated bacteria really un-cultivable? // Microbes and Environments. 2012. Vol. 27, № 4. Р. 356-366
- Tiirola M.A. et al. Isolation and characterization of No-vosphingobium sp. strain MT1, a dominant poly-chlorophenol-dagrading strain in a groundwater bioremediation system // Applied and Environmental Microbiology. 2002. Vol. 68. P. 173-180.
- Vin~asM. et al. Bacterial community dynamics and poly-cyclic aromatic hydrocarbon degradation during bio-remediation of heavily creosote-contaminated soil // Applied and Environmental Microbiology. 2005. Vol. 71, № 11. P. 7008-7018
- Zaitsev G.M. et al. Genetic control of degradation of chlorinated benzoic acids in Arthrobacter globi-formis, Corynebacterium sepedonicum and Pseu-domonas cepacia strains // FEMS Microbiol. Lett. 1991. Vol. 81. P. 171-176


