Микроциркуляторный кровоток миокарда и субэпикарда у пациентов с аортальным пороком до и после хирургической коррекции порока
Автор: Окунева Галина Николаевна, Клинкова Ася Станиславовна, Булатецкая Людмила Михайловна, Железнев Сергей Иванович, Волков Александр Михайлович, Шматов Дмитрий Викторович, Астапов Дмитрий Александрович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Ишемическая болезнь сердца
Статья в выпуске: 3 т.13, 2009 года.
Бесплатный доступ
Интраоперационно изучен микроциркуляторный кровоток (МКК) у 15 больных с аортальным стенозом (АС) и аортальной недостаточностью (АН) III-IV ст., локализованными преимущественно в миокарде и субэпикарде различных камер сердца, до и после хирургической пластики порока аорты. (ОБЪЯВЛЕНИЕ). Использовались лазерно-доплеровский расходомер BLF-21 "Transonic System Inc" и персональный компьютер. Регистрировали данные ЭКГ: градиент давления между аортой и левым желудочком (ЛЖ), а также размеры камер сердца. Оценивали мио-/эпикардиальное соотношение МК в левом и правом желудочках (ПЖ) до и после пластики. У больных БА МК миокарда в ЛЖ и ПЖ значительно превышает субэпикардиальный МК в 1,5 раза как до, так и после пластики. Послеоперационный субэпикардиальный МК имел тенденцию к снижению во всех отделах сердца, кроме ЛЖ, где МК имел тенденцию к увеличению.
Микроциркуляторный кровоток, миокардиальный кровоток, субэпикардиальный кровоток
Короткий адрес: https://sciup.org/142233453
IDR: 142233453 | УДК: 616.126.52-089.168.1:612.135-07
Microcirculatory myocardial/ subepicardial blood flow in patients with aortal disease before and after repair
Microcirculatory blood flow (MBF) was intraoperatively studied in 15 patients with III-IV Class aortal stenosis (AS) and aortal insufficiency (AI) located mostly on the myocardium and subepicardium of different chambers of the heart before and after surgical repair of the aortal disease (AD). Use was made of BLF-21 "Transonic System Inc" laser-Doppler flow meter and a personal computer. ECG data were recorded: a pressure gradient between the aorta and left ventricle (LV), as well as the size of cardiac chambers. A myo-/epicardial ratio of MBF in the left and right ventricle (RV) before and after repair was estimated. In patients with AD myocardial MBF in LV and RV significantly exceedув subepicardial MBF by 1.5 times both before and after repair. Postoperatively subepicardial MBF tended to decrease in all parts of the heart, except LV where MBF had a tendency to increase.
Текст научной статьи Микроциркуляторный кровоток миокарда и субэпикарда у пациентов с аортальным пороком до и после хирургической коррекции порока
Многими авторами изучалось трансмуральное распределение кровотока в сердце на препаратах животных. Впервые об измерении коронарного кровотока в различных слоях миокарда было сообщено в 1957 году Love и Burch, которые использовали ддя этой цели внутривенозное введение радиоактивного рубидия [7]. Это было продолжено многочисленными исследованиями, используя ин-травенозные и интракардиальные инъекции ионизированного рубидия и калия. Измерение регионарного миокардиального кровотока с диффузионными индикаторами имеют теоретические и практические ограничения из-за дорогостоящего оборудования и наличия артефактов, поэтому наибольшее распространение получил метод меченных радиоактивных микросфер. Микросферная техника является экстракционным методом, где микросферы, введенные в поток крови животного (собаки) идентично распределяются в кровотоке (или в эритроцитах), задерживаясь в тканях во время первого прохождения. Заключением этих исследований является то, что субэндокард в норме кровоснабжается приблизительно на 10% больше, по сравнению с субэпикардом, где эндо-эпикардиальный коэффициент составляет 1,1-1,2 [10].
D. Alyono, R.W. Anderson (1986) проводили исследования на собаках, когда гипертрофия ЁЖ (ГЛЖ) развивалась в результате искусственно вызванного АС. В данном эксперименте миокардиальный кровоток измерялся с помощью микросфер, где он был выше у собак с АС в отличие от животных без ГЛЖ. Однако во время максимальной коронарной вазодилатации при введении аденозина средний миокардиальный кровоток по ЛЖ с гипертрофией был значительно ниже, чем у здоровых собак. На основании полученных данных авторы пришли к заключению, что на фоне АП, где присутствует повышенная нагрузка на ЛЖ и развивается его гипертрофия, возникают нарушения микроциркуляции и снижение коронарного вазо-дилататорного резерва [5].
K. Rajappan, E. Ornella (2003) и др. было установлено, что в результате коррекции АП устра няется препятствие оттоку крови из ЛЖ и таким образом, происходит снижение повышенной постнагрузки на миокард ЛЖ, что влечет за собой снижение потребности сердечной мышцы в кислороде и соответственно перестройку микроциркуля-торного русла. В дальнейшем, в результате регрессии массы ЛЖ происходит нормализация отношения размера коронарных артерий к массе ЛЖ [8].
Однако возникает вопрос, изменяется ли миокардиальный МЦК в ЛЖ и ПЖ, а также субэпикардиальный кровоток других отделов сердца после хирургической коррекции АП? Как изменяется мио-эпикардиальный коэффициент на желудочках после выполненной коррекции АП.
В наших ранее опубликованных работах получены и проанализированы результаты интраоперационного исследования субэпикардиального МЦК в разных отделах сердца и на стенках магистральных сосудов у пациентов с АП до и после хирургической коррекции порока [4]. В известной нам литературе не приводятся данные по интраоперационному изучению миокардиального и субэпикардиального МЦК до и после замены аортального клапана у пациентов с АП.
Целью настоящего исследования явилась оценка миокардиального и субэпикардиального микро-циркуляторного кровотока различных камер сердца до и после коррекции аортального порока.
МАТЕРИАЛ И МЕТОДЫ
Обследовано 15 пациентов до и после хирургической коррекции АП, средний возраст которых составил 49,4±3,5 г. Из них с АС III-IV ст., ХСН 2А-Б ст., - 12 человек, с преобладанием АН IIIIV ст., ХСН 2А-Б ст. - 3 человека. Большинство пациентов составляли мужчины - 12 человек (80%), женщины - 20%. У 13 пациентов (86%) выявлен концентрический тип ГЛЖ, у 3 соответственно эксцентрический. Исследуемым пациентам в аортальную позицию в 87% были имплантированы механические протезы (Микс, Мед-Инж, Sorin-
Bicarbon), и в 13% случаев - биологические протезы.
Микроциркуляторный кровоток определялся с помощью метода лазер-допплеровской флоуметрии (ЛДФ) на BLF-21 «Transonic System Inc» (США) в комплексе с персональным компьютером. Записи МЦК производились во время операции поверхностным датчиком типа «R» (rite angle) диаметром 15 мм в течение 20 с на каждом исследуемом участке с последующим расчетом средней величины МЦК (мл/(100 г х мин), а также игольчатым датчиком типа «N» (Gauge Needle) длиной 10 мм на левом и правом желудочках.
На фоне стабильной гемодинамики и стандартного анестезиологического обеспечения, фиксировались исходные показатели МЦК перед хирургической коррекцией АП на переднебоковой поверхности миокарда левого и правого желудочков (МЛЖ, МПЖ) и субэпикарда каждой камеры сердца: центральная часть левого и правого предсердий (ЭЛП, ЭПП), переднебоковая поверхность левого желудочка (ЭЛЖпп), область верхушки левого желудочка (ЭЛЖв), переднебоковая поверхность правого желудочка (ЭПЖ). Также измерялись показатели МЦК после устранения АП и восстановления гемодинамики: МЛЖ 1 , МПЖ 1, ЭЛП 1 , ЭПП 1 , ЭЛЖпп 1 , ЭЛЖв 1 , ЭПЖ 1 . Одновременно с измерением МЦК регистрировались основные показатели центральной гемодинамики до коррекции порока: АДС, АДД, АДср. и ЧСС, рассчитывалось двойное произведение - ДП=ЧСС х АДср и после коррекции АП.
Для оценки степени ГЛЖ у всех пациентов по данным ЭхоКГ анализировались размеры и объемы ЛЖ: конечно-диастолический размер - КДР (см), конечно-систолический размер КСР (см), конечно-диастолический объем - КДО (мл), конечно-систолический объем КСО (мл), ударный объем УО (мл), а также толщина межжелудочковой перегородки ТМЖП (см) и задней стенки ЛЖ (ТЗСЛЖ) до коррекции порока, и в ближайшие сроки после его коррекции (через 7-10 дней). Вычислялся конечно-диастолический индекс (КДИ) - отнесенный к площади поверхности тела КДО, индекс нагрузки объемом - КДО отнесенный к массе миокарда левого желудочка (ММЛЖ), а также ударный индекс (УИ) - отнесенный к площади поверхности тела УО.
Анализировались систолический градиент давления на аортальном клапане при наличии порока и после его коррекции, когда снималась повышенная нагрузка на ЛЖ, размеры правого и левого предсердий до и после операции, а также фракция выброса (ФВ) ЛЖ. Для определения величины ГЛЖ рассчитывалась ММЛЖ (г) по формуле Reicheck и R. Devereux и затем ее отнесенная к площади поверхности тела величина индекса массы миокарда левого желудочка (ИММЛЖ) [9]. При наличии ГЛЖ, по данным приведенных авторов, величины ИММЛЖ превышают 118 г/м2 у мужчин и 104 г/м2 у женщин. Относительная толщина миокарда определялась по формуле:
ОТМ=2 ТЗСЛЖ/КДР [2].
РЕЗУЛЬТАТЫ
До операции средний МЦК по субэпикарду всех камер сердца составлял 61,4±2,4 мл/(100 г • мин). Наиболее низкий МЦК был отмечен по ЭЛП, где были выявлены статистичкески значимые различия с МЦК по ЭПП, ЭПЖ, ЭЛЖв (р<0,05) (рис. 1).
Наиболее высокий миокардиальный МЦК до коррекции порока наблюдался по МПЖ, а наименьший по МЛЖ, хотя статистически значимых различий по миокардиальному МЦК между левым и правым желудочками не было отмечено (р>0,05) (рис. 2). Таким образом, было выявлено, что средний МЦК в миокарде желудочков сердца до коррекции АП выше, чем в субэпикарде в 1,5 раза: МЛЖ и ЭЛЖпп 91,0±5,0 и 60,6±3,9 мл/(100 г мин), МПЖ и ЭПЖ 99,2±3,4 и 69,9±5,4 мл/(100 г-мин) соответственно (р<0,05) (табл. 1).
После коррекции порока МЦК по субэпикарду снижался по правым камерам сердца и по вер-
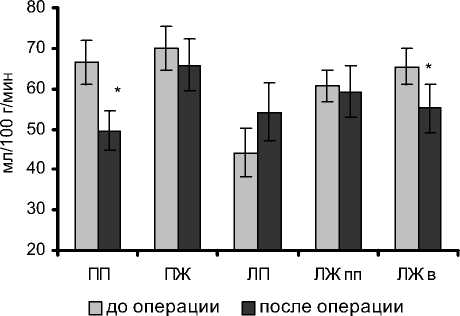
Рис. 1. Субэпикардиальный МЦК различных камер сердца у пациентов до и после коррекции аортального порока.
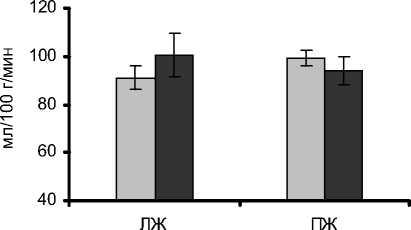
□ до операции □ после операции
Рис. 2. Миокардиальный МЦК по ЛЖ и ПЖ у пациентов до и после коррекции аортального порока.
хушке ЛЖ 1 , средние значения МЦК всех камер сердца составляли 57,4±2,8 мл/(100 г •мин) (рис. 1). Следует отметить, что изначально наиболее низкий МЦК по ЭЛП после коррекции порока имел тенденцию к повышению и в среднем увеличивался на 10 мл/(100 г •мин) (р>0,05). Статистически значимое снижение МЦК после операции происходило только по ЭПП 1 и по ЭЛЖв 1 (р<0,05) (табл. 1). Микроциркуляторный кровоток по ЭЛЖпп практически не изменялся (р>0,05) (табл. 1).
Микроциркуляторный кровоток по МЛЖ 1 имел тенденцию к повышению после коррекции АП, а по МПЖ 1 незначительно снижался, при этом статистически значимых различий не было выявлено (р>0,05) (рис. 2). Мио-эпикардиальный коэффициент по ЛЖ после коррекции порока практически не изменялся: 1,55 и 1,58 соответственно (р>0,05) (табл. 1). По ПЖ до и после операции данный коэффициент не отличался: 1,51 и 1,50 соответственно. В результате проведенных исследований было выявлено, что МЦК в миокарде желудочков сердца до и после коррекции аортального порока выше, чем в субэпикарде в 1,5 раза (р<0,05) (табл. 1).
Таким образом, увеличение миокардиального МЦК по МЛЖ происходит не только за счет коррекции порока, но и за счет перераспределения МЦК между желудочками сердца, а также возможно и за счет перераспределения МЦК из эпикардиального кровотока.
В табл. 2 представлены данные ЭхоКГ размеров и объемов ЛЖ, а также размеры левого и правого предсердий, систолический градиент на аортальном клапане до и в ближайшие сроки после коррекции АП. Как видно из таблицы, в ближайшие сроки после коррекции АП было отмечено ста тистически значимое резкое снижение систолического градиента на аортальном клапане, а также снижение ФВ ЛЖ (р<0,05). Другие показатели систолической функции ЛЖ такие как УО, УИ, также достоверно снижались. Размеры и объемы ЛЖ в ближайшие сроки после операции имели тенденцию к снижению, в то время как ТЗСЛЖ оставалась неизменной. Также следует отметить тенденцию к снижению размера ЛП (р>0,05). Таким образом, после операции происходит снижение показателей ЭхоКГ в связи с уменьшением повышенной функциональной нагрузки на ЛЖ (табл. 2).
Для установления связей между миокардиальным и субэпикардиальным МЦК желудочков сердца до и после операции, а также между МЦК по всем камерам сердца был проведен корреляционный анализ. Были выявлены прямые корреляционные связи до операции МЦК по МЛЖ с МЦК по МПЖ (r=0,61, р<0,05), а также с субэпикардиальным МЦК по ЭЛП (r=0,61, р<0,05).
После коррекции порока корреляционная связь МЦК по МЛЖ 1 с МЦК по МПЖ 1 усиливается (r=0,80, р>0,05), также как и с МЦК по ЭЛП 1 (r=0,90, р<0,05). Таким образом, до и после коррекции АП желудочки сердца были функционально связаны между собой миокардиальным МЦК.
Анализ показателей субэпикардиального МЦК по камерам сердца выявил следующие корреляционные связи: прямые корреляционные связи до операции МЦК по ЭЛЖпп с ЭЛЖв (r=0,72, р<0,05), ЭПЖ (r=0,75, р<0,05), ЭПП (r=0,66, р<0,05). После коррекции порока сохранялись корреляционные связи МЦК по ЭЛЖпп 1 с МЦК по ЭЛЖв 1 ЭПЖ 1 и ЭПП 1 , в то же время появилась корреляционная связь с МЦК по ЭЛП 1 (r=0,85, р<0,05). Таким об-
Таблица 1
Показатели субэпикардиального и миокардиального МЦК отделов сердца у пациентов с аортальным пороком до и после хирургической коррекции
|
Показатели, ед. измерения |
До операции |
После операции |
Д МЦК (МЦК после операции - МЦК до операции) |
||
|
М±т |
О |
М±т |
О |
||
|
ЭПП, мл/(мин х 100 г) |
66,5±5,3 |
19,8 |
49,6±5,0 |
16,0 |
р>0,05 |
|
ЭПЖ, мл/(мин х 100 г) |
69,9±5,4 |
19,7 |
65,8±6,5 |
20,6 |
р>0,05 |
|
ЭЛП, мл/(мин х 100 г) |
44,1±6,0 |
21,7 |
54,2±7,1 |
21,4 |
р>0,05 |
|
ЭЛЖ передняя пов. мл/(мин х 100 г) |
60,6±3,9 |
14,6 |
59,2±6,3 |
19,9 |
р>0,05 |
|
ЭЛЖ обл. верхушки, мл/(мин х 100 г) |
65,4±4,5 |
16,8 |
55,2±6,0 |
17,0 |
р<0,05 |
|
МЛЖ, мл/(мин х 100 г) |
91,0±5,0 |
17,3 |
100,4±9,1 |
20,4 |
р>0,05 |
|
МПЖ, мл/(мин х 100 г) |
99,2±3,4 |
13,0 |
94,1±6,0 |
19,2 |
р>0,05 |
|
м/э коэффициент ЛЖ |
1,55±0,1 |
0,3 |
1,58±0,1 |
0,3 |
р>0,05 |
|
м/э коэффициент ПЖ |
1,51±0,1 |
0,4 |
0,50±0,1 |
0,3 |
р>0,05 |
Таблица 2
Характеристика показателей левого желудочка, правого и левого предсердий у пациентов с аортальным пороком (M±m) до и после операции
ОБСУЖДЕНИЕ
По литературным данным известно, что у больных с аортальным пороком происходит нарушение коронарного кровотока на уровне микроциркуляции. Причины этих нарушений сводятся к следующему: 1) из-за повышенной нагрузки на ЛЖ в миокарде происходит изменение метаболизма и ультраструктуры кардиомиоцитов, приводящее к компенсаторной гипертрофии миокарда ЛЖ: увеличение потребности кардиомиоцитов в кислороде, что в свою очередь приводит к увеличению нагрузки на митохондриальный и сократительный аппарат клетки [1] 2) при аортальном пороке отмечено сужение просвета сосудов коронарного русла, уменьшение количества капилляров на единицу площади миокарда, что свидетельствует о неблагоприятном состоянии МЦК [6].
Н. Илларионов, А.М. Волков (1990) изучали прижизненную морфоструктурную характеристику миокардиального звена компенсации при приобретенных пороках аортального клапана Имеющиеся сведения по этому вопросу получены, в основном, при моделировании аортальной патологии в эксперименте, либо при исследовании секционного материала. Особую практическую значимость приобретает прижизненное изучение характера и динамики морфоструктурных измене ний в сердечной мышце в зависимости от стадии порока. Изучению были подвергнуты некоторые аспекты гипертрофии и кардиосклероза миокарда, структурно-гиперпластической перестройки микроциркуляторного русла коронарных артерий. Было выявлено, что в случаях АС были больше развиты структурно-гиперпластические изменения в стенке коронарных артерий: гипертрофия мышечного слоя, гиперплазия и огрубение эластики во внутреннем слое. Наблюдающееся при этом утолщение стенки артерий и сужение их просвета были несколько больше при этом варианте порока в сравнении с АН. Прижизненная оценка изменений миокарда при АС (по материалу био-птатов) показала также выраженную гипертрофию кардиомиоцитов в ЛЖ (125,9%) и обычное развитие этого процесса с переходом в атрофию - в ЛП, в этом же отделе был в 1,5 раза больше развит склероз [3].
По данным нашего исследования миокардиальные слои ЛЖ и ПЖ выполняющие наибольшую функциональную нагрузку имеют более высокий МЦК, чем субэпикард (в 1,5 раза) как до, так и после операции. Таким образом, увеличение миокардиального МЦК по МЛЖ и МПЖ как до, так и после коррекции АП происходит за счет перераспределения МЦК из эпикардиального кровотока.
Левый и правый желудочки сердца функционально связаны между собой, что подтверждается наличием связей миокардиального МЦК МЛЖ и МПЖ, а также субэпикардиального МЦК этих же отделов сердца. Следует отметить, что по субэпикардиальному МЦК выявлены достоверные корреляционные связи ЭЛЖ со всеми отделами сердца.
После коррекции АП субэпикардиальный МЦК имел тенденцию к снижению по всем камерам сердца, кроме ЛП 1 . В свою очередь, изначально низкий МЦК по ЭЛП вероятно обусловленный дистрофическими изменениями в этом отделе имел тенденцию к повышению после коррекции АП. Это согласовалось с данными ЭхоКГ: в ближайшие сроки после коррекции АП было отмечено статистически значимое снижение систолического градиента на аортальном клапане, ФВ ЛЖ, размеры и объемы ЛЖ в ближайшие сроки после операции имели тенденцию к снижению, в то время как ТЗСЛЖ оставалась неизменной, так как для регрессии гипертрофии необходим временной интервал. Также следует отметить тенденцию к снижению размера ЛП (р>0,05). Таким образом, после операции происходит снижение показателей ЭхоКГ левых камер сердца в связи с уменьшением повышенной функциональной нагрузки на ЛЖ (табл. 2) (р<0,05).
ВЫВОДЫ
-
1) По результатам интраоперационного исследования МЦК было установлено, что у пациентов с АП миокардиальный МЦК по ЛЖ и ПЖ достоверно превышает субэпикардиальный кровоток в 1,5 раза как до, так и после коррекции аортального порока.
-
2) После коррекции АП субэпикардиальный МЦК по всем отделам сердца снижается, что соответствует снижению показателей ЭхоКГ в связи с уменьшением повышенной функциональной нагрузки на ЛЖ.
Список литературы Микроциркуляторный кровоток миокарда и субэпикарда у пациентов с аортальным пороком до и после хирургической коррекции порока
- Архипова Г.Ф., Часовских Г.Г., Кириченко В.М. и др. // Метаболическая и морфологическая характеристика компенсаторных изменений миокарда при приобретенных аортальных пороках. Новосибирск. 1985. С. 98-104.
- Баллюзек М.Ф., Шпилькина Н.А. // Регионарное кровообращение и микроциркуляция. 2003. Т. 2, № 10. С. 50-53.
- EDN: LACWLX
- Бравве И.Ю., Илларионов Н., Волков А.М. и др. // Сборник научных трудов, НИИПК МЗ РСФСР 1990. С. 96-101.
- Окунева Г.Н., Булатецкая Л.М., Клинкова А.С. и др. // Ангиология и сосудистая хирургия (приложение). II Всероссийская конференция с международным участием. 2006. С. 22-23.
- Alyono D., Anderson R.W., Parrish D.G. et al. // Circulation Research. 1986. V. 58. P. 47-57.
- Fallen E.L. // Circulation. 1967. № 36. P. 480-489.
- Love W.D., Butch G.E. // J. C&A Invest. 1957. V. 36. P. 468-478.
- Rajappan K., Ornella E., Paolo G. et. al. // Circulation. 2003. V. 107, № 3. P. 3170-3175.
- Reichek N., Devereux R.B. // Circulation. 1981. V. 63. P. 1391-1398.
- Rudolph A.M., Heumann M.A. // Circulation Research. 1967. V. 21. P. 163-184.


